常规超声及CEUS诊断肺周围性病变
胡美娟,张 诚,周爱云,黄文孜
(南昌大学第一附属医院超声科,江西 南昌 330006)
周围型肺癌早期症状不明显,常不能被准确诊断[1]。早期准确诊断周围型肺癌对制定治疗策略、改善预后有重要意义[2]。临床常用胸部CT、纤维支气管镜等检查肺部疾病,但前者费用较昂贵且辐射量大,不宜多次使用,后者不能全面观察贴近胸膜的病变,且检查时患者耐受性差并有出血、心律失常等并发症可能。超声作为一种无创、无辐射的检查手段,沿肋间扫查时可探及贴于胸膜下或存在肺实变的病灶,故可用于肺周围性病变的探查。CEUS可反映病灶内微血流灌注情况,为判断病灶的良恶性提供参考[3]。本研究探讨常规超声和CEUS诊断肺周围性病变的价值。
1 资料与方法
1.1 一般资料收集2013年6月—2017年1月因胸部CT发现存在邻近胸膜的肺周围性病变患者120例,其中男80例,女40例,年龄36~75岁,平均(52.5±7.8)岁。所有患者CEUS及穿刺前均签署知情同意书。所有病灶均经穿刺活检或手术后病理证实。
1.2 仪器与方法采用Philips iU Elite彩色多普勒超声诊断仪,C5-1扇形探头,频率1~5 MHz。嘱患者取方便操作的舒适体位(如骑跨位、仰卧位、俯卧位等)。先采用常规超声明确病灶的位置、大小、形态、内部回声、血流情况及与毗邻组织的关系,然后行CEUS检查,造影剂为声维诺冻干粉末,加入5.0 ml生理盐水摇匀,形成微气泡混悬液,再经前臂肘静脉团注2.5 ml,随后注入5.0 ml生理盐水。注射造影剂的同时启动图像存储功能,实时监测病变内造影剂灌注及增强情况,并进行时间-强度曲线分析,获得相关参数,包括病灶的始增时间(rise time, RT)、峰值强度(peak intensity, PI)、平均渡越时间(mean transit time, MTT)、曲线下面积(area under curve, AUC)、半洗出时间(half washout time, TPH)、开始廓清时间、下降支斜率(descending slope, DS)。
采用巴德自动活检枪,选取病灶内均匀增强区进行穿刺活检,避开病灶内的粗大血管,一般穿刺2针,将所得穿刺标本置入福尔马林溶液中固定,送病理检查。
1.3 统计学分析采用SPSS 17.0统计分析软件,对计量资料行正态性检验,以±s表示,采用独立样本t检验比较良恶性病变CEUS各定量参数;采用χ2检验比较良恶性病灶形态;以P<0.05为差异有统计学意义。
2 结果
120例患者中,良性52例,其中炎性病变41例,结核10例,肺脓肿1例;恶性68例,其中鳞癌38例,腺癌20例,小细胞癌6例,淋巴瘤4例。52例良性病变患者中,46例呈楔形或类三角形,3例呈类圆形,3例呈不规则形;68例恶性病变患者中,9例呈楔形或类三角形,41例呈类圆形,18例呈不规则形。良恶性病变的形态比较差异有统计学意义(χ2=67.167,P<0.001);良恶性病变时间-强度曲线参数比较见表1,良性病变RT快于恶性病变(P<0.001),相对于恶性病变,良性病变呈“快进”;良性病变DS低于恶性病变(P<0.001),开始廓清时间慢于恶性病变(P<0.001),呈“慢退”型(图1、2)。而良恶性病变的PI、MTT、AUC、TPH差异均无统计学意义(P均>0.05)。
3例患者病变形态呈楔形或类三角形,病灶RT为3 s,但病灶中央均出现类圆形低增强区,且低增强区的RT约8 s,后经超声引导穿刺活检,取病灶内低增强区,病理结果为腺癌。
3 讨论
在过去几十年中,肺癌的发病率及死亡率均居恶性肿瘤首位[4-5]。以肺癌为主的肺周围性病变早期临床症状不典型,常延误诊断。早期准确诊断肺周围性病变对临床治疗方案的制定有重要指导意义,同时对患者的预后也有重要影响。目前,临床对肺部病变的诊断主要采用纤维支气管镜、胸部X线和胸部CT检查等,纤维支气管镜较易显示肺部中央的病灶,但有时难以显示一些肺周围性病变,且存在出血、心律失常等并发症,而胸部X线和CT检查虽可提供一定的诊断信息,但因辐射较大,故不宜多次重复使用。
表1 肺周围性病变CEUS时间-强度曲线各参数的比较(±s)
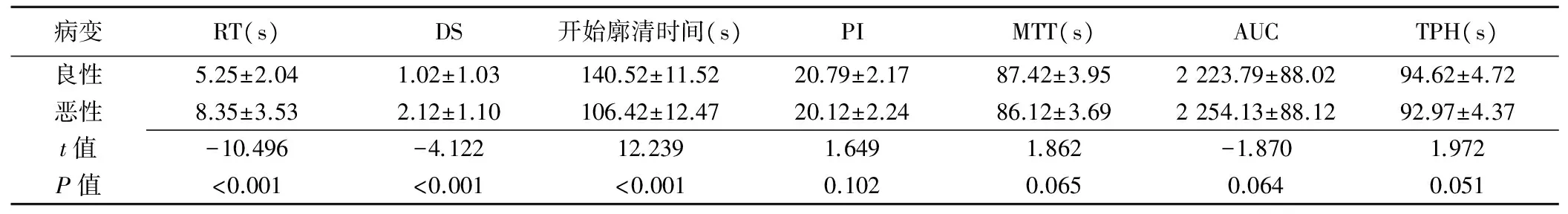
表1 肺周围性病变CEUS时间-强度曲线各参数的比较(±s)
病变RT(s)DS开始廓清时间(s)PIMTT(s)AUCTPH(s)良性5.25±2.041.02±1.03140.52±11.5220.79±2.1787.42±3.952223.79±88.0294.62±4.72恶性8.35±3.532.12±1.10106.42±12.4720.12±2.2486.12±3.692254.13±88.1292.97±4.37t值-10.496-4.12212.2391.6491.862-1.8701.972P值<0.001<0.001<0.0010.1020.0650.0640.051
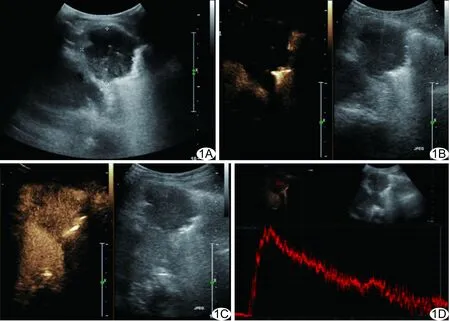
图1 患者男,45岁,咳嗽、咳血半年,肺鳞癌 A.常规超声示左下肺约3.7 cm×3.7 cm低回声团,边界清晰; B.造影 13 s病灶出现增强; C.造影 41 s病灶呈不均匀低增强; D.CEUS时间-强度曲线呈“慢进快退”模式
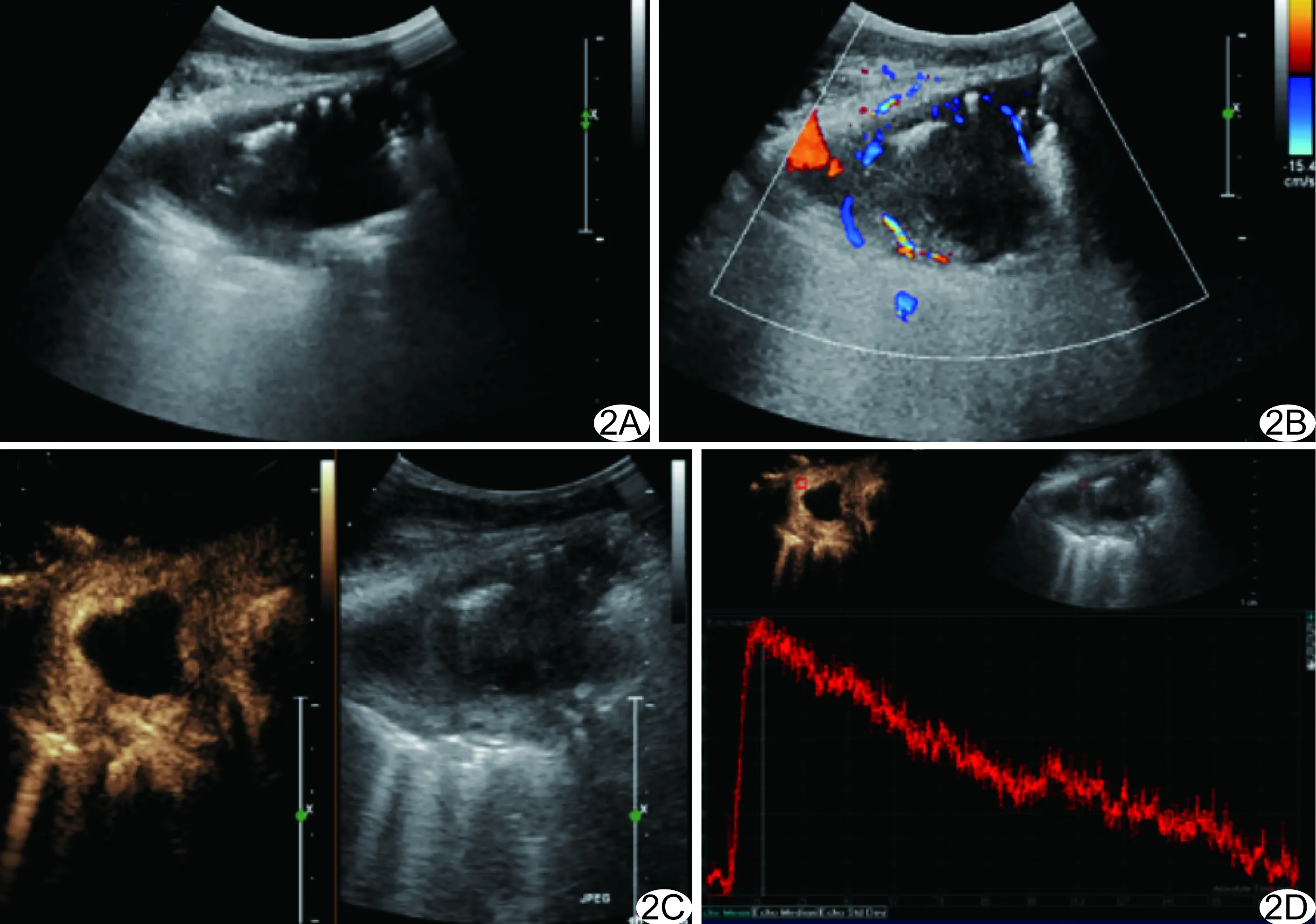
图2 患者女,56岁,咳嗽不适3月余,机化性肺炎 A. 二维超声示病灶呈楔形改变,内可见条状强回声 “支气管”征; B.CDFI示病灶周边可见较丰富血流信号; C.造影 5 s病灶开始增强,中央出现类圆形坏死区; D.时间-强度曲线呈“快进慢退”改变
超声可清晰显示贴近胸膜的肺周围性病变[6-8],常规超声可显示肺周围性病变的形态、回声、病变内是否存在支气管气相或液相、是否存在强回声斑点、病灶的边界及内部血流情况及与毗邻组织的关系等。陈敏华等[9-10]提出肺周围良性病变的声像图多显示为楔形或直方形,呈等或低回声,病变内可存在支气管气相或液相。本研究中肺周围性良性病变多呈楔形或类三角形,恶性病变多呈类圆形或不规则形,与陈敏华等[9]的研究结果一致。因肺周围性良性病变主要累及肺段或叶而多呈楔形或类三角形,恶性病变可能因组织的异常增生破坏肺段或叶结构而多呈类圆形或不规则形。CDFI示良性病变血流多较丰富、分布规律,呈树枝状或环绕、点线状分布,动脉与静脉常相伴行,肺不张内的血管与正常肺动脉的分支相同,呈树枝状走行;恶性肿块内血流多呈低速低阻、具有搏动性或动静脉瘘血流信号,血管走行纡曲、不规律,血流信号可伸向肿瘤内,呈穿入、转折、分叉或出现“血管集束征”[11]。
CEUS技术是将微泡造影剂经静脉注入体内,使其随血液进入病灶,以显示病灶内血流灌注情况。CEUS对显示低速血流信号十分敏感[12-13]。本研究肺周围性良性病变CEUS呈“快进慢退”,恶性病变呈“慢进快退”模式;通常良性病变RT≤6 s,恶性病变RT>6 s,可能因正常肺组织为肺动脉和支气管动脉双重动脉供血,造影剂注入肘静脉后先进入右心房,然后进入右心室以及肺动脉,因良性病变的正常肺动脉大部分不被破坏,故主要供血来源仍为肺动脉,而恶性病变可侵蚀正常肺动脉,其生长依赖新生血管,故多以支气管动脉供血为主,因此本组以正常肺动脉供血的肺周围性良性病变组织造影剂达峰时间早,而以支气管动脉供血为主的恶性病灶达峰时间较晚,两者差异有统计学意义。但也有部分良性病变如炎性假瘤及萎缩的肺组织供血肺动脉减少或闭塞,病变通过其他邻近的支气管动脉供血;另外由于异常的肺动脉血管阻力增加或通过其他支气管动脉供血也可导致造影剂到达病灶时间延长;本研究结果发现部分肺周围性恶性病变RT<6 s,可能因恶性病变明显侵犯肺动脉所致[14]。由于恶性病变多以支气管动脉供血为主,造影剂进入支气管动脉后很快经支气管动脉的分支通过呼吸排出体外,同时因大部分恶性肿瘤存在动静脉瘘或动静脉吻合,所以恶性病变相对良性病变DS低,造影剂廓清时间快,故肺良性病变CEUS模式为“快进慢退”,恶性病变造影模式为“慢进快退”,另外,本研究3例患者二维超声表现形态呈楔形改变,胸部CT提示为炎性病变,但CEUS后发现病灶内存在类圆形低增强区,且造影剂进入时间相对周边组织慢,穿刺活检时取楔形病灶内类圆形低增强区,病理结果为腺癌,提示对肺周围性楔形病灶行CEUS检查,发现病灶内出现类圆形低增强区或有球体感的低增强区时,需明确是否为炎性病灶内合并恶性肿瘤,最佳诊治方案是行穿刺活检术,穿取楔形病灶内的类圆形低增强区。临床部分肺恶性病变合并炎性改变,且肺良恶性病变可能同时受疾病不同阶段血供变化的影响,故可能为本组肺周围性良恶性病变CEUS的PI、MTT、AUC、TPH差异无统计学意义的原因。
综上所述,CEUS检查实时、便捷、无辐射,对肺周围性病变的诊断具有一定临床价值,可为临床诊治提供重要信息。
[参考文献]
[1]刘静,黄鑫,袁爽,等.超声造影在周围型肺及胸膜肿块病变诊断和穿刺活检中的应用价值.武汉大学学报(医学版),2017,38(1):57-60.
[2]Paoletti L, Pastis NJ, Denlinger CE, et al. A decade of advances in treatment of early-stage lung cancer. Clin Chest Med, 2011,32(4):827-838.
[3]Perera RH, Hernandez C, Zhou H, et al. Ultrasound imaging beyond the vasculature with new generation contrast agents. Wiley Interdiscip Rev Nanomed Nanobiotechnol, 2015,7(4):593-608.
[4]Jemal A, Bray F, Center MM, et al. Global cancer statistics. CA Cancer J Clin, 2011,61(2):69-90.
[5]段纪俊,严亚琼,杨念念,等.中国恶性肿瘤发病与死亡的国际比较分析.中国医学前沿杂志(电子版),2016,8(7):17-23.
[6]Lai SH, Wong KS, Liao SL. Value of lung ultrasonography in the diagnosis and outcome prediction of pediatric community-acquired pneumonia with necrotizing change. PLoS One, 2015,10(6):e0130082.
[7]Sartori S, Postorivo S, Vece FD, et al. Contrast-enhanced ultrasonography in peripheral lung consolidations: What's its actual role. World J Radiol, 2013,5(10):372-380.
[8]郭瑞军,梁晓宁,于泽兴,等.彩色多普勒超声引导自动穿刺活检在周围型肺肿块及胸膜病变中的应用.中国医学影像技术,2007,23(3):441-443.
[9]陈敏华,严昆,张劲松,等.超声对肺周围型占位性病变的鉴别诊断.中华医学杂志,1994,74(1):19-22.
[10]张红霞,何文,程令刚,等.超声造影在肺占位病变诊断中的价值.首都医科大学学报,2014,35(2):150-154.
[11]吴霞玲,孟娜,黄星月,等.超声造影时间-强度曲线在肺周围性病变及胸腺肿瘤诊断中的应用价值.武汉大学学报(医学版),2015,36(3):416-420.
[12]Konge L, Vilmann P, Clementsen P, et al. Reliable and valid assessment of competence in endoscopic ultrasonography and fine-needle aspiration for mediastinal staging of non-small cell lung cancer. Endoscopy, 2012,44(10):928-933.
[13]Ohnishi R, Yasuda I, Kato T, et al. Combined endobronchial and endoscopic ultrasound-guided fine needle aspiration for mediastinal nodal staging of lung cancer. Endoscopy, 2011,43(12):1082-1089.
[14]王丹,廖锦堂,李芬橞.超声造影在肺外周良恶性肿块鉴别诊断中的应用.中国现代医学杂志,2016,26(10):75-79.
致谢
科研工作的顺利完成离不开他人的帮助,在正文的最后应向对本研究提供过帮助的人致以谢意。致谢的对象包括:对研究工作提出指导性建议者,论文审阅者,资料提供者,技术协作者,帮助统计者,为本文绘制图表者,提供样品、材料、设备以及其他方便者。
致谢必须实事求是,应防止剽窃掠美之嫌,也勿强加于人,如未经允许写上专家、教授的名字,以示审阅来抬高自己。致谢一般要说明被谢者的工作的内容,如“技术指导”、“收集资料” 、“提供资料”等。

