术中多点活检提高囊性肾癌的诊断率
朱德胜 吴海啸★ 吴汉 徐旻
囊性肾癌在所有肾脏肿瘤中约占5%~7%[1],在临床上常发现囊性肾癌漏诊的现象,尤其在复杂性肾囊肿中更普遍。因此,如何提高囊性肾癌的诊断率是临床研究的重点。本实验中采用术中多点取材活检的方法检测113例囊性肾病患者合并肾癌情况,现报道如下。
1 临床资料
1.1 一般资料 选择本院泌尿外科2006年3月至2016年11月收治的囊性肾病患者113例,男82例,女31例,平均年龄51.3岁(中位46岁)。影像学上肿瘤平均直径4.78 cm(1.3~15.0cm),左肾病变59例(52.21%),右肾病变54例(47.79%);肿物中存在钙化53例(46.90%);存在分隔者31例(27.43%),单囊者82例(72.57%)。
1.2 纳入标准 所有纳入研究组的患者均行双肾CT平扫+增强扫描及双肾彩超检查,无并发其他恶性肿瘤,无家族遗传性疾病如多囊肾等。选择穿刺硬化术或保守观察治疗的患者除外。
1.3 方法 依据囊肿形态、囊壁、间隔、边界及囊液特征,自制评分表进行评分,评分表见表1。113例囊性肾病患者中,对评分高>4分,典型囊性肾癌直接行保留肾单位手术(NSS)或根治性肾切除术,并对标本不同部位取材送病理。对不能准确判断性质且拒绝NSS或根治性肾切除手术的患者行腹腔镜手术或者开放手术。术中均采用单纯囊肿壁切除+囊肿腔内不同部位多点活检方法。将送检病理组织分为A组:单纯囊壁组织;B组:单纯囊肿壁组织+囊肿腔内不同部位活检组织。根据快速病理检查结果,术中如发现恶性肾癌细胞,立即行NSS或根治性肾切除术。分析两组病理结果阳性率差异及评分结果与病理阳性率的关系。

表1 囊性肾病评分表
1.4 统计学方法 采用SPSS13.0 统计软件。计数资料组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 手术结果 15例行开放手术,98例行腹腔镜手术,最终病理确定囊性肾癌32例,其中病理分期学检查Ⅰ期28例,Ⅱ期3例,Ⅲ期1例。16例根据影像学评分7~10分,提示囊性肾癌可能,建议行NSS或根治性肾切除术,最终13例行NSS,3例行根治性肾切除术,病理证实15例为囊性肾癌,1例为复杂性囊肿,术中与术后病理一致。14例术中冰冻切片镜检诊断为囊性肾癌,立即改行肾癌根治性或NSS。2例术中病理切片检查诊断为囊肿,术后活检组织石蜡切片中发现肾癌细胞,二次行肾癌根治术(病理切片见图1)。术中发现囊肿中存在结节,且CT增强下有强化的结节影合并囊性肾癌最高(见图2)。囊肿壁厚,表面粗糙,且CT增强有不均匀强化合并囊性肾癌其次(见图3)。
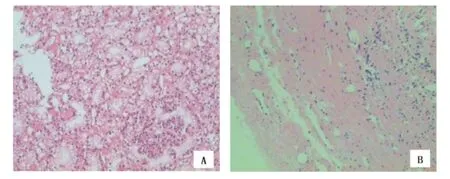
图1 病理切片图[A:囊性肾细胞癌病理切片(HE染色,×100);B:肾囊肿病理切片(HE染色,×100)]
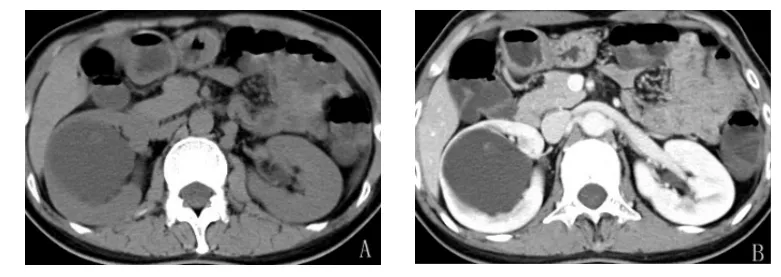
图2 右肾囊性肾癌CT片(A:CT平扫提示右肾囊性病变,囊液内有絮状物;B:动脉强化期见囊肿内有点状强化灶)
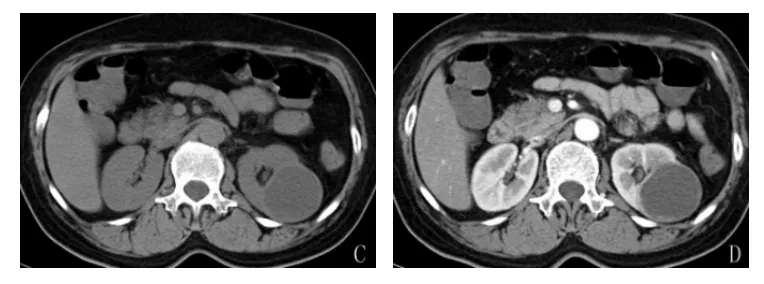
图3 左肾囊性肾癌CT片(C:CT平扫提示左肾囊性病变,壁较厚,D:动脉强化期见囊壁厚,伴局部强化灶)
2.2 各个评分中不同标本病理结果比较 见表2。

表2 各个评分中不同标本病理结果比较[n(%)]
2.3 评分与恶性的相关性 见表3。
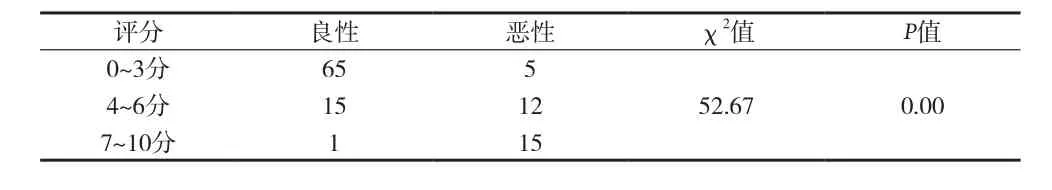
表3 评分与恶性的相关性
2.4 随访 所有手术患者均行随访,术后3例失访,1例术后2年并发冠心病死亡,1例术后6个月死于外伤。其余患者随访3~66个月,平均31个月,随访期内均未发现新增囊性肾癌病例及肿瘤复发、转移现象。
3 讨论
囊性肾病是一种常见的疾病,>50岁的人群中发病率可达50%[1]。有学者发现,在部分多房性肾囊肿和单房性肾囊肿中存在肾癌细胞,提出了关于囊性肾癌的概念[2]。Herraiz等[3]提出将囊性肾癌分为单囊性肾癌、多囊性肾癌、肾癌囊性变和肾囊肿恶性变四种类型。囊性肾癌是肾细胞癌中一种少见的类型,多数病理类型为透明细胞癌,其预后均优于传统的肾透明细胞癌[4]。在权威组织制定的治疗指南中囊性肾癌并未作为一个独立的类型,更多而被认为代表的是一类临床病例。目前囊性肾癌的概念在病理学医师和临床医师之间存在分歧,2002年肾癌分类标准中从病理学角度重新定义了囊性肾癌的概念,将多房囊性肾癌列为肾癌的独立类型,而未提及囊性肾癌的概念。
目前在临床上主要通过外科手术或穿刺活检方法获取病理标本确定囊性肾病变的性质[5],但随访中发现仍有漏诊现象。有文献报道,对于术前怀疑囊性肾癌的患者行术中病理学检查可以明确诊断,是一种理想的诊断方法。也有学者发现术后病理检查与术中病理检查结果不一致,需行二次手术治疗[6]。本资料中也发现2例术后病理与术中病理不一致情况,所以单纯依靠术中病理来确定病变性质尚存不足。对于穿刺活检的应用价值评价不一,但是多数学者认为穿刺的诊断价值有限。
临床工作中发现部分患者仅靠B超而未行CT等检查,会造成部分患者的误诊。根据作者自制的评分表,≤3分的患者,病检阳性率无差别,而>3分的则有差别,研究中发现评分>7分的16例患者仅1例为复杂性囊肿,其余均为囊性肾癌。故对于临床上评分<3分的囊性肾病患者可以选择穿刺硬化术或手术治疗,而>3分的患者,作者认为不管囊肿大小,禁忌穿刺硬化治疗。建议4~6分患者行去顶手术治疗,并在术中多点活检排除囊性肾癌可能,而7~10分的患者,建议直接行NSS或根治手术治疗。
虽然影像学能提供诊断囊性肾癌最直接的线索,但在诊断囊性肾癌的准确性仍存在较大不足。本资料发现利用CT检查结果,结合自制评分表,CT判断囊性病变性质的准确率可达69.8%,说明传统囊性肾病行腹腔镜手术切除部分囊壁行病理检查存在缺陷可能。不同学者研究囊性肾病患者合并肾癌比例存在较大差异,原因可能是检查方法及患者纳入标准不同等存在较大差异。本资料中,囊性肾癌的比例占28.32%,恶性率较高的原因可能有3个:(1)未纳入,导致良性的比例相对下降。(2)不同于常规手术仅行囊壁切除,而是囊壁和间隔及基底组织均送病理检查。(3)术中采用了多点活检的方式钳取可疑病变,可能提高了恶性病变诊断率。术中多点活检较传统手术存在明显的优势:(1)囊性肾癌细胞多数在囊壁表面或间隔中,活检操作方便,只需使用活检钳夹取疑重部位组织,在开放手术或腔镜下均能顺利完成。(2)相对手术切除标本,活检部位均表浅,创伤小,出血少,术中止血彻底,术后并发出血的几率明显下降,降低手术风险。(3)活检时可对多处可疑组织送检,减少了恶性组织漏检,提高诊断率。
本资料发现,评分>4分B组恶性率均比A组高,说明囊肿壁阳性率较囊肿基底及间隔低,术中即筛选阳性患者,减少二次手术的风险,多点活检可提高囊性肾癌的诊断率。因此,传统手术仅切除囊壁送病理检查存在漏诊的可能性。随着评分的提高,囊性肾癌的发生率升高,且呈正相关,说明根据囊性肾病的特点,采用自制评分表筛选出需行多点活检患者的可行性。
综上所述,囊性肾癌是一种少见的临床病理亚型,病理分型多以透明细胞癌为主,根据本资料随访的结果未发现肿瘤复发、转移,其预后较实质性肿瘤好。根据囊肿特点进行评分分级能在一定程度上指导囊性肾病治疗方案的选择。囊性肾病患者评分>4分建议行手术治疗,采用术中多点取材活检可以有效地提高囊性肾癌的诊断率。
[1] McGuire BB,Fitzpatrick JM.The diagnosis and management of complex renal cysts.Current opinion in urology,2010,20(5):349-354.[2] Bonsib SM.Renal cystic diseases and renal neoplasms:a minireview.Clinical journal of the American Society of Nephrology:CJ ASN,2009,4(12):1998-2007.
[3] Herraiz DOF,Merino SC,Sanchez DE,et al.Multilocular cystic nephroma:diagnosis by imaging tests.Arch Esp Urol,2004,57(7):745-748.
[4] Bhatt JR,Jewett MAS,Richard PO,et al.Multilocular Cystic Renal Cell Carcinoma:Pathologic T-staging makes no difference to favourable outcomes and should be reclassified.The Journal of urology,2016,196(5):1350-1355.
[5] Williamson SR,Halat S,Eble JN,et al.Multilocular cystic renal cell carcinoma:similarities and differences in immunoprofile compared with clear cell renal cell carcinoma.The American Journal of Surgical Pathology,2012,36(10):1425.
[6] 王杭,郭剑明,林宗明,等.BosniakⅡ~Ⅲ类型肾囊肿处理方式的再思考.中华泌尿外科杂志,2013,34(3):188-190.

