磺胺类药物HCD高能裂解与CID裂解的差异性研究
锡全
(1. 北京出入境检验检疫局,北京 100026;2. 国家质检总局国际检验检疫标准与技术法规研究中心,北京 100088)
1 引言
高能诱导裂解技术(Higher energy Collision induced Dissociation,HCD)是一项新型的质谱裂解技术,与离子阱质谱常用的碰撞诱导解离技术(collision induced dissociation,CID)相比,HCD技术提供了稳定的高能裂解方式,并可改善CID裂解中产生的低质量碎片丢失(cut-off)效应,与Orbitrap质量分析器结合还可提供高分辨质谱数据[1-3]。HCD技术在蛋白质、肽段的鉴定和测序领域具有突出优势,在代谢物鉴定、食品添加物分析也有文献报道[1-13]。HCD裂解是通过离子阱进行离子的捕获和选择后,在特定的HCD裂解池中进行高能裂解,经Orbitrap质量分析器得到高分辨的串联质谱图,被称为是一种类三重四极杆模式(triple quadruple like)的裂解技术[4]。
磺胺类(sulphonamides,SAs)是目前广泛应用在畜禽抗感染治疗中的重要药物之一,在家禽养殖业方面,SAs可预防球虫病、霍乱和感染性鼻炎,但SAs有副作用,可导致过敏反应和造血紊乱。国际食品法典委员会(CAC)和许多国家对食品和饲料中的SAs含量作了明确的规定[9, 10]。
有关SAs在三重四级杆和离子阱质谱中的裂解方式已有文献报道[14-22],但其高能裂解机理还未见报道。本实验通过对SAs药物结构母核鉴定技术的研究,掌握LTQ-Orbitrap XL多级高分辨质谱对药物特征基团的判定在兽药中的应用,对常见的6种SAs在高能裂解池中的裂解规律进行了研究,得到更为丰富的离子信息,并对比了HCD和CID两种裂解模式的差异。同时,通过研究已知SAs的裂解途径和规律,对未知SAs的裂解途径和结构解析研究也有很大的参考和指导作用。为我国的食品安全监控提供定性确证检测手段。
2 实验部分
2.1 仪器和设备
LTQ-Orbitrap XL线性离子阱-轨道离子阱高分辨组合式质谱仪(美国Thermo Fisher公司),配置电喷雾离子源(ESI源)。
2.2 试剂与材料
所有SAs标准品均购自Dr. Ehrenstorfer公司,纯度均在98%以上。其他试剂均为色谱纯,标准品溶于50%甲醇水溶液。试验用水为Milli-Q超纯水。
2.3 质谱条件
LTQ-Orbitrap XL线性离子阱-轨道离子阱高分辨组合式质谱仪(美国ThermoFisher Scientific公司),配置电喷雾离子源(ESI源)。ESI正离子模式下蠕动泵直接进样,流速10 μL·min-1。喷雾电压4.5 kV,毛细管温度150℃,壳气流速10 arb,HCD裂解碰撞气为高纯氮气,HCD归一化碰撞能量55.0%。CID裂解碰撞气为高纯氦气,CID归一化碰撞能量55.0%。
3 结果与讨论
3.1 磺胺胍
英文名称:sulfaguanidne monohydrate
结构式:

分子量:214.05245,母离子:[M+H]+=215.05972
对[M+H]+进行二级质谱扫描(HCD),m/z215.05965是[M+H]+峰,在分辨率为30,000时高分辨质谱测得的质量误差为-0.33mg/kg,符合最新的欧盟(SANCO/10684/2009)化合物确证指令。碎片离子m/z156.01122、m/z108.04418、m/z92.04927和m/z65.03833是磺胺类化合物共有的特征碎片离子。碎片离子m/z156.01122是S-N键断裂后,正电荷保留在含S端而形成的[C6H6NSO2]+;碎片离子m/z108.04418是离子[C6H6NSO2]+再失去一分子SO后产生的[C6H6NO]+;碎片离子m/z92.04927则是离子[C6H6NSO2]+失去一分子SO2产生的[C6H6N]+;碎片离子m/z65.03833则是离子[C6H6N]+裂解产生的[C5H5]+。推导裂解途径如图1。
当HCD和CID的碰撞能量均为55%时,CID裂解生成碎片离子m/z156.01118。推断其裂解机理为:S-N键断裂,生成[C6H6NSO2]+m/z156.01118。
HCD与CID相比(图2),具有共同的碎片离子峰m/z156.01138,都是在-SO2-基团两端进行的裂解。除此之外,HCD还生成了m/z108.04418、m/z92.04927和m/z65.03833碎片离子。在相同碰撞能量的CID模式下,未得到这些离子碎片,且HCD谱图更为直观清晰。

图1 磺胺胍的HCD质谱裂解途径

图2 磺胺胍在HCD(A)与CID(B)模式下的质谱图比较(碰撞能量:55%eV)
3.2 磺胺吡啶
英文名称:sulfapyridine
结构式:

分子量:249.05720,母离子:[M+H]+=250.06447
对[M+H]+进行二级质谱扫描(HCD),m/z250.06444是[M+H]+峰,在分辨率为30,000时高分辨质谱测得的质量误差为-0.12mg/kg,符合最新的欧盟(SANCO/10684/2009)化合物确证指令。碎片离子m/z156.01111、m/z108.04418、m/z92.04925和m/z65.03830是磺胺类化合物共有的特征碎片离子。碎片离子m/z156.01111是S-N键断裂后,正电荷保留在含S端而形成的[C6H6NSO2]+;碎片离子m/z108.04418是离子[C6H6NSO2]+再失去一分子SO后产生的[C6H6NO]+;碎片离子m/z92.04925则是离子[C6H6NSO2]+失去一分子SO2产生的[C6H6N]+;碎片离子m/z65.03830则是离子[C6H6N]+裂解产生的[C5H5]+。除上述共有的特征碎片离子外,磺胺吡啶还产生了其他丰度较高的碎片离子,这些碎片离子反应了R基的取代信息:离子碎片m/z95.06021是S-N键断裂后失去C6H5NO2S,正电荷保留在含N端产生的[C5H7N2]+;离子碎片m/z184.08679是S-N键和C-S键同时断裂,失去HSO2,发生偶氮反应形成的[C11H10N3]+。推导裂解途径如下(图3):
当HCD和CID的碰撞能量均为55%时,CID裂解主要生成碎片离子m/z156.01141、m/z184.08696和m/z108.04425。推断其裂解机理为:S-N键断裂,生成[C6H6NSO2]+m/z156.01138;碎片离子m/z156.01161失去一分子SO或SO2产生的[C6H6NO]+m/z108.04424。
HCD与CID相比(图4),具有共同的碎片离子峰m/z156.01138、m/z184.08692和m/z108.04439,都是在-SO2-基团两端进行的裂解。除此之外,HCD还生成了m/z95.06021、m/z92.04925和m/z65.03830碎片离子+。在相同碰撞能量的CID模式下,未得到该离子碎片,且HCD谱图更为直观清晰。

图3 磺胺吡啶的HCD质谱裂解途径
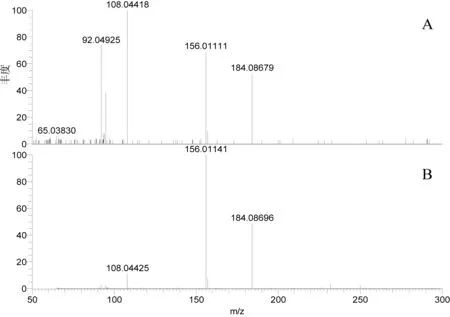
图4 磺胺吡啶在HCD(A)与CID(B)模式下的质谱图比较(碰撞能量:55%eV)
3.3 磺胺嘧啶
英文名称:sulfadiazine
结构式:

分子量:250.05245,母离子:[M+H]+=251.05972
对[M+H]+进行二级质谱扫描(HCD),m/z251.05998是[M+H]+峰,在分辨率为30,000时高分辨质谱测得的质量误差为1.0mg/kg,符合最新的欧盟(SANCO/10684/2009)化合物确证指令。碎片离子m/z156.01140、m/z108.04433、m/z92.04939和m/z65.03832是磺胺类化合物共有的特征碎片离子。碎片离子m/z156.01140是S-N键断裂后,正电荷保留在含S端而形成的[C6H6NSO2]+;碎片离子m/z108.04433是离子[C6H6NSO2]+再失去一分子SO后产生的[C6H6NO]+;碎片离子m/z92.04939则是离子[C6H6NSO2]+失去一分子SO2产生的[C6H6N]+;碎片离子m/z65.03832则是离子[C6H6N]+裂解产生的[C5H5]+。除上述共有的特征碎片离子外,磺胺嘧啶还产生了其他丰度较高的碎片离子,这些碎片离子反应了R基的取代信息:离子碎片m/z96.05553是S-N键断裂后失去C6H5NO2S,正电荷保留在含N端产生的[C4H6N3]+;离子碎片m/z158.00177是C-S键断裂后,正电荷保留在含S端生成的[C4H4N3O2S]+;而离子碎片m/z185.08226则是S-N键和C-S键同时断裂,失去HSO2,发生偶氮反应形成的[C10H9N4]+。推导裂解途径如下(图5):

图5 磺胺嘧啶的HCD质谱裂解途径
当HCD和CID的碰撞能量均为55%时,CID裂解主要生成碎片离子m/z156.01160、m/z108.04440、m/z158.00204、m/z92.04945和m/z185.08234。推断其裂解机理为:S-N键和C-S键同时断裂,失去HSO2,发生偶氮反应形成[C10H9N4]+m/z185.08234;C-S键断裂生成[C4H4N3O2S]+m/z158.00204;S-N键断裂,生成[C6H6NSO2]+m/z156.01161;而碎片离子m/z156.01161失去一分子SO或SO2产生的[C6H6NO]+m/z108.04431和[C6H6N]+m/z92.04938。
HCD与CID相比(图6),具有共同的碎片离子峰m/z185.08217、m/z158.00187、m/z156.01138、m/z108.04439和m/z92.04948,都是在-SO2-基团两端进行的裂解。除此之外,HCD还生成了m/z96.05553和m/z65.03838等离子。在相同碰撞能量的CID模式下未得到这些离子碎片,且HCD谱图更为直观清晰。

图6 磺胺嘧啶在HCD(A)与CID(B)模式下的质谱图比较(碰撞能量:55%eV)
3.4 磺胺甲基异噁唑
英文名称:sulfamethoxazole
结构式:

分子量:253.05211,母离子:[M+H]+=254.05939
对[M+H]+进行二级质谱扫描(HCD),m/z254.05916是[M+H]+峰,在分辨率为30,000时高分辨质谱测得的质量误差为-0.90mg/kg,符合最新的欧盟(SANCO/10684/2009)化合物确证指令。碎片离子m/z156.01115、m/z108.04415、m/z92.04924和m/z65.03820是磺胺类化合物共有的特征碎片离子。碎片离子m/z156.01115是S-N键断裂后,正电荷保留在含S端而形成的[C6H6NSO2]+;碎片离子m/z108.04415是离子[C6H6NSO2]+再失去一分子SO后产生的[C6H6NO]+;碎片离子m/z92.04924则是离子[C6H6NSO2]+失去一分子SO2产生的[C6H6N]+;碎片离子m/z65.03820则是离子[C6H6N]+裂解产生的[C5H5]+。除上述共有的特征碎片离子外,磺胺甲基异噁唑还产生碎片离子m/z99.05528,该碎片离子反应了R基的取代信息:是S-N键断裂后失去C6H5NO2S,正电荷保留在含N端产生的[C5H8N3]+。推导裂解途径如图7。

图7 磺胺甲基异噁唑的HCD质谱裂解途径
当HCD和CID的碰撞能量均为55%时,CID裂解主要生成碎片离子m/z156.01122、m/z188.08170和m/z108.04417。推断其裂解机理为:S-N键断裂,生成[C6H6NSO2]+m/z156.01138;碎片离子m/z156.01161失去一分子SO产生的[C6H6NO]+m/z108.04424;S-N键和C-S键同时断裂,失去HSO2,发生偶氮反应形成[C10H10N3O]+m/z188.08170。
HCD与CID相比(图8),具有共同的碎片离子峰m/z156.01138和m/z108.04439,都是在-SO2-基团两端进行的裂解。除此之外,HCD还生成了m/z99.0552、m/z92.04924和m/z65.03820碎片离子。在相同碰撞能量的CID模式下,未得到该离子碎片。另外,CID还产生碎片离子m/z188.08170。(图8)
3.5 磺胺噻唑
英文名称:sulfathiazole
结构式:

分子量:255.01362,母离子:[M+H]+=256.02089
对[M+H]+进行二级质谱扫描(HCD),m/z256.02075是[M+H]+峰,在分辨率为30,000时高分辨质谱测得的质量误差为-0.55mg/kg,符合最新的欧盟(SANCO/10684/2009)化合物确证指令。碎片离子m/z156.01132、m/z108.04430、m/z92.04937和m/z65.03827是磺胺类化合物共有的特征碎片离子。碎片离子m/z156.01137是S-N键断裂后,正电荷保留在含S端而形成的[C6H6NSO2]+;

图8 磺胺甲基异噁唑在HCD(A)与CID(B)模式下的质谱图比较(碰撞能量:55%eV)
碎片离子m/z108.04431是离子[C6H6NSO2]+再失去一分子SO后产生的[C6H6NO]+;碎片离子m/z92.04940则是离子[C6H6NSO2]+失去一分子SO2产生的[C6H6N]+;碎片离子m/z65.03831则是离子[C6H6N]+裂解产生的[C5H5]+。除上述共有的特征碎片离子外,磺胺甲基嘧啶还产生碎片离子m/z101.01657,该碎片离子反应了R基的取代信息:是S-N键断裂后失去C6H5NO2S,正电荷保留在含N端产生的[C3H5N2S]+。推导裂解途径如图9。
当HCD和CID的碰撞能量均为55%时,CID裂解主要生成碎片离子m/z156.01157和m/z108.04424。推断其裂解机理为:S-N键断裂,生成[C6H6NSO2]+m/z156.01138;碎片离子m/z156.01161失去一分子SO产生[C6H6NO]+m/z108.04424。

图9 磺胺噻唑的HCD质谱裂解途径
HCD与CID相比(图10),具有共同的碎片离子峰m/z156.01138和m/z108.04439,都是在-SO2-基团两端进行的裂解。除此之外,HCD还生成了m/z101.01657、m/z92.04937和m/z65.03827碎片离子。在相同碰撞能量的CID模式下,未得到该离子碎片,且HCD谱图更为直观清晰。

图10 磺胺噻唑在HCD(A)与CID(B)模式下的质谱图比较(碰撞能量:55%eV)
3.6 磺胺甲基嘧啶
英文名称:sulfamerazine
结构式:

分子量:264.06810,母离子:[M+H]+=265.07537
对[M+H]+进行二级质谱扫描(HCD),m/z265.07547是[M+H]+峰,在分辨率为30,000时高分辨质谱测得的质量误差为0.39mg/kg,符合最新的欧盟(SANCO/10684/2009)化合物确证指令。碎片离子m/z156.01137、m/z108.04431、m/z92.04940和m/z65.03831是磺胺类化合物共有的特征碎片离子。碎片离子m/z156.01137是S-N键断裂后,正电荷保留在含S端而形成的[C6H6NSO2]+;碎片离子m/z108.04431是离子[C6H6NSO2]+再失去一分子SO后产生的[C6H6NO]+;碎片离子m/z92.04940则是离子[C6H6NSO2]+失去一分子SO2产生的[C6H6N]+;碎片离子m/z65.03831则是离子[C6H6N]+裂解产生的[C5H5]+。除上述共有的特征碎片离子外,磺胺甲基嘧啶还产生了其他丰度较高的碎片离子,这些碎片离子反应了R基的取代信息:离子碎片m/z110.07117是S-N键断裂后失去C6H5NO2S,正电荷保留在含N端产生的[C5H8N3]+;离子碎片m/z172.01747是C-S键断裂后,正电荷保留在含S端生成的[C5H6N3O2S]+;而碎片离子m/z190.02812则是离子m/z172.01747经分子离子反应,加合一分子H2O后形成的[C5H6N3O2S·H2O]+。推导裂解途径如图11。
当HCD和CID的碰撞能量均为55%时,CID裂解主要生成碎片离子m/z156.01138、m/z172.01755、m/z190.02803、m/z110.07116、m/z108.04424和m/z92.04929。推断其裂解机理为:C-S键断裂生成[C5H6N3O2S]+m/z172.01755,再经分子离子反应,加合一分子H2O后形成离子[C5H6N3O2S·H2O]+m/z190.02803;S-N键断裂,生成[C6H6NSO2]+m/z156.01138和[C5H8N3]+m/z110.07116;碎片离子m/z156.01161失去一分子SO或SO2产生的[C6H6NO]+m/z108.04424和 [C6H6N]+m/z92.04929。

图11 磺胺甲基嘧啶的HCD质谱裂解途径
HCD与CID相比(图12),具有共同的碎片离子峰m/z156.01138、m/z172.01752、m/z190.02809、m/z110.07127、m/z108.04439和m/z92.04948,都是在-SO2-基团两端进行的裂解。除此之外,HCD还生成了m/z65.03831碎片离子,它是离子m/z92.04939裂解产生的[C5H5]+。在相同碰撞能量的CID模式下,未得到该离子碎片,且HCD谱图更为直观清晰。

图12 磺胺甲基嘧啶在HCD(A)与CID(B)模式下的质谱图比较(碰撞能量:55%eV)
4 结论
磺胺类药物是一类传统的合成抗菌药物,因其具有对氨基苯磺酰胺结构,在ESI正离子模式中产生[M+H]+分子离子,在HCD裂解过程中以-SO2-NH-基团为中心,发生S-N键的断裂,并伴随着重排,产生特征离子m/z156.01138、m/z108.04439、m/z92.04948和m/z65.03858。另外磺胺类药物还发生C-S键的断裂。HCD二级质谱产生的特征碎片离子可作为磺胺类药物的判断依据,而通过R基团断裂的碎片离子峰可以推测取代基的结构。与CID相比,HCD技术提供了稳定的高能裂解方式,并可改善CID裂解中产生的cut-off效应。HCD裂解模式结合高分辨质谱数据,为推测化合物结构、质谱裂解机理等提供更为详实的裂解碎片信息,为化合物的确证提供可靠的理论依据。该质谱裂解规律可以应用于磺胺及其类似物的质谱分析,对磺胺及其类似物的快速筛选鉴别、定量分析和药动学研究起到一定的参考作用。
[1] 张娟. 磺胺二甲氧嘧啶钠在斑点叉尾鮰体内毒性及代谢的研究. 学位论文. 华中农业大学 水产品加工及贮藏工程 2010.
[2] 彭金友. 肾毒性抗菌素. 海峡药学 2000,(12): 83.
[3] 谢秀琼. 复方磺胺甲唑片致肾脏毒性1例. 海峡药学 2000, (12): 76.
[4] 杨俊超. 磺胺类药物过敏诊治方案. 中国全科医学 2005, 8(11): 935.
[5]林海丹, 谢守新, 冯德雄,等. 动物源性食品中磺胺类药物残留的固相萃取-高效液相色谱法测定. 分析测试学报 2003, 22(1): 94-96.
[6] Kishida K, Furusawa N. Matrix solid-phase dispersion extraction and high-performance liquid chromatographic determination of residual sulfonamides in chicken. Journal of Chromatography A, 2001, 937(1-2): 49-55.
[7]Sergi M, Gentili A, Perret D, et al. MSPD extraction of sulphonamides from meat followed by LC tandem MS determination. Chromatographia, 2007, 65(11-12): 757-761.
[8] 李存, 王战辉, 石玉祥,等. 免疫亲和色谱-液相色谱-串联质谱法同时检测动物肌肉组织中喹诺酮类和磺胺类药物残留. 2008年京津冀畜牧兽医科技创新交流会暨新思想、新观点、新方法论坛论文集2008:457-464.
[9] 龚明辉. 免疫亲和色谱-高效液相色谱法检测鸡肌肉中的3种磺胺类药物. 福建省畜牧兽医学会2009年学术年会论文集 2009: 26-29.
[10]Arancibia V, Valderrama M, Rodriguez P,et al. Quantitative extraction of sulfonamides in meats by supercritical methanol-modified carbon dioxide: A foray into real-world sampling. Journal of Separation Science,2003, 26(18): 1710-1716.
[11]卢立泓, 陶建伟, 蔡蒲,等. 微波萃取鳗鱼中磺胺类药物的HPLC测定方法. 现代科学仪器,2005,(1): 57-59.
[12] 耿士伟, 曲斌, 姜加华,等. QuEChERS-UPLC-MS/MS快速测定鸡肝中七种磺胺类药物残留. 中国兽药杂质,2011, (10): 16-19.
[13] 董静, 宫小明, 张立,等. QuEChERS-高效液相色谱法同时检测动物组织中的克球酚、地克珠利和磺胺类药物残留量. 中国卫生检验杂志,2008, 18(1): 26-28.
[14] Msagati T A M, Nindi M. M. Multiresidue determination of sulfonamides in a variety of biological matrices by supported liquid membrane with high pressure liquid chromatography-electrospray mass spectrometry detection. Talanta, 2004, 64(1): 87-100.
[15]Roybal José E, Pfenning Allen P, Turnipseed Sherri B.et al. Application of size-exclusion chromatography to the analysis of shrimp for sulfonamide residues. Analytica Chimica Acta, 2003, 483(1-2): 147-152.
[16]Barham R, Black W D, Claxton J, et al, Rapid ashy for detecting sulfonamidesin tissues of slaughtered animals. J Food Protection, 2001, 64(10): 1565-1573.
[17] 刘雪红, 李 娟, 董紫凌,等. 鸡肉中磺胺类药物残留的薄层色谱检测方法.中国畜牧兽医,2007, 34(5): 31-33.
[18] Giovanardi C, Barbieri L, Tantillo M G. Determination of Sulfonamide Residues in Raw Hams. Industrie Alimentari, 1994, 33(329): 828-832
[19] 赵晓凤, 杨 中. 气相色谱-串联质谱法检测猪肉组织中的磺胺二甲嘧啶残留量. 饲料工业,2007, 28(2): 54-57.
[20] Reeves V B. Confirmation of multiple sulfonamide residues in bovine milk by gas chromatography-positive chemical ionization mass spectrometry. Journal of Chromatography B, 1999, 723(1-2): 127-137.
[21] Tarbin J A, Clarke P, Shearer G. Screening of sulphonamides in egg using gas chromatography-mass-selective detection and liquid chromatography-mass spectrometry. Journal of Chromatography B, 1999, 729(1-2): 127-138.
[22] 李存, 江海洋, 吴银良,等. 高效液相色谱-荧光-紫外法测定动物肌肉组织中多类药物残留. 分析化学,2009, 37(8): 1102-1106.

