人工颈椎间盘置换联合前路减压融合术治疗多节段颈椎病的临床疗效分析
龚全娄纪刚刘浩*孟阳洪瑛王贝宇
随着人口老龄化的进展,多节段颈椎病的发生率与复杂性也相应的提高,不同病变节段退变的严重程度不一,相应的手术治疗方式也不尽相同。对于多节段颈椎病的手术治疗,若全部采用传统的颈椎前路融合术,则会造成颈椎运动功能的较大损失和邻近节段椎间盘的加速退变[1];而人工颈椎间盘置换术(artificial cervical disc replacement,ACDR)虽较传统的颈前路减压融合术而言,具有保留手术节段活动度并减小相邻节段活动度代偿增大的优点[2,3],但因其具有严格的手术指征和较高的医疗花费,故多节段颈椎间盘置换术的临床应用相对较少[4]。因此,介于二者之间的联合融合与置换的混合手术(hybrid surgery,HS)是治疗多节段颈椎病患者的一种可供选择的手术方式,且更利于多节段颈椎病患者的个性化治疗[5-8]。而采用 HS治疗三节段及以上颈椎病的相关报道较少,因此,本研究回顾性分析2009年1月~2013年4月于我院脊柱外科行HS治疗多节段颈椎病患者的临床资料,探讨其临床疗效。
1 资料与方法
1.1 一般资料
1.2 手术方法
所有患者术前均行气管推移训练,且手术均由同一组医生完成,全麻满意后患者仰卧位,颈部垫枕,维持颈椎适度后伸。取颈前右侧横切口,短针头置于相邻椎体后C臂X射线机透视以明确病变椎间隙,安装CCRS自动撑开器以暴露视野。拟行 ACDR节段:去除病变椎间盘组织、终板下软骨及椎体后缘增生的骨赘,细口径椎板咬骨钳咬除后纵韧带,磨钻打磨上下椎体前缘,使上下椎腰部齐平,打磨上位椎体前下缘,使前后缘连线与终板平行。应用配套专业器械行试模、打磨及开槽后,植入合适型号人工颈椎间盘,假体后缘平行于上下椎体后缘。拟行 ACDF节段:同上行经椎间隙减压,试模后植入合适的加人工骨的椎间融合器。拟行ACCF节段:上下相邻椎间隙均减压完毕后,咬除两椎间隙之间的大部分骨质、留下蛋壳样皮质骨,去除的碎骨备植骨用。磨钻磨去后份皮质骨至后纵韧带,神经剥离子突破后纵韧带、椎板咬骨钳环绕边缘咬除后纵韧带,中间部分剥离并取出,处理上下软骨终板,植入合适的加自体碎骨或髂骨的钛网,固定合适长度的钛板于椎体前方。
本研究中人工椎间盘为ProDisc-C(Synthes Spine,USA)和Prestige-LP(Medtronic Sofamor Danek,USA),Cage为Zero-P(Synthes Spine,USA),开槽后固定钛板为Atlantis系统。
1.3 术后处理
术后12~24 h拔除引流管,常规行抗生素预防感染。术后2天开始下床活动,在医生指导下行颈椎功能锻炼(屈伸、左右侧偏及左右轴向旋转活动),并逐渐增加活动量及活动范围,间断活动3周后佩戴颈托制动至术后8周。术后3天,3、6、12月,及之后每隔一年均门诊随访,并行颈椎正侧位、功能位X线片检查,必要时行CT检查。
1.4 疗效评价
1.4.1 一般指标
包括手术时间、出血量及手术并发症。
1.4.2 神经功能
术前、术后各随访时间点均采用日本整形外科协会评分(Japanese orthopaedic association,JOA)、颈椎功能残障指数 (neck disability index,NDI)、疼痛视觉模拟评分 (visual analogue scale,VAS)以评估神经功能。
1.4.3 影像学评价
置换节段活动度 (range of motion,ROM),于颈椎侧位X线片上测量置换节段上位椎体下缘及下位椎体上缘连线的夹角即置换节段Cobb角,动力位(伸屈位)X线片上置换节段Cobb角的变化即为置换节段活动度;颈椎整体活动度,动力位X线片上C2椎体下缘与C7椎体下缘连线Cobb角的变化;手术相邻节段活动度,动力位X线片上相邻节段Cobb角的变化;观察异位骨化、假体松动及融合节段融合情况。测量各节段活动度时定义前屈角为“-”,后伸角为“+”。
1.4.4 融合标准
1.5 统计学方法
2 结果
本研究18例患者中11例行ACDR联合ACDF术(见图1),7例行ACDR联合ACCF术(见图2),随访时间为18~54个月,平均26.3个月;平均手术时间(104.7±23.4)min(80 min~185 min),平均出血量(125.1±14.8)mL(45 mL~380 mL),全部患者围手术期一般情况良好,切口一期愈合,体温正常。
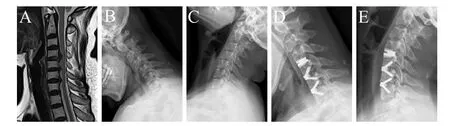
图1,患者,女,53岁。A~C颈椎术前MRI示C4/5 C5/6 C6/7椎间盘突出压迫脊髓,动力位X线片示颈椎整体活动度35.87°,置换节段(C4/5)活动度10.79°,D~E术后12月动力位X线片示内固定及假体位置良好,颈椎整体活动度32.47°,C4/5活动度12.17°。

图2,患者,女,37岁。A~C颈椎术前MRI示C3/4 C4/5 C5/6椎间盘突出压迫脊髓,动力位X线片示颈椎总活动度49.47°,C3/4(置换节段)活动度10.55°,D~E术后12月动力位X线片示内固定及假体位置良好,颈椎总活动度39.06°,C3/4活动度9.87°。
术后各随访点JOA、VAS、NDI评分与术前相比均不同程度改善,且差异均有统计学意义(P<0.05)(见表1)。术后 3天时 HS组置换节段活动度(6.90°±2.46°)较术前(8.23°±3.36°)显著下降(P<0.05),之后逐渐恢复,术后3、6、12、24 月时置换节段活动度分别为:7.86°±2.74°、8.1°±2.97°、8.45°±2.81°、8.37°±2.77°,与术前比较无统计学差异(P>0.05)(见表2)。术后24个月时颈椎整体活动度较术前显著减小(P<0.05)。术后3天置换与融合邻近节段活动度较术前均显著下降,之后逐渐增大,术后12个月时置换邻近节段活动度达到术前水平并得到良好维持(P>0.05);术后12、24月时融合邻近节段活动度较术前显著增大(P<0.05)。本组病例行融合手术节段术后6个月融合率为94.4%,术后12个月融合率为100%。患者术后X线、CT片示颈椎稳定性良好,无内植物断裂、松动、脱出,未观测到异位骨化。但本组病例中,3例术后出现颈肩部疼痛,予以非甾体抗炎药后症状缓解;1例出现吞咽异物感,5月后自行缓解。
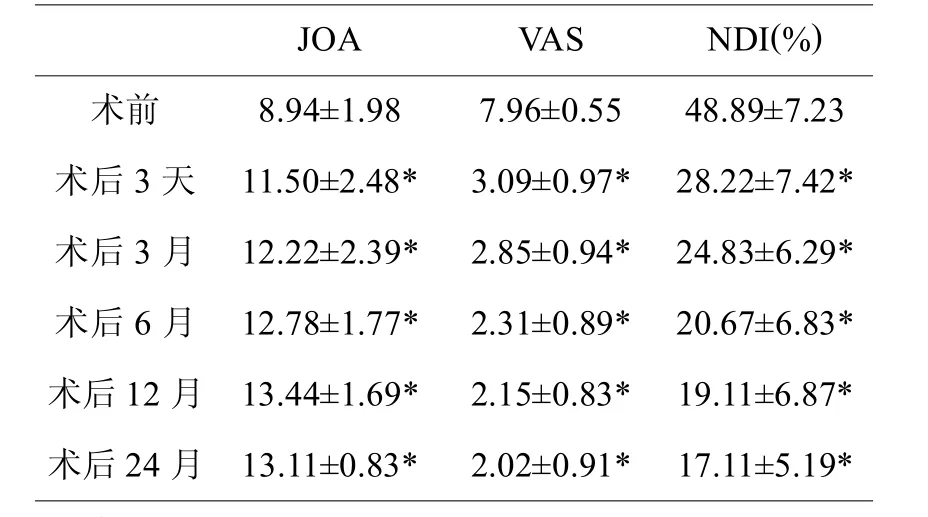
表1,患者术前与术后不同时间点JOA、VAS、NDI评分
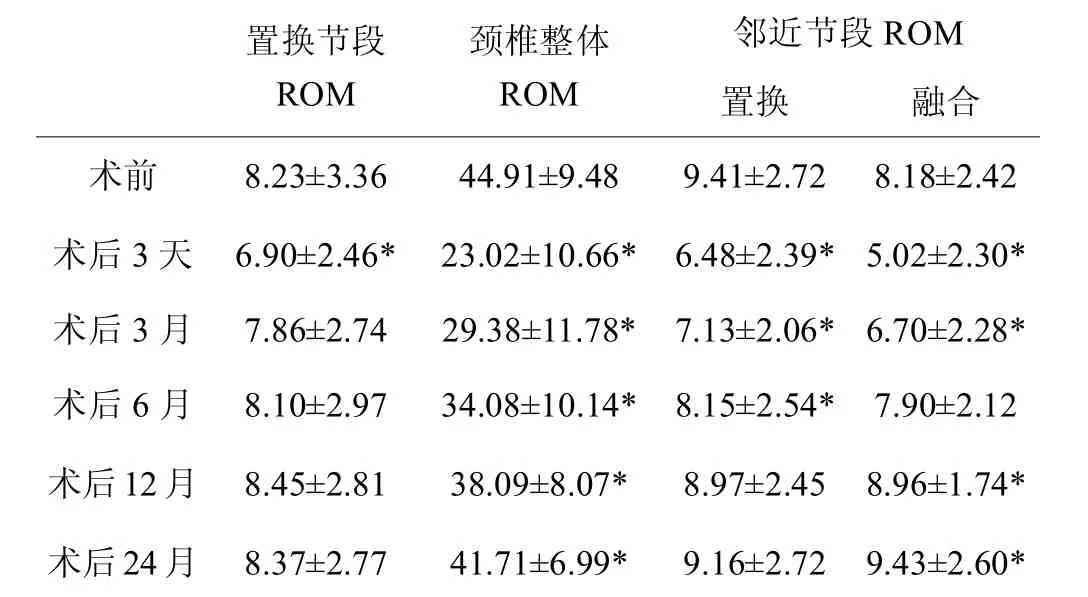
表2,患者术前与术后不同时间点节段活动度(°)
3 讨论
3.1 HS治疗多节段颈椎病的临床疗效
多节段颈椎病是指在影像学上存在连续或不连续三个节段或以上的颈椎椎体后缘骨赘形成以及椎间盘变性、突出等多种病理改变,造成颈髓或硬膜囊多个平面受压,并有相应临床表现的一类颈椎病。多节段颈椎病在临床上并不少见,且病情较重常需手术治疗,既往颈前路减压融合术是治疗多节段颈椎病的经典术式[9-11],但近年来随着研究的深入,其术后邻近节段活动度增大及相邻节段加速退变(adjacentsegmentdegenerative,ASD)的发生受到了众多学者的关注[12,13]。相邻节段退变是影响颈前路减压融合术远期疗效的重要并发症之一,文献报道其发生率为 2.2%~ 25%[14,15]。Hilibrand等[14]报道ACDF术后患者中每年约2.9%患者出现典型ASD,约25%患者术后10年内出现ASD,并指出ASD的发生与融合相邻节段活动度及应力增加有关。
人工颈椎间盘的设计理念为保留手术节段活动度,提供更好的生物力学稳定性,减缓ASD的发生。Sasso等[16]对99例单节段颈椎病患者行2年的随机对照研究,发现置换组NDI、VAS、SF-36评分较融合组改善更佳。理论上多节段ACDR也是治疗多节段颈椎病的手术方式,但目前相关研究较少,有学者提出多个人工椎间盘植入会引起颈椎活动的异常增大,且高昂的手术费用也限制了此类手术实施[17,18]。Barbagallo等[7]提出ACDR联合ACDF的混合手术能最大程度保留颈椎活动度,减小长节段融合所致相邻节段活动度代偿增大,是一种可供选择的治疗多节段颈椎病的手术方式。Shin等[8]将40例双节段颈椎病患者随机分为 HS和ACDF组,术后1年及2年时HS组NDI评分优于ACDF组,术后1个月及1年时HS组颈部VAS评分更佳,而两组上肢VAS评分差异无统计学意义。本组病例术后各随访时间点JOA、NDI、VAS评分均较术前明显改善(P<0.05),术后 24个月与术后 12个月比较,差异无统计学意义(P>0.05),其可能是因为术后神经功能的恢复在术后12个月后趋于稳定。
3.2 HS对颈椎活动度的影响
颈椎活动度是影响颈椎病患者术后疗效的重要因素,已有研究表明颈椎节段活动度的增大可能引起或加重颈椎节段的退变,置换较融合手术的优势之一在于可以保留手术节段活动度,更均匀的分担颈椎应力,重建颈椎动态稳定[12-16]。Hou等[19]比较149例行单、双节段ACDR和196例行单、双节段融合术患者的影像学资料,发现术后2年时单、双节段置换患者颈椎整体活动度、手术节段及上下邻近节段活动度均维持在术前水平;融合组患者颈椎整体及手术节段活动度均较术前显著减小,而上下邻近节段活动度较术前显著增大。本组病例术后3天时置换节段活动度较术前显著减小,考虑可能和患者术后颈托制动、精神紧张有关,术后3个月恢复到术前水平并在随访期内得到良好的维持,术后24个月时置换节段活动度为8.37°±2.77°,与国内外学者报道基本一致[7,8,18,20]。本组病例术后24个月时颈椎整体活动度 较 术 前 减 小,但 两 者 差 异 不 大(44.91°±9.48°vs 41.71°±6.99°,P=0.044),笔者认为随着颈部功能的锻炼及随访时间的延长,颈椎整体活动度存在恢复到术前水平的趋势。混合手术颈托制动存在矛盾,因融合术要求患者术后长期的颈部制动,而人工椎间盘置换术则要求患者早期积极进行颈椎功能锻炼。我们目前采用折中的方法来处理这一矛盾,术后3周内鼓励患者活动颈椎,以减少粘连,在之后的8周内要求患者颈部制动,以利于植骨融合。理由是术后3周内为纤维瘢痕形成的高峰期,此时植入骨的爬行替代尚处于早期,短暂的活动对融合的影响相对较小,此时应集中减少粘连,维持人工椎间盘良好的运动功能;而3周后粘连的发生已明显减少,此时应着重考虑制动以促进植骨融合。但如何处理活动和制动的问题尚缺乏进一步的实验支持,国内外对此也无统一的标准,而我们团队目前正在进行相关的前瞻性研究,希望未来能对HS术后颈托制动提供一个可供参考的临床依据。
目前,HS患者邻近节段活动度的报道并不一致,Kang等[18]研究发现HS组患者邻近节段活动度较术前无显著差异,Faizan等[21]通过体外生物力学研究发现上下位邻近节段活动度分别增大30%和40%,Cho等[22]研究发现双节段HS标本组相邻节段活动度较术前无明显差异;Lee等[5]报道HS患者下位相邻节段活动度较上位相邻节段活动度显著增大。有学者提出上述不一致的原因可能为实验条件的不同,笔者认为HS组上下位邻近节段中置换或融合节段邻近节段所占的比例不一致而导致的偏倚可能为其主要原因。本组病例术后24个月时置换相邻节段活动度维持在术前水平,融合相邻节段活动度较术前显著增大,上诉研究表明置换或融合相邻节段活动度的差异是影响HS患者邻近节段活动度的重要因素。
有体外生物力学研究发现颈前路融合术后融合节段上下邻近节段椎间盘内压力较实验前升高73.2%和45.3%[23],理论上与融合节段相邻的置换节段应力的升高可能会影响椎间盘假体的稳定性,且术后早期活动也可能会阻碍融合节段骨的生长。本研究HS组置换节段随访期内维持了良好的活动度,未发现椎间盘假体的松动、脱出,术后12个月融合节段均获得骨性融合,此与Lee[5],Barbagallo[7],Kang[18]和Cardoso等[20]报道的结果类似。短期研究表明人工椎间盘假体与周围融合节段存在良好的生物力学相容性,但融合与置换的相互影响仍需后续的长期随访研究。
3.3 多节段HS术中置换节段的选择
ACDR的手术适应症较前路减压融合术更为严格,Barbagallo等[7]提出HS中置换节段的选择主要基于以下因素考虑:致压因素的性质及程度;病变节段活动度;椎间隙及小关节退变程度;减压过程中需去除骨结构的范围;手术节段上下终板形态;手术相邻节段退变程度。Hilibrand等[14]报道颈椎各节段退变危险度不同,随各节段自然活动度增大而相应增加。本研究中如手术节段均满足椎间盘置换要求时优先选择生理活动度较大的间隙行椎间盘置换术(C5/6>C4/5>C6/7>C3/4)。本组病例置换节段的选择标准为:病变节段无节段不稳、无椎间隙及小关节严重退变、无椎间高度明显下降;椎间隙后方无大骨赘或后纵韧带骨化;节段活动度>3°;病变节段上下终板形态相对规整无严重穹隆或凹陷。对于多节段颈椎病患者拟行人工颈椎间盘置换联合前路减压融合术时,术前应仔细阅读患者影像学资料,明确手术节段,并综合考虑选取置换节段。
3.4 HS术内植物植入注意事项
多节段颈椎病患者病变节段较多,脊髓压迫常较重,且人工椎间盘的植入程序较复杂,需要敲击的操作较多,为减小手术并发症的发生,笔者认为行HS植入内植物时应注意以下几点:对于脊髓压迫较重的患者,应先减压全部手术节段再行内植物植入,以避免内植物植入时敲击操作加重已有的脊髓损害;应先植入人工椎间盘再行椎间融合器或钛网的植入,以避免植入人工椎间盘时的敲击操作影响已植入内植物的位置及稳定性;对于相邻 Prestige-LP假体植入时应遵循由上到下的顺序,以避免植入上位假体行敲击操作时,已植入下位假体的上板中心球向后滑动受到下板凹槽后缘的阻挡而导致上板松动或脱出。
总之,人工颈椎间盘置换联合前路减压融合术治疗多节段颈椎病可有效缓解疼痛、改善神经功能、维持颈椎生理活动度,取得满意疗效。本研究为回顾性研究,样本量偏少,希望能借此展开应用人工颈椎间盘置换联合前路减压融合术治疗多节段颈椎病大样本前瞻性随机对照研究。
[1]Yue WM,Brodner W,Highland TR.Long-term results after anterior cervical discectomy and fusion with allograft and plating:a 5-to 11-year radiologic and clinical follow-up study[J].Spine(Phila Pa 1976),2005,30(19):2138-2144.
[2] 李志钢,李锋,熊伟,等.人工颈椎间盘置换术后邻近节段椎间盘活动度的临床观察[J].生物骨科材料与临床研究,2007,4(01):18-20.
[3] Ding C,Hong Y,Liu H,et al.Intermediate clinical outcome of Bryan cervical disc replacement for degenerative disk disease and its effect on adjacent segment disks[J].Orthopedics,2012,35(6):e909-e916.
[4] 杨毅,马立泰,刘浩,等.多节段ProDisc-C人工颈椎椎间盘置换5年临床随访报道[J].生物骨科材料与临床研究,2017,14(03):28-32.
[5] Lee SB,Cho KS,Kim JY,et al.Hybrid surgery of multilevel cervical degenerative disc disease:review of literature and clinical results[J].J Korean Neurosurg Soc,2012,52(5):452-458.
[6] 刘浩,刘熹,石锐,等.双节段人工椎间盘置换加融合在多节段颈椎间盘突出症的应用[J].中国修复重建外科杂志,2006,20(4):383-386.
[7] Barbagallo GM,Assietti R,Corbino L,et al.Early results and review of the literature of a novel hybrid surgical technique combining cervical arthrodesis and disc arthroplasty for treating multilevel degenerative disc disease:opposite or complementary techniques?[J].Eur Spine J,2009,18(Suppl 1):29-39.
[8] Shin DA,Yi S,Yoon DH,et al.Artificial disc replacement combined with fusion versus two-level fusion in cervical two-level disc disease[J].Spine(Phila Pa 1976),2009,34(11):1153-1159.
[9] Ashkenazi E,Smorgick Y,Rand N,et al.Anterior decompression combined with corpectomies and discectomies in the management of multilevel cervical myelopathy:a hybrid decompression and fixation technique[J].J Neurosurg Spine,2005,3(3):205-209.
[10]Zhu B,Xu Y,Liu X,et al.Anterior approach versus posterior approach for the treatment of multilevel cervical spondylotic myelopathy:a systemic review and meta-analysis[J].Eur Spine J,2013,22(7):1583-1593.
[11]Odate S,Shikata J,Kimura H,et al.Hybrid Decompression and Fixation Technique Versus Plated 3-Vertebra Corpectomy for 4-Segment Cervical Myelopathy:Analysis of 81 Cases With a Minimum 2-Year Follow-Up[J].Clin Spine Surg,2016,29(6):226-233.
[12]Bydon M,Xu R,Garza-ramos RDL,et al.Adjacent segmentdisease after anteriorcervical discectomy and fusion:Incidence and clinical outcomes of patients requiring anterior versus posterior repeat cervical fusion[J].Surg Neurol Int,2014,5(Suppl 3):S74-S78.
[13]Xu R,Bydon M,Macki M,et al.Adjacent segment disease after anterior cervical discectomy and fusion:clinical outcomes after first repeat surgery versus second repeat surgery[J].Spine(Phila Pa 1976),2014,39(2):120-126.
[14]Hilibrand AS,Carlson GD,Palumbo MA,etal.Radiculopathy and myelopathy at segments adjacent to the site of a previous anterior cervical arthrodesis[J].J Bone Joint Surg,1999,81(4):519-528.
[15]Matsumoto M, Okada E, Ichhara D, et al. Anterior cervical decompressionand fusion accelerates adjacent segment degenerationcomparison with asymptomatic volunteers in a ten-year magneticresonance imaging follow -up study [J]. Spine, 2010, 35(1): 36-43.
[16]Sasso RC,Best NM.Cervical kinematics after fusion and bryan disc arthroplasty[J].Journal of spinal disorders&techniques,2008,21(1):19-22.
[17]Auerbach JD,Jones KJ,Fras CI,et al.The prevalence of indications and contraindications to cervical total disc replacement[J].Spine J,2008,8(5):711-716.
[18]Kang L,Lin D,Ding Z,et al.Artificial disk replacement combined with midlevelACDF versus multilevelfusion for cervical disk disease involving 3 levels[J].Orthopedics,2013,36(1):88-94.
[19]Hou Y,Liu Y,Yuan W,et al.Cervical kinematics and radiological changes after Discover artificial disc replacement versus fusion[J].Spine J,2014,14(6):867-877.
[20]Cardoso MJ,Mendelsohn A,Rosner MK.Cervical hybrid arthroplasty with 2 unique fusion techniques[J].J Neurosurg Spine,2011,15(1):48-54.
[21]Faizan A, Goel VK, Biyani A, et al. Adjacent level effects of bi leveldisc replacement, bi level fusion and disc replacement plus fusion incervical spine-a finite element based study [J]. Clin Biomech (Bristol,Avon), 2012, 27(3): 226-233.
[22]Faizan A, Goel VK, Biyani A, et al. Adjacent level effects of bi leveldisc replacement, bi level fusion and disc replacement plus fusion incervical spine-a finite element based study [J]. Clin Biomech (Bristol,Avon), 2012, 27(3): 226-233.
[23]Barrey C, Campana S, Persohn S, et al. Cervical disc prosthesis versusarthrodesis using one-level, hybrid and two-level constructs: an in vitroinvestigation [J]. Eur Spine J, 2012, 21(3): 432-442.

