替吉奥所致重症药物性间质性肺疾病一例报道并文献复习
杨霄霄,孙亚萍,薛旗山,李德强,赵丽君,闫春良*
替吉奥(S-1)为氟尿嘧啶类口服抗癌药物,可用于胃癌、头颈部癌、结直肠癌及非小细胞肺癌等治疗。有关使用S-1导致药物性间质性肺疾病(drug-induced interstitial lung disease,DILD),鲜见报道。本文报道了2016年9月北京航天总医院收治的1例S-1导致重症DILD患者的临床资料、诊疗经过,并对相关文献进行复习,以提高临床医生对S-1导致DILD的认识。
1 病例简介
患者,男,66岁,身高173 cm,体质量80 kg,体表面积2.0 m2,主因“间断发热20余天,再发3 d”于2016-09-23收入北京航天总医院。既往史:2013年因膀胱癌行根治性膀胱全切除术;2016年8月因膀胱癌颈部淋巴结转移口服S-1(早餐后40 mg,晚餐后60 mg,服21 d、休14 d为1个疗程),于第2个疗程第5天出现发热(最高体温38 ℃),查血常规示白细胞计数(WBC)1.31×109/L〔参考范围:(4.00~10.00)×109/L〕,中性粒细胞(NE)0.67×109/L〔参考范围:(2.00~7.00)×109/L〕,血小板计数(PLT)88×109/L〔参考范围:(100~300)×109/L〕,C反应蛋白(CRP)55.0 mg/L(参考范围:<100.0 mg/L);2016-08-31查肺部CT:双下肺近胸膜处可见细网格影(见图1)。予以重组人粒细胞刺激因子升高白细胞及间断服用非甾体抗炎药后体温降至正常。2016-09-20(第3个疗程第3天)因服用S-1后再次出现低热,3 d后入院。入院查体:左颈部及锁骨上窝可触及多枚鸽子蛋大小淋巴结,质韧、活动差、无压痛,双下肺可闻及Velcro啰音,无杵状指。于2016-09-24查血常规:WBC 3.76×109/L,NE 2.47×109/L,淋巴细胞计数(LY)1.14×109/L〔参考范围:(0.80~4.00)×109/L〕,尿常规、肝肾功能、电解质等正常。入院后继续予以S-1化疗,同时予以胸腺五肽、乌苯美司等提高免疫力。患者仍间断低热,但可自行降至正常。2016-09-27(入院第5天)复查WBC 1.38×109/L,NE 0.46×109/L,PLT 56×109/L,CRP 129.0 mg/L,降钙素原(PCT)0.22 ng/ml(参考范围:0~0.25 ng/ml)。予以皮下注射重组人粒细胞刺激因子(生产厂家:山东齐鲁制药有限公司)300 μg,1次/d。于2016-10-01(入院第9天)患者出现呼吸困难,满肺可闻及细湿啰音。予面罩吸氧10 L/min,血气分析:血液酸碱度(pH)7.388,氧分压(PO2)61.6 mm Hg(1 mm Hg=0.133 kPa),二氧化碳分压(PCO2)35.1 mm Hg,碱剩余(BE)-3.6 mmol/L(参考范围:-3.0~3.0 mmol/L),HCO3-20.7 mmol/L(参考范围:22.0~26.0 mmol/L)。血常规:WBC 21.26×109/L,NE 18.79×109/L,CRP 172.1 mg/L,PCT 1.18 ng/ml。肺部CT提示双肺底大片网格样改变伴实变,双侧胸腔积液(见图2)。血细菌、真菌培养均为阴性;痰培养阴性;血清和支气管肺泡灌洗液(BALF)病毒、非典型病原体、结核杆菌、1,3-β-D葡聚糖检测(G试验)和半乳甘露聚糖检测(GM试验)均为阴性;BALF六胺银染色阴性;免疫学指标抗核抗体(ANA)、抗SSA抗体、抗SSB抗体、抗中性粒细胞胞质抗体(ANCA)、髓过氧化物酶(MPO)、抗蛋白酶3(PR-3)抗体、抗Jo-1抗体均阴性;心肌酶、脑钠肽(BNP)、超声心动图均未见明显异常。诊断为S-1导致DILD,立即停用S-1。患者呼吸困难进行性加重,予以气管插管,呼吸机辅助通气,于2016-10-02予以甲泼尼龙静脉滴注1.00 mg·kg-1·d-1(40.00 mg/次,1次/12 h)治疗。患者呼吸机支持条件下降〔呼气末正压(PEEP)由10 cm H2O(1 cm H2O=0.098 kPa)下降至6 cm H2O,吸入氧浓度分数(FiO2)由80%下降至35%〕,2016-10-07将甲泼尼龙减为0.50 mg·kg-1·d-1(40.00 mg/次,1次/d,静脉滴注)。2016-10-09因患者脱机困难,再次完善上述细菌、病毒、非典型病原体、真菌等感染相关指标均为阴性,肺部CT无明显变化,考虑为激素减量过快,将甲泼尼龙增加至1.00 mg·kg-1·d-1。2016-10-12患者顺利脱机拔管。2016-10-16改口服甲泼尼龙片60 mg/次,1次/d。2016-10-19复查肺部CT,双肺病变较前明显吸收(见图3)。
2 文献复习
2.1 资料来源 分别以“替吉奥,药物性间质性肺疾病”和“替吉奥,间质性肺炎”为中文检索词检索万方数据知识服务平台和中国知网,以“S-1,interstitial lung disease”为英文检索词检索PubMed,检索时间为2000—2017年,共检索34篇文献,纳入由S-1导致肺损伤的个案报道,最终纳入8篇文献[1-8],加上本例患者,共9例S-1导致DILD患者。
2.2 基本特征 9例患者中男8例,女1例;年龄40~80岁;服药后出现DILD的潜伏期长短不一,停止服药并予以激素治疗,预后较好(见表1)。
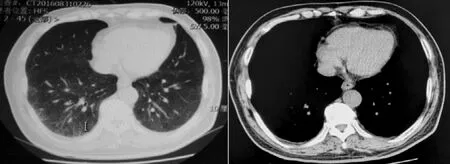
图1 病情加重前患者CT表现:胸膜下少量磨玻璃样影Figure 1 CT findings before aggravation:a few subpleural ground-glassopacity abnormalities

图2 病情加重后患者CT表现:大片肺实变,网格样改变,双侧胸腔积液Figure 2 CT findings after aggravation:massive pulmonary consolidation,reticular changes,and bilateral pleural effusion

图3 治疗后患者CT表现:双肺实变影、双侧胸腔积液明显吸收,可见网格样改变Figure 3 CT findings after treatment:bilateral pulmonary consolidation,pleural effusions,andreticular changes

表1 8例S-1导致DILD患者的基本特征Table 1 Basic characteristic of S-1-induced DILD
3 讨论
间质性肺疾病是一组累及肺实质(肺泡腔、肺泡上皮细胞)、肺间质、肺毛细血管内皮细胞和细支气管炎的一大类疾病。DILD为一类病因明确的间质性肺疾病。抗生素、化疗药物、非甾体抗炎药(non-steroidal anti-inflammatory drug,NSAIDs)、抗心律失常药等多种药物均可导致DILD,其主要作用机制包括直接氧化应激损伤、对肺泡毛细血管内皮细胞的毒性作用、免疫介导及亲水性药物致使磷脂在细胞内沉积等导致支气管痉挛(阿司匹林、β-受体阻滞剂等)、闭塞性细支气管炎(两性霉素B、胺碘酮等)、肺纤维化(阿达木单抗、博来霉素等)、超敏反应(阿糖胞苷、NSAIDs等)、肺嗜酸粒细胞增多症(胺碘酮、卡托普利等)以及非心源性肺水肿(阿糖胞苷、普萘洛尔等)等[1]。虽然每种药物导致DILD的病理生理机制不同,但临床表现、治疗及预后相似。DILD的诊断主要为排除性诊断,需明确患者服药史、服药剂量、疗程、临床表现与服药的先后关系。部分情况停药后会自行好转,再次用药疾病复发。高分辨率CT(high-resolution CT,HRCT)是目前诊断DILD常用的无创检查方法。HRCT不仅为诊断提供方向,还可监测治疗后反应。不同药物导致肺损伤的CT表现变化多样。部分化疗药物导致肺损伤起初表现为肺实质及间质浸润、肺水肿及胸腔积液,2个月后逐渐进展为肺纤维化[9]。部分药物导致肺损伤为剂量依赖性,如服用表皮生长因子受体(EGFR)抑制剂吉非替尼1个月后肺部CT才出现肺实变、双肺弥漫性磨玻璃样改变[9]。BALF对药物性肺损伤的诊断有一定指导意义。药物导致过敏性肺炎患者,BALF中淋巴细胞分数>50%,CD4/CD8下降[10]。已有研究报道,血清学标志物如涎液化糖链抗原(KL-6)、肺表面活性物质A(SP-A)、肺表面活性物质D(SP-D)等对肺间质纤维化的诊断具有特异性[11-12],但目前尚未广泛应用于临床。
本例患者在服用S-1的第2个疗程中出现发热,停药后好转,服药第3个疗程再次出现发热、呼吸困难,且进行性加重,肺部CT以弥漫性肺间质纤维化为主,排除感染性疾病、心力衰竭、肺转移癌及其他类型间质性肺疾病后,诊断为S-1导致DILD。
S-1是一种氟尿嘧啶衍生物,由替加氟(Tegafur,FT)、吉美嘧啶(Gimeracil,CDHP)和奥替拉西钾(Potassium Oxonate,OXO)组成。FT是5氟尿嘧啶(5-Fluorouracil,5-FU)的前体药物,在体内转变为5-FU而发挥抗肿瘤作用。CDHP可抑制5-FU分解,增强抗肿瘤作用。OXO可阻断5-FU磷酸化,口服后在胃肠道浓度较高,减少5-FU在胃肠道的分布,进而降低毒性。1999年,S-1在日本被批准用于治疗晚期胃癌,后被批准用于治疗头颈部癌、结直肠癌及非小细胞肺癌[13]。
临床S-1治疗头颈部肿瘤试验表明,白细胞减少症发生率为3.6%~5.2%,中性粒细胞减少症发生率为3.6%~3.8%,黏膜炎发生率为2.4%~3.8%[14-15]。S-1胶囊单药用于晚期非小细胞肺癌的临床研究显示单药客观有效率为12.5%~14.0%,且无严重毒副作用发生[16],提示S-1安全性较高。S-1耐受性良好,剂量限制性毒性为骨髓抑制,常见毒副作用包括恶心、呕吐、转氨酶升高、食欲减退、疲劳等。
随着S-1在临床中广泛应用,S-1对肺部的损伤逐渐被发现。2001年KURAKAWA等[1]首次报道了S-1导致DILD的案例。已报道病例中,患者多为中老年男性,潜伏期长短不一,经常规氧疗及激素治疗后病情均得到改善。本例患者为老年男性,在服用S-1的第2个疗程开始出现发热,第3个疗程病情加重,需要呼吸机辅助通气,排除其他疾病后,予以激素治疗后好转,符合DILD特点。
治疗DILD,首先要停药,部分患者需加用激素治疗。目前激素治疗药物导致肺损伤的所需剂量尚无统一意见。施举红等[17]对7例DILD的报道中指出,对于DILD患者,予以激素治疗后,除1例未复查肺部CT外,其余病情均逐渐稳定。既往文献报道,对于S-1导致DILD,首先予以160.00~500.00 mg甲泼尼龙冲击治疗3~5 d,此后减为1.00 mg·kg-1·d-1,病情好转[2-3,6-7]。本例患者病情较重,需要机械通气,与既往文献[2,5-6,8]比较,激素剂量少,治疗1周后未能脱机拔管,增加激素剂量治疗后,病情逐渐好转。对于S-1导致重症DILD,激素给药剂量和减量方法仍不明确,需在临床实践中进一步积累经验。
综上所述,S-1治疗恶性肿瘤的有效性及安全性已得到肯定,但随着其在临床中广泛应用,S-1导致DILD不断得到新认识,需予以密切关注。在激素治疗S-1导致重症DILD的过程中,需密切观察治疗反应,评估疗效,根据患者情况逐渐减量。
作者贡献:杨霄霄、赵丽君进行病例资料收集整理;孙亚萍、李德强、闫春良指导病例诊治,进行质量控制;杨霄霄撰写论文并对文章负责;孙亚萍、薛旗山、闫春良进行论文修改和审核。
本文无利益冲突。
[1]KURAKAWA E,KASUGA I,ISHIZUKA S,et al.Interstitial pneumonia possibly due to a novel anticancer drug,TS-1:first case report[J].Jpn J Clin Oncol,2001,31(6):284-286.
[2]TADA Y,TAKIGUCHI Y,FUJIKAWA A,et al.Pulmonary toxicity by a cytotoxic agent,S-1[J].Intern Med,2007,46(15):1243-1246.
[3]YAMAMOTO N,OHSHIMA T,SATO T,et al.A case of interstitial pneumonia after S-1 administration for gastric cancer[J].Gan To Kagaku Ryoho,2008,35(11):1935-1937.
[4]UEYAMA Y,YAMAMOTO D,YOSHIDA H,et al.A case of interstitial pneumonitis induced by S-1[J].Gan To Kagaku Ryoho,2010,37(8):1603-1606.
[5]YAMANE H,KINUGAWA M,UMEMURA S,et al.An oral fluoropyrimidine agent S-1 induced interstitial lung disease:a case report[J].World J Clin Oncol,2011,2(7):299-302.DOI:10.5306/wjco.v2.i7.299.
[6]李芳芳,鞠艳芳,关印,等.替吉奥胶囊导致的急性间质性肺病1例报道[J].中国肺癌杂志,2014,17(1):53-56.DOI:10.3779/j.issn.1009-3419.2014.01.09.LI F F,JU Y F,GUAN Y,et al.Tegafur gimeracil oteracil potassium capsule induced acute interstitial lung disease:a case report[J].Chinese Journal of Lung Cancer,2014,17(1):53-56.DOI:10.3779/j.issn.1009-3419.2014.01.09.
[7]侯钦猛,刘超,毛伟征.替吉奥联合多西他赛化疗致急性间质性肺炎1例报道[J].临床普外科电子杂志,2015,3(4):56-58.HOU Q M,LIU C,MAO W Z.Acute interstitial pneumonia induced by tegafur gimeracil oteracil potassium capsule combined with docetaxel:a case report[J].Journal of General Surgery for Clinicians(Electronic Version),2015,3(4):56-58.
[8]张翠芳,封小强,李伟.替吉奥胶囊治疗肺癌致急性间质性肺炎1例报道[J].医学研究与教育,2016,33(6):78-80.DOI:10.3969/j.issn.1674-490X.2016.06.015.ZHANG C F,FENG X Q,LI W.An oral fluoropyrimidine agent S-1 used for treating lung carcinoma induced acute interstitial lung disease:a case report[J].Medical Research and Education,2016,33(6):78-80.DOI:10.3969/j.issn.1674-490X.2016.06.015.
[9]ENDO M,JOHKOH T,KIMURA K,et al.Imaging of gefitinibrelated interstitial lung disease:multi-institutional analysis by the West Japan Thoracic Oncology Group[J].Lung Cancer,2006,52(2):135-140.DOI:10.1016/j.lungcan.2006.02.002.
[10]JANZ D R,O'NEAL H R Jr,ELY E W.Acute eosinophilic pneumonia:a case report and review of the literature[J].Crit Care Med,2009,37(4):1470-1474.DOI:10.1097/CCM.0b013e31819cc502.
[11]VAHID B,MARIK P E.Pulmonary complications of novel antineoplastic agents for solid tumors[J].Chest,2008,133(2):528-538.DOI:10.1378/chest.07-0851.
[12]INOMATA S,TAKAHASHI H,NAGATA M,et al.Acute lung injury as an adverse event of gefitinib[J].Anticancer Drugs,2004,15(5):461-467.
[13]陈莉林,曾茹.替吉奥胶囊联合紫衫类或草酸铂治疗62例晚期胃癌临床分析[J].福建医药杂志,2012,34(5):97-99.DOI:10.3969/j.issn.1002-2600.2012.05.045.CHEN L L,ZENG R.S-1 combined with paclitaxel or oxaliplatin for the treatment of clinical analysis of 62 cases of advanced gastric cancer[J].Fujian Medical Journal,2012,34(5):97-99.DOI:10.3969/j.issn.1002-2600.2012.05.045.
[14]INUYAMA Y,KIDA A,TSUKUDA M,et al.Early phaseⅡstudy of S-1 in patients with advanced head and neck cancer.S-1 Cooperative Study Group(Head and Neck Working Group)[J].Gan To Kagaku Ryoho,1998,25(8):1151-1158.
[15]TSUKAHARA K,KUBOTA A,HASEGAWA Y,et al.Randomized phase Ⅲ trial of adjuvant chemotherapy with S-1 after curative treatment in patients with squamous-cell carcinoma of the head and neck(ACTS-HNC)[J].PLoS One,2015,10(2):e0116965.DOI:10.1371/journal.pone.0116965.
[16]TAKEDA K.Clinical development of S-1 for non-small cell lung cancer:a Japanese perspective[J].Ther Adv Med Oncol,2013,5(5):301-311.DOI:10.1177/1758834013500702.
[17]施举红,严晓伟,许文兵,等.药物性肺损伤的临床诊断与治疗[J].中华结核和呼吸杂志,2007,30(3):161-166.DOI:10.3760/j.issn:1001-0939.2007.03.001.SHI J H,YAN X W,XU W B,et al.Clinicopathological manifestations of drug-induced lung disease[J].Chinese Journal of Tuberculosis and Respiratory Diseases,2007,30(3):161-166.DOI:10.3760/j.issn:1001-0939.2007.03.001.

