单增李斯特菌、副溶血弧菌和沙门氏菌液相芯片检测方法的建立
党亚丽 周亭屹
摘 要:目的是建立一种快速检测单增李斯特菌、副溶血弧菌和沙门氏菌的液相芯片检测方法。采用基于间接竞争法的原理,将3种细菌抗原分别与不同的聚苯乙烯微球偶联,以藻红蛋白(PE)荧光标记二抗为信号,优化反应条件,对建立的方法进行灵敏度、特异性和可重复性验证。结果显示,3种细菌检测抗体最佳加入量分别为10ng、10ng、5ng,建立的方法检测单增李斯特菌、副溶血弧菌和沙门氏菌的最低检测限均可达到103 CFU/mL,检测其他常见食源性致病菌无交叉反应。结论表明,建立了一种快速检测食品中金黄色葡萄球菌的液相芯片检测方法,能够应用于实际样品的检测。
关键词:单增李斯特菌 副溶血弧菌 沙门氏菌 液相芯片 检测
前言
近年来,食源性疾病已成为世界上最突出、最广泛的食品安全问题,病原微生物引起的食源性疾病则是影响食品安全的最主要因素之一[ 1 ]。微生物性食物中毒事件主要由食物污染或变质、生熟交叉污染等原因引起,且气温较高、气候潮湿的环境适于细菌生长繁殖,导致食物易于腐败变质,一旦储存、加工不当,极易发生由沙门氏菌、副溶血性弧菌等微生物引起的食物中毒。现行检测手段已无法满足日常对食源性致病菌检测的需要,目前检验检疫工作中常用于检测和鉴定食源性致病菌的方法主要有PCR、Southem Blot杂交、酶联免疫吸附法(ELISA)等一些简单的分子生物学和免疫学方法[ 2 ]。现行的检测方法一般以检测致病菌为主,需要增菌培养,检测时间长,无法满足高通量的检测要求,远不能满足食品检测的需要,市场迫切需要能同时检测食源性致病菌的灵敏度更高、特异性更强、简便快捷的高通量技术和方法[ 3 ]。因此,目前迫切需要发展一种快速、准确的方法来检测和追踪病原体和污染物的来源[4]。
液相芯片技术是在流式细胞技术、酶联免疫吸附技术和传统芯片技术基础上开发的新一代生物芯片技术和新型蛋白质研究平台,能同时检测多种致病菌。邱杨等[ 5 ]通过该法建立了对沙门氏菌、单增李斯特菌、金黄色葡萄球菌、霍乱弧菌、副溶血弧菌的快速液相芯片检测方法,检测灵敏度达到50~100copies/mL。郭启新等[ 6 ]建立了对金黄色葡萄球菌、单核增生李斯特氏菌、志贺氏菌的检测方法,具有很好的特异性,检测灵敏度分别达38、44、21CFU/mL。Sun等[ 7 ]利用该法建立了高通量的同时检测6种食源性致病菌的方法,检测灵敏度达到20.4×103CFU/mL,远高于PCR。
但基于多重PCR的液相芯片技术对单管样本进行大量不同指标的高通量多重PCR方法建立仍存在困难,至今鲜见液相芯片用于检测多种致病菌方法建立的相关报道。将液相芯片技术应用到食源性致病菌检测中,可在短时间内实现对多个样品同时进行多种致病菌灵敏、准确的检测,因而有望大大提高食源性致病菌的检测效率,在有效控制食物中毒事件的发生、食品安全控制、海关进出口检验检疫、临床诊断等方面具有广阔的应用前景。
1 材料与方法
1.1 材料
Luminex 200液相悬浮芯片系统(美国Luminex公司);4625型孔板振荡器;ST16R冷冻离心机(美国Thermo公司);编号No.18、No.29、No.52的微球(美国Luminex公司)。活化缓冲液:0.1mol/L NaH2P04- N a2 HP04,pH6.2;磷酸盐缓冲液(PBS):138mmol/L NaCI,2.7mmol/L KCl,8mmol/ L Na2HP04,1.5mmol/L KH2P04,pH7.4;洗涤缓冲液:PBS,0.05%Tween-20,pH7.4;分析缓冲液:PBS,1%BSA,pH7.4;封闭缓冲液:50mmol/L Tris,153mmol/L NaCl,2%BSA,0.05%Tween-20,pH7.4;储存缓冲液:PBS,0.1%BSA,0.02%Tween-20,0.05%叠氮化钠,pH7.4。菌种为本实验室保藏与西北农林科技大学食品实验室馈赠。
1.2 方法
1.2.1 微球偶联抗原
①取微球50μL(1.25×106个/mL)置于EP管,14000g离心4min,弃上清液。
②加入40μL活化缓冲液重悬微球,漩涡混合30s。
③加入50mg/mL NHS和EDC各5μL,混匀,避光室温下旋转混合600rpm,20min。
④加入150μL PBS,漩涡混合10s,14000g离心4min,弃上清液。
⑤用PBS洗涤3次后,加入150μL PBS重悬,再加入抗原,用PBS补齐至500μL,避光室温旋转混合600rpm,2h。
⑥14000g离心4min,弃上清液。
⑦加入150μL封闭缓冲液,漩涡混合15s,避光室温旋转混合600rpm,30min。
⑧16000g离心4min,弃上清液,加入100μL储存缓冲液4℃保存偶联的微球。抗原加入量为50ng。1.2.2 检测
①取出偶联微球,恢复至室温后漩涡30s。
②96孔板中加入100μL PBS预湿实验孔,抽去孔内液体,每孔中加入适量预混好的偶联微球(约2000个),用150μL PBS洗滌两次。
③将适量标准品或样品分别加入合适的孔中,空白孔加入等量PBS,再加入适量的抗体,用PBS补齐各孔至100μL。
④用移液器反复抽吸混匀孔内溶液,避光条件下37℃,600rpm振荡60min。
⑤反应完毕后,抽去孔内液体,用150μL PBS洗涤两次。
⑥每孔中加入100μL经适当稀释的PE标记二抗,移液器反复抽吸混匀。
⑦避光条件下,37℃,600rpm振荡45min后,抽去孔内液体,用150μL PBS洗涤两次。
⑧加入100μL PBS,900rpm震荡3min重悬浮微球并混匀,置于液相芯片系统进行测试,每种微球读取100个。
1.3 实验条件优化以及标准曲线的建立
1.3.1 最佳抗体加入量的确定
在不加样品和标准品的情况下,分别加入对应抗体1、5、10、20和40ng,加入过量的PE标记二抗,采用液相芯片系统测试。
1.3.2 单一标准曲线建立
3种标准品按照一定的比例稀释成梯度液,采用液相芯片系统测试。按照ELISA所采用的抑制率计算方式(抑制率B=(A0-An)/A0,其中A0为不加样品孔MFI值;An为加标准品或者样品孔MFI值),将各孔MFI值换算成抑制率,以抑制率为纵坐标,浓度的对数值为横坐标,建立单一标准曲线。
1.3.3 灵敏度
用PBS缓冲液将培养的菌10倍系列稀释,取1 08~102CFU/mL用已建立的方法进行检测。每个浓度重复检测3次,验证该方法的灵敏度。
1.3.4 特异性
用已建立的方法检测7种常见的食源性致病菌,每个样品重复检测3次,验证该方法的特异性。
1.3.5 重复性
在1d、5d、7d用此方法分别检测阳性菌和阴性菌,验证该方法的重复性。
2 结果与讨论
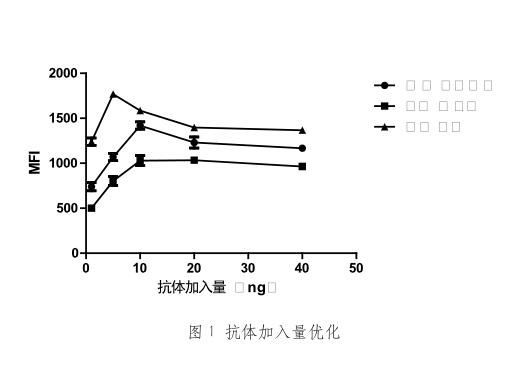
2.1 抗体加入量优化
如图1所示,低浓度时,随着抗体加入量的增加,MFI值迅速升高。抗体量增大至一定值后,种抗体的MFI值均趋于平稳,此时抗原的位点已被全部占据。选择MFI的拐点为最佳抗体加入量,因为此时靶标物和探针竞争结合兽药抗体的竞争结果变化最显著。单增李斯特菌、副溶血弧菌、沙门氏菌抗体加入量分别为10ng、10ng、5ng。
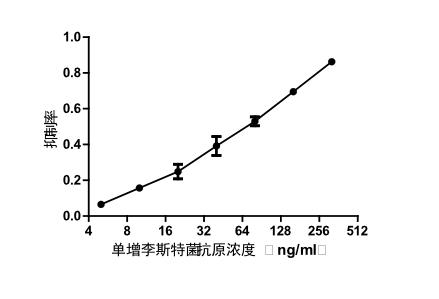
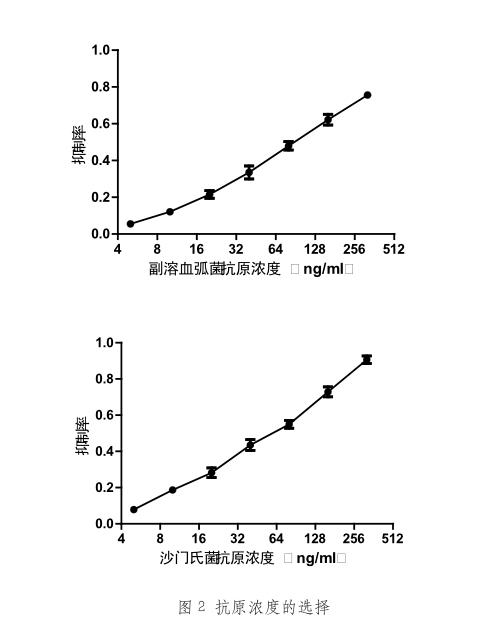
2.2 一元标准曲线建立
在加入最优抗体量的条件下,建立了一元标准曲线。在一定浓度范围内,抑制率与抗原浓度呈现良好的线性关系。单增李斯特菌方程为y=0.1935ln(x)-0.2924,R2=0.9869,副溶血弧菌方程为y=0.1748ln(x)+0.2054,R2=0.9909,沙门氏菌方程为y=0.2469ln(x)-0.1658,R2=0.9887。

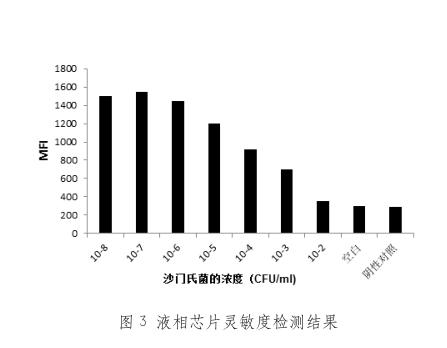
2.3 灵敏度检测
由图3可看出,三种细菌在浓度达到103CFU/mL时仍可被检出。因此本方法的灵敏度较高,可达到103CFU/mL。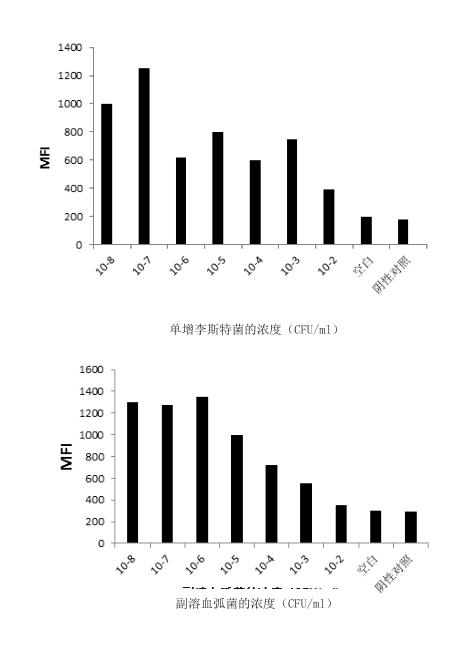
2.4 特异性的检测
用已建立的方法进行检测,从图4中可看出此方法特异性良好,与其它菌无交叉反应。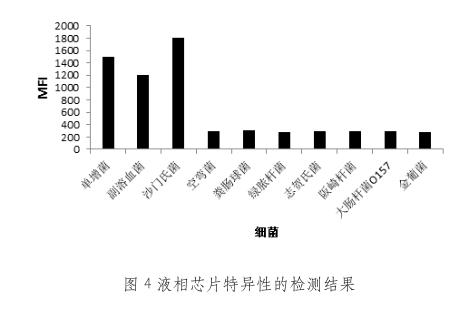
2.5 重复性试验
在1d、5d、7d用此方法分别检测阳性菌和阴性菌,由图5可见阳性菌,阴性菌MFI值上下浮动都不大,可证明本方法重复性较好。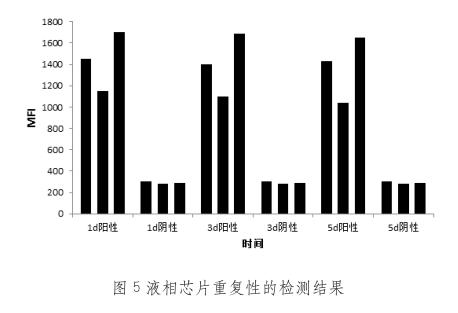
3 结论
2001年,美国FDA批准液相芯片技术可应用于临床诊断,这是唯一由美国FDA批准用于临床诊断的生物芯片技术。目前,液相芯片技术已应用于病原菌的检测、肿瘤标志物的检测、细胞因子检测、自身免疫性疾病诊断等方面。
国家标准方法检测食品中的病原微生物,需先对可疑样品增菌1~2d,然后接种于平板进行分离培养,之后再进行生化试验等进行鉴定,所需材料和试剂繁多,而且分型鉴定等需有经验的人员来完成;使用PCR检测病原体也存在一定缺陷,特别是在大量样本的检测中,单一PCR费时费力,而多重PCR体系尚不成熟,扩增背景高,灵敏度和特异性较低。
本实验建立了一种应用液相芯片技术检测单增李斯特菌、副溶血弧菌和沙门氏菌的方法。由于整个反应过程完全在液相环境中进行,故灵敏度较高,可达到103CFU/mL;该方法特异性好,检测选择的几种常见食源性致病菌,特异性可达100%。与传统方法相比,本方法耗时短,4h即可完成检测;需要样品量少,只需10 μL的菌液。
综上所述,本实验建立了一种快速检测单增李斯特菌、副溶血弧菌和沙门氏菌的液相芯片技术,其为一种优于传统检测方法的快速、准确、高通量的新型检测技术,在食品检验检疫方面具有广阔的开发前景。该方法的建立也为其他致病菌快速、高通量检测提供了参考。
参考文献:
[1] Tayel A A, Tras W F E. Anticandidal activity of pomegranate peel extract aerosol as an applicable sanitizing method[J]. Mycoses, 2010, 53(2):117-122.
[2] 聂萌.通用芯片技术检测和鉴定食源致病菌方法的研究[D].西北大学,2006.
[3] Schrenzel J. Clinical relevance of new diagnostic methods for bloodstream infections. Int. J. Anti.Agen, 2007, 30(Suppl.), 2-6.
[4] CDC health protection research guide 2006-2015 (2005).
[5] 邱杨,肖性龙,吴晖等.五种致病菌流式液相芯片检测方法的建立[J].现代食品科技,2010,26(8):889-893.
[6] 郭啟新,张蕾,张柏棋,等.液相基因芯片法同时检测3种食源性病原菌[J].食品科学,2013,34(16):191-195.
[7] Sun Z, Peng Y, Zhang M, et al. Simultaneous and highly sensitive detection of six different foodborne pathogens by high-throughput suspension array technology [J]. Food Contr.,2014,40(2):300-309.
浙江省医药卫生项目(项目号:2014C02023)。

