螺旋手性SWBNNT尺寸对Lys分子手性转变反应限域的影响
刘 戎, 佟 华, 王佐成, 佟海霞, 张雪婷, 张金猛
(1. 白城师范学院 化学学院, 吉林 白城 137000; 2. 白城师范学院 物理与电子信息学院, 吉林 白城 137000)
赖氨酸(lysine, Lys)是生命体中必须的氨基酸, 根据其构象和旋光性的不同, 分为左旋赖氨酸(S-Lys)与右旋赖氨酸(R-Lys)两种异构体. 在生命体内S-Lys具有活性, 是优构体;R-Lys无活性, 是劣构体.S-Lys对改善免疫系统、 降低甘油三酯及促进钙的吸收等具有重要作用, 也用于食品添加剂;R-Lys主要用于生物化学研究. 目前, 关于Lys的研究已有很多成果: 文献[1]研究了S-Lys在水溶液中的构象; 文献[2]研究了S-Lys与还原糖Maillard反应产物的理化特性及抗氧化活性; 文献[3-6]研究了裸环境、 MOR分子筛以及扶手椅型单壁碳纳米管限域环境下, 具有氨基和羧基间分子内双氢键的Lys分子手性转变机理. 研究表明: 以氨基N为质子迁移媒介进行旋光异构的反应通道具有绝对优势, 其裸反应的决速步骤Gibbs自由能垒为252.60 kJ/mol; MOR分子筛12元环孔道有限域催化作用, 可使优势通道上的决速步骤Gibbs自由能垒降为229.78 kJ/mol; 在SWCNT(5,5)内, 优势通道上的决速步骤Gibbs自由能垒降至192.81 kJ/mol. 纳米管材料分为碳材料和硼氮材料, 氮化硼纳米管有良好的耐高温性能. 计算表明, Lys分子有两种能量最低的构象. 基于此, 本文研究两种稳定构象的Lys分子限域在不同尺寸孔径的螺旋手性单壁氮化硼纳米管(SWBNNT)内, 以氨基N为质子迁移媒介进行旋光异构的机理.
1 模型的选取与计算研究方法
Lys分子的线度为0.794 7 nm×0.383 1 nm, 取限域环境为SWBNNT(6,4),SWBNNT(7,4)和SWBNNT(8,4), 其孔径分别为0.677 7,0.749 7,0.822 7 nm. 计算表明: 当管径小于0.677 7 nm时, Lys分子与纳米管为化学吸附; 当管径大于0.822 7 nm时, 已不存在限域效应, 故选取这3种模型为纳米限域环境. 为充分考虑孔道的限域效应, 截取的纳米管长度约为2.15 nm, 用H原子饱和模型截断处的N原子.
采用QM/MM组合的ONIOM(our ownn-layered integrated molecule orbit and molecule mechanics)方法[7]研究螺旋手性SWBNNT尺寸对Lys分子手性转变反应限域的影响. 将纳米管与反应底物分子包结物分为两层: 底物分子设为高层QM区, 考虑到底物分子与纳米管间的长程作用, 用CAM(Coulomb-attenuated hybrid exchange-correlation functional)结合密度泛函理论(DFT)的长程校正泛函CAM-B3LYP[8-9]方法, 采用6-31+G(d,p)基组; 纳米管设为低层MM区, 采用分子力学的UFF(universal force field)力场[10]处理, 优化稳定点和过渡态[11-12]. 为得到相对高水平的反应势能面, QM区采用微扰理论的MP2方法[13-14], 在ONIOM(MP2/6-311++G(2df,pd): UFF)理论水平计算各包结物的单点能, 利用Gtotal=Gtc+ESP计算总Gibbs自由能. 其中Gtc和ESP分别为Gibbs自由能热校正和单点能. 通过对过渡态进行内禀反应坐标(IRC)计算[14], 对过渡态的可靠性进行确认. 左旋Lys分子构型1记为S-Lys_1, 其限域在SWBNNT(6,4)内的包结物记为S-Lys_1@SWBNNT(6,4), 其他体系表示方法类似. 计算均利用Gaussian 09软件[15]完成.
2 结果与讨论
文献[16]研究表明, 氨基酸的羧基与氨基间为单氢键和双氢键时氨基酸分子构型最稳定. 基于此, 在B3LYP/6-31+G(d,p)水平优化得到两种S-Lys分子构象和一种R-Lys_1分子构象, 如图1所示. 计算表明,S-Lys_1比S-Lys_2的能量低2.86 kJ/mol,S-Lys_1的构象相对更稳定. 结构分析表明:S-Lys_1具有羧基与氨基间的单氢键,S-Lys_2具有羧基与氨基间的双氢键. 不同构象的S-Lys分子限域在相同孔径纳米管内的旋光异构机理不同, 相同构象的S-Lys分子限域在不同孔径纳米管内的旋光异构机理也不同, 下面分别进行讨论.
2.1 S-Lys分子限域在SWBNNT(6,4)内的手性转变机理
2.1.1S-Lys_1S-Lys_1限域在SWBNNT(6,4)内的旋光异构反应过程如图2所示, 反应过程的Gibbs自由能曲线如图3所示.

图1 S型与R型Lys分子的几何结构Fig.1 Geometries of S- and R-type Lys molecules

图3 S-Lys_1限域在纳米管内手性转变反应的Gibbs自由能曲线Fig.3 Gibbs free energy curves of S-Lys_1 chiral transition reaction confined in nanotube
1) 反应物包结物S-Lys_1@SWBNNT(6,4)经过渡态包结物S-TS1_1@SWBNNT(6,4), 异构成第一中间体产物包结物S-INT1_1@SWBNNT(6,4). 在该基元反应过程中, 羧基的11H绕8C—9O键轴旋从羧基外侧旋转至内侧, 二面角11H-9O-8H-10O从-165.84°变为1.08°, 羧基从反式平面结构向顺式平面结构异构. 同时, 氨基团的6H和7H绕1C—5N键轴沿俯视顺时针旋转, 二面角6H-5N-1C-12H从-49.51°变为-131.15°, 5N有孤对电子的一面朝纸外, 负电荷增多, 其正面获得质子的能力显著增强. 从S-Lys_1@SWBNNT(6,4)到S-TS1_1@SWBNNT(6,4)过程, 二面角11H-9O-8H-10O从-165.84°变为126.42°, 二面角6H-5N-1C-12H从-49.51°变为-130.52°, 该基元反应为羟基和氨基协同非同步旋转机理. 其中心骨架二面角5N-1C-3C-8C和1C-8C-10O-9O分别从121.85°和-163.85°变为129.53°和-159.22°. 该过程主要是两个二面角旋转异构, 骨架结构形变很小, 所需能量较小, 过渡态S-TS1_1@SWBNNT(6,4)产生的能垒为54.22 kJ/mol.S-INT1_1@SWBNNT(6,4)相对于S-Lys_1@SWBNNT(6,4)的能量为-38.1 kJ/mol, 该基元反应为放热反应.S-INT1_1@SWBNNT(6,4)相对于S-Lys_1@SWBNNT(6,4)的能量显著下降, 主要原因是S-INT1_1@SWBNNT(6,4)体系的偶极矩(1.54)比S-Lys_1@SWBNNT(6,4)体系的偶极矩(7.72)小很多, 前者电荷分离的程度小, 体系稳定.
2) 包结物S-INT1_1@SWBNNT(6,4)经过渡态包结物TS2_1@SWBNNT(6,4), 实现12H从手性碳(1C)向氨基氮(5N)的迁移, 异构成第二中间体包结物INT2_1@SWBNNT(6,4). 从S-INT1_1@SWBNNT(6,4)到TS2_1@SWBNNT(6,4)过程中, 1C—12H键长从0.105 61 nm增至0.127 79 nm, 键断裂, 伸长量为0.022 18 nm; 1C—5N键长从0.138 66 nm增至0.148 79 nm, 伸长量为0.010 13 nm; 反应活性中心骨架二面角5N-1C-3C-8C从125.26°变为129.26°, 增加了4.00°, 形变很小. 在该过程中, 一个化学键断裂, 一个化学键伸长, 需要较高的能量, 过渡态TS2_1@SWBNNT(6,4)产生的能垒为211.40 kJ/mol. 远低于裸反应的252.60 kJ/mol[10], 这是由于SWBNNT(6,4)的限域作用使S-Lys_1,S-INT1_1和TS2_1产生了较大形变, 使该基元反应1C—12H和1C—5N的伸长量以及反应活性中心骨架的形变远小于裸反应[10]所致, 表明SWBNNT(6,4)的限域催化作用十分明显.
3) INT2_1@SWBNNT(6,4)经过渡态TS3_1@SWBNNT(6,4), 实现了6H从5N向1C在纸面内迁移, 异构成产物包结物P_R-Lys_1@SWBNNT(6,4), 实现手性转变. 从INT2_1@SWBNNT(6,4)到TS3_1@SWBNNT(6,4)过程, 5N—6H键长从0.100 01 nm增至0.118 03 nm, 键断裂; 1C—5N键长从0.141 38 nm增至0.147 33 nm; 活性中心骨架形变不明显. 该过程仅5N—6H键拉长断裂, 因此TS3_1@SWBNNT(6,4)远小于TS2_1@SWBNNT(6,4)产生的能垒, 为92.59 kJ/mol.
由图3可见, 整个反应为放热过程, 释放的热量为43.95 kJ/mol. 这是由于产物包结物体系P_R-Lys_1@SWBNNT(6,4)的偶极矩(2.80)远小于反应物S-Lys_1@SWBNNT(6,4)体系的偶极矩(7.72), 电荷分离程度小, 体系稳定.
2.1.2S-Lys_2S-Lys_2限域在SWBNNT(6,4)内的旋光异构反应过程如图4所示, 反应过程的Gibbs自由能曲线如图5所示.
1)S-Lys_2@SWBNNT(6,4)经12H从1C向5N迁移与7H从5N向9O协同非同步迁移的过渡态TS1_2@SWBNNT(6,4), 异构成中间体产物包结物INT1_2@SWBNNT(6,4). 该过程中, 1C—12H键长从0.105 71 nm增至0.124 47 nm, 键断裂; 1C—5N键长从0.138 75 nm增至0.148 52 nm; 5N—7H键长从0.099 72 nm增至0.102 54 nm; 反应活性中心二面角5N-1C-3C-8C从117.23°变为121.80°. 比从S-INT1_1@SWBNNT(6,4)到TS2_1@SWBNNT(6,4)过程多了5N—7H键增长过程, 因此, TS1_2@SWBNNT(6,4)高于TS2_1@SWBNNT(6,4)产生的內禀能垒, 为230.44 kJ/mol. TS1_2@SWBNNT(6,4)可视为前过渡态, 这是由于TS1_2@SWBNNT(6,4)的5N—7H(0.102 54 nm)与INT1_2@SWBNNT(6,4)的5N—7H(0.160 08 nm)距离相差较远所致. 该基元反应为质子从1C迁移至羟基上, 使体系电荷分离, 导致INT1_2@SWBNNT(6,4)体系能量升高; INT1_2@SWBNNT(6,4)的1C具有获得质子的能力, 同时质子化的羧基容易失去质子, 这也使INT1_2@SWBNNT(6,4)体系的能量升高. 因此, INT1_2@SWBNNT(6,4)体系不稳定, 在势能面较高的位置.

图4 S-Lys_2限域在SWBNNT(6,4)内的手性转变反应过程Fig.4 Chiral transition process of S-Lys_2 confined in SWBNNT(6,4)

图5 S-Lys_2限域在纳米管内手性转变反应的Gibbs自由能曲线Fig.5 Gibbs free energy curves of S-Lys_2 chiral transition reaction confined in nanotube
2) INT1_2@SWBNNT(6,4)经与TS1_2@SWBNNT(6,4)准对称的过渡态TS2_2@SWBNNT(6,4), 实现了7H从9O向5N和6H从5N在纸面内向1C协同非同步的双质子迁移过程, 异构成产物包结物P_R-Lys_2@SWBNNT(6,4), 完成旋光异构. 从INT1_2@SWBNNT(6,4)到TS2_2@SWBNNT(6,4)过程, 类似于INT2_1@SWBNNT(6,4)到TS3_1@SWBNNT(6,4)过程, 但多了7H从9O向5N的质子迁移过程, 是双质子协同非同步迁移, TS2_2@SWBNNT(6,4)高于TS3_1@SWBNNT(6,4)产生的能垒, 为110.14 kJ/mol. 由图5可见, 整个反应为吸热过程, 吸收热量为19.85 kJ/mol.
2.2 S-Lys分子限域在SWBNNT(7,4)和SWBNNT(8,4)内的手性转变反应机理
S-Lys分子限域在SWBNNT(7,4)和SWBNNT(8,4)内的反应过程相同, 因此仅给出S-Lys_1和S-Lys_2分子限域在SWBNNT(7,4)内的反应过程, 分别如图6和图7所示, 其Gibbs势能曲线分别如图3和图5所示.
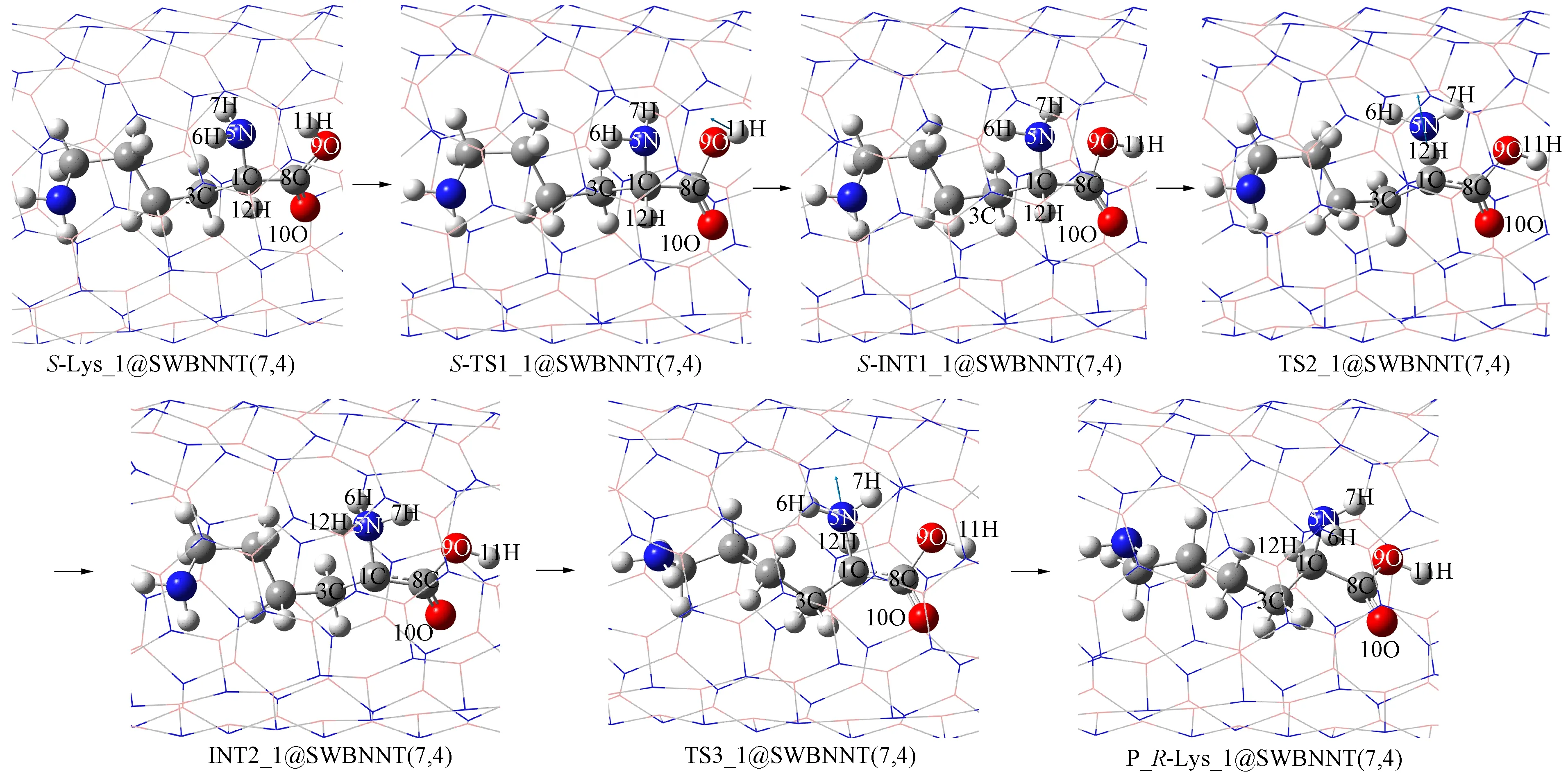
图6 S-Lys_1限域在SWBNNT(7,4)内的手性转变反应过程Fig.6 Chiral transition process of S-Lys_1 confined in SWBNNT(7,4)

图7 S-Lys_2限域在SWBNNT(7,4)内的手性转变反应过程Fig.7 Chiral transition process of S-Lys_2 confined in SWBNNT(7,4)
2.2.1S-Lys_1S-Lys_1限域在SWBNNT(7,4)和SWBNNT(6,4)内的旋光异构机理类似, 仅由于纳米管尺寸增加, 限域影响减小, 因此基元反应的能垒不同. 首先,S-Lys_1@SWBNNT(7,4)经过渡态S-TS1_1@SWBNNT(7,4), 异构成中间体S-INT1_1@SWBNNT(7,4), 完成羧基从反式平面结构向顺式平面结构的异构. 该过程为羟基旋转同时伴随氨基旋转, 反应能垒为35.79 kJ/mol. 其次,S-INT1_1@SWBNNT(7,4)经过渡态TS2_1@SWBNNT(7,4)异构成中间体INT2_1@SWBNNT(7,4). 从S-INT1_1@SWBNNT(7,4)到TS2_1@SWBNNT(7,4)过程, 1C—12H键长从0.107 85 nm增至0.132 70 nm, 增加了0.024 85 nm; 1C—5N键长从0.141 32 nm增至0.152 14 nm, 增加了0.010 82 nm; 反应中心骨架二面角5N-1C-3C-8C从129.20°变为135.89°, 增加了6.69°. 对应的参数变化均大于S-INT1_1@SWBNNT(6,4)到TS2_1@SWBNNT(6,4)过程的参数变化. 因此, TS2_1@SWBNNT(7,4)大于TS2_1@SWBNNT(6,4)产生的能垒, 为248.26 kJ/mol, 小于裸反应能垒252.60 kJ/mol, 即仍存在限域催化作用. 最后, 中间体INT2_1@SWBNNT(7,4)经与TS3_1@SWBNNT(6,4)相似的过渡态TS3_1@SWBNNT(7,4), 实现了质子12H在纸面内向1C的迁移, 异构成产物P_R-Lys_1@SWBNNT(7,4), 实现了手性转变. 该基元反应能垒为102.29 kJ/mol.
S-Lys_1限域在SWBNNT(8,4)和SWBNNT(6,4)内的旋光异构机理类似: 在第一基元反应中, 羧基和氨基协同旋转的过渡态TS1_1@SWBNNT(8,4)产生的能垒为45.26 kJ/mol; 在第二基元反应中, 质子6H从1C向5N迁移的过渡态TS2_1@SWBNNT(8,4)产生的能垒为262.19 kJ/mol, 略高于裸反应的能垒252.60 kJ/mol; 在第三基元反应中, 质子6H在纸面内从5N向1C迁移的过渡态TS3_1@SWBNNT(8,4)产生的能垒为126.42 kJ/mol. 整个反应的总能垒为292.19 kJ/mol, 远高于裸反应与限域在SWBNNT(6,4)和SWBNNT(7,4)的情形. 表明较大孔径的螺手性SWBNNT可抑制Lys分子的消旋化, 光学纯的Lys分子对氮化硼纳米管可手性识别.
2.2.2S-Lys_2S-Lys_2限域在SWBNNT(7,4)和SWBNNT(6,4)内旋光异构的情形不同, 质子迁移仅为质子在1C和5N间的单质子迁移过程. 这是由于SWBNNT(7,4)小于SWBNNT(6,4)的极性, SWBNNT(7,4)的极化和羟基氧9O电性力的共同作用未使质子7H脱离氨基氮向羰基氧迁移所致. 首先, 反应包结物S-Lys_2@SWBNNT(7,4)经过渡态TS1_2@SWBNNT(7,4), 实现了12H从1C向5N的迁移, 异构成中间体产物包结物INT1_2@SWBNNT(7,4), INT1_2的氨基是质子化的. 结构分析表明, 从S-Lys_2@SWBNNT(7,4)到TS1_2@SWBNNT(7,4)过程, 反应活性中心几何参数的变化大于S-Lys_2@SWBNNT(6,4)到TS1_2@SWBNNT(6,4)过程, 所需越过的能垒为249.37 kJ/mol, 接近裸反应能垒252.6 kJ/mol, 几乎不存在限域催化作用. 其次, INT1_2@SWBNNT(7,4)经与TS1_2@SWBNNT(7,4)准对称的过渡态TS2_2@SWBNNT(7,4), 异构成产物包结物P_R-Lys_2@SWBNNT(7,4), 实现了6N在纸面内向1C的迁移, 完成旋光异构. 该基元反应能垒为128.63 kJ/mol.
S-Lys_2分子限域在SWBNNT(8,4)和SWBNNT(7,4)内的手性转变机理类似. 反应包结物S-Lys_2@SWBNNT(8,4)经过渡态TS1_2@SWBNNT(8,4), 实现了质子12H从1C向5N的迁移, 异构成中间体产物包结物INT1_2@SWBNNT(8,4). 该基元反应从S-Lys_2@SWBNNT(8,4)到TS1_2@SWBNNT(8,4)过程中, 1C—12H键长、 1C—5N键长与反应活性中心骨架二面角5N-1C-3C-8C增加, 均大于S-INT1_2@SWBNNT(7,4)到TS2_2@SWBNNT(7,4)过程. TS2_2@SWBNNT(8,4)产生的能垒为260.30 kJ/mol, 表明SWBNNT(8,4)的限域催化作用已消失. 该能垒略高于裸反应能垒252.60 kJ/mol, 可能是计算方法导致的误差或SWBNNT(8,4)限域效应已不存在, 但将SWBNNT视为无极性的溶剂, 由于Lys是有极性的氨基酸, 因此溶剂效应对该反应有阻碍作用.
由图3和图5可见, 随着螺旋手性SWBNNT管径的增加, 其对Lys分子旋光异构的限域催化作用逐渐减弱.S-Lys_1和S-Lys_2限域在SWBNNT(6,4)内实现手性转变的表观能垒分别为175.90,230.44 kJ/mol, 即S-Lys_1在SWBNNT(6,4)内相对容易进行旋光异构.S-Lys_1在SWBNNT(6,4)内旋光异构的决速步骤为第二基元反应, 决速步骤内禀自由能垒为211.40 kJ/mol;S-Lys_2在SWBNNT(6,4)内旋光异构的决速步骤为第一基元反应, 决速步骤内禀自由能垒与表观能垒均为230.44 kJ/mol.S-TS1_1@SWBNNT(6,4)产生的能垒升高, 这是由于S-Lys_1在SWBNNT(6,4),SWBNNT(7,4),SWBNNT(8,4)内8C—9O键长分别为0.131 5,0.133 1, 0.133 6 nm, 在SWBNNT(6,4)内的键长最短, 化学键强, 导致羧基的11H绕8C—9O键轴旋转困难, 所需能垒较高, 此时限域催化作用较小.
综上所述, 结构分析表明: 限域在小管径螺旋手性SWBNNT内的Lys分子骨架形变明显. 随着螺旋手性SWBNNT管径的增加, 其对Lys分子旋光异构的限域催化作用逐渐减弱, 较大孔径的螺旋手性SWBNNT可抑制Lys分子消旋, 光学纯的Lys分子对螺旋手性氮化硼纳米管存在手性识别.
[1] 王建军, 王晓春, 欧阳一山, 等. 用镧系位移试剂研究L-赖氨酸在水溶液中的结构 [J]. 物理化学学报, 1992, 8(7): 647-653. (WANG Jianjun, WANG Xiaochun, OUYANG Yishan, et al. The Solution Structure Studies ofL-Lysine by Means of NMR Lanthanide Shift Reagent [J]. Acta Physico-Chimica Sinica, 1992, 8(7): 647-653.)
[2] 李菁, 刘骞, 孔保华, 等.L-赖氨酸与3种还原糖美拉德反应产物的理化特性及抗氧化活性研究 [J]. 食品科学, 2013, 34(3): 80-85. (LI Jing, LIU Qian, KONG Baohua, et al. Physico-Chemical Properties and Antioxidant Activity of Maillard Reaction Products fromL-Lysine and Reducing Sugar Model System [J]. Food Science, 2013, 34(3): 80-85.)
[3] 刘凤阁, 辛春雨, 闫红彦, 等. 气相赖氨酸分子手性转变机制的理论研究 [J]. 武汉大学学报(理学版), 2015, 61(1): 93-98. (LIU Fengge, XIN Chunyu, YAN Hongyan, et al. Theoretical Research on Chiral Change Mechanism of Gaseous Lysine Molecules [J]. Journal of Wuhan University (Natural Science Edition), 2015, 61(1): 93-98.)
[4] 王晓玲, 高峰, 佟华, 等. 基于氨基作为质子转移桥梁的赖氨酸分子手性转变机理 [J]. 吉林大学学报(理学版), 2016, 54(5): 1161-1167. (WANG Xiaoling, GAO Feng, TONG Hua, et al. Chiral Transition Mechanism of Lysine Molecules Based on Amino as Proton Transfer Bridge [J]. Journal of Jilin University (Science Edition), 2016, 54(5): 1161-1167.)
[5] 闫红彦, 赵晓波, 高峰, 等. MOR分子筛对赖氨酸分子手性转变反应的限域催化 [J]. 吉林大学学报(理学版), 2016, 54(6): 1437-1444. (YAN Hongyan, ZHAO Xiaobo, GAO Feng, et al. Confined Catalysis of the MOR Molecular Siere on Chiral Transition Reaction of Lysine Molecule [J]. Journal of Jilin University (Science Edition), 2016, 54(6): 1437-1444.)
[6] 闫红彦, 王佐成, 刘逸轩, 等. 扶手椅型单壁碳纳米管的尺寸对赖氨酸分子手性转变反应的限域影响 [J]. 复旦学报(自然科学学版), 2017, 56(1): 124-134. (YAN Hongyan, WANG Zuocheng, LIU Yixuan, et al. The Confined Effect of the Size of Armchair Single-Walled Carbon Nanotubes on the Chiral Transition of Lysine Molecules [J]. Journal of Fudan University (Natural Science), 2017, 56(1): 124-134.)
[7] Svensson M, Humbel S, Froese R D J, et al. ONIOM: A Multilayered Integrated MO+MM Method for Geometry Optimizations and Single Point Energy Predictions. A Test for Diels-Alder Reactions and Pt(P(t-Bu)3)2+H2Oxidtivae Addition [J]. Physical Chemistry, 1996, 100(70): 19357-19363.
[8] Kobayashi R, Amos R D. Erratum to ‘the Application of CAM-B3LYP to the Charge-Transfer Band Problem of the Zincbacteriochlorin-Bacteriochlorin Complex’ [J]. Chem Phys Letts, 2006, 420: 106-109.
[9] YIN Shiwei, Dahlbom M G, Canfield P J, et al. Assignment of the Qy Absorption Spectrum of Photosystem-Ⅰ from Thermosynechococcus Elongatus Based on CAM-B3LYP Calculatins at the PW91-Optimized Protein Structure [J]. Phys Chem B, 2007, 111(33): 9923-9930.
[10] Rappe A K, Casewit C J, Colwell K S, et al. UFF, a Full Periodic Table Force Field for Molecular Mechanics and Molecular Dynamics Simulations [J]. Journal of the American Chemical Society, 1992, 114(25): 10024-10035.
[11] Garrett B C, Truhlar D G. Generalized Transition State Theory. Classical Mechanical Theory and Applications to Collinear Reactions of Hydrogen Molecules [J]. Journal of Physical Chemistry, 1979, 83(8): 1052-1079.
[12] Garrett B C, Truhlar D G. Criterion of Minimum State Density in the Transition State Theory of Bimolecular Reactions [J]. The Journal of Chemical Physics, 1979, 70(4): 1793-1798.
[13] 徐光宪, 黎乐民, 王德民. 量子化学: 中册 [M]. 北京: 科学技术出版社, 1987: 962-986. (XU Guangxian, LI Lemin, WANG Demin. Quantum Chemistry: Middle [M]. Beijing: Science Press, 1987: 962-986.)
[14] Ishida K, Morokuma K, Komornicki A. The Intrinsic Reaction Coordinate. AnabinitioCalculation for HNC→HCN and H-+CH4→CH4+H-*[J]. The Journal of Chemical Physics, 1977, 66(5): 2153-2156.
[15] Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 09. Revision E.01 [CP/CD]. Pittsburgh, PA: Gaussian Inc, 2013.
[16] 黄志坚. 氨基酸的构型和性质研究 [D]. 合肥: 中国科学技术大学, 2006: 11. (HUANG Zhijian. Structures and Properties of the Amino Acids [D]. Hefei: University of Science and Technology of China, 2006: 11.)

