维生素E对PM2.5急性染毒致大鼠心血管损伤的保护作用
李莉珊 马琼锦 刘洁等
摘要:目的 探讨维生素E(VE)对PM2.5急性染毒致大鼠心血管损伤的干预作用。方法 将36只雄性sD大鼠随机分为玉米油对照组(溶剂对照组)、VE对照组、PM2.5染毒组(8.0 mg/kg,以体重计,下同)、PM2.5+VE低、中、高给药组,剂量分别为15.0、30.0、60.0 mg/kg。VE给药组均经VE灌胃28 d后,气管滴注PM2.5悬浊液染毒,隔天1次,共3次。末次染毒24 h后,腹主动脉取血,分析测定血清中白细胞介素1-β(IL-1B)、白细胞介素6(IL-6)、肿瘤坏死因子α(TNF-ot)、超敏C反应蛋白(HS-CRP);谷胱甘肽(GSH)、谷胱甘肽过氧化物酶(GSH-Px)、丙二醛(MDA)、总超氧化物歧化酶(T-SOD)、血清一氧化氮(NO)、内皮素1(ET-1)和心肌缝隙连接蛋白(Cx43)的含量。结果溶剂对照组IL-1B、IL-6、TNF-a、HS-CRP、GSH、GSH-Px、MDA、T-SOD、NO、ET-1及Cx43分别为(68.73±6.21)μg/L、(15.86+0.45)μg/L、(41.12±7.66)μg/L、(1.29±0.26)μg/L、(15.30±2.52)μmol/L、(492.29±28.28)、(10.19±0.74)μmol/L、(272.98±8.59)U/mL,(3.22±0.22)μmol/L、(0.28±0.021)μg/L、(0.42±0.04)μg/L。PM2 5染毒组IL-1 B[(1 155.98±100.28)μg/L]、IL-6[(24.94±2.06)μg/L]、TNF-α[(821.45±14.26)μg/L]、HS-CRP[(3.10±0.28)μg/L]、MDA[(15.88±1.41)μmol/L]和ET-1[(0.38±0.03)μg/L]的释放量升高,GSH[(4.62±0.37)μmol/L]、GSH-Px[(289.28±30.65)]、NO[(0.97±0.074)tLmol/L]、Cx43[(0.26±0.10)μg/L和T-SOD[(239.26±4.97)U/mL]含量降低,差异有统计学意义(P<0.05);与PM2.5染毒组相比,VE给药组的各项指标均有一定缓解作用,差异均有统计学意义(P<0.05),且存在一定的剂量反应关系。
结论急性PM2,染毒可引起大鼠心血管损伤,导致炎性因子、氧化应激指标、血管内皮功能和心肌缝隙链接蛋白的变化,而VE喂饲对PM2,引起的大鼠急性肺部损伤具有一定的保护作用。
关键词:维生素E;大气细颗粒物;气管滴注;血清;心血管损伤 中图分类号:R144 文献标志码:A
大气颗粒物是我国城市空气中的主要污染物之一。直径≤2.5μm的细颗粒物(PM2.5)在大气颗粒物中约占70%。随着对大气颗粒物研究的深入,越来越多的研究表明,粒径≤10μm的颗粒物是大气颗粒物中对环境和人体健康危害最大的一类。随着工业的发展和机动车数量的增加,大气中颗粒物污染越来越严重,如果长期吸入颗粒物污染的空气,将严重危害人类健康。Pope等研究显示,环境污染导致的心血管疾病中,死亡率上升的主要有缺血性心肌病、心律失常、心力衰竭和心脏骤停。颗粒物质作用的主要机制包括炎症反应、动脉粥样硬化及自主神经功能紊乱,而动脉粥样硬化是心血管系统中最常见的疾病,是众多心脑血管疾病共同的病理基础。PM诱导的炎性因子可以作用于血管内皮细胞,导致内皮功能障碍,从而加速动脉粥样硬化进展,这可能是颗粒物质和心血管事件联系的基础。维生素E(VE)是人体内具有广泛生理功能的脂溶性维生素,也是一种有效的抗氧化剂和免疫调节剂。研究证明,它能够有效地减少心血管病的发病率,对克山病、缺血再灌注损伤均有疗效,能够保护机体组织结构的完整性,促进机体正常的免疫和生殖功能,并在生命发育过程中起非常重要的作用。本研究探讨VE对PM2.5引起的心血管损伤的干预作用,观察其对心血管炎症反应、氧化应激损伤和内皮功能损伤的缓解作用。
1材料与方法
1.1主要仪器与试剂
Thermo Anderson G-2.5大流量采样器为美国热力公司产品,冷冻真空干燥/LGJ-10D由北京四环科学仪器有限公司提供,超声波清洗机/JL-180H为南京科捷分析仪器有限公司产品,MK3型酶联免疫检测仪为广州DENLEY公司产品,紫外可见分光光度计型号为UV-1600。VE为上海铭睿生物科技有限公司产品,纯度≥98%,白细胞介素1-β(interleukin 1-beta,IL-1β)、白细胞介素6(in-terleukin 6,IL-6)、肿瘤坏死因子仅(tumor necrosisfactor alpha,TNF-α)和超敏C反应蛋白(high sensi-tive C-reaction protein,HS-CRP)试剂盒均为美国eBioscience公司产品,谷胱甘肽(glutathione,GSH)、谷胱甘肽过氧化物酶(glutathione peroxi-dase,GSH-Px)、丙二醛(malondialdehyde,MDA)内皮功能指标(NO、endothelin-1)、心肌缝隙连接蛋白(Cx43)和总超氧化物歧化酶(superoxide dis-mutase,T-SOD)测定试剂盒均由南京建成生物工程研究所提供。
1.2 PM2.5采集與悬浊液制备
2013年9月—2014年3月,在上海市徐汇区某高校建筑物楼顶(高10 m左右,周围没有明显的工业污染源),利用大流量采样器采集大气PM2.5。采样完成后,将滤膜折叠放在干燥器内备用。将载有细颗粒物的玻璃纤维滤膜剪成长条,浸没于双蒸水中,超声震荡,洗脱颗粒物。纱布过滤,收集滤液,冷冻真空干燥,4℃保存备用。染毒前,用无菌生理盐水配制成相应浓度的悬浊液,超声震荡混匀。
1.3 PM2.5染毒剂量的确定
动物染毒剂量组的设置需考虑多种综合因素,包括大鼠每天的通气量(0.80 L/kg,以体重计,下同),大气PM2.5在肺部的沉积率(7%左右),同时参考美国大气颗粒物质量标准(日均浓度不超过65μg/m3),计算得出每日大鼠沉积在肺部的PM2.5浓度为16μg/kg[(0.07×0.8L/(kg·min)×60 min×24 h×3次×65μg/m3×0.001≈16μg/kg)]。通过实验发现,由于人体与动物之间的换算有不确定系数,乘以100,得到动物实验的最低剂量为1.6mg/kg。通过预实验发现,2.5滴注剂量为8.0 mg/kg预期效果较佳。
1.4动物实验
选取6周龄SPF级雄性SD大鼠36只(180~200 g,购买于上海西普尔-必凯实验动物有限公司,合格证号:2008001631780;饲养在SPF级动物房,温度控制在22~26℃,相对湿度40%~70%),随机分为6组,每组6只,分笼饲养。分别标记为溶剂对照组(玉米油对照组),PM2.5染毒组,VE高剂量对照组和PM2.5+VE低、中、高给药组。VE给药组首先进行28 d VE灌胃,灌胃剂量分别为15.0、30.0、60.0 mg/kg,以体重计;然后进行大鼠气管滴注细颗粒物悬浊液,隔天1次共3次,滴注量为8.0 mg/kg(滴注期间同时给予VE)。溶剂对照组仅进行玉米油灌胃35 d,PM2.5染毒组则先正常饲养28 d,再进行气管滴注PM2.5染毒1周。最后一次染毒24 h后,使用10%水合氯醛(0.30mL/kg)麻醉,打开腹腔,腹主动脉取血,37℃温浴,3000转/min冷冻离心20 min(离心半径为7cm),再取上清液进行分析。
1.5指标测定
严格按照测试盒说明进行各项指标测定,包括炎性损伤指标(IL-1β、IL-6、TNF-α、HS-CRP),氧化应激指标(MDA、T-SOD、GSH、GSH-Px),内皮功能指标(NO、Endothelin-1)和Cx43。其中,细胞因子试剂盒购买于eBioscience公司,其他指标试剂盒均由南京建成生物工程研究所提供。高剂量药物对照组用于检验药物的安全性,单纯的高剂量药物不会引起动物的不适或者各项指标的异常。
1.6统计学分析
采用Excel 2003建立数据库,数据用x±s表示。用SPSS 16.0软件进行统计分析。用单因素方差分析进行PM2.5与各实验组的比较,LSD检验进行实验组之间的比较。Levene检验进行两独立样本间的方差齐性检验。检验水准α=0.05。
2结果
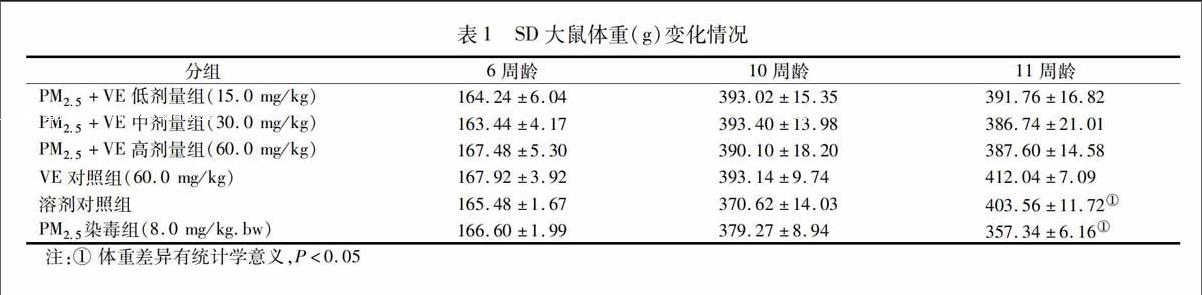
2.1大鼠体重变化
未进行PM2.5染毒之前,各组大鼠体重均呈上升趋势,且皮毛光泽度较高。PM2.5染毒后,染毒组大鼠的皮毛光泽度下降,呼吸有哮鸣音;PM2.5+VE给药组的大鼠体重变化不大,而PM2.5染毒组体重下降。PM2.5染毒组与溶剂对照组相比,末次体重测定差异有统计学意义(P<0.05),提示PM2.5可能具有损伤作用。见表1。
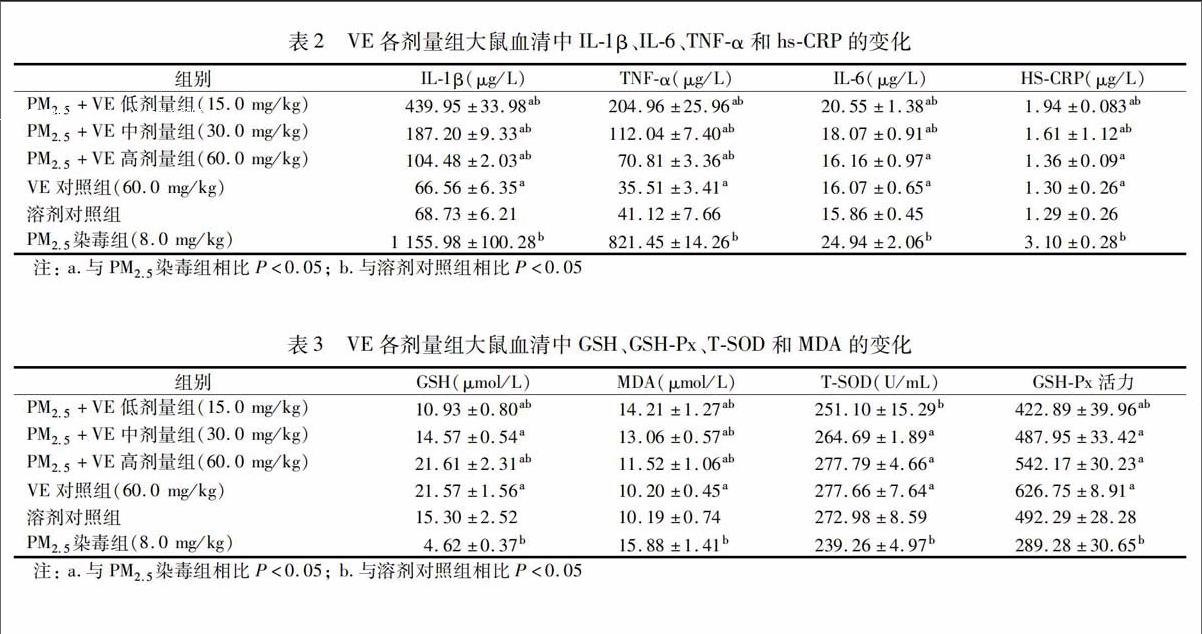
2.2大鼠心血管炎性损伤指标的变化
通过对血清中IL-1B、IL-6、TNF-α和hs-CRP的测试,观察各组动物炎性损伤的变化情况。与溶剂对照组相比,PM2.5染毒组的IL-6、TNF-α、IL-1β和hs-CRP含量均较高,且差异有统计学意义(P<0.05);PM2.5+VE各组指标中,除了高剂量组IL-6和hs-CRP外,其他各组指标值差异均有统计学意义(P<0.05)。与PM2.5染毒组相比,各组IL-1β、IL-6、TNF-α和hs-CRP指标值均降低,差异均有统计学意义(P<0.05),且各指标值在PM2.5+VE给药组中存在一定的剂量反应关系。VE高剂量对照组与溶剂对照组相比,各指标值差异均无统计学意义(P>0.05)。见表2。
2.3大鼠心血管氧化应激损伤指标的变化
通过对GSH、GSH-Px、T-SOD和MDA指标的测定,观察氧化应激损伤的情况。与溶剂对照组相比,PM2.5染毒组的各指标值差异均有统计学意义(P<0.05);PM2.5+VE中、高剂量给药组的T—SOD和GSH-Px指标差异无统计学意义,中剂量给药组的GSH含量差异无统计学意义,其他各组指标差异均有统计学意义。与PM2.5染毒组相比,除PM2.5+VE低剂量给药组的T-SOD含量差异无统计学意义外(P>0.05),其他各组的指标值差异有统计学意义(P<0.05),且存在一定的剂量反应关系。VE高剂量对照组和溶剂对照组相比,除MDA外,其他指标值差异均有统计学意义(P<0.05)。见表3。
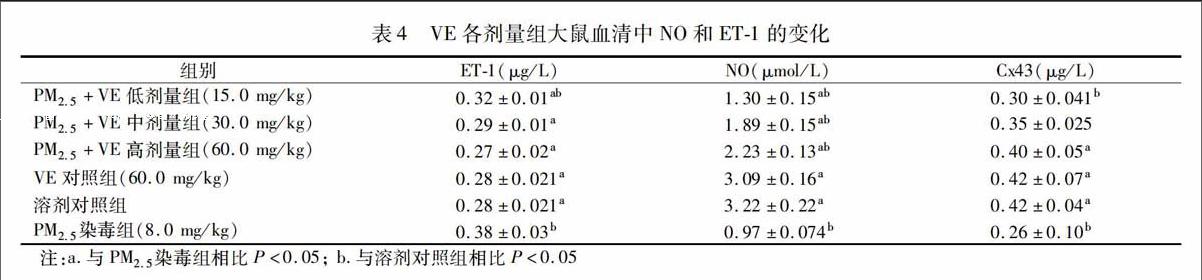
2.4大鼠内皮功能损伤指标的变化
通过对NO和ET-指标的测定,观察VE对PM2.5引起大鼠血管内皮功能损伤情况的影响。与溶剂对照组相比,PM2.5染毒组的各指标值差异均有统计学意义;PM2.5+VE中、高劑量给药组的ET-1含量差异无统计学意义(P>0.05),低剂量给药组的ET-1含量和各给药组NO含量差异有统计学意义(P<0.05),且NO含量在VE给药组中存在剂量反应趋势;VE高剂量对照组NO和ET-1含量差异均无统计学意义(P>0.05)。与PM2.5染毒组相比,PM2.5+VE各组ET-1含量降低,NO含量升高,差异有统计学意义(P<0.05),且在VE给药组中存在剂量反应关系。
通过对大鼠Cx43含量变化的测定,观察各组大鼠发生心率失常的情况。与溶剂对照组相比,PM2.5染毒组的Cx43含量较低,差异有统计学意义;Cx43含量在PM2.5+VE低剂量给药组中差异有统计学意义(P<0.05),中、高剂量给药组的含量差异无统计学意义(P>0.05)。与PM2.5染毒组相比,Cx43含量与VE低、中给药组中的含量差异无统计学意义(P>0.05),其他各组的含量差有统计学意义(P<0.05)。VE高剂量对照组与溶剂对照组相比,Cx43含量差异无统计学意义(P>0.05)。见表4。
3讨论
颗粒物质是一种复杂的混合物,对健康影响的性质和程度除了与其颗径大小有关,还与其来源及其表面所吸附的化学物和生物病原体有关。研究表明,急性暴露于细颗粒物的水溶性组分,可以改变离子运输通道的表达及血管内皮通透性,水溶性过渡金属也可引起血管内皮细胞功能障碍,导致内皮细胞功能衰减和死亡。有研究显示,PM2.5中的有机成分可作用于大鼠心血管内皮细胞,通过改变血管内皮细胞的功能而与心血管疾病高度相关。PM诱导的炎性因子也可以作用于血管内皮细胞,导致内皮功能障碍,从而加速动脉粥样硬化进展,这可能是颗粒物质和心血管事件之间的作用基础。血管内皮细胞具有多种生理功能,血管内皮损伤是许多心血管疾病的病理基础,有研究采用经鼻腔滴入PM2.5悬浊液的方法,但能够进入肺泡中的PM2.5很少入气管内。本实验在气管插管后直接注射PM2.5悬浊液可最佳模拟该剂量PM2.5的作用。
流行病学研究发现在PM2.5急性暴露和出现呼吸系统症状之间存在24 h的延迟。有研究使用不同组分的PM2.5染毒實验均证实,24 h后PM2.5造成的损伤效应达到最大值。因此,实验动物在末次染毒结束后进行实验操作。在大多数情况下,VE的抗氧化作用是与脂氧自由基或脂过氧自由基反应,向它们提供氢离子,使脂质过氧化链式反应中断,具有增强细胞的抗氧化作用,抑制脂质过氧化作用等。VE作为抗氧化剂及氧自由基清除剂与SOD、GSH-Px等一起构成体内抗氧化系统,保护细胞膜及细胞内的核酸免受自由基的攻击。VE可阻止糖化低密度脂蛋白发生氧化反应,还可以降低CRP水平。CRP水平降低表明机体炎症状态好转,很可能是VE减少了促炎性细胞因子的分泌及促使CRP在肝脏中的合成增加。Devaraj等研究发现,健康人群饮食补充高剂量VE可以阻止IL-1β的释放。IL-1β这一促炎性细胞因子会刺激IL-6的表达,继而增加CRP的合成。IL-6作为一种多效应的细胞因子可由多种细胞产生,它能够抑制巨噬细胞释放TNF-α,减轻炎症反应。IL-6在慢性气道炎症急性发作期的高表达可能与其抗炎症的负反馈机制有关。实验发现,与溶剂对照组相比,PM2.5各指标值差异有统计学意义,表明PM2.5可引起大鼠血管炎症反应,给予VE后,炎性损伤减轻。
在正常生理状况情况下,体内活性氧的产生和清除处于低水平的平衡状态对机体有利,但在某些病理情况下,由于某种原因使得活性氧产物过量,累积于体内,对机体造成氧化损伤。活性氧既会造成对生物大分子的损伤,也可触发多不饱和脂肪酸的脂质过氧化反应,其中MDA是反应的终产物之一。血清MDA直接反映机体的脂质过氧化速率和强度。SOD是生物体内重要的抗氧化酶,主要生理作用是歧化氧自由基,及时清除机体生成的氧自由基,切断自由基链锁反应,防止自由基对组织细胞产生毒害作用,从而保护细胞免受氧自由基的攻击。SOD是生物体内清除自由基的首要物质,反映自由基清除能力,即抗脂质过氧化的能力。氧自由基还可攻击生物膜中的不饱和脂肪酸,使其发生氧化,引起脂质过氧化产物MDA升高,而脂质过氧化是造成生物体氧化损伤的主要原因。因此,通过测定体内MDA含量,可反映机体内脂质过氧化的程度,间接反映体内自由基对细胞的损伤程度。MDA与SOD是一对相互对立的指标,分别代表脂质过氧化与抗脂质过氧化的物质。GSH是体内重要的抗氧化剂和自由基清除剂,能与自由基、重金属等结合,从而把有害的毒物转化为无害的物质排出体外。GSH-Px是机体内广泛存在的一种重要的催化过氧化氢分解的酶,它特异性催化还原型谷胱甘肽(GSH)对过氧化氢的还原反应。GSH与超氧阴离子自由基(O2-)反应可产生O2,GSH-Px对其他抗氧化剂具有调节作用。
作为体内抗氧化的VE,可直接清除自由基,抑制脂质过氧化反应,进而增强细胞抵抗氧化损伤的能力。研究发现,PM2.5可引发大鼠心血管氧化应激损伤,给予VE灌胃,可以提高T-SOD、GSH和GSH-Px氧化酶的活性,减少MDA水平,抑制脂质过氧化反应,提升大鼠抗氧化能力。
早在1986年,纽约州立大学和加州大学的学者分别提出内皮细胞舒张因子的本质是NO。NO作为机体内重要的信使分子、效应分子和免疫调节分子,在维持内皮功能方面有很重要的作用,具有抗血小板和抗氧化功能,同时可防止炎症反应并能阻止动脉硬化症的进一步发展。ET-1具有很强的收缩血管和促血管平滑肌细胞增殖的作用,ET三种形态中的ET-1主要在内皮细胞中表达,在高血压、脑血管病和心力衰竭等心血管系统疾病中发挥着病理生理功能。ET-1还与动脉粥样硬化明显相关,有研究发现心力衰竭的病人血浆中ET-1含量成倍增加,而发生心肌梗死时血浆ET-1也明显增加,且持续的ET-1增加与心肌梗死患者发病之后12个月内的死亡率明显相关。ET-1和NO的合成、释放失衡直接影响血管的基础张力、冠状动脉的血流储备等,所以ET和NO与心血管疾病的发生、发展密切相关。实验发现,PM2.5染毒后,大鼠心血管内皮功能受损,ET-1升高,NO降低,给予VE可以减轻这种状况。
细胞缝隙连接通讯(GJIC)是人和动物体内细胞间通讯的重要方式之一,Cx43作为心室肌细胞间隙连接组成中主要的连接蛋白,在维持心室肌细胞的连接通讯功能,电信号传导和正常的节律性的收缩中起重要作用,Cx43的分布或表达异常是导致心律失常发生的一个重要机制。结果发现,PM2.5可引起大鼠Cx43含量降低,对心律失常产生影响,给予大鼠VE可以减轻大鼠心律失常的状况。
VE作为一种有效的脂溶性抗氧化剂,包含8种生育酚,其中仅一生育酚具有更好的抗氧化潜能。VE因其高效的抗氧化性,被用来治疗多种疾病,例如癌症等。研究表明:过量VE的补充可导致机体产生过氧化效应,并降低机体内抗氧化酶的活性,破坏了机体内的氧化和抗氧化系统。
目前本试验研究的仅是空气污染对心血管的短期影响,短期暴露与长期暴露对健康的影响机制不同,因此还需要大量人群的长期追踪调查。

