Ag/AgCl/ZnO纳米复合材料的制备及其光催化性能
艾建平,林初诚,廖伟秀 ,周 涛,张 豪,程丽红,杨艳玲,李文魁江西科技师范大学材料与机电学院,南昌008 江西省材料表面工程重点实验室,南昌008 中国科学院上海硅酸盐研究所 无机材料分析测试中心,上海00050
过去几十年间,环境污染的控制和治理成为人类社会面临和亟待解决的重大问题之一[1]。与其他传统处理方法相比,半导体光催化技术具有能够将有机污染物彻底分解为小分子无机物,且分解的能量来源为光能、无二次污染、可选择的光催化剂种类繁多等优点,逐渐成为研究者关注的重要技术领域[2]。ZnO作为一类重要的半导体功能材料,由于其价格低廉、无毒、形貌多样化和高反应活性等优点,已经在光催化领域得到广泛应用[3-5]。但是,纳米 ZnO半导体材料在光激发下产生的电子-空穴容易复合,导致光催化效率较低;ZnO半导体材料禁带宽度3.37 eV,只能吸收占太阳光能量比例不足5% 的紫外光,且ZnO材料的光化学腐蚀现象比较严重,这些都严重限制了其在光催化领域的应用。因此,抑制纳米ZnO中光生载流子的复合、拓展纳米ZnO的光谱吸收范围是提高其光催化活性的主要途径。
离子掺杂是一种简单而有效的调控半导体能带结构的方法,不仅可以拓展半导体的光响应范围,还能微调半导体的氧化还原能力。傅天华等人[6]采用溶液法制备了 (Fe,Ni) 共掺杂ZnO光催化剂,实验结果表明 (Fe,Ni) 共掺杂显著提高了ZnO光催化降解甲基橙的活性。Šutka等人[7]采用溶剂热法制备高长径比的Co 掺杂ZnO纳米线,Co的掺杂量为5 mol% 时所制备的材料可见光降解甲基橙活性最优,降解速率为4.3 × 10-3min-1。诸多研究表明,只有适量的掺杂浓度才能提高ZnO的光催化效率。掺杂离子往往很难均匀地分散在基体中,形成的杂质能级结构不连续,导致载流子难以快速迁移到ZnO催化剂表面,且掺杂的物质容易沉积到光催化剂表面,限制了ZnO光催化性能的进一步提高[8,9]。另外,也有研究人员采用半导体复合 (例如ZnO/ZnAl2O4[10]、ZnO/TiO2[11]、ZnO/g-C3N4[12]等)、染料敏化[13]、贵金属修饰[14]等方法改善 ZnO光催化性能。其中,通过贵金属沉积来修饰光催化半导体材料时,贵金属与半导体二者界面间形成肖特基势垒,改变了半导体材料表面的载流子分布,可以显著提高ZnO的光催化效率,成为提升ZnO光催化活性和拓展其光谱响应范围的重要研究方向[15,16]。
近年来,Ag/AgX (X = Cl, Br) 基[17,18]的新型表面等离子体光催化剂引起了科研人员极大的关注。它结合了贵金属的表面等离子体共振效应、金属半导体接触和半导体光催化材料的特性,开辟了一条通过金属表面等离子体共振效应拓展光催化材料可见光吸收、促进光催化体系中光生电子-空穴对分离,进而提高光催化材料性能的新途径。黄柏标等人[19]首次以 Ag2MoO4和 HCl为原料,通过光还原技术制备出高效、结构稳定的 Ag@AgCl表面等离子体光催化剂。随之,部分研究人员陆续开展了与Ag/AgX复合材料 (例如:Ag/AgCl/TiO2[20]、Ag/AgBr/WO3⋅H2O[21]) 的光催化性能研究,结果表面Ag/AgX不仅是一种良好的光催化剂,而且是一种有效的助催化剂。但到目前为止,只有少数学者报道了通过两步法制备Ag/AgCl/ZnO复合光催化剂,研究其光降解甲基橙溶液的性能[22],而关于沉淀-煅烧法制备Ag/AgCl/ZnO复合光催化剂及Ag/AgCl组分含量对ZnO光催化性能影响规律的研究鲜有报导。
本研究采用沉淀法结合热分解法制备了不同Ag/AgCl组分含量的Ag/AgCl/ZnO复合光催化剂,以罗丹明B为目标污染物,对所制备的Ag/AgCl/ZnO复合材料光催化性能进行了评价。通过多种表征手段系统研究了材料结构与光催化性能之间的关系,并提出了可能的光化学反应机制。
1 实 验
1.1 实验原料
本研究所使用的原料包括硝酸锌 (Zn(NO3)2⋅6H2O)、柠檬酸钠 (Na3C6H5O7⋅2H2O)、硝酸银(AgNO3)、碳酸钠 (Na2CO3)、氯化1-丁基-3甲基咪唑 (C8H15ClN2)、罗丹明B、无水乙醇等,均为分析纯试剂。
1.2 样品制备
称取12.5 mmol Zn(NO3)2⋅6H2O (3.7187 g) 溶于50 mL水中,磁力搅拌10 min之后,准确称量0.2125 g AgNO3(Ag+: Zn2+= 0.1 : 1) 加入到上述溶液中持续搅拌制备出溶液A。将氯化1-丁基-3甲基咪唑0.1092 g和柠檬酸钠0.1471 g溶于20.8 mL浓度为1.5 mol/L的碳酸钠溶液当中,均匀搅拌30 min之后制备出溶液B。继续磁力搅拌B溶液,用20 min将A溶液匀速逐滴地加入到B溶液中,获得混合溶液;将混合溶液加热到60°C保温4 h,充分反应结束之后自然冷却至室温,除去上层液体,真空抽滤取出沉淀物,并用去离子水和无水乙醇洗涤至中性,在60°C烘箱干燥12 h;将干燥后的粉体装入坩埚置于管式炉中,通入氮气,以10°C/min的升温速率在200°C预处理30 min,在350°C保温4 h,经冷却、研磨后得到Ag/AgCl/ZnO复合材料,将该样品编号为S1。
采用相同的制备流程,改变硝酸银用量分别为Ag+: Zn2+= 0.2 : 1和0.3 : 1,同时对应改变氯化1-丁基-3甲基咪唑用量分别为0.3275 g和0.7642 g,制得同类系列样物S2和S3。
为了进行光催化性能对比实验,采用水热法制备了纯 ZnO,具体过程为:称取 1.75 mmol Zn(NO3)2⋅6H2O (0.5206 g) 溶于67 mL水中,磁力搅拌30 min得到混合溶液,然后继续在磁力搅拌下缓慢滴加2 mol/L NaOH调节pH值至12,继续磁力搅拌30 min后将混合物转移到有聚四氟乙烯内衬的100 mL不锈钢水热釜中密封,控制混合溶液体积为70 mL,于120°C下反应3 h,待反应釜自然冷却后,除去上层液体,真空抽滤并用去离子水和无水乙醇洗涤至中性,在60°C烘箱干燥12 h即可得到纯ZnO。
1.3 样品表征和测试
采用日本Rigakug公司的X-射线粉末衍射仪分析样品的晶型和组成,管电压为40 kV,Cu靶Kα辐射 (λ = 0.154178 nm),扫描速率 4°/min,扫描范围 2θ = 10° ~ 80°。采用日本 Hitachi公司的 S-4800型场发射扫描电镜 (FFE-SEM) 观测样品的形貌,采用扫描电镜所附的能谱仪 (EDS) 对材料成分元素进行定量分析。采用日本JEOL公司的JEM-2010F型透射电子显微镜 (TEM) 观察样品的形貌和晶体结构。采用美国 PerkinElmer公司的 Lambda750型紫外-可见分光光度计测定样品的吸收光谱(标准参比样品为BaSO4)。
1.4 催化活性评价
用300 W汞灯产生365 nm紫外光作为光源,以罗丹明B作为降解对象,在南京胥江XPA-7型光催化反应仪中考察Ag/AgCl/ZnO样品的紫外光催化活性,具体步骤为:取30 mg样品分散至60 mL浓度为15 mg/L的罗丹明B水溶液 (不调节溶液pH) 中得到悬浊液;在光催化反应进行之前,将此悬浊液置于暗箱中搅拌30 min,使体系达到吸附/解吸附平衡。然后,将悬浊液放到距离光源11 cm处光照,不断磁力搅拌,反应时间180 min。每隔30 min用滴管取上层溶液5 mL,在转速为3000 r/min下离心10 min ~ 20 min,取上清液用PerkinElmer Lambda35紫外-可见分光光度计在553 nm波长处测定罗丹明B溶液的吸光度。
2 结果与讨论
2.1 物相结构与形貌
采用扫描电镜的能谱仪定量分析样品中的Ag含量,结果表明样品S1、S2和S3中Ag含量分别为8.70 wt%、11.92 wt% 和23.17 wt.%。
图1为不同Ag含量Ag/AgCl/ZnO复合材料的XRD图谱。从图中可以看出,水热法制备的纯ZnO为六方纤锌矿结构 (与JCPDS 36-1451吻合),对应的衍射峰用符号“●”标示。Ag/AgCl/ZnO复合材料则由三种物相组成,分别为面心立方Ag (JCPDS 04-0783)、面心立方AgCl (JCPDS 31-1238)和六方纤锌矿氧化锌。其中,Ag含量为8.70 wt.%时,产物中AgCl物相的衍射峰几乎可以忽略,说明粉体中含有的AgCl含量极少。随着Ag含量的逐渐增加,样品中AgCl物相对应衍射峰变得更加尖锐,说明硝酸银加入量增加更有利于AgCl物相的生成。与纯ZnO的衍射峰相比,Ag/AgCl/ZnO复合材料中的ZnO物相衍射峰没有发生偏移,说明产物中形成的Ag/AgCl物相存在于在ZnO颗粒表面,而没有进入到ZnO晶格中[23]。
图2为纯ZnO和不同Ag质量分数Ag/AgCl/ZnO的SEM照片。从图2 (a) 可以看出水热法制备的纯ZnO呈花状棒簇,这主要是因为前驱液在较高pH下,生长单元Zn(OH)42-浓度增加,更容易吸附在ZnO晶体带正电荷的 (0001) 极性面上,沿c轴方向生长,形成直径约100 nm ~ 220 nm的纳米棒组成的花状ZnO[24]。从图2 (b) 可以看出Ag质量分数为8.70 wt.% 的Ag/AgCl/ZnO复合物具有纳米网络结构,晶粒尺寸约为20 nm ~ 80 nm,这些网络结构的形成是因为ZnO表面沉积了Ag或者AgCl颗粒所致[25]。随着Ag质量分数增加,样品晶粒尺寸逐渐变大,粉体形貌为颗粒状 [图2 (c)和图2 (d)]。 EDS数据结果表明样品中存在Zn、O、Ag和Cl元素。结合XRD结果,可以推断出Ag/AgCl物相沉积在ZnO表面。
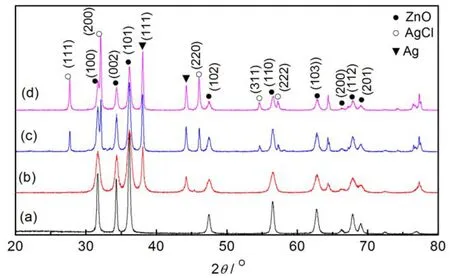
图1 不同Ag质量分数Ag/AgCl/ZnO复合材料的XRD图谱Figure 1 XRD patterns of Ag/AgCl/ZnO system with different Ag contents(a) pure ZnO;(b) 8.7 wt% Ag; (c) 11.92 wt% Ag; (d) 23.47 wt% Ag

图2 纯ZnO和不同Ag质量分数Ag/AgCl/ZnO粉体的SEM照片Figure 2 SEM images of synthesized pure ZnO and Ag/AgCl/ZnO powders:(a) pure ZnO; (b) Ag/AgCl/ZnO (8.70 wt%); (c) Ag/AgCl/ZnO (11.92 wt%); (d) Ag/AgCl/ZnO (23.17wt%)

图3纯ZnO和不同Ag质量分数Ag/AgCl/ZnO粉体的TEM照片Figure 3 TEM images of synthesized synthesized pure ZnO and Ag/AgCl/ZnO powders:(a) pure ZnO; (b) Ag/AgCl/ZnO (8.70 wt%); (c) Ag/AgCl/ZnO (11.92 wt%); (d) Ag/AgCl/ZnO (23.17wt%)
图3 为纯ZnO和不同Ag质量分数Ag/AgCl/ZnO粉体的TEM照片。从图3 (a) 可以看到,水热法制备的纯ZnO棒直径大约在250 nm ~ 300 nm之间,与SEM结果一致,充分说明ZnO作为一种极性晶体,具有明显的各向异性生长特性。当Ag质量分数为8.70 wt% 时,可以看出Ag/AgCl/ZnO复合材料形成网络状结构,在网络之间分布着尺寸为20 nm ~ 100 nm左右的孔隙。图3 (c) 和 (d)中箭头所指衬度较黑的区域为沉积了Ag/AgCl物相的ZnO表面。随着样品中Ag质量分数的增加,照片的黑色衬度区域面积变大,表明Ag/AgCl物相含量增加,与XRD数据结果一致。此外,还可以看出Ag质量分数为11.92 wt% 时,Ag/AgCl物相在材料内部的分布更细密,这将更有利于Ag/AgCl与ZnO形成较大面积的接触界面。
为了弄清Ag/AgCl/ZnO复合材料详细的微观结构信息,本研究拍摄了材料的高分辨率透射电镜照片,如图4所示。从图中可以看出,Ag/AgCl/ZnO复合材料存在很多ZnO-Ag或者ZnO-Ag/AgCl接触界面,也观察到一些Ag颗粒附着在ZnO表面。从样品S1的高分辨率照片中可以清晰地看到ZnO和Ag的晶格条纹,其中ZnO纳米颗粒晶格条纹的距离为0.257 nm,与六方纤锌矿型ZnO的 (002)晶面间距吻合。同样,在样品S2和S3的高分辨率照片也可以观测到ZnO的晶格条纹,分别与六方纤锌矿型ZnO的 (101)、(100) 晶面间距吻合。以上结果表明,Ag的引入并没有改变ZnO的晶格结构,与XRD数据结果相吻合。
2.2 复合光催化剂合成过程
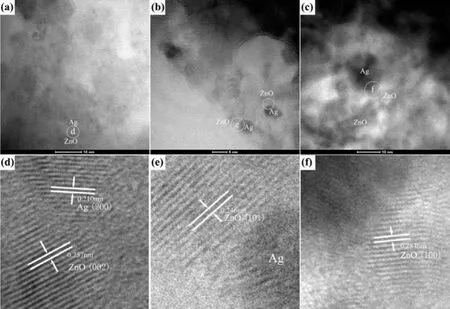
图4 不同Ag质量分数Ag/AgCl/ZnO粉体的TEM照片:(a) 样品S1; (b) 样品S2; (c) 样品S3;(d)、(e)和 (f) 分别对应于(a)、(b) 和 (c) 的高分辨率TEM照片Figure 4 TEM images of Ag/AgCl/ZnO powders: (a) 8.70 wt% Ag; (b) 11.92 wt% Ag; (c) 23.17 wt% Ag;(d), (e) and (f) are high resolution micrographs corresponding to (a), (b) and (c) respectively.
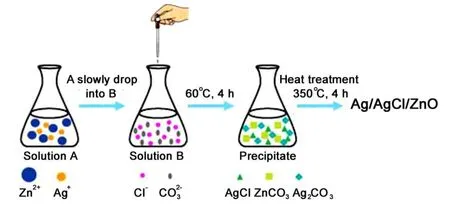
图5 沉淀-煅烧法制备Ag/AgCl/ZnO纳米复合材料原理示意图Figure 5 The schematic diagram for one-pot preparation of Ag/AgCl/ZnO nanocomposites
基于上述表征结果,根据胶体平衡理论,本研究认为Ag/AgCl/ZnO纳米复合材料的形成过程大致如图5所示:在将含有Zn2+和Ag+的A溶液缓慢地滴加到B溶液的过程中,在反应初期,AgCl、ZnCO3和Ag2CO3沉淀物缓慢形成:


在煅烧热处理阶段,干燥后的粉体发生热分解反应:在这些反应的进行过程中,粉体发生碎裂,容易形成尺寸更小且带有尖锐边角的ZnO和Ag晶核。根据胶态平衡理论可知物相的曲率半径越小,溶解度越高。因此,在热处理阶段保温阶段,晶核尖锐的边角逐渐溶解,然后曲率半径较大的部位沉积。随着反应不断进行,各物相逐渐长大,最后形成边角钝化的多边形颗粒。
2.3 光催化活性与机制
图 6所示为纯 ZnO和不同 Ag质量分数Ag/AgCl/ZnO粉体的紫外-可见漫发射光谱。从图中可以看出,纯ZnO在波长380 nm附近存在陡峭的带隙吸收峰,但在可见光区域没有明显的光谱吸收,这说明 ZnO晶体结晶度很高。ZnO被Ag/AgCl修饰之后并没有明显改变其吸收带。当Ag/AgCl被引入到ZnO表面,S1、S2和S3样品就产生了明显的表面等离子体吸收峰,且在可见光波长区域都存在明显的吸收,表明Ag/AgCl/ZnO纳米复合材料光谱响应范围明显宽于纯ZnO。因此,在可见光降解有机污染物具有潜在的应用价值。
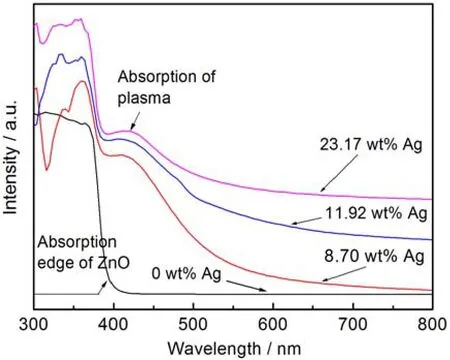
图6纯ZnO和不同Ag质量分数Ag/AgCl/ZnO粉体的紫外-可见漫发射光谱Figure 6 UV-vis diffuse reflectance spectrum of synthesized synthesized pure ZnO and Ag/AgCl/ZnO powders
图7 为紫外光照射下ZnO和Ag/AgCl/ZnO降解罗丹明B的光催化活性和动力学图。图中,C0是罗丹明B溶液达到吸附平衡时的浓度,Ct是随着光照时间而不断变化的罗丹明B溶液瞬时浓度。从图中可以看出,紫外光照射180 min之后,罗丹明B原液自身几乎没有降解。在光照射之前,放有光催化剂的罗丹明B染料在黑暗中放置30 min以达到吸附平衡,罗丹明B的浓度有明显降低,说明光催化剂材料对染料具有较强的吸附能力。从图中可以看出,Ag/AgCl/ZnO样品的光降解效率比纯ZnO高。其中,Ag质量分数为11.92 wt.%时,Ag/AgCl/ZnO复合材料 (样品S2) 的光催化活性最高,大约在120 min内即可将罗丹明B溶液降解完全,而Ag质量分数分别为8.70 wt% (样品S1) 和23.17 wt% (样品S3) 的Ag/AgCl/ZnO则需要180 min以上才能完全降解罗丹明B溶液。
对图7 (b) 所示数据进行线性拟合,得到各种情况下的反应速率常数如表1所示。注意到所有情况下的线性相关系数平方均大于0.92,因此可以将降解过程看作准一级反应。样品S2降解罗丹明B的速度大约是0.01938 min-1,是纯ZnO降解罗丹明B速度的2.5倍。
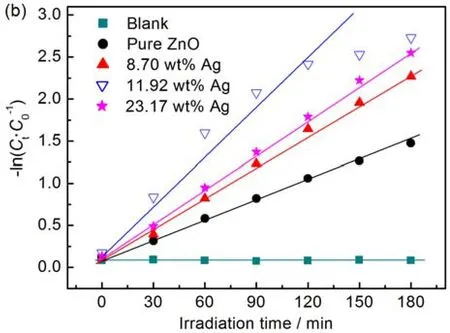
图7 紫外光照射下ZnO和Ag/AgCl/ZnO对罗丹明B降解率随时间变化曲线 (a) 及降解动力学图 (b)Figure 7 (a) The photocatalytic degradation curves and (b) kinetic curves of RhB over ZnO and Ag/AgCl/ZnO under UV-light irradiation
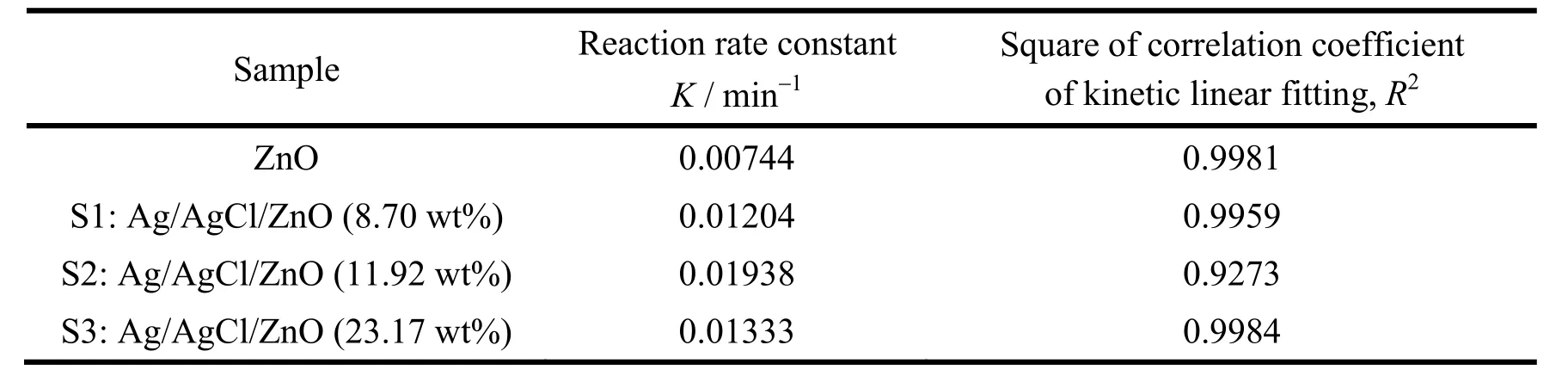
表1 紫外光照射下ZnO和Ag/AgCl/ZnO降解罗丹明B的动力学参数Table 1 Kinetic parameters for photodegradation of RhB by ZnO and Ag/AgCl/ZnO under UV-light
根据以上实验结果,可以将在紫外光照射下Ag/AgCl/ZnO体系光催化反应过程概述如下 (如图8 所示):
首先,在紫外光照射下,ZnO和AgCl半导体中形成电子-空穴对

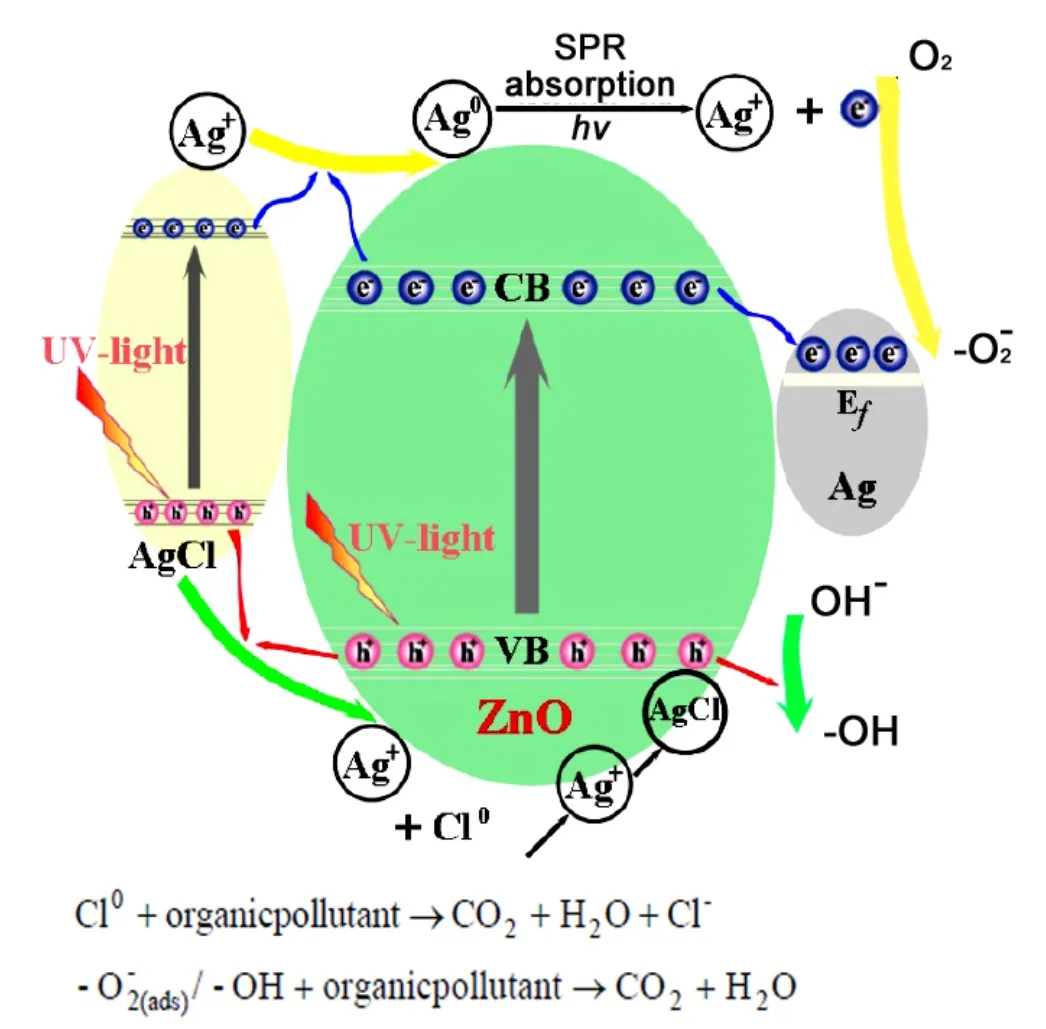
图8 紫外光照射下Ag/AgCl/ZnO体系光催化反应过程示意图Figure 8 The proposed reaction mechanism of Ag/AgCl/ZnO system under UV-light irradiation

其中,ZnO导带的电子容易迁移到费米能级比较低的Ag纳米颗粒中,促进载流子分离,从而有更多的电子与催化剂表面吸收的溶解氧反应生成超氧自由基:
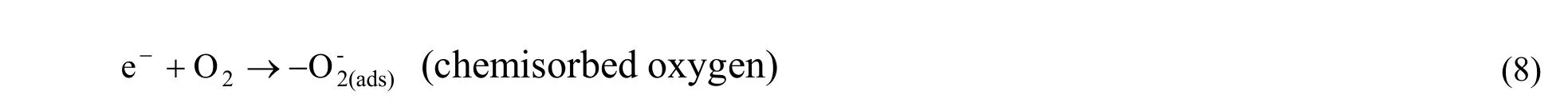
而ZnO价带中的部分空穴则与水中的OH-反应生成羟基自由基 (-OH):

超氧自由基和羟基自由基可以使有机染料发生降解[26,27]:
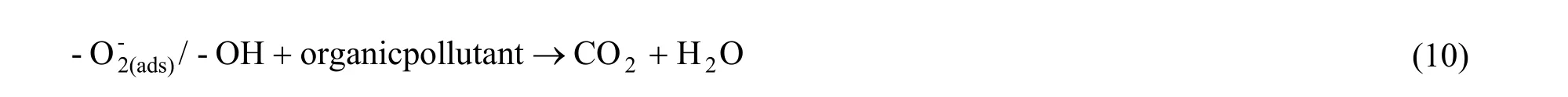
另外,ZnO和AgCl价带上的部分空穴还会与AgCl反应生成Ag+和Cl0[19]:

部分Ag+会与半导体导带中的电子反应变成Ag0。生成的Cl0则具有强氧化性,使得有机染料降解,自身变成Cl-:

而氧化锌表面附着的银纳米颗粒由于表面等离子体共振效应产生强烈的光吸收,吸收光子能量后生成Ag+和电子,部分Ag+与生成的Cl-反应重新形成AgCl物相:产生的电子与吸附氧反应生成具有降解能力的超氧自由基。

从上述光催化反应过程可知,Ag/AgCl/ZnO体系降解罗丹明B反应活性比纯ZnO更高的原因有两方面:一是表面等离子效应使得Ag纳米颗粒对光的吸收能力增强,与此同时,Ag纳米颗粒可以转移ZnO导带的电子,使得体系产生更多具有降解能力的超氧自由基;另一方面,AgCl半导体的引入使得体系产生了具有强降解能力的活性物种Cl0。但是,Ag/AgCl的引入存在最佳含量,在本研究工作中,Ag质量分数为11.92 wt% 时Ag/AgCl/ZnO复合材料 (样品S2) 的光催化活性最高。Ag/AgCl物相含量过高时,Ag/AgCl难以均匀地覆盖在ZnO表面,不能形成足够的ZnO与Ag/AgCl接触界面,容易使得 Ag纳米颗粒反而成为光生载流子的复合中心[28],同时体系产生活性物种 Cl0的能力大大降低,从而导致Ag/AgCl/ZnO体系的光催化活性降低。
3 结 论
本文采用沉淀法结合热分解法制备了Ag/AgCl/ZnO复合光催化剂。Ag/AgCl物相分布于ZnO表面。当Ag质量分数为11.92 wt% (样品S2) 时,Ag/AgCl物相在材料内部的分布更细密,Ag/AgCl与ZnO之间形成较大面积的接触界面,Ag/AgCl/ZnO复合光催化剂降解效率最佳。在紫外光照射下,S2样品在120 min内可将罗丹明B溶液完全降解,降解速率是纯ZnO光催化剂的2.5倍。
Ag/AgCl/ZnO体系降解罗丹明B反应活性比纯ZnO更高的原因有两方面:一是表面等离子效应使得Ag纳米颗粒对光的吸收能力增强,与此同时,Ag纳米颗粒可以转移ZnO导带的电子,使得体系产生更多具有降解能力的超氧自由基;另一方面,AgCl半导体的引入使得体系产生具有强降解能力的活性物种Cl0。但Ag/AgCl物相含量过高时,Ag/AgCl难以均匀地覆盖在ZnO表面,不能形成足够的ZnO与Ag/AgCl接触界面,容易使得Ag纳米颗粒反而成为光生载流子的复合中心,同时体系产生活性物种Cl0的能力大大降低,从而导致Ag/AgCl/ZnO体系的光催化活性降低。
[1] 朱永法, 姚文清, 宗瑞隆. 光催化-环境净化与绿色能源应用探索[M]. 北京: 化学工业出版社, 2014.
[2] 谢志强. 氧化锌纳米棒的水热法制备及其光催化性能的研究[D]. 南宁: 广西大学硕士学位论文,2012.
[3] DUO SW, LI YY, LIU TZ, et al. Preparation of ZnO from 2D nanosheets to diverse 1D nanorods and their structure, surface area, photocurrent, optical and photocatalytic properties by simple hydrothermal synthesis [J]. Journal of Alloys and Compounds, 2017, 695: 2563-2579.
[4] BAUDYS M, KRÝSA, ZLÁMAL M, et al. Weathering tests of photocatalytic façade paints containing ZnO and TiO2[J]. Chemical Engineering Journal, 2015, 261: 83-87.
[5] RANASINGHA O, WANG CJ, MATRANGA C, et al. Synthesis, characterization and photo-catalytic activity of Au-ZnO heterostructured nano-pyramids [J]. Journal of Materials Chemistry A, 2015, 3 (29):15141-15147.
[6] 傅天华, 高倩倩, 刘斐, 等. Fe-Ni共掺杂ZnO的制备及其光催化降解甲基橙活性[J]. 催化学报, 2010,31 (7): 797-802.
[7] ŠUTKA A, KÄÄMBRE T, PÄRNA R, et al. Co doped ZnO nanowires as visible light photocatalysts [J].Solid State Sciences, 2016, 56: 54-62.
[8] QIU X, LI G, SUN X, et al. Doping effects of Co2+ions on ZnO nanorods and their photocatalytic properties [J]. Nanotechnology, 2008, 19 (21): 215703.
[9] JIA TK, WANG WM, LONG F, et al. Fabrication, characterization and photocatalytic activity of La-doped ZnO nanowires [J]. Journal of Alloys and Compounds, 2009, 484: 410-415.
[10] 张丽, 阎建辉, 周民杰, 等. 高比表面空心球状 ZnO/ZnAl2O4复合光催化剂制备及活性[J]. 无机化学学报, 2012, 28 (9): 1827-1834.
[11] CHEN SF, ZHAO W, LIU W, et al. Preparation, characterization and activity evaluation of p-n junction photocatalyst p-ZnO/n-TiO2[J]. Applied Surface Science, 2008, 255: 2478-2484.
[12] SUN JX, YUAN YP, QIU LG, et al. Fabrication of composite photocatalyst g-C3N4-ZnO and enhancement of photocatalytic activity under visible light [J]. Dalton Transactions, 2012, 41: 6756-6763.
[13] LAN CM, WU HP, PAN TY, et al. Enhanced photovoltaic performance with co-sensitization of porphyrin and an organic dye in dye-sensitized solar cells [J]. Energy & Environmental Science, 2012, 5: 6460-6464.[14] JIANG RB, LI BX, FANG CH, et al. Metal/semiconductor hybrid nanostructures for plasmon-enhanced applications [J]. Advanced Materials, 2014, 26: 5274-5309.
[15] UDAWATTE N, LEE M, KIM J, et al. Well-defined Au/ZnO nanoparticle composites exhibiting enhanced photocatalytic activities [J]. ACS Applied Materials & Interfaces, 2011, 3: 4531-4538.
[16] DENG Q, DUAN XW, H. L. NG D, et al. Ag nanoparticle decorated nanoporous ZnO microrods and their enhanced photocatalytic activities [J]. ACS Applied Materials & Interfaces, 2012, 4: 6030-6037.
[17] AN CH, PENG S, SUN YG. Facile synthesis of sunlight-driven AgCl:Ag plasmonic nanophotocatalyst [J].Advanced Materials, 2010, 22: 2570-2574.
[18] BI YP, YE JH. In situ oxidation synthesis of Ag/AgCl core-shell nanowires and their photocatalytic properties [J]. Chemical Communications, 2009, 43: 6551-6553.
[19] WANG P, HUANG BB, QIN XY, et al. Ag@AgCl: a highly efficient and stable photocatalyst active under visible light [J]. Angewandte Chemie International Edition, 2008, 47: 7931-7933.
[20] YU JG, DAI GP, HUANG BB. Fabrication and characterization of visible-light-driven plasmonic photocatalyst Ag/AgCl/TiO2nanotube arrays [J]. Journal of Physical Chemistry C, 2009, 113:16394-16401.
[21] WANG P, HUANG BB, QIN XY, et al. Ag/AgBr/WO3⋅H2O: visible-light photocatalyst for bacteria destruction [J]. Inorganic Chemistry, 2009, 48: 10697-10702.
[22] XU YG, XU H, LI HM, et al. Enhanced photocatalytic activity of new photocatalyst Ag/AgCl/ZnO [J].Journal of Alloys and Compounds, 2011, 509: 3286-3292.
[23] XU H, LI HM, WU CD, et al. Preparation, characterization and photocatalytic properties of Cu-loaded BiVO4[J]. Journal of Hazardous Materials, 2008, 153: 877-884.
[24] LV XZ, LIU XC, SUN Q, et al. Growth and optical properties of hierarchical flower-like ZnO nanostructures [J]. Ceramics International, 2017, 43: 3306-3313.
[25] MENG A, XING J, LI ZJ, et al. Ag/AgCl/ZnO nano-networks: Preparation, characterization, mechanism and photocatalytic activity [J]. Journal of Molecular Catalysis A, 2016, 411: 290-298.
[26] YATMAZ HC, AKYOL A, BAYRAMOGLU M. Kinetics of the photocatalytic decolorization of an AZO reactive dye in aqueous ZnO suspensions [J]. Industrial & Engineering Chemistry Research, 2004, 43 (19):6035-6039.
[27] LU WW, GAO SY, WANG JJ. One-pot synthesis of Ag/ZnO self-assembled 3D hollow microspheres with enhanced photocatalytic performance [J]. Journal of Physical Chemistry C, 2008, 112: 16792-16800.
[28] REN CL, YANG BF, WU M, et al. Synthesis of Ag/ZnO nanorods array with enhanced photocatalytic performance [J]. Journal of Hazardous Materials, 2010, 182: 123-129.

