气凝胶研究进展
章 婷,赵春林,乐 弦,贾欢欢,向军辉中国科学院大学材料科学与光电技术学院,北京0408 中国建筑材料科学研究总院有限公司,北京0004
气凝胶是由胶体粒子或高聚物分子相互聚集构成纳米多孔网络结构、并在孔隙中充满气态分散介质的一种高分散固态材料,其固体相和孔隙结构均为纳米尺度,是湿凝胶干燥过程中将其中的液体成分替换成气体而仍然保持其凝胶网络的三维多孔纳米材料[1]。图 1给出了气凝胶与干凝胶之间的主要区别。
目前制得的气凝胶孔隙率一般在80% ~ 99.8%,典型孔洞尺寸在50 nm范围内,比表面积可高达l000 m2·g-1。此外,气凝胶的密度极低,且易通过工艺条件来调控。
气凝胶的连续三维网络结构使得其在热学、力学、声学、光学、电学、吸附等方面都显示出独特的性质,引起了研究者们极大的兴趣。正是由于其微观结构呈现出“蜂窝状”的多孔形貌,加之其具有比表面积大、孔隙率高、密度低、热导率低等特点,气凝胶在分离材料[3]、绝热材料[4]、高能物理[5]、高效催化剂及催化剂载体[6]、气体及生物传感器[7]、低介电常数材料[8]等很多方面均具有巨大的应用潜力,如图2所示。
气凝胶最初是在1931年由斯坦福大学的Kistler[10]采用盐酸水解水玻璃的方法及超临界干燥技术 (采用乙醇为超临界干燥介质) 制得的。同时,Kistler还制备了其它许多氧化物气凝胶材料,如Al2O3、ZrO3、WO3等[11],并详细探讨了气凝胶的各项性能。由于气凝胶制备过程繁琐而漫长,且当时并未发现气凝胶的实际应用价值,因此在之后的30多年里气凝胶并未引起人们的很大兴趣。
之后,Teichner等人[12]以正硅酸甲酯为前驱体,首次在醇溶剂中制备出了醇凝胶,但由于干燥处理很棘手,制备气凝胶仍很困难。Teichner在此基础上也研究了许多简单氧化物气凝胶的合成[13]。无机气凝胶中最主要的一类就是这些氧化物气凝胶。
1966年,Peri[14]采用甲醇为超临界干燥介质来干燥水凝胶,大大缩短了干燥周期,气凝胶的研究才得到进一步的发展。20世纪80年代之后,随着溶胶-凝胶法的深入发展和超临界干燥技术的逐步完善,构成气凝胶的固体微粒更趋于细化,微孔分布更趋于均匀,从而使得材料的密度更低,孔隙率更高。同时, Lindquist等合成的硼气凝胶[15]以及美国Livermore国家实验室通过间苯二酚甲醛缩聚制备的新型有机气凝胶[16]等扩充了气凝胶的种类,极大丰富了气凝胶的体系。1985年,在德国Wüerzburg组织并举办了首届“气凝胶国际研讨会”(International Symposium on Aerogels,简称ISA),气凝胶材料得到了进一步的发展。
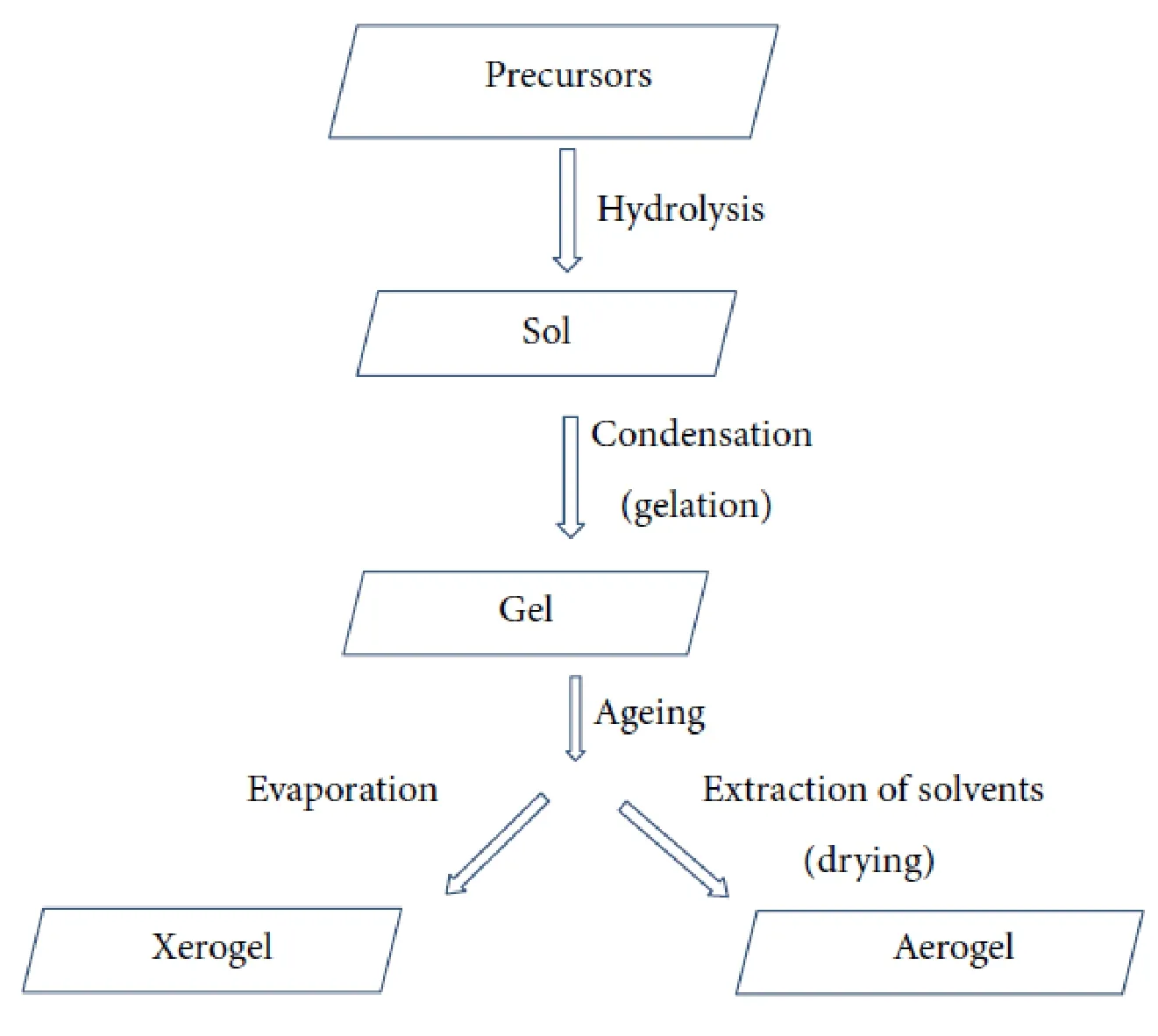
图1 干凝胶与气凝胶区别[2]Fig. 1The differences between dry gel and aerogel

图2 气凝胶材料的应用领域[9]Figure 2 Application areas of aerogels

图3 气凝胶合成过程Figure 3 Aerogels synthesis process
根据 Gessar[17]以及之后的很多研究者对于气凝胶的结构、合成方法及制备机理系统全面的论述,气凝胶的合成过程主要可分为聚合、凝胶、老化和干燥四步 (图3)。
1987年,美国Lawrence Livermore国家实验室的Pekala等人[18]首次以间苯二酚和甲醛为原料,在碱性条件下经溶胶-凝胶过程和超临界干燥制得了有机单体缩聚的气凝胶,标志着有机气凝胶研究的开端。
到目前为止,已报道的有机气凝胶材料还有聚丙烯腈[19]、聚乙烯醇[20]、聚酰亚胺[21]和聚氨酯[22]等。从气凝胶的前驱体看,有机气凝胶可分为树酯基气凝胶和多糖机 (纤维素基) 气凝胶。
而碳气凝胶 (简称CRF气凝胶) 作为一种新型轻质纳米多孔的无定形炭素材料,最早就是通过碳化间苯二酚和甲醛 (Resorcinol Formaldehyde, RF) 气凝胶获得。Pekala等人[23]采用NaCO3催化间苯二酚和甲醛的缩聚反应,然后经过溶胶-凝胶过程制备出有机气凝胶,最后经碳化制备出碳气凝胶。1996年,Hanzawa等人[24]采用CO2活化碳骨架获得了具有超高比表面积的新型CRF气凝胶,这种活化实质上类似于腐蚀骨架来生成更多的孔隙 (通常是微孔) 以提供更多的活化界面。

图4 制备碳化RF气凝胶(CRF),活化的CRF气凝胶以及钻石气凝胶的流程图[25]Figure 4 The scheme of the preparation of a carbonized RF (CRF) aerogel, activated CRF aerogel and diamond aerogel
2011年对于碳气凝胶而言是一个关键的时间点。在这一年,Pauzauskie等人[25]在激光加热金刚石对顶砧形成的高压高温气氛中将无定形态碳气凝胶模板晶化成金刚石气凝胶 (图4)。之后,随着碳纳米管和石墨烯的兴起[26-30],碳纳米管气凝胶和石墨烯气凝胶开始出现。不同于传统意义上的气凝胶,这两种气凝胶本质上并不是由胶粒聚集形成的多孔网络结构:碳纳米管气凝胶是由纳米管之间的交联缠绕构成,而石墨烯气凝胶则是由石墨烯片层之间的相互作用力将片层堆积形成的网络结构。
另一种新型的气凝胶则是最近兴起的金属气凝胶。

图5 大规模制备的铜纳米线气凝胶块体。(a) 铜纳米线气凝胶的制备过程;(b) 制备出的铜纳米气凝胶块体图像;(c) 和(d) 分别为铜纳米线气凝胶不同放大倍数下的SEM图像[31]Figure 5 Large-scale fabrication of CuNW aerogel monoliths: (a) Schematic illustration of the fabrication process; (b) Photographic image; (c and d) SEM images at different magnifications.
金属气凝胶这个概念由Tang等人[31]第一次提出,他们在较温和的实验条件下,采取冷冻铸造方法将一维铜纳米线制备成超低密度的铜气凝胶块体材料,最低密度可以达到4.6 mg·cm-3,导电率为 0.90 S·cm-1~ 1.76 S·cm-1,机械强度在1.74 Pa到12.96 Pa之间,并且其导电性、机械强度以及表面的润湿性能均可精细调控。图5为大规模制备的铜纳米线气凝胶块体[31]。可以看出,这种金属气凝胶的网络结构是由金属纳米线相互交织构成的,这个相互结合的作用力来源于水结成冰时体积膨胀所产生的压力。之后,Leventis等人[32-35]通过纳米熔炼可碳化杂化聚合物-金属氧化物气凝胶获得了包括Fe、Co、Ni、Sn和Cu在内的各种金属气凝胶。但是,Leventis等人采用的这种方法一般只能应用于那些可以碳热还原其氧化物的金属。
掺杂Pt、Pd、Au和Cu的SiO2、TiO2、Al2O3气凝胶[14,36-38]和碳气凝胶[39-41]很早之前就已经通过溶胶-凝胶法制备,但采用直接溶胶-凝胶法制备具备金属骨架的纯金属气凝胶则是最近才首次被提出[42-49]。
金属气凝胶包含金属组成的纳米网络结构,它们可以将金属的独特性能 (如导电性、热导性、催化活性、延展性以及可加工性等) 与气凝胶的特性 (如高比表面积、超轻以及高孔隙率等) 相结合,这赋予了金属气凝胶更多的性能,同时也扩展了气凝胶的应用领域。
本文主要从气凝胶种类 (即无机气凝胶,有机气凝胶,碳气凝胶以及金属气凝胶这四类) 出发讨论相应气凝胶的制备工艺以及性能,同时探讨了目前气凝胶研究存在的问题以及今后的主要研究发展方向。
1 无机气凝胶
1.1 无机气凝胶的制备工艺
气凝胶的制备主要包含两个过程,即湿凝胶的制备及干燥。制备湿凝胶最常用的方法为溶胶-凝胶法,而干燥方法则包括超临界干燥、真空冷冻干燥、常压干燥等。干燥过程中应尽量避免凝胶网络中孔隙坍塌导致凝胶体积的收缩,这是气凝胶材料干燥的关键问题。
1.1.1凝胶法制备湿凝胶
无机氧化物凝胶通常采用醇盐或盐类作为前驱体,采用酸碱两步催化方法制备。这里以正硅酸四乙酯 (C8H20O4Si,TEOS) 为例简要介绍其制备原理。凝胶网络的形成主要包含水解和缩聚两个过程。其中,水解过程可以表示为:

缩聚过程则可以表示为:

在上述过程中,TEOS首先发生水解反应,且反应是分级进行的,反应活性逐级递减。随着反应的进行,水解产物之间相互发生缩聚,进而形成胶体颗粒或溶胶;溶胶粒子的大小和交联程度与反应的剧烈程度相关。水解和缩聚反应均在酸或碱催化下进行。酸性条件下缩聚反应相对较慢,而在碱催化条件下缩聚反应较快。反应的剧烈程度决定了湿凝胶的形态结构。在酸性条件下,由于缩聚反应较慢,凝胶时间比较长,溶胶粒子之间的交联程度比较疏松,最终形成三维分子网络凝胶。而在碱性条件下,缩聚反应迅速进行,生成比较致密的胶体颗粒,最终形成的凝胶网络为珍珠串式结构。在强碱性条件下,由于缩聚反应剧烈进行,最终形成的是由光滑胶粒构成的凝胶[50]。图6为凝胶形成过程原理示意图。

图6 凝胶形成过程原理结构图[51]Figure 6 Principle of gel formation process[51]
许多氧化物气凝胶 (例如 Al2O3气凝胶[52]、ZrO2气凝胶[53]、TiO2气凝胶[54]、CuO 气凝胶[55]等) 都是通过上述过程合成的。目前已经研制出的无机氧化物气凝胶有几十种之多,其中一元氧化物气凝胶包括 SiO2、Al2O3、TiO2、MgO、Cr2O3、MoO2、ZrO2、Nb2O5、SnO2、B2O3等;金属-氧化物气凝胶包括 Cu/Al2O3、Pd/Al2O3、Ni/Al2O3等;二元氧化物气凝胶包含 Al2O3/SiO2、P2O5/SiO2、B2O3/SiO2、Nb2O5/SiO2、Er2O3/SiO2、CuO/Al2O3、NiO/Al2O3等;三元氧化物气凝胶有 CuO/ZnO/Al2O3、B2O3/P2O5/SiO2、MgO/Al2O3/SiO2、Pb/Mg1/3/Nb2/3O3、B2O3/P2O5/SiO2等。表 1列出了几种常见无机氧化物气凝胶的一些性能参数。
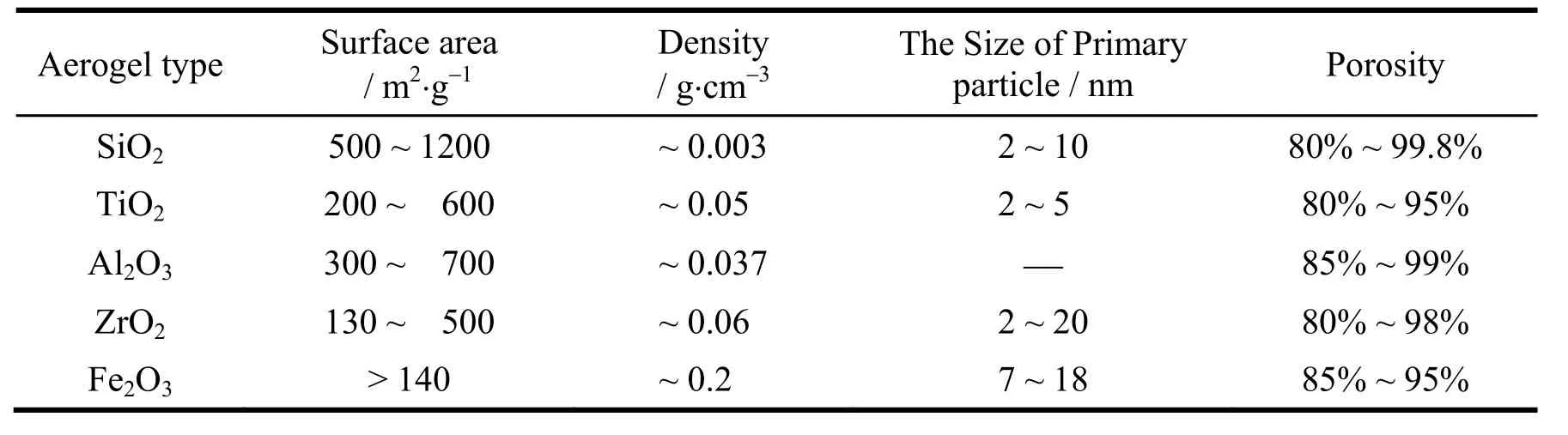
表1 几种常见无机氧化物气凝胶的性能参数[56-68]Table 1 Performance parameters of several common inorganic oxide aerogels [56-68]
1.1.2 湿凝胶的干燥
凝胶的干燥关键在于将湿凝胶网络中的液体用气体替代,这个过程中应尽量保持凝胶的网络结构不被破坏,因而干燥方法对凝胶的性质有很大的影响。在干燥过程中,网状凝胶孔隙中的液体开始蒸发时,由于分子力的作用而产生表面张力,由此产生的毛细管力为:

其中,γL为气液之间的界面能,θ为接触角,r为孔洞的半径。正是这个作用力使得湿凝胶的网络结构收缩[69]。当凝胶结构的强度不能抵抗液体产生的张力时,就会导致孔隙的收缩和塌陷。目前,避免这种现象发生最有效的方法是超临界干燥方法[70-72]。
超临界干燥:当流体的温度和压力处于其临界压力和临界温度之上时,则称该流体处于超临界状态[73]。当流体处于超临界状态时,其区别于一般流体最大的优势在于其气液界面的消失。因而,进行超临界干燥可使对孔隙结构有破坏作用的毛细张力急剧减小甚至消失,从而避免孔洞的塌陷,保持湿凝胶原有的结构。这种方法是最普遍的一种干燥方法 (图7)。
超临界干燥法按交换溶剂的临界温度高低可分为两类:高温超临界干燥法和低温超临界干燥法。表2列出了几种常用超临界溶剂的临界温度 (TC) 和临界压力 (PC)。
高温超临界干燥采用的溶剂主要有醇类和酮类等,这几种溶剂的临界温度都很高 (超过 200°C)。采用高温超临界干燥方法进行干燥时,首先在密闭环境中缓慢地对凝胶进行加热加压,使凝胶骨架间的流体逐渐达到超临界状态,然后再通过恒温状态下放气的方式缓慢地释放压力,使超临界状态的流体直接转化为气态,并逐渐扩散出凝胶骨架,最终获得超临界干燥的气凝胶材料。Kocon等人[75]就采用了高温超临界干燥技术制备出了完整且透明的二氧化硅气凝胶。

图7 超临界干燥过程原理示意图[74]Figure 7 The principle of supercritical drying process
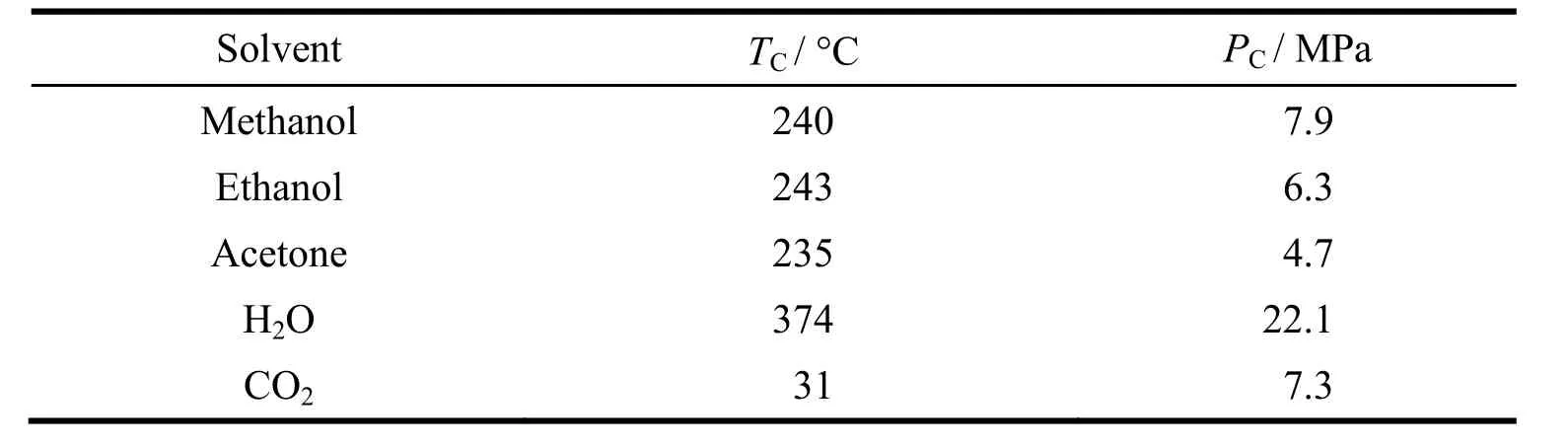
表2 常用超临界溶剂的参数[24]Table 2 Parameters of conventional supercritical solvents [24]
虽然高温超临界干燥技术消除了毛细管力对孔结构的破坏作用,但由于操作须在高温高压下进行,对设备的性能也提出了较高的要求,增加了操作难度。进行溶剂交换的介质均为有机溶剂,不仅存在一定的毒性,而且存在着易燃易爆的危险。另外,超临界干燥虽然可以得到完整的气凝胶材料,但是湿凝胶在高温干燥的过程中,凝胶骨架的微观结构会受到一定的影响。
相比而言,低温超临界干燥采用了临界温度较低 (低于50°C) 的CO2作为介质。制备过程中,CO2无毒且自身不会燃烧,不存在安全隐患,操作安全,制备的气凝胶纯度也非常高。而且,CO2还可循环利用,在一定程度上节约了资源。但低温超临界干燥比高温超临界干燥多了一个步骤,即干燥前在5 MPa ~ 6 MPa、10°C ~ 20°C条件下用CO2交换凝胶中的溶剂,然后再进行干燥。Van Bommel等人[76]采用低温超临界干燥法成功制备了SiO2气凝胶。
在工业上使用超临界干燥时会面临着设备过于昂贵以及相关生产成本过高等经济问题。同时,大尺寸样品在生产过程中会明显增加溶剂置换以及超临界干燥过程中泄压所需要的时间。此外,即使是以CO2作为超临界干燥的介质,其一般要达到80 Bar的高压,仍然会使生产过程面临较高的风险。因此,尽管目前超临界干燥依旧是制备气凝胶时干燥效果最理想的方法,但研究人员仍在不断探索更加安全、方便、低廉的干燥方式来获得气凝胶材料。
非超临界干燥:由于超临界干燥对设备要求高、工艺复杂,且实际操作过程中存在着安全隐患,因此在常压下对气凝胶进行干燥是目前比较热门的研究课题。常压干燥方法不仅能大大降低成本,而且能在常温常压下制备出和超临界干燥效果十分接近的气凝胶材料,具有很高的实际应用价值。因而,目前非超临界干燥技术的主要研究方向是常压干燥[77-80]。
研究人员采用含有惰性基团的硅烷修饰剂如三甲基氯硅烷 (TMCS)、甲基三甲氧基硅烷(MTMS)、甲基三乙氧基硅烷 (MTES)、乙烯基三甲氧基硅烷 (VTMS)、苯基三甲氧基硅烷 (PTMS)、苯基三乙氧基硅烷 (PTES)、二甲基二甲氧基硅烷 (DMDMS) 等对凝胶骨架进行疏水化修饰后再常压干燥,可以更好地避免空气中水汽对凝胶骨架的破坏,从而在常压下得到气凝胶材料[81-84](图8)。
Smith等人[85]最先采用常压干燥法来制备SiO2气凝胶。他们采用溶剂置换的方法使凝胶骨架的液体变为界面张力较低的溶剂,然后对凝胶孔道表面的Si-OH进行修饰,使其无法与空气中的水分子发生反应,最后将其常压静置24 h又加热至50°C处理24 h以获得最终气凝胶材料。这种方法与超临界干燥法相比,气凝胶的比表面积孔结构损失并不明显。
相对于超临界干燥而言,常压干燥在保持气凝胶微观结构的同时也有效地降低了干燥过程的危险性。但是,常压干燥依然面临着一些问题。例如,要想获得完整的气凝胶材料,其制备条件要求过于苛刻,限制了气凝胶性能的调控;而且对液体挥发速率的严格控制也使得其干燥过程过于漫长;同时凝胶修饰过程产生的强酸性副产物也是需要解决的一个难题。

图8 (a) 甲基三甲氧基硅烷 (MTMS) 和 (b) 三甲基氯硅烷 (TMCS) 的修饰过程[81]Figure 8 Modification process of (a) methyltrimethoxysilane (MTMS) and (b) trimethylchlorosilane (TMCS)
除了常压干燥之外,采用冷冻干燥也能得到结构较完整的气凝胶材料[86]。冷冻干燥是在低温、低压下使三维网络中的液体结冰成固态 (这种转变可以避免凝胶孔内的液体产生弯曲液面的张力作用),之后使固态介质直接升华,进一步消除毛细管力,从而实现凝胶的干燥。冷冻干燥是一种新型的气凝胶干燥技术。通过冷气体对流的方法使其表面温度稳定在一定范围内,能有效地避免干燥时网络结构的坍塌。但冷冻干燥的成本相对还是偏高,而且冷冻干燥得到的样品多为粉末状。
Ren等人[87]提出了一种利用机溶剂真空升华气凝胶的简便干燥方法 (图 9),成功得到了不同氧化物气凝胶材料。首先,将湿凝胶浸泡到低表面张力、易升华、高冰点的有机溶剂 (如叔丁醇、乙腈) 中,然后再在真空条件下缓慢干燥。这种方法虽然简便易行,但干燥时间较长,且获得的样品体积收缩较大,需要进一步加以改进。
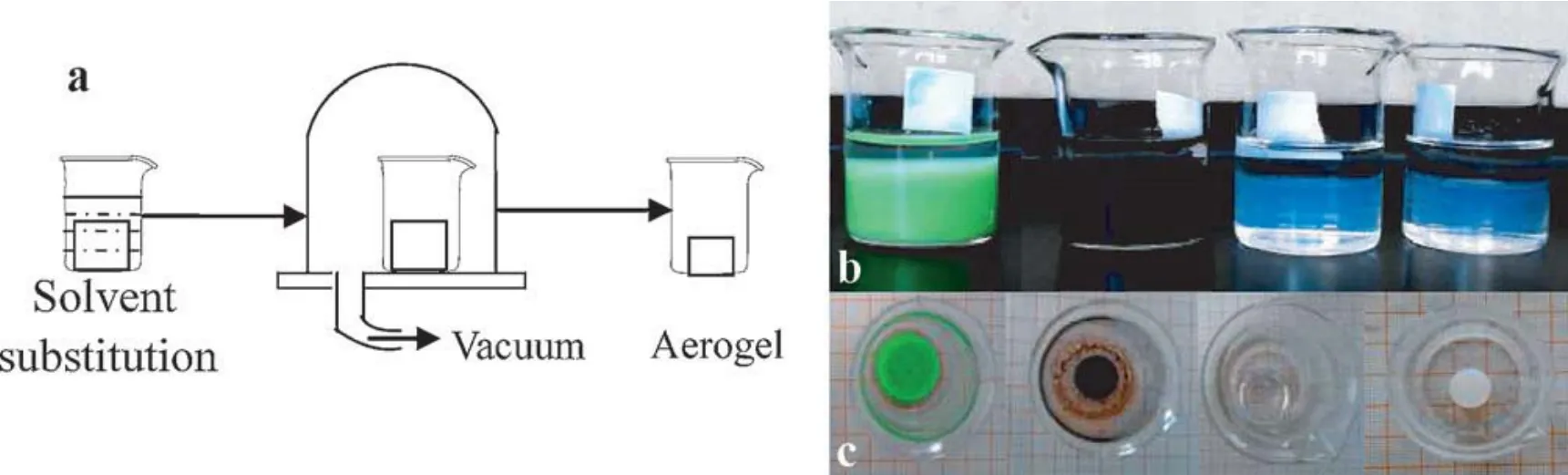
图9 有机溶剂真空升华干燥示意图[87]Figure 9 Organic solvent vacuum sublimation drying process
Smith等人[88]通过将凝胶浸入到溶剂中进行加热,所采用的溶剂自身不能进入凝胶内部,这种新型的干燥工艺被称为传导干燥。传导干燥受外部溶剂的影响较大,且干燥时其密度会逐渐降低。随着干燥的进行,部分胶体会浮在溶剂表面,不利于凝胶的进一步干燥。这种方法与传统的干燥方法相比,虽然干燥效果较好,但受到加热溶剂的局限,需选择合适的溶剂且需要在加热之前对凝胶进行一定表面处理,工艺复杂,因此目前很少利用这种方法对气凝胶进行干燥。
研究发现,利用恒沸蒸馏的方法可以脱除SiO2气凝胶中的水份并成功实现对凝胶的干燥。利用蒸馏干燥不仅能有效减弱颗粒之间的团聚和结块现象,而且蒸馏过程也不会对SiO2气凝胶的网络结构造成破坏。但这种方法干燥条件比较苛刻,目前很少采用。
总之,干燥过程中保证凝胶骨架完整性是成功制备气凝胶的必要条件,而干燥方法的简便易行则是大规模应用气凝胶的前提。
1.2 无机气凝胶的性能及应用
1.2.1热学性能
无机气凝胶的主要特征之一是其具有非常低的导热性。以 SiO2气凝胶为例,其热导率通常为0.015 W·(m·K)-1,低于相同环境条件下空气的热导率0.025 W·(m·K)-1,因而SiO2气凝胶可用作优异的绝热温材料[89],广泛应用于建筑保温,设备保温等[90]。此外,无机氧化物气凝胶是不可燃的,虽然机械性能较差,如果对其进行机械加固,在制备透明绝缘组件及采光装置上则具有巨大的应用潜力[91]。另外,SiO2等氧化物气凝胶作为绝热材料越来越多地被应用于航空领域[92]。例如,美国NASA的火星探测器Mars Pathfinder最近在执行Sojourner Mars Rover任务时就使用了气凝胶材料进行保温,在夜间温度下降到 -67°C以下时,航天器内部温度能够稳定保持在21°C左右,这样可以保证其内部的电子设备在外部温度极端低的情况下能正常运作。此外,欧洲研究协调机构 (European Research Coordination Agency, EUPECA) 的项目European Retrieval Carrier中同样也使用了气凝胶保温材料[93]。
1.2.2光学及光催化性能
SiO2气凝胶的光学透射和散射性质是其另一种重要特征,结合其热性能可制成透明的隔热物体,如窗户[94](图10)。气凝胶的这种用途首先由Pajonk提出[94]。尽管某些方向上存在一定程度的散射降低了光学性能,但SiO2气凝胶的透明度和可见光透射率非常高,例如,以TMOS为前驱体、甲醇为溶剂制得的SiO2气凝胶,在900 nm波长范围内透光率可达到93% 以上[95]。
二氧化钛材料具有优异的光催化性能,在光催化降解和太阳能电池等领域具有广阔的应用前景,TiO2气凝胶结合了气凝胶的特性和二氧化钛的催化性能已经被广泛应用于光催化降解对氯苯酚、对羟基苯甲酸[96]和水杨酸[97]等。
1.2.3声学性能
SiO2气凝胶的声学特性与其热学性质密切相关。气凝胶中的声传播取决于凝胶间隙中孔隙性质及气凝胶密度等。SiO2气凝胶是优异的隔音材料,由于声波在凝胶网络中传播的过程中波能量逐渐转移衰减,所以在振幅和速度上都大大减弱,通过气凝胶的纵向声速通常为100 ms量级,这使得 SiO2气凝胶非常适用于声学隔音装置[98]。

图10 气凝胶保温玻璃Figure 10 Aerogel insulation glass
1.2.4 机械性能
气凝胶的抗压强度、拉伸强度和弹性模量都非常低,并且在很大程度上取决于凝胶网络连接情况和凝胶密度[99]。事实上,采用一些特殊前驱体制备的多孔SiO2气凝胶可以被弹性地压缩,且压缩幅度可以达到50% 以上[100]。
目前为止研究了许多增强 SiO2气凝胶的方法,最常见的方法是老化和复合[101]。例如,以聚二甲基硅氧烷 (PDMS) 和烷氧基硅共前驱体方法获得的复合SiO2气凝胶具备很好的柔韧性。当PDMS质量分数为20% 时,将其弹性压缩至自身体积的30% 也不会发生任何损坏[102]。采用二氧化锆纤维增强二氧化锆气凝胶能克服其本身易碎的缺点,很大程度上提高了二氧化锆气凝胶的机械性能[103]。
此外,气凝胶与聚合物聚合相互交联也能大大提高其机械性能[104]。Li等人[105]成功制备了芳族聚酰胺纤维增强二氧化硅气凝胶复合材料 (AF/气凝胶),其具有低密度,显示出优良的柔韧性和保温性能。三点弯曲实验表明,可以通过约5% 的纤维含量实现柔性的改善而不降低其隔热性能。但随着使用时间的延长,气凝胶的抗压强度和弹性模量增加,而断裂应变下降,其亚临界裂纹扩展符合应力腐蚀机制[106]。如果对气凝胶进行疏水修饰则可大大降低其裂纹扩展速度[107]。
Shao等人[108]用硅酸钠与共前体甲基三乙氧基硅烷 (MTES) 混合,然后通过离子交换过程来消除钠杂质,再采用正己烷稀释的三甲基氯硅烷 (TMCS) 进行修饰,得到的二氧化硅气凝胶体积收缩率小于10%,表现出优异的物理性能。尽管其显示低密度和脆性特征,但其机械性能在某些特殊场合具有很好的应用前景。例如,它们的良好压缩性可以有效地用于吸收在压缩冲击中的动能[109]。
SiO2气凝胶是能够有效地限制几个 eV等离子体低冲击的阻抗材料,可以用于捕获高冲击压力下产生的冷冻矿物,或作为介质来研究需要X射线诱导流体的混合冲击[110,111]。
1.2.5吸附和存储性能
氧化物气凝胶由于具有高孔隙率,因而可有效地用于捕获各种发光分子或纳米颗粒[112-114]。Kim等人[115]提出了空心硅胶气凝胶液滴模型,Jang等人[116]将氧化物气凝胶成功地应用于流体的惯性约束。
氧化物气凝胶的可控孔径和高比孔容使得其具有药物释放或向环境释放农药的功能[117]。
气凝胶也可用于吸附或提取一些化合物,例如处理废水、限制放射性废物或过滤气体等[118]。而烧结后机械性更强的气凝胶则可储存或运输液体,如利用SiO2气凝胶进行储存作为火箭燃料的不对称1,1-二甲基肼 (UDMH)[16]。
采用掺杂的方式也可以使气凝胶获得优异的性能,Owens等人[119]在 SiO2气凝胶中掺杂金属钒和铜并结合超临界干燥技术制备了具备吸附性能的SiO2气凝胶,其在NOx等气体的脱除方面的具有广泛应用。研究同时表明,掺杂多种金属的SiO2气凝胶稳定性会更好[119]。
此外,有些气凝胶颗粒也可以用作复合材料的分散相以增加材料的硬度、耐磨性[120]。
2 有机气凝胶
2.1 有机气凝胶的制备工艺
自20世纪80年代末Pekala等人[23]以间苯二酚和甲醛为原料首次成功合成了间苯二酚-甲醛 (RF)有机气凝胶以来,近年来又相继制备出许多不同种类的有机气凝胶,如由三聚氰胺和甲醛合成三聚氰胺-甲醛 (MF) 气凝胶[121]、由线性酚醛树酯和糠醛合成出的酚醛树酯-糠醛 (PF) 气凝胶[122]等。
有机气凝胶制备过程与无机气凝胶制备过程相似,采用有机物单体或低聚体溶于溶剂中,经过化学反应生成链状或无序枝状网络结构,经溶胶-凝胶过程实现凝胶化;溶剂置换后,再经超临界干燥除去溶剂得到干燥后的气凝胶。下面简单介绍研究最多的MF和RF气凝胶制备方法。
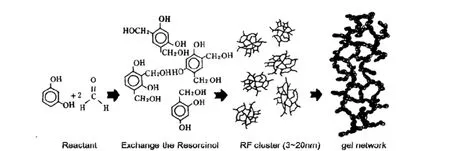
图11 RF凝胶的溶胶-凝胶聚合过程[23]Figure 11 Sol-gel process of RF aerogels
2.1.1 RF湿凝胶的制备
RF凝胶的制备过程如图11所示[23,123],由间苯二酚 (R) 和甲醛 (F) 经溶胶-凝胶过程聚合得到湿凝胶,二者按质量比1:2混合并加入适量去离子水配成溶液,同时加入适量碱 [如Na2CO3、Ca(OH)2等] 作为催化剂进行亲电取代反应。由于亲电取代反应较为迅速,同时又有催化剂残余,因而在反应初期会生成大量的羟甲基取代物,这些羟甲基取代物通过相互之间的脱水缩聚反应生成粒径约为3 nm ~ 10 nm的聚合簇。此类聚合簇表面仍存在大量的官能团。在进一步的反应中,聚合簇之间通过表面官能团进行进一步缩和,形成三维网络状结构,即完成凝胶化过程。但是,此时的凝胶无论在表观的凝胶强度还是其内部交联程度上都较弱,因此在凝胶形成之后必须对凝胶进行老化处理。通常在凝胶中加入老化剂 [有机类的老化剂通常为三氟乙酸 (CF3COOH) 等],或者直接将凝胶静置一段时间使其自然老化。在老化过程中,骨架上的表面官能团将进一步交联,对已经形成的网络状结构起到增强作用,最终形成 RF湿凝胶。过程中涉及的反应有:间苯二酚与甲醛反应形成单元或多元羟甲基间苯二酚、羟甲基间苯二酚经脱水缩合形成以亚甲基桥或亚甲基醚桥为连接的聚合簇、聚合簇之间通过表面官能团之间的反应,相互交联或者物理缠绕形成三维网络状体结构。
2.1.2 MF湿凝胶的制备
MF凝胶由三聚氰胺 (M) 与甲醛 (F) 缩聚而成,可通过两种途径合成:
(1) 单体途径:三聚氰胺与甲醛以 1:3.7的质量比混合,加入去离子水作为反应溶剂,同时控制反应物含量,以求得到不同密度的湿凝胶,其间加入适量的碱作为初始反应催化剂,混合液被加热使三聚氰胺完全溶解,冷却至室温后再加入盐酸调节pH值为1.5 ~ 1.8,密闭后加热反应一定时间即可得到MF湿凝胶。
(2) 齐聚体途径:被甲醛部分羟甲基化的三聚氰胺低分子量缩合物用适量去离子水稀释,用盐酸调节pH值为1.8 ~ 2.3,于50°C下加热1 d,然后再于95°C下加热5 d,即可得到MF湿凝胶,然后经溶剂置换处理得到体系内不含水的MF湿凝胶。
图12所示为单体途径的凝胶化反应过程[122]。MF湿凝胶形成过程中,先是甲醛与三聚氰胺中三个氨基形成羟甲基取代物,酸化过程促进其进一步缩合,形成二氨基亚甲基桥和二氨基亚甲基醚桥,最终交联成三维网络状结构,完成凝胶化过程。
2.1.3有机无机复合凝胶的制备
溶胶-凝胶法是目前制备有机无机复合凝胶的主要途径,可以分为以下几类[37,55,124-134]:
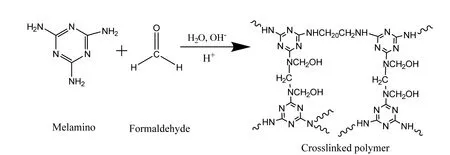
图12 MF凝胶的溶胶-凝胶聚合过程[122]Figure 12 Sol-gel process of MF aerogels

图13 硅凝胶表面氨基接枝反应 [104]Figure 13 Grafting reaction of silicon aerogel [104]
(1) 有机物直接掺入到溶胶-凝胶基质中是制备有机无机复合材料最直接的方法。无机前驱体在有机化合物溶液中发生水解缩合形成无机网络,将有机物包埋在无机网络中;或者无机前驱体先进行水解缩合得到多孔的无机网络,然后将其浸渍在有机物溶液中,使有机物进入凝胶的孔隙而得到有机无机复合材料。若是有机聚合物单体,还可通过热激发或紫外光激发使单体聚合。图13所示为Capadona等人[104]研究的硅凝胶表面氨基接枝反应图。
(2) 原位产生的无机粒子填充在聚合物中。这种合成方法通常是无机前驱体在聚合物溶液中原位水解缩合形成纳米级颗粒,直接填充在聚合物中。这种方法能有效地防止粒子的团聚,均匀性好,粒子分散程度高。在一定范围内,随着无机物含量的增加,材料的拉伸模量和拉伸强度增加,断裂伸长减小。
(3) 同时形成有机无机网络。在同一体系中,无机单体水解缩合形成无机网络,同时有机单体通过自由基聚合或开环聚合形成有机网络,即同时形成有机无机复合网络。调节催化剂或引发剂的浓度可以控制有机和无机聚合反应的速度,从而控制材料的微观结构。该方法可以将溶胶-凝胶溶液中完全不溶的聚合物均匀地结合到无机物中。
2.1.4 其他有机气凝胶的制备
其他有机聚合物各有不同的凝胶机理。
(1) 果胶必须在具有足够的糖和酸存在的条件下才能凝胶。当果胶溶液pH值足够低时,羧酸盐基团转化为羧酸基团,分子不带电荷,分子间斥力下降,水合程度降低,分子间能够彼此亲近,缔合形成凝胶。而糖的作用则是夺取果胶分子链上的水分子,使得分子链溶剂化程度下降,分子链间相互作用,形成三维网状结构,把水和溶质固定在网孔中,从而形成凝胶。
(2) 卡拉胶由硫酸基化或非硫酸基化的半乳糖和3,6-脱水半乳糖通过α-1,3-糖苷键和β-1,4-糖苷键交替连接而成,多糖链中总硫酸酯基含量为15% ~ 40%。这些硫酸酯基使得分子半径变大,旋转阻力增强,分子间的相互作用也增强,从而黏度提高,凝胶强度增大。卡拉胶稳定性强,干粉长期放置不易降解。它在中性和碱性溶液中也很稳定,即使加热也不会水解,但在酸性溶液中 (尤其是当pH值 ≤ 4.0时) 卡拉胶易发生酸水解,凝胶强度和黏度下降。值得注意的是,在中性条件下,卡拉胶在高温长时间加热也会发生水解,导致凝胶强度降低。
(3) 海藻酸盐是由 (1→4)-β-交联的 D-甘露糖醛酸和 (1→4)-α-交联的古洛糖醛酸组成的长链聚合物。1个海藻酸盐分子往往存在3区,即“M区”(富含甘露糖醛酸区)、“G区”(富含古洛糖醛酸区) 和“MG区”(两种糖醛酸都有)。Ca2+和其他二价阳离子易与 G区结合,故海藻酸钙凝胶被认为是一种由Ca2+把长链分子的G区相互交联起来的一种三维网络分子[135]。
(4) 通过老化以及稀释水凝胶或醇凝胶中的几丁质溶液可以形成甲壳质凝胶[136];同时 pH值转换或醛类的加入,也可以形成壳聚糖凝胶。
2.1.5 湿凝胶的干燥
为了最大限度地减少凝胶在干燥过程中基本网络结构的收缩坍塌,以获得与湿凝胶骨架结构相似的气凝胶,目前几种可行的干燥方法包括:冷冻干燥法、凝胶改性后的常压干燥法以及超临界干燥法等。
2.2 有机气凝胶的种类及应用
2.2.1 树酯基气凝胶
1991年Pekala[137]首次以三聚氰胺和甲醛为原料制备出三聚氰胺-甲醛 (MF) 气凝胶,并使其密度在 100 kg·m-3~ 800 kg·m-3之间实现可控,比表面积约为 1000 m2·g-1。1995 年 Pekala[23]第一次通过Na2CO3催化间苯酚与甲醛的溶液缩聚制备了酚醛 (RF) 气凝胶。制备RF气凝胶最重要的参数是催化剂浓度和溶液的 pH值,样品的密度、比表面积以及颗粒和孔尺寸等性能都会受到这两个因素影响。不同的催化剂也可用于制备 RF气凝胶[18]。随后人们陆续制备出了其他前驱体的树酯基气凝胶,如酚醛树酯-甲醛、间苯酚-糠醛等[122,138]。然而,由于具有良好的成型性,易于控制显微结构和性能可调, NaCO3催化的 RF气凝胶和相应的溶胶-凝胶法迄今为止仍被广泛应用。2007年Mulik[139]发现以丙酮为溶剂,利用盐酸催化可大大提高生产效率。
RF气凝胶具有热导率低、耐热性好、力学性能好、难燃、吸水率低、电绝缘性优良等优点,适合于一些特殊场合用作隔热保温材料。在阻燃、隔热方面,酚醛树酯可以长期工作,瞬时工作温度可达 1000°C,在耐热方面也优于聚氨酯发泡材料。此外,RF气凝胶与其它材料通过共混改性还可以制备出性能优良的复合保温材料。
2.2.2多糖类 (纤维素基) 气凝胶
多糖类物质来源广泛,成本低廉,也是制备有机气凝胶的理想材料。
Kistler[10]在1931年首先用多糖 (琼酯、硝化纤维素和纤维素) 制备气凝胶,并发起了扩展这项研究的挑战,声明“我们看不出为什么这个名单不能无限期地延伸”。从那时起,许多研究工作开始集中于制备多糖类气凝胶。
气凝胶具有大的比表面积和特定的开孔结构,是活性物质 (特别是药物) 的优良载体。二氧化硅气凝胶作为药物输送系统[140,141]就是因为其具有较大的比表面积,可以达到高的药物负荷[142]。然而,生物相容性好的二氧化硅基质不是可生物降解的,这不利于其在药学上的应用。多糖气凝胶可生物降解,并且易于在干燥条件下负载高活性化合物,因此研究人员对于多糖气凝胶在药物输送和生物医学系统方面的优异性能产生了极大的研究兴趣。
同时,多糖基气凝胶的载药性能还可以通过与无机材料的复合而得到进一步提升[143]。形成的复合气凝胶可以具有无机材料的机械性能、生物聚合物的功能以及多糖基气凝胶的生物可降解性、高孔隙率和大的表面积等固有性质。此外,使用这些复合气凝胶可以提高多糖基气凝胶中官能团的含量[144]。
对可生物降解材料的表面微结构、形貌和尺寸的精确控制是多糖基气凝胶用于组织工程的重要挑战[145-148]。通过创造一个精确的微环境来促进组织发育是构造多糖基气凝胶多孔网络结构的一个解决办法[148-150]。最近报道了多糖 (壳聚糖) 组织工程气凝胶的制备[151]。但是如何将气凝胶的孔径分布控制在目标值这方面仍有待进一步研究。
2.2.3 纤维素
纤维素是地球上最丰富的可再生资源,将成为未来的主要化学资源。通常,纤维素凝胶通过纤维素在LiCl/DMAc、NMMO、碱/尿素或硫脲体系以及离子液体等中的溶解和溶胶-凝胶过程、超分子组装而形成[152]。随着对环保和生物相容性产品需求的不断增长,基于纤维素的许多新功能材料被逐渐开发出来。Tan等人[121]发现通过用交联剂交联纤维素凝胶骨架,气凝胶 (干凝胶) 易于成形,机械性能显著提高。纤维素气凝胶可通过物理和化学改性制备出不同功能、不同形状的材料,如块状体可做为隔热材料,膜状体材料可应用于吸附、药物缓释等方面,圆型球状体材料可将其他功能化分子包埋制备具有磁性等功能凝胶材料。导电材质和纤维素气凝胶复合形成的复合导电材料同时具有相容性、易降解特性和导电性。Liew等人[137]采用氢氧化钠/尿素/水作为混合溶剂溶解纤维素,以再生纤维素凝胶膜作为反应基体,利用成膜之后的三维网络空隙作为反应器进行原位聚合反应,最终形成纤维素/聚吡咯复合导电材料。此项工作为制备环保型复合导电材料提出了一种新的思路。
东华大学俞建勇课题组提出一种超轻超弹 (聚丙烯腈) 纤维气凝胶的制备方法[153],经中国计量认证结果显示,该“纤维气凝胶”固态材料密度仅为 0.12 mg·cm-3,其压缩回弹性能十分优异,经过上千次压缩后塑性形变仅为14.5%,相比于传统的碳气凝胶,其压缩回弹性能提升了110%。除了超轻和超弹特性,纤维气凝胶还展现了其它优异性能,例如其导热系数低至0.026 W·(m·k)-1,接近于室温条件下空气的导热系数。一块5 mm厚的“纤维气凝胶”可以轻松实现在100 Hz ~ 6300 Hz宽频段内的高效吸音。超轻多孔的纤维气凝胶还是一种高性能的吸附材料,可快速吸附自身重量200倍以上的液体污染物,有望为近年来频发的海上石油污染灾害提供新的解决途径。除了上述应用,这种超轻的“纤维气凝胶”材料还可应用于组织工程、电子器件等领域 (如图14)。
纤维素气凝胶还具有优异的吸附性能。Jiang 等人[154]制备了两亲性的自组装纳米纤维素气凝胶(图15),其中亲水性气凝胶对水和氯仿的吸附量分别为210 g·g-1和375 g·g-1,经辛基三乙氧基硅烷处理后可以获得疏水性纤维素气凝胶,它对非极性烃类化合物、极性非质子溶剂和油的吸附量范围在 139 g·g-1~ 356 g·g-1。Korhonen等人[155]制备出了疏水性纳米纤维素气凝胶 (如图 16所示),对多种有机物如甲苯、氯仿、己烷、辛烷、辛醇、十二烷、十六烷、石油苯、石蜡油和矿物油等的吸附量达到 20 g·g-1~ 40 g·g-1。

图14 超轻纳米纤维气凝胶[153]Figure 14 Ultralight nanofiber aerogels
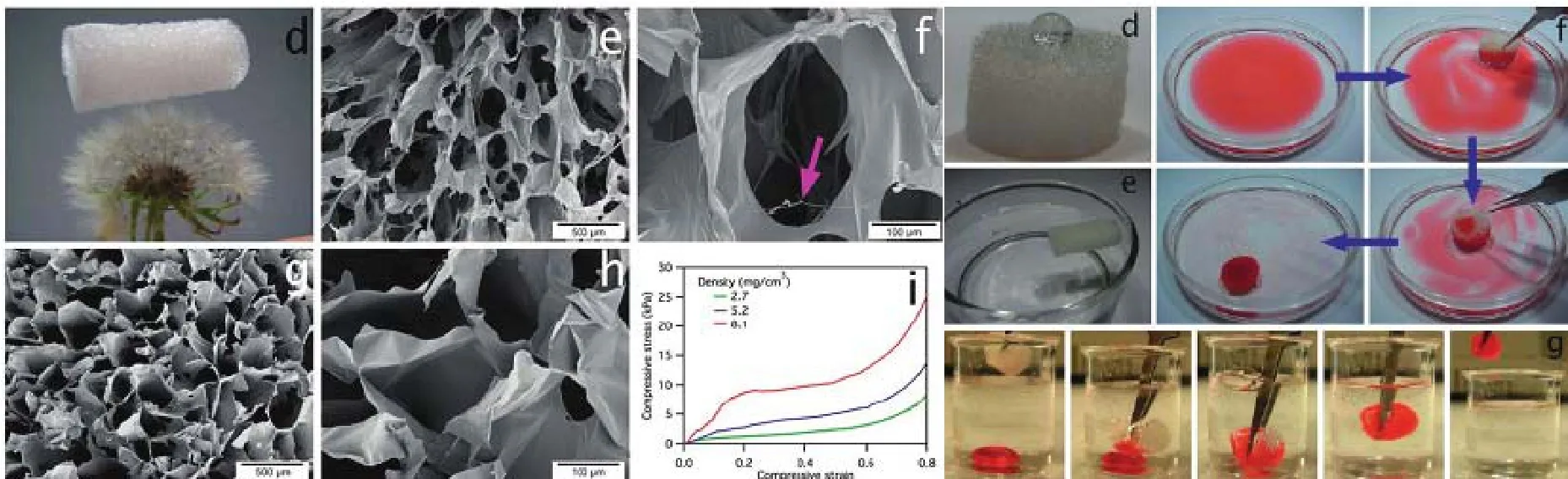
图15 Jiang报道的两亲性碳气凝胶作为超强吸附剂[154]Figure 15 Amphiphilic superabsorbent cellulose nanofibril aerogels reported by Jiang

图16 Korhonen报道的疏水性纳米纤维素气凝胶作为可回收吸油材料[155]Figure 16 Hydrophobic nanocellulose aerogels as recyclable oil absorbents reported by Korhonen
2.2.4淀粉气凝胶
直链淀粉和支链淀粉是淀粉的两个主要成分。这些组分的相对比例因淀粉来源 (例如马铃薯、玉米、小麦、木薯淀粉) 的变化而变化,并影响多糖的结晶度和分子顺序。
淀粉凝胶化主要包括以下三步:(1) 通过亲水淀粉颗粒吸附水发生膨胀[156];(2) 通过加热溶解淀粉后,观察到糊化,导致直链淀粉分子浸出,发生不可逆的物理变化和颗粒结构的破坏;(3) 最后,在冷却和老化后形成淀粉水凝胶结构,随后进行重组以及多糖结构的部分再结晶。
直链淀粉含量和胶凝温度是影响凝胶形成的主要工艺参数。直链淀粉分子在糊化期间与淀粉颗粒分离,在凝沉时它们重新结合并沉积在支链淀粉上。直链淀粉是向所得淀粉凝胶提供无序(无定形) 特征的成分,有助于在材料中产生介孔,而有序支链淀粉对局部结构排序施加一定的控制作用。此外,直链淀粉含量越高,凝沉速度越快。高凝胶化温度促进直链淀粉从颗粒中的释放,高于一定值时,所得气凝胶的结晶度、刚度和密度将会发生变化[142,157]。在凝沉过程中,由于成核速率 (结晶度) 低于结晶速率 (晶体生长)[158],凝胶中的低冷却温度容易达到更高的表面积。为了避免干燥过程中孔结构的坍塌及颗粒的聚结,淀粉凝胶的过程中需要进行水和乙醇的溶剂交换[159]。采用超临界干燥可以获得来自不同前体 (例如马铃薯和玉米) 的淀粉气凝胶 (图17)。
2.2.5果胶气凝胶
果胶是一种含有数百至约1000个脱水半乳糖醛酸残基的线形多糖聚合物。
果胶可以通过热、酸或阳离子处理进行凝胶化。果胶类型以及凝胶化过程的选择显著影响到所得凝胶的纳米结构[160]。实际上,每种果胶类型的酯化程度和甲氧基酯的分布决定了聚合物链之间的主要相互作用 (氢键、疏水和离子相互作用)[161]。加热可以促进果胶在水中的溶解,并且在冷却到凝固温度以下时,通过果胶分子上的游离羧基以及相邻分子的羟基进行凝胶化。最后,低甲基酯化的果胶需要借助阳离子与半乳糖醛酸的相互作用通过“蛋盒”凝胶化模型机制与二价阳离子 (通常为Ca2+) 结合形成凝胶[160-162]。添加10 wt% ~ 20 wt% 的糖可能有助于减少凝胶收缩,并且使凝胶更坚固。果胶凝胶用乙醇溶剂交换后,经超临界干燥,便具有高表面积和孔隙率[163],避免了使用其它干燥技术导致的大量收缩。
2.2.6海藻酸盐
藻酸盐凝胶的性质最主要受交联离子含量 (主要为二价阳离子) 的影响。可以通过将藻酸盐溶液滴入阳离子溶液 (扩散法)[164-166]或通过控制释放藻酸盐溶液中的交联离子 (这些交联离子已经经过惰性处理分散在藻酸盐溶液中) (内部凝固法)[135,167]添加交联离子。海藻酸盐凝胶也可以通过降低藻酸钠溶液[168]或天然海藻酸[169]的pH来形成。藻酸盐凝胶的收缩主要发生在水-乙醇溶剂交换期间,并且可以通过交换步骤和频率来控制[157]。凝胶中乙醇浓度的增加推动水从凝胶结构中伴随释放,导致凝胶孔中的表面张力降低[157]。凝胶结构的毛细管压力的下降是藻酸盐凝胶收缩的原因。通过多步骤和低频率的溶剂交换降低凝胶中水分的扩散速率,减少凝胶的收缩。文献报道了藻酸盐气凝胶的不同形态:整料,珠粒和微球体,如图18所示。
2.2.7几丁质与壳聚糖气凝胶

图17 淀粉气凝胶Figure 17 Starch aerogels

图18 藻酸盐气凝胶的不同形态:整料[142],珠粒和微球体[135]Figure 18 Calcium-alginate aerogel obtained in different shapes: (a) monoliths, (b) beads; (c) microparticles
几丁质 (又称甲壳素) 是一种丰富的自然界线性氨基多糖,由 N-(乙酰氨基葡萄糖) 单元通过β-(1,4) 键连接形成。几丁质由于其基于强氢键的高结晶度而难溶于常规溶剂,但可以使用一些特殊的有机溶剂 (例如浓甲酸、氯化钙脱水饱和甲醇、氯化锂与N,N-二甲基乙酰胺混合物等[170,171]) 溶解。因此,几丁质凝胶可以通过简单的老化或通过大量的水 (水凝胶) 或酒精 (Alcogel)[136]稀释得到的几丁质溶液来形成。同时,几丁质水凝胶也可以从再乙酰化壳聚糖的水性醇溶液中获得[172]。在与醇溶剂交换后,通过将几丁质凝胶进行超临界干燥,可以获得具有高孔隙率、高表面积和低密度的几丁质气凝胶[170]。
壳聚糖是几丁质 (即甲壳素) 脱N-乙酰基的产物,通过甲壳素脱去55% 以上的N-乙酰基获得,易溶于稀酸 (pH < 6)。壳聚糖的胶凝性质主要受去乙酰化程度和壳多糖前体来源的影响[173]。壳聚糖的物理水凝胶可以通过在碱性溶液中沉淀酸性壳聚糖溶液获得[168]。老化一定时间后,用蒸馏水将壳聚糖凝胶洗涤数次,直到 pH达到中性[174]。经过水-乙醇溶剂交换后,在超临界条件下干燥凝胶,整个过程中体积收缩率为 60%[173]。此外,文献还报道了使用单醛和二醛作为交联剂在酸性溶液中制备壳聚糖的化学水凝胶[175]。在室温老化和乙醇溶剂交换后,超临界干燥制备的壳聚糖气凝胶随着壳聚糖浓度的增加而显示出表面积增加的介孔结构。通常,从化学凝胶获得的壳聚糖气凝胶具有比从物理凝胶获得的更好的结构性能。
各类有机气凝胶的基本结构性质列于表3。
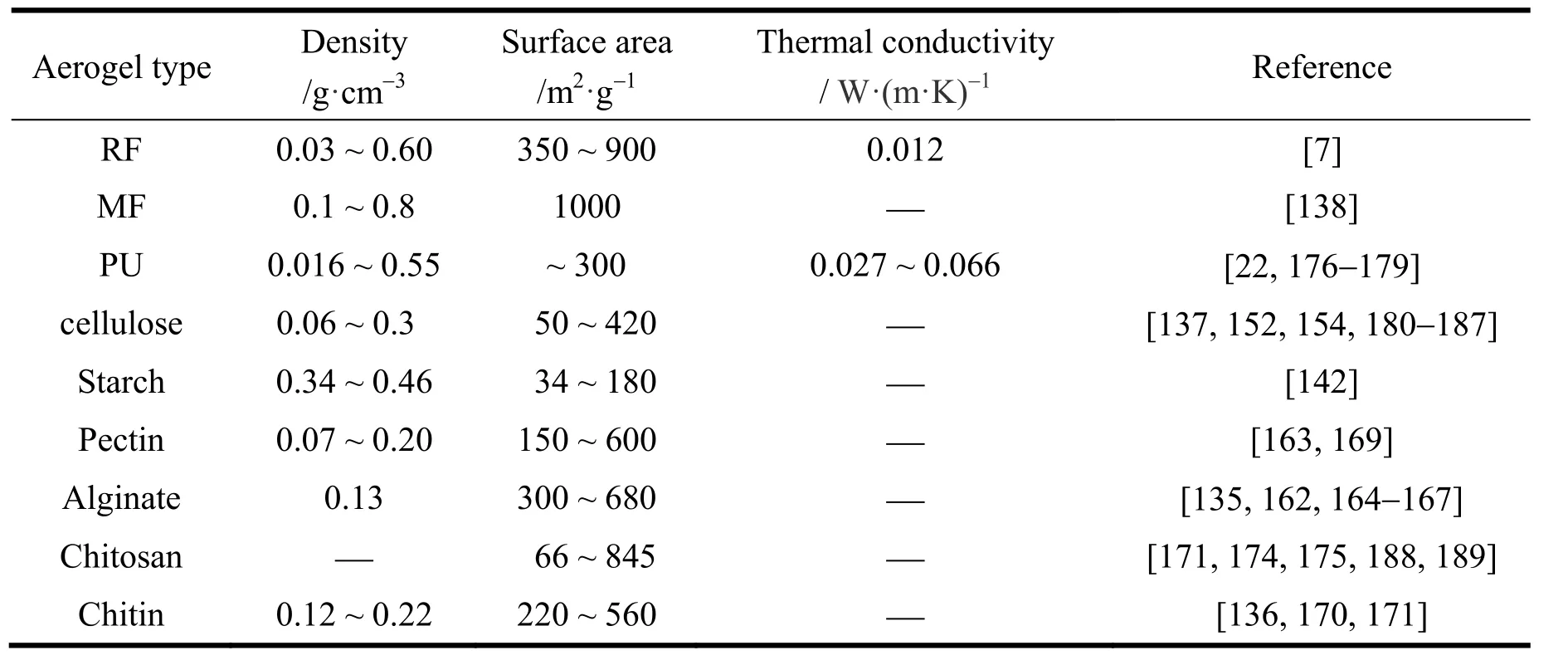
表3 部分有机气凝胶的结构性质Table 3 The structure and properties of organic aerogels
2.2.8 有机无机复合凝胶
材料复合化是现代材料发展的新趋势。将两种或两种以上功能材料进行复合,可以有效达到功能互补的目的。改善硅气凝胶脆性大、柔韧性差的方法之一就是引入有机基团或者有机聚合体。通过溶胶-凝胶法制备的有机无机复合硅材料可以使无机硅网络和有机网络的界面面积变得非常大,界面之间的作用力更强,使尖锐的界面变得模糊,甚至使无机网络和有机网络达到分子水平复合,使复合的新型有机硅材料同时具有无机和有机材料的优良性能。
用于复合凝胶的有机气凝胶有PVA[190-193]、PU[194]、纤维素等。
将硅气凝胶与纤维复合则可以在力学性能、阻燃性能方面对硅气凝胶进行显著的改善[195,196]。目前已经报道的复合无机有机气凝胶多以SiO2为基体。Sai[197-199]等人将纤维素与 SiO2复合形成复合气凝胶,提升了SiO2气凝胶柔韧性和力学性能,该复合气凝胶对乙醇、丙醇、己烷、甲苯和二氯甲烷等有机物具有优异的吸附特性,吸附量约为 185 g·g-1(图 19)。SiO2气凝胶填充纤维骨架后,对SiO2凝胶骨架的脆性有一定的改善。这主要是因为SiO2气凝胶/多孔骨架复合材料可以看作是纤维增强SiO2气凝胶复合材料,当基体裂纹扩展至纤维时,应力集中导致结合较弱的纤维与气凝胶基体的界面解离,在进一步应变时将导致纤维在弱点处断裂,随后纤维的断头从基体中脱出。纤维的断裂和脱出增加了能量的消耗,使得材料的脆性得到了一定改善。
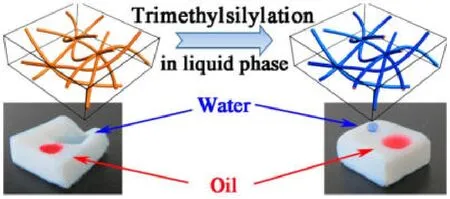
图19 Sai报道的三甲基硅烷疏水性细菌纤维素气凝胶用于油水分离[199]Figure 19 Trimethylsilylation modification of bacterial cellulose aerogels for oil/water separation reported by Sai [199]
3 碳气凝胶
3.1 碳气凝胶的制备工艺
最早碳气凝胶的制备通常是采用热解方法,如最早的碳化 RF (间苯二酚和甲醛) 气凝胶 (简称CRF气凝胶)[23]以及1996年Hanzawa等人[24]采用CO2活化碳骨架来获得具有超高比表面积的新型CRF气凝胶等。
随着碳纳米管和石墨烯的兴起[26-30],碳纳米管气凝胶和石墨烯气凝胶开始出现。最初是通过冷冻干燥单壁碳纳米管的悬浮水溶液来得到块状的气凝胶 (图 20)[200],但是由于悬浮的碳纳米管之间作用很弱,制备得到的气凝胶较脆,易碎裂。这种现象主要是因为通过酸处理原始碳纳米管得到均一的分散液,在一定程度上削减了最终产品的机械强度。采用聚乙烯醇为添加剂可以极大地改善碳纳米管气凝胶强度,所制备的碳纳米管气凝胶可以承受大于自身 8000倍的重量。随后,Aliev等人[201]从多壁碳纳米管中提取碳纳米管气凝胶片层来合成人造肌肉,这种人造肌肉在80 K到1900 K温度下可以提供大约为220% 的伸长以及每秒 (3.7 × 104)% 的延伸率,具有优异的超弹性。Worsley等人[202-205]制备出了碳增强的单壁碳纳米管气凝胶,其机械性能也有较大的改善。而之后Islam课题组[206]则通过包覆石墨烯来改善单壁碳纳米管气凝胶的强度,结果发现石墨烯包覆的碳纳米管气凝胶机械强度和弹性均有了较大的提升。这个发现为此后石墨烯气凝胶的产生奠定了坚实的基础。

图20 单壁碳纳米管气凝胶的SEM图像[200]Figure 20 SEM of single-walled carbon nanotube aerogel
2009年,Wang等人[207]首次合成出了导电的石墨烯气凝胶。之后,许多研究者证明了单个碳原子厚度的石墨烯具有优异的弹性[208,209],这就促进了石墨烯制备方法的研究,如水热还原法[210-215]、化学还原法[216-219]、电化学合成法[220,221]、“Breath Figure”法[222,223]以及模板导向CVD法[224]等。研究石墨单体的工作主要集中于机械强度及吸附性能。Qiu课题组[225]采用化学转换的方法制备出了超轻且高度可压缩的石墨烯气凝胶。Ling等人[226]合成出了仿生的超弹性石墨烯基气凝胶块体。
碳气凝胶的制备工艺主要可以分为两类:一类是先采用溶胶-凝胶法制备有机气凝胶,之后在高温及惰性气氛下进行热解制备 (如CRF气凝胶的制备);另一类则是采用先制备初级组成单元,之后采用物理或化学方法将组成单元进行交联,再干燥获得相应的碳气凝胶 (如碳纳米管气凝胶及石墨烯气凝胶)。
第一类方法主要用于CRF气凝胶的制备。优异的成型性、微观结构的易控性以及可调节性使得这种制备方法在当前仍然有广泛的应用[40]。然而这种方法所需的高温条件在一定程度上限制了其大规模的应用。
第二类方法主要用于碳纳米管气凝胶及石墨烯气凝胶的制备。但就碳纳米管气凝胶而言,这类方法又可以分为化学气相沉积或催化热解直接合成以及液相处理碳纳米管粉末再进行干燥两类。
对于化学气相沉积或催化热解直接合成方法,化学气相沉积 (Chemical Vapor Deposition, CVD)技术能够有效地生长高质量、有序的碳纳米管薄膜或者各向同性的块体,产品具有优异的机械和导电性能[227,228]。Lin等人[229]发现采用二氯苯为碳源可以打破碳纳米管生长过程中的有序性,从而形成三维的随机堆积形貌。Hata课题组[230-232]也采用CVD技术合成了橡胶状的弹性碳纳米管宏观泡沫,其热稳定性的温度范围在 -196°C到1000°C之间。一般都是采用平板的基体来进行碳纳米管的CVD生长,但是各向同性的碳纳米管宏观结构也可以通过采用三维的催化剂模板来制备[233]。2009年,He课题组[234]就采用催化剂随机分散的模板方法制备出各向同性的多壁碳纳米管块体。相似的,静电纺丝的Ni纳米纤维模板也被用于制备三维碳纳米管网络结构[235]。但是采用CVD方法如何在生长过程中原位控制碳纳米管的类型仍然是个挑战,同时也很难做到除去剩余催化剂的同时保持原有的多孔结构。
相对而言,从碳纳米管的悬浮液中制备碳纳米管气凝胶则是一种低成本且可规模化的有效方法,同时还可以调节其微观结构[200,236-238]。典型的制备过程包含三个阶段 (如图21所示):首先,碳纳米管粉末以及高化学活性、可溶性的前驱体均一分散在溶液或有机溶剂中形成胶体溶液 (溶胶);其次,溶胶开始水解形成整体的网络结构 (凝胶);最后,通过空气干燥或冷冻干燥凝胶得到多孔碳纳米管气凝胶。
Islam课题组[239]采用溶胶-凝胶法制备了单壁碳纳米管气凝胶。纯化的单壁碳纳米管气凝胶先均匀分散于蒸馏水中 (十二烷基苯磺酸钠作为表面活性剂),再经过超声、离心、浓缩、溶剂置换以及超临界干燥后,得到密度为7.3 g·m-3的超轻气凝胶。这种方法可以制备出不同形状的气凝胶块体,如圆柱体、立方体以及圆锥体等。单壁碳纳米管相互交联形成多孔且各向同性的结构,具有高的比表面积以及优异的机械性能。除了超临界干燥,其他方法如在空气中缓慢干燥以及冷冻干燥[240-242]都可以被用来制备碳纳米管气凝胶。
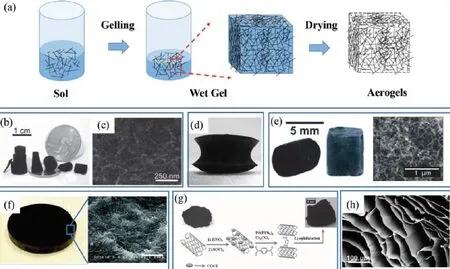
图21 溶胶-凝胶组装制备碳纳米管气凝胶[233]:(a) 碳纳米管气凝胶的制备过程[243]; (b) 不同形状和大小的碳纳米管气凝胶[243]; (c) 碳纳米管气凝胶的电镜图像 (多孔形貌) [239];(d) 空气干燥多壁碳纳米管悬浮液制备得到的双曲面形状的气凝胶[240];(e) 纯碳纳米管气凝胶 (左) 和PVA增强的碳纳米管气凝胶 (中) 的照片以及PVA包覆的碳纳米管的电镜图像[200];(f) 氟化多壁碳纳米管去氟化的完整固体的照片以及其相应的电镜图像[244];(g) 从粉末合成碳纳米管气凝胶[245];(h) 多壁碳纳米管气凝胶蜂巢状结构的电镜图[243]Figure 21 Preparation of CNT aerogels by sol-gel assembly: (a) Illustration of the process in which a dispersed CNT suspension (sol) is converted into a wet gel and then an aerogel by freeze-drying; (b) Photograph of as-prepared CNT aerogels in different shapes and sizes; (c) SEM image of the aerogel showing a porous CNT network. Reproduced with permission; (d) A hyperboloid shape aerogel formed by air-drying MWNT slurry;(e) Macroscopic blocks of a pristine (left, black one) and PVA-reinforced CNT aerogel (right, gray one), and SEM image of PVA-coated CNTs; (f) Photograph of an orbiculate solid by defluorination of fluorinated MWNTs and corresponding SEM image; (g) Synthesis of CNT aerogels from powders; (h) SEM image of a MWNT aerogel with a honeycomb porous structure.
相比于CVD生长的碳纳米管海绵,从粉末悬浮液制备出的碳纳米管气凝胶一般强度较低并且结构稳定性也较差,因而通常需要引入聚合物或粘结剂来制备增强型的气凝胶[246]。冷冻干燥制备的单壁碳纳米管气凝胶通常易碎,但添加聚乙烯醇[200]后制备出来的气凝胶强度和弹性都有很大的提升。聚乙烯醇通过包覆在碳纳米管表面或管间的结点处来增强碳纳米管网络。其他粘结剂如聚二甲硅氧烷[247]和六方氮化硼[248]都发现具有相似的增强效应。但添加聚合物或粘结剂可能会带入杂质,增大密度并且降低孔隙率,从而降低了相应的性能。例如,加入聚乙烯醇的单壁碳纳米管气凝胶密度增大了近两倍。此外,也可以通过在纳米管之间构建化学键的方式来提升气凝胶的机械性能。Zou等人[243]通过化学键合的方式形成蜂巢的形貌,通过冷冻干燥制备出气凝胶。由于其各向异性的蜂巢结构,气凝胶具有许多独特的性质如超轻的密度 (4 g·cm-3)、大的比表面积 (580 m2·g-1)、优异的电导性及机械性能。
除了碳纳米管,溶胶-凝胶法也通过化学或热交联的方式被广泛地用来组装剥离石墨烯氧化物片层形成块状的多孔气凝胶[226,249]。最初的石墨烯气凝胶就是通过真空热还原石墨烯氧化物气凝胶的方式得到的[207]。2011年,Worsley等人[250]通过碳化RF交联的石墨烯氧化物气凝胶制备出了石墨烯气凝胶。Hu等人[251]先将石墨烯氧化物均一地分散在乙二胺溶液中,组装成石墨烯水凝胶,然后利用微波辐射消除官能团以形成超轻的石墨烯气凝胶,其密度仅有3 mg·cm-3,在经受90% 的压缩之后仍能完全恢复而没有任何碎裂迹象。
3.2 碳气凝胶的性能及应用
3.2.1机械性能及应用
碳气凝胶的机械行为很有趣,它们可以在不同的条件下变形 (如弯曲、压缩、扭转等),并且在外力撤除后恢复到原来的形状;即使在空气或流体中经历重复的压缩拉伸 (50%) 后也只是减少了一些厚度[252]。各向同性的结构是这种结构恢复的关键所在。另外,橡胶状碳纳米管材料即使在极端的环境以及不同的频率下也都具有优异的机械性能[253],这使其在机械及热能储存领域有潜在的应用。
石墨烯是具有优异的机械性能、导电性能及物理性能的超薄碳材料,而在过去的几十年里,碳纳米管也由于其优异的机械性能而一直被广泛用作机械增强材料。目前,有研究者将石墨烯和碳纳米管复合来制备气凝胶。Zhang等人[254]用Fe2+进行水热的氧化还原反应合成了超轻石墨烯-碳纳米管气凝胶,发现可以通过调节复合到石墨烯气凝胶上的多壁碳纳米管的比例来增强石墨烯三维网络结构,从而提高其机械性能。这种气凝胶的密度在0.011 g·cm-3~ 0.087 g·cm-3之间 (与合成中使用的亚铁离子数量有关),弹性模量在0.011 MPa到0.29 MPa之间。
Gao等人[251]制备出了一种超轻的“碳海绵” (图22),密度仅有0.16 mg·cm-3左右,低于氦气的密度。他们先冷冻干燥碳纳米管和超大面积氧化石墨烯片层的溶液,接着用肼蒸汽将氧化石墨烯片层化学还原成石墨烯,制备出超轻“碳海绵”。这种“碳海绵”可以任意调节形状,弹性也很优异,被压缩80% 后仍可恢复原状。
3.2.2电、催化性能及应用
多孔碳气凝胶的三维网络结构不仅可以形成电荷运输的高端导电通道,同时也可以作为掺杂或包覆各种有机或无机活性材料的骨架,因此碳气凝胶在能源储存、催化等领域有着广泛的应用前景。
碳纳米管气凝胶可以被切割成任意形状或压缩成薄膜,直接在液相或有机电解质中用作体相电极[257]。制备电极的传统方法通常是混合碳纳米管粉末与聚合物粘结剂。相比较而言,使用碳纳米管气凝胶则更为简单。尽管纯的碳纳米管气凝胶具有优异电机械行为,但其电容非常低 (通常小于50 F·g-1),因而通常通过与一些具备赝电容性能的材料杂化来提高相应的性能[258,259]。Chen等人[260]通过将 α-Fe2O3与碳纳米管复合制备出了性能优异的杂化电极,其电容从80.2 F·g-1提高到300 F·g-1。碳纳米管网络骨架具有弹性且机械性能优异,复合后的气凝胶在承受 70% 的压力时仍然具有 90%的电容。Zhong等人[258]利用碳纳米管气凝胶作为导电基体电沉积聚苯胺,制备出的复合材料电容增加到189 F·g-1。与聚合物复合不仅可以提高复合电极的电容,同时也通过固定碳纳米管结点来增强碳纳米管网络结构的强度,使得复合后的材料具备更优异的机械强度和弹性恢复性能。
除了在超级电容器方面的应用,由于具有高的孔隙率和优异的机械稳定性,碳纳米管气凝胶也可以用作锂离子电池的三维多孔电极。Hu等人[261]采用CVD技术在碳纳米管气凝胶上沉积了无定形态的硅作为锂离子电池电极。三维导电网络结构可以促进电子转移,同时也作为嫁接活化材料的稳定骨架,这使得制备得到的材料在C/5的充电速率下具有优异的充放电容量 (分别为3200 mAh·g-1和 2750 mAh·g-1)。Rubloff课题组[262-264]通过原子层沉积技术在碳纳米管海绵上包覆 V2O5来获得CNT/V2O5核壳海绵,这种杂化的海绵具备较高的电容 (818 µAh·cm-1)。

图22 超轻碳气凝胶图像 (“碳海绵”) [251]Figure 22 The photo of ultra-flyweight aerogels(UFAs)
除了上述方面的应用,碳纳米管基材料同时也是催化领域中的潜在材料,可以作为催化剂或者作为负载催化剂的骨架。如Shen等人[265]通过在碳纳米管气凝胶上负载高性能的催化剂Pd来加速锂空气电池的电化学反应。此外,许多其他的催化剂如TiO2[266],CdS[267]也被负载在碳纳米管气凝胶上提高催化性能。相比于Pt/C催化剂,N掺杂的碳纳米管或石墨烯气凝胶显现出更高的电流密度和稳定性[246, 249]。
3.2.3物理性能及应用
由于碳气凝胶具有高孔隙率,同时还具有生物机体相容性及可生物降解特性,因而在医学领域具有广泛用途,可应用于诊断剂、人造组织、人造器官、器官组件等,特别适用于药物控制释放体系,药物可在溶胶-凝胶过程加入,或利用干燥后的气凝胶进行药物浸渍也可实现担载。气凝胶用于药物控制释放体系,可获得很高的药物担载量,是低毒高效的胃肠外给药体系。通过控制制备条件可以获得具有特殊降解特性的气凝胶,这种气凝胶可以根据需要在生物体中稳定存在一定时间后开始降解,并且降解产物无毒。Alnaief等人[268]研制了一种新的过程来控制药物释放,通过在气凝胶表面涂覆聚合物涂层来阻断由于气凝胶的多孔结构所引起液体渗透,从而减少了液体渗透所造成的气凝胶组织性能的破坏。

表4 部分碳气凝胶的性能参数Table 4 The parameters of some carbon aerogels
气凝胶是性能优良的吸附剂,可用于污水处理。和现有的离子交换、蒸发、反相渗透等技术相比,用碳气凝胶进行电吸附去除溶液中的金属离子具有可以再生、减少二次污染、节约能量等很多优势。Ying等人[269]的研究表明,碳气凝胶的吸附容量会随着溶液浓度、电压以及比表面积的增加而增加。Goel等人[270]用碳气凝胶吸附水溶液中的Hg2+,吸附能力几乎达100%。碳气凝胶也能吸附Cd2+、Pd2+、Cu2+、Ni1+、Mn2+、Zn2+、Cr2+等重金属离子。当气凝胶中含有催化剂时还能有效降解有毒物质。Gao等人[255,256]制备的碳海绵对有机溶剂吸收超快,能吸收自身质量250倍左右的液体,最高可达900倍。这一特性对于处理海上原油泄漏有较大的优势,而且可以循环利用。表4给出了部分碳气凝胶的性能参数。
尽管控制合成碳气凝胶的进程发展迅速,并且在很多领域上都有潜在应用,但是要实现碳气凝胶更广泛的应用仍然需要克服很多技术障碍,在基础研究和实际应用方面都需要付出更多的努力才能带来重大的突破。主要有以下几方面:(1) 单壁碳纳米管是最细的纳米管,其结构缺陷也最少,因而探究新方法来制备高质量的单壁碳纳米管气凝胶具有重要的意义;(2) 目前制备的碳气凝胶微观结构及其孔径等均是随机形成的,结合理论研究和模拟来探究微观结构的形成机理,从而可以根据实际应用设计出更优化的结构;(3) 碳气凝胶的应用领域需要进一步拓宽。尽量碳纳米管气凝胶在三维多孔的导电电极方面来说是理想材料,同时也是理想的过滤吸附剂,但仍有许多新的领域可以去扩展。例如,如果把陶瓷和金属引入到碳气凝胶上,这种特殊的复合物可能具备更优异的机械强度;(4) 低成本且规模化的制备方法仍需要进一步的努力。目前气相沉积系统能一次合成面积为10 cm2、厚度为1 cm的样品,但这个过程成本较高。而海上的油污通常都是大面积,若是用于海上油污的清理则性价比太低。因而开发设计出更简单且成本更低的制备方法是进一步实现碳气凝胶工业化实际应用的动力。
4 金属气凝胶
4.1 金属气凝胶的制备工艺
溶胶-凝胶技术已经普遍应用于合成金属和含金属的纳米颗粒,但要想采用这种技术使得金属纳米颗粒直接形成凝胶,然后采用超临界干燥法或冷冻干燥法干燥成气凝胶,仍然是一个挑战。Tappan等人[275]认为金属纳米颗粒完成溶胶-凝胶转变的一个关键条件是其在极性溶剂中具有高的溶解能力,但满足这个条件的金属纳米颗粒在应用方面仍然有很大的局限性。
金属气凝胶的制备目前主要采用溶胶-凝胶过程,有以下两种方法 (如图23所示)[42,47]:(1) 通过凝胶化贵金属纳米颗粒;(2) 采用原位自发凝胶过程。
在第一种方法中,首先采用NaBH4还原贵金属前驱体 (如HAuCl4、AgNO3、H2PtCl6或 PdCl2) 来制备柠檬酸包覆的单金属纳米颗粒 (图24),其中柠檬酸钠作为稳定剂[42,45]。制备出的Au、Pt和Pd纳米颗粒直径分别为3 nm ~ 5 nm、3 nm ~ 6 nm及3 nm ~ 6 nm,而Ag纳米颗粒的直径则呈现双模型尺寸分布,3 nm ~ 6 nm和8 nm ~ 15 nm。近来也有人通过柠檬酸稳定的Ag纳米颗粒和贵金属前驱体之间的共价置换反应制备出中空的双金属纳米颗粒[276,277],一般通过以下步骤来获得稳定金属纳米颗粒分散液[276,277]:首先采用离心设备或旋转蒸发对分散液进行浓缩,在浓缩过程中,通过水洗来去除多余的稳定剂和杂质;之后将浓缩的纳米颗粒分散液置于室温或高温环境中,或者添加如乙醇、水等去稳定剂来诱发凝胶[278]。通过上述办法,许多贵金属水凝胶 (如单一的Au、Ag、Pt和Pd水凝胶等) 和多金属水凝胶 (如 Au-Ag、Au-Pd、Pt-Ag、Pd-Ag、Pt-Pd、Au-Ag-Pt、Au-Pt-Pd、Ag-Pt-Pd、和 Au-Ag-Pt-Pd等) 都可以制备出来[42,47]。
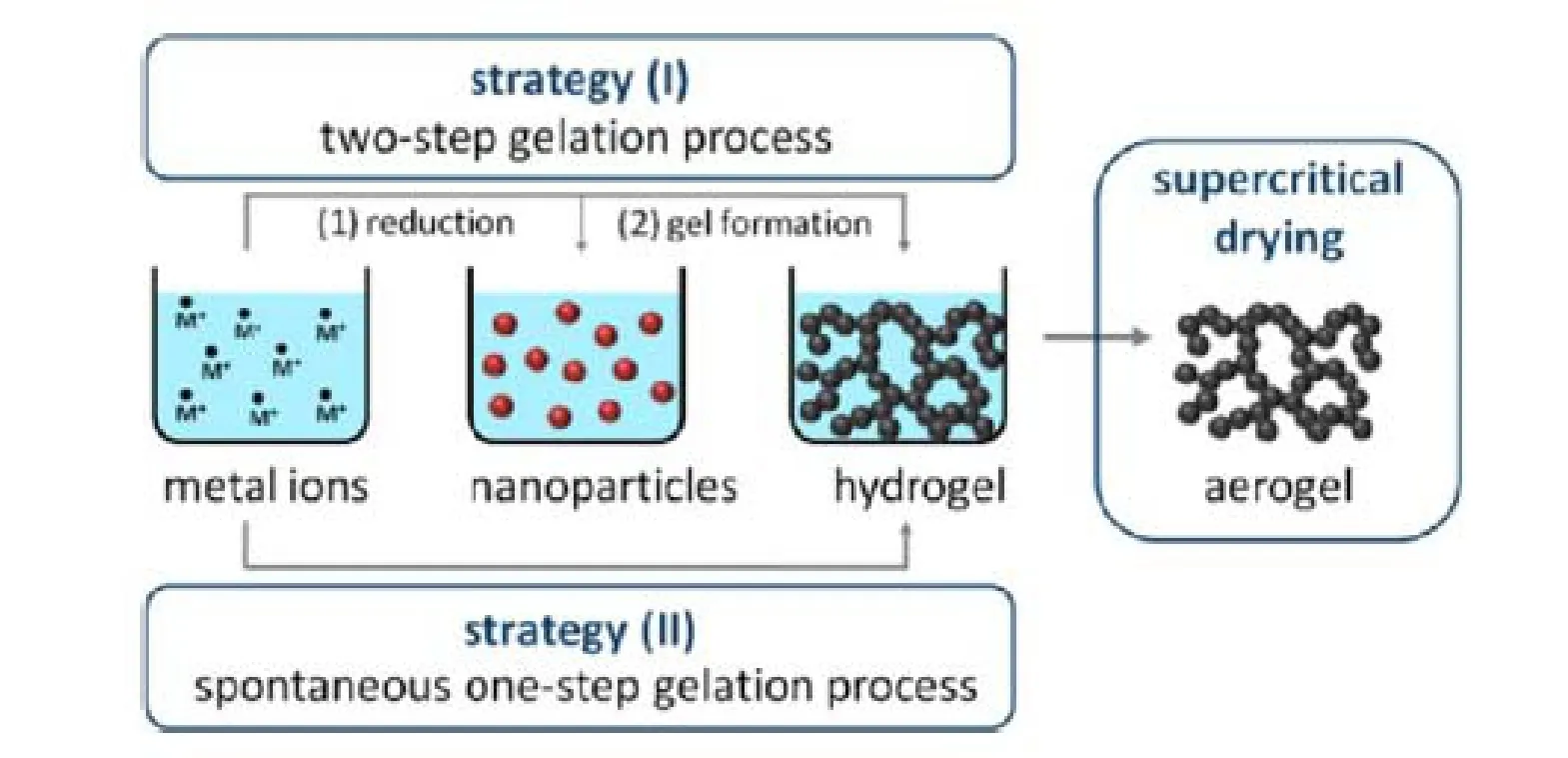
图23 贵金属气凝胶的制备方法:(1) 两步凝胶过程;(2) 自发一步凝胶过程[47]Figure 23 Schematic Illustration of Noble Metal Aerogel: preparation via gelation of preformed nanoparticles(Strategy (I)) and via an in situ spontaneous gelation process (Strategy (II)).

图24 铂纳米颗粒气凝胶 (添加乙醇作为去稳剂) 的SEM (A,B) 和TEM (C,D) 照片[42]Figure 24 (A, B) SEM and (C, D) TEM images of aerogels from platinum nanoparticles destabilized from solution by the addition of ethanol.
在第二种方法中,水凝胶可以通过原位还原贵金属前驱体自发形成,而不需要对纳米颗粒采取稳定化措施[279,280]。目前,包括 α,β,γ-环糊精 (Cyclodextrins, CD) 稳定的 (CD)Pd (Pdα,β,γ-CD) 水凝胶、纯Pd和Pt水凝胶以及双金属的PtnPd100-n水凝胶 (可调Pt和Pd的比例) 在内的一系列贵金属水凝胶已经通过这种方法制备得到[279,280]。形成这种水凝胶主要是通过先形成过渡态的纳米颗粒,再慢慢交联成短的纳米线,随之形成纳米线的网络结构,最终形成水凝胶。整个过程是一个自发组装的形成方式。过程中形成的盐类在凝胶形成中具有重要的作用,它们提高了溶液的离子强度,并且降低了纳米颗粒间的静电排斥作用,从而导致了非稳定化纳米颗粒的快速聚集或组装[42]。
在干燥过程中,由于高表面张力及毛细压力的存在,直接蒸发湿凝胶中的液体会导致骨架的收缩甚至网络结构的坍塌。而超临界干燥避免了溶剂从液相到气相的直接相转变,减小了导致孔结构坍塌的作用力,从而可以最大程度上保持结构的完整性。因而,目前将水凝胶干燥成气凝胶的过程主要采用超临界干燥工艺[42]。但超临界干燥工艺成本昂贵,操作复杂,这对金属气凝胶的进一步规模化应用造成了阻碍。
4.2 金属气凝胶的性能及应用前景
金属气凝胶作为一种新型材料在异质气相催化、电催化和传感器等领域具有潜在的应用。在这些领域的潜在应用主要是由于金属气凝胶具有的以下特性:(1) 分形的多孔结构使这些材料具有大的比表面积和有效的孔间传质运输,使得反应物易于在活性位点扩散,这些均有利于提高相应的催化活性[279,281-283];(2) 气凝胶的网络主要由相互交联的几个纳米长的纳米链组成,这是电催化过程中最优的尺寸范围[284,285];(3) 网络中相互交联的纳米链大多是熔合的纳米线状结构,这种结构在电催化过程中具有更高的持久性[286-288]。而且,金属气凝胶具有“自我支撑”的特性,且耐久性好。如果是用碳气凝胶负载贵金属,催化剂易被腐蚀从而影响耐久性[289]。通过表征和对比Pdα,β,γ-CD气凝胶[279]和商业用Pt/C (10 wt%) 的电催化性能发现,Pdα-CD和Pdβ-CD气凝胶的质量比电流密度高于商业Pt/C很多,并且其起始电位相对于Pt/C 47 mv ~ 69 mV 的负移进一步说明了优异的乙醇电催化氧化性能。通过对比PtnPd100-n气凝胶和Pt/C的氧还原活性发现,PtnPd100-n气凝胶是一种高度活化的聚合物电解质燃料电池阴极催化剂,制备得到的Pt80Pd20气凝胶显示出最高的质量比活性,是商业Pt/C的五倍。当PtnPd100-n气凝胶中Pt的比例大于40% 时可以达到甚至超过美国能源部制定的燃料电池中氧还原催化剂的目标 (在0.9 V下达到0.44 A mgPt-1)[286]。
气凝胶历史悠久,但是金属气凝胶的发展以及应用仍然处于最初的阶段,要想实现这种材料在更多领域的应用仍然需要克服许多问题。首先,可以通过对不同形貌的金属纳米晶体进行凝胶或者采用新的凝胶制备方法,使金属气凝胶的形貌更加丰富[42]。其次,金属气凝胶的组成有限,因而其他金属组成的金属气凝胶有待进一步研究。尽管目前已经制备得到一些贵金属气凝胶,但制备方法的简单化和普遍化仍然需要研究者们的努力。金属气凝胶规模化生产的一个重要前提是采用过渡金属作为前驱体的金属气凝胶的开发和制备。目前对金属气凝胶的应用研究较少,仅集中于各种电化学反应的电催化剂领域或是作为终产物。深入探究金属气凝胶作为电催化剂的应用机理和扩大其应用领域仍然需要不断的努力。
5 结论及展望
用溶胶-凝胶技术制备气凝胶在理论上和技术上已经有了一定的发展。但是,除硅体系以外,关于其它体系的动力学系统研究还很少,对多组分体系的研究也很少,凝胶在陈化过程中所发生的物理化学变化也不清楚。对不同种类和组成的气凝胶,各种制备参数对其性质的影响规律尚有待进一步的探索,尤其是各种制备参数对气凝胶性质影响的协同效应使情况更为复杂,很难得出规律性结论。目前的研究大部分仅仅停留在宏观上。气凝胶的高度松脆性、有限透明度以及吸湿性等问题仍然没有得到很好的解决。尽管人们做了很多这方面的研究,除了在SiO2气凝胶上取得了一些进展,在其它种类的气凝胶上仍旧进展不大,难以通过调控制备参数来设计气凝胶的结构和性质,实现气凝胶材料的可控合成。这方面还需要开展大量的研究工作。
今后气凝胶的研究将向以下几个方向发展:(1) 由廉价的无机原料代替昂贵的金属醇盐;(2) 由常压干燥代替传统的超临界干燥;(3) 开发新的品种,对气凝胶结构进行优化,制备性能更为优异的多组分气凝胶;(4) 研究结构和性质之间的关系,达到设计合成的目的;(5) 加强对气凝胶性质的研究,开发气凝胶新的应用领域。
[1] PIERRE AC, PAJONK GM. Chemistry of aerogels and their applications [J]. Chemical Reviews, 2002,102: 4243-4265.
[2] BLASZCZYNSKI T, SLOSARCZYK A, MORAWSKI M. Synthesis of silica aerogel by supercritical drying method [J]. Procedia Engineer, 2013, 57: 200-206.
[3] BAG S, KANATZIDIS MG. Chalcogels: porous metal-chalcogenide networks from main-group metal ions.effect of surface polarizability on selectivity in gas separation [J]. Journal of the American Chemical Society, 2010, 132: 14951-14959.
[4] WHITE S, DEMKO J. TOMICH A. Flexible aerogel as a superior thermal insulation for high temperature superconductor cable applications [J]. AIP Conference Proceedings, 2010, 1218: 788-795.
[5] ALIKOFER Y, AMSER C, HORIKAWA S, et al. A new aerogel Cherenkov detector for DIRAC-II [J].Nuclear Instruments and Methods A, 2008, 595: 84-87.
[6] PAJONK GM. Aerogel catalysts [J]. Applied Catalysis, 1991, 72: 217-266.
[7] MELDE BJ, JOHNSON BJ, CHARLES PT. Mesoporous silicate materials in sensing [J]. Sensors-Basel,2008, 8: 5202-5228.
[8] HE ZW, LIU XQ, SU Q, et al. Improvement of electrical properties of low dielectric constant nanoporous silica films prepared using sol-gel method with catalyst HF [J]. Applied Physics A, 2006, 82: 349-355.
[9] SCHMIDT M, SCHWERTFEGER F. Applications for silica aerogel products [J]. Journal of Non-Crystalline Solids, 1998, 225: 364-368.
[10] KISTLER SS. Coherent expanded aerogels and jellies [J]. Nature, 1931, 127: 741-741.
[11] KISTLER SS. Coherent expanded aerogels [J]. Journal of Physical Chemistry, 1932, 36: 52-64.
[12] NICOLAON GA, TEICHNER SJ. Preparation of silica aerogels from methyl orthosilicate in alcoholic medium and their properties [J]. Bulletin de la Societe Chimique de France, 1968, 5: 1906-1911.
[13] TEICHNER SJ, NICOLAON GA, PAJONK G. New method for preparation of aerogels of inorganic oxides and some properties of these materials [J]. Abstracts of Papers of the American Chemical Society,1980, 179: 184-189.
[14] PERI JB. Infrared study of OH and NH2groups on the surface of a dry silica aerogel [J]. Journal of Physical Chemistry, 1966, 70: 2937-2939.
[15] LINDQUIST DA, BOREK TT, KRAMER SJ, et al. Formation and pore structure of boron-nitride aerogels[J]. Journal of the American Ceramic Society, 1990, 73: 757-760.
[16] PEKALA RW. Organic aerogels from the polycondensation of resorcinol with formaldehyde [J]. Journal of Materials Science, 1989, 24: 3221-3227.
[17] GESSER HD, GOSWAMI PC. Aerogels and related porous materials [J]. Chemical Reviews, 1989, 89:765-788.
[18] PEKALA RW. Low density: resorcinol-formaldehyde aerogels; 美国, US4997804 [J]. 1989-12-09.
[19] GOUEREC P, MIOUSSE D, TRAN-VAN F, et al. Characterization of pyrolyzed polyacrylonitrile aerogel thin films used in double-layer supercapacitors [J]. Journal of New Materials for Electrochemical Systems,1999, 2: 221-226.
[20] CHEN HB, HOLLINGER E, WANG YZ, et al. Facile fabrication of poly(vinyl alcohol) gels and derivative aerogels [J]. Polymer, 2014, 55: 380-384.
[21] GUO H, MEADOR MAB, MCCORKLE L, et al. Polyimide aerogels cross-linked through amine functionalized polyoligomeric silsesquioxane [J]. ACS Applied Materials & Interfaces, 2011, 3: 546-552.
[22] BIESMANS G, MERTENS A, DUFFOURS L, et al. Polyurethane based organic aerogels and their transformation into carbon aerogels [J]. Journal of Non-Crystalline Solids, 1998, 225: 64-68.
[23] PEKALA RW, KONG FM. Resorcinol-formaldehyde aerogels and their carbonized derivatives [J].Abstracts of Papers of the American Chemical Society, 1989, 197: 113-113.
[24] HANZAWA Y, KANEKO K, PEKALA RW, et al. Activated carbon aerogels [J]. Langmuir, 1996, 12:6167-6169.
[25] PAUZAUSKIE PJ, CROWHURST JC, WORSLEY MA, et al. Synthesis and characterization of a nanocrystalline diamond aerogel [J]. Proceedings of the National Academy of Science of the United States of America, 2011, 108: 8550-8553.
[26] BRYNING MB, ISLAM MF, KIKKAWA JM, et al. Very low conductivity threshold in bulk isotropic single-walled carbon nanotube-epoxy composites [J]. Advanced Materials, 2005, 17: 1186-1191.
[27] HERNANDEZ Y, NICOLOSI V, LOTYA M, et al. High-yield production of graphene by liquid-phase exfoliation of graphite [J]. Nature Nanotechnology, 2008, 3: 563-568.
[28] LI X, ZHANG G, BAI X, et al. Highly conducting graphene sheets and Langmuir-Blodgett films [J].Nature Nanotechnology, 2008, 3: 538-542.
[29] LIU N, LUO F, WU HX, et al. One-step ionic-liquid-assisted electrochemical synthesis of ionic-liquidfunctionalized graphene sheets directly from graphite [J]. Advanced Functional Materials, 2008, 18:1518-1525.
[30] LEE JH, SHIN DW, MAKOTCHENKO VG, et al. One-step exfoliation synthesis of easily soluble graphite and transparent conducting graphene sheets [J]. Advanced Materials, 2009, 21: 4383-4387.
[31] TANG Y, YEO KL, CHEN Y, et al. Ultralow-density copper nanowire aerogel monoliths with tunable mechanical and electrical properties [J]. Journal of Materials Chemistry A, 2013, 1: 6723-6726.
[32] MAHADIK-KHANOLKAR S, DONTHULA S, SOTIRIOU-LEVENTIS C, et al. Polybenzoxazine aerogels: I, high-yield room-temperature acid-catalyzed synthesis of robust monoliths, oxidative aromatization, and conversion to microporous carbons [J]. Chemistry of Materials, 2014, 26: 1303-1317.
[33] MAHADIK-KHANOLKAR S, DONTHULA S, BANG A, et al. Polybenzoxazine aerogels: II,interpenetrating networks with iron oxide and the carbothermal synthesis of highly porous monolithic pure iron (0) aerogels as energetic materials [J]. Chemistry of Materials, 2014, 26: 1318-1331.
[34] LEVENTIS N, CHANDRASEKARAN N, SOTIRIOU-LEVENTIS C, et al. Smelting in the age of nano:iron aerogels [J]. Journal of Materials Chemistry, 2009, 19: 63-65.
[35] LEVENTIS N, CHANDRASEKARAN N, SADEKAR AG, et al. One-pot synthesis of interpenetrating inorganic/organic networks of CuO/resorcinol-formaldehyde aerogels: nanostructured energetic materials[J]. Journal of the American Chemical Society, 2009, 131: 4576-4576.
[36] TANG J, DU A, XU W, et al. Fabrication and characterization of composition-gradient CuO/SiO2composite aerogel [J]. Journal of Sol-Gel Science and Technology, 2013, 68: 102-109.
[37] SCHUBERT U, SCHWERTFEGER F, HUSING N, et al. Inorganic-organic hybrid aerogel [J]. MRS Proceedings, 1994, 346: 151-162.
[38] BHEEKHUN N, ABU TALIB AR, HASSAN MR. Aerogels in aerospace: an overview [J]. Advances in Materials Science and Engineering, 2013, 1-18.
[39] HSING N, SCHUBERT U. Aerogels-airy materials: chemistry, structure, and properties [J]. Angewandte Chemie International Edition, 1998, 37: 22-45.
[40] ZHANG SQ, WANG J, SHEN J, et al. The investigation of the adsorption character of carbon aerogels [J].Nanostructured Materials, 1999, 11: 375-381.
[41] TEWARI PH, HUNT AJ, LOFFTUS KD. Ambient-temperature supercritical drying of transparent silica aerogels [J]. Materials Letters, 1985, 3: 363-367.
[42] BIGALL NC, HERRMANN AK, VOGEL M, et al. Hydrogels and aerogels from noble metal nanoparticles [J]. Angewandte Chemie International Edition, 2009, 48: 9731-9734.
[43] LEVENTIS N, CHANDRASEKARAN N, LEVENTIS CS, et al. Smelting in the age of nano: iron aerogels[J]. Journal of Materials Chemistry, 2008, 19: 63-65.
[44] GAPONIK N, HERRMANN AK, EYCHMULLER A. Colloidal nanocrystal-based gels and aerogels:material aspects and application perspectives [J]. Journal of Physical Chemistry Letters, 2012, 3: 8-17.
[45] HERRMANN AK, FORMANEK P, BORCHARDT L, et al. Multimetallic aerogels by template-free self-assembly of Au, Ag, Pt, and Pd nanoparticles [J]. Chemistry of Materials, 2014, 26: 1074-1083.
[46] WEN D, HERRMANN AK, BORCHARDT L, et al. Controlling the growth of palladium aerogels with high-performance toward bioelectrocatalytic oxidation of glucose [J]. Journal of the American Chemical Society, 2014, 136: 2727-2730.
[47] LIU W, HERRMANN AK, BIGALL NC, et al. Noble metal aerogels-synthesis, characterization, and application as electrocatalysts [J]. Accounts of Chemical Research, 2015, 48: 154-162.
[48] ZHU C, WEN D, LEUBNER S, et al. Nickel cobalt oxide hollow nanosponges as advanced electrocatalysts for the oxygen evolution reaction [J]. Chemical Communications, 2015, 51: 7851-7854.
[49] SCHAEDLER TA, JACOBSEN AJ, TORRENTS A, et al. Ultralight metallic microlattices [J]. Science,2011, 334: 962-965.
[50] SCHAEFER DW. Polymers, fractals, and ceramic materials [J]. Science, 1989, 243: 1023-1027.
[51] ZHANG GH, DASS A, RAWASHDEH AMM, et al. Isocyanate-crosslinked silica aerogel monoliths:preparation and characterization [J]. Journal of Non-Crystalline Solids, 2004, 350: 152-164.
[52] POCO JF, SATCHER JH, HRUBESH LW. Synthesis of high porosity, monolithic alumina aerogels [J].Journal of Non-Crystalline Solids, 2001, 285: 57-63.
[53] STOCKER C, BAIKER A. Zirconia aerogels: effect of the use of mono-and dicarboxylic acids in the sol-gel process on structural properties [J]. Journal of Sol-Gel Science and Technology, 1997, 10:269-282.
[54] LIAO YH, CHOU JC. Preparation and characterization of the titanium dioxide thin films used for pH electrode and procaine drug sensor by sol-gel method [J]. Materials Chemistry and Physics, 2009, 114:542-548.
[55] DU A, ZHOU B, SHEN J, et al. Monolithic copper oxide aerogel via dispersed inorganic sol-gel method[J]. Journal of Non-Crystalline Solids, 2009, 355: 175-181.
[56] SOLEIMANI DORCHEH A, ABBASI MH. Silica aerogel; synthesis, properties and characterization [J].Journal of Materials Processing Technology, 2008, 199: 10-26.
[57] DAGAN G, TOMKIEWICZ M. TiO2aerogels for photocatalytic decontamination of aquatic environments[J]. Journal of Physical Chemistry, 1993, 97: 12651-12655.
[58] WARD DA, KO EI. Synthesis and structural transformation of zirconia aerogels [J]. Chemistry of Materials, 1993, 5: 956-969.
[59] HIRASHIMA H, KOJIMA C, IMAI H. Application of alumina aerogels as catalysts [J]. Journal of Sol-Gel Science and Technology, 1997, 8: 843-846.
[60] AYERS MR, HUNT AJ. Titanium oxide aerogels prepared from titanium metal and hydrogen peroxide [J].Materials Letters, 1998, 34: 290-293.
[61] STOCKER C, BAIKER A. Zirconia aerogels: effect of acid-to-alkoxide ratio, alcoholic solvent and supercritical drying method on structural properties [J]. Journal of Non-Crystalline Solids, 1998, 223:165-178.
[62] LONG JW, LOGAN MS, RHODES CP, et al. Nanocrystalline iron oxide aerogels as mesoporous magnetic architectures [J]. Journal of the American Chemical Society, 2004, 126: 16879-16889.
[63] BAUMANN TF, GASH AE, CHINN SC, et al. Synthesis of high-surface-area alumina aerogels without the use of alkoxide precursors [J]. Chemistry of Materials, 2005, 17: 395-401.
[64] GAN LH, WANG YD, HAO ZX, et al. Preparation of TiO2/SiO2aerogels by non-supercritical drying method and their photocatalytic activity for degradation of pyridine [J]. Chinese Journal of Chemical Engineering, 2005, 13: 758-763.
[65] LI WC, LU AH, SCHMIDT W, et al. High surface area, mesoporous, glassy alumina with a controllable pore size by nanocasting from carbon aerogels [J]. Chemistry A, 2005, 11: 1658-1664.
[66] SUI RH, RIZKALLA AS, CHARPENTIER PA. Direct synthesis of zirconia aerogel nanoarchitecture in supercritical CO2[J]. Langmuir, 2006, 22: 4390-4396.
[67] ZU GQ, SHEN J, WEI XQ, et al. Preparation and characterization of monolithic alumina aerogels [J].Journal of Non-Crystalline Solids, 2011, 357: 2903-2906.
[68] JINMORI D, MASUBUCHI Y, KIKKAWA S. Magnetic porous iron oxide monoliths prepared through epoxide-mediated sol-gel process [J]. Materials Research Bulletin, 2017, 88: 214-217.
[69] BISSON A, RIGACCI A, LECOMTE D, et al. Drying of silica gels to obtain aerogels: phenomenology and basic techniques [J]. Drying Technology, 2003, 21: 593-628.
[70] KAWAKAMI N, FUKUMOTO Y, KINOSHITA T, et al. Preparation of highly porous silica aerogel thin film by supercritical drying [J]. Japanese Journal of Applied Physics, 2000, 39 (3AB): 182-184.
[71] WALLACE CB. Drying supercritical CO2demands care [J]. Oil Gas Journal, 1985, 83: 98-104.
[72] TAKAHAMA K, YOKOYAMA M, HIRAO S, et al. Supercritical drying of SiO2-TiO2sol-pillared clays[J]. Journal of Materials Science, 1992, 27: 1297-1301.
[73] LAUDISE RA, JOHNSON DW. Supercritical drying of gels [J]. Journal of Non-Crystalline Solids, 1986,79: 155-164.
[74] HUSING N, SCHUBERT U. Aerogels airy materials: chemistry, structure, and properties [J]. Angewandte Chemie International Edition, 1998, 37: 23-45.
[75] KOCON L, DESPETIS F.PHALIPPOU J. Ultralow density silica aerogels by alcohol supercritical drying[J]. Journal of Non-Crystalline Solids, 1998, 225: 96-100.
[76] VANBOMMEL MJ, DEHAAN AB. Drying of silica-gels with supercritical carbon-dioxide [J]. Journal of Materials Science, 1994, 29: 943-948.
[77] YANG HS, JANSSEN BH. Analysis of impact of farming practices on dynamics of soil organic matter in northern China [J]. European Journal of Agronomy, 1997, 7: 267-275.
[78] CHANDRADASS J, KANG S, BAE DS. Synthesis of silica aerogel blanket by ambient drying method using water glass based precursor and glass wool modified by alumina sol [J]. Journal of Non-Crystalline Solids, 2008, 354: 4115-4119.
[79] LIU MX, GAN LH, PANG YC, et al. Synthesis of titania-silica aerogel-like microspheres by a water-in-oil emulsion method via ambient pressure drying and their photocatalytic properties [J]. Colloid Surface A,2008, 317: 490-495.
[80] YAO LF, YUE CX, LU FQ, et al. Hydrophobic silica aerogel films with low dielectric constant via ambient-pressure drying [J]. Rare Metal Materials and Engineering, 2008, 37: 163-166.
[81] RAO AP, RAO AV, PAJONK GM. Hydrophobic and physical properties of the ambient pressure dried silica aerogels with sodium silicate precursor using various surface modification agents [J]. Applied Surface Science, 2007, 253: 6032-6040.
[82] RAO AP, RAO AV, PAJONK GM, et al. Effect of solvent exchanging process on the preparation of the hydrophobic silica aerogels by ambient pressure drying method using sodium silicate precursor [J]. Journal of Materials Science, 2007, 42: 8418-8425.
[83] YANG HS, CHOI SY, HYUN SH, et al. Ambient-dried low dielectric SiO2aerogel thin film [J]. Journal of Non-Crystalline Solids, 1997, 221: 151-156.
[84] PRAKASH SS, BRINKER CJ, HURD AJ, et al. Silica aerogel films prepared at ambient-pressure by using surface derivatization to induce reversible drying shrinkage (Vol 374, Pg 439, 1995) [J]. Nature, 1995, 375:431-431.
[85] SMITH DM, DESHPANDE R.BRINKER CJ. Preparation of low-density aerogels at ambient pressure [J].MRS Proceedings, 1992, 271: 104-112.
[86] ABDELWAHED W, DEGOBERT G, STAINMESSE S, et al. Freeze-drying of nanoparticles: formulation,process and storage considerations [J]. Advanced Drug Delivery Reviews, 2006, 58: 1688-1713.
[87] REN L, CUI S, CAO F, et al. An easy way to prepare monolithic inorganic oxide aerogels [J]. Angewandte Chemie International Edition, 2014, 53: 10147-10149.
[88] SMITH DM, ACKERMAN WC, ROTH R, et al. Aerogel synthesis using extractive drying [J]. MRS Proceedings, 1996, 431: 291-296.
[89] YOLDAS BE, ANNEN MJ, BOSTAPH J. Chemical engineering of aerogel morphology formed under nonsupercritical conditions for thermal insulation [J]. Chemistry of Materials, 2000, 12: 2475-2484.
[90] BAETENS R, JELLE BP, GUSTAVSEN A. Aerogel insulation for building applications: a state-of-the-art review [J]. Energy and Buildings, 2011, 43: 761-769.
[91] QUENARD D, CHEVALIER B, SALLEE H, et al. Heat transfer by conduction and radiation in building materials: review and new developments [J]. Revue de Metallurgie, 1998, 96: 599-600.
[92] FESMIRE JE, SASS JP. Aerogel insulation applications for liquid hydrogen launch vehicle tanks [J].Cryogenics, 2008, 48: 223-231.
[93] TSOU P. Silica aerogel captures cosmic dust intact [J]. Journal of Non-Crystalline Solids, 1995, 186:415-427.
[94] PAJONK GM. Transparent silica aerogels [J]. Journal of Non-Crystalline Solids, 1998, 225: 307-314.
[95] TAJIRI K, IGARASHI K. The effect of the preparation conditions on the optical properties of transparent silica aerogels [J]. Solar Energy Materials & Solar Cells, 1998, 54: 189-195.
[96] MALINOWSKA B, WALENDZIEWSKI J, ROBERT D, et al. Titania aerogels: preparation and photocatalytic tests [J]. International Journal of Photoenergy, 2003, 5: 147-152.
[97] DAGAN G, TOMKIEWICZ M. TiO2aerogels for photocatalytic decontamination of aquatic environment[J]. Journal of Physical Chemistry, 1993, 97: 12651-12655.
[98] BURGER T, FRICKE J. Aerogels: production, modification and applications [J]. Berichte Der Bunsengesellschaft Fur Physikalische Chemie, 1998, 102: 1523-1528.
[99] WOIGNIER T, PHALIPPOU J. Scaling law variation of the mechanical-properties of silica aerogels [J].Le Journal de Physique Colloques, 1989, 50: 4179-4184.
[100] FRICKE J, EMMERLING A. Aerogels: recent progress in production techniques and novel applications[J]. Journal of Sol-Gel Science and Technology, 1998, 13: 299-303.
[101] HAEREID S, DAHLE M, LIMA S, et al. Preparation and properties of monolithic silica xerogels from TEOS-based alcogels aged in silane solutions [J]. Journal of Non-Crystalline Solids, 1995, 186: 96-103.
[102] KRAMER SJ, RUBIOALONSO F, MACKENZIE JD. Organically modified silicate aerogels [J]. MRS Proceedings, 1996, 435: 295-300.
[103] GUO XZ, YAN LQ, YANG H, et al. Modification of zirconia fiber to reinforce ZrO2aerogels [J]. Rare Metal Materials and Engineering, 2012, 41: 436-438.
[104] CAPADONA LA, MEADOR MAB, ALUNNI A, et al. Flexible, low-density polymer crosslinked silica aerogels [J]. Polymer, 2006, 47: 5754-5761.
[105] LI Z, GONG LL, CHENG XD, et al. Flexible silica aerogel composites strengthened with aramid fibers and their thermal behavior [J]. Materials & Design, 2016, 99: 349-355.
[106] PARMENTER KE, MILSTEIN F. Mechanical properties of silica aerogels [J]. Journal of Non-Crystalline Solids, 1998, 223: 179-189.
[107] DESPETIS F, ETIENNE P, PHALIPPOU J. Crack speed in ultraporous brittle amorphous material [J].Physics and Chemistry of Glasses, 2000, 41: 104-106.
[108] SHAO Z, LUO F, CHENG X, et al. Superhydrophobic sodium silicate based silica aerogel prepared by ambient pressure drying [J]. Materials Chemistry and Physics, 2013, 141: 570-575.
[109] HOLMES NC, RADOUSKY HB, MOSS MJ, et al. Silica at ultrahigh temperature and expanded volume[J]. Applied Physical Letters, 1984, 45: 626-628.
[110] AMENDT P, GLENDINNING SG, HAMMEL BA, et al. New methods for diagnosing and controlling hohlraum drive asymmetry on Nova [J]. Physics of Plasmas, 1997, 4: 1862-1871.
[111] BUZYKAEV AR, DANILYUK AF, GANZHUR SF, et al. Measurement of optical parameters of aerogel[J]. Nuclear Instruments and Methods A, 1999, 433: 396-400.
[112] ZHOU B, WANG J, ZHAO L, et al. Preparation of C-60-doped silica aerogels and the study of photoluminescence properties [J]. Journal of Vacuum Science and Technology B, 2000, 18: 2001-2004.
[113] CHARLTON A, MCKINNIE IT, MENESESNAVA MA, et al. A Tunable visible solid-state laser [J].Journal of Modern Optics, 1992, 39: 1517-1523.
[114] SHEN J, WANG J, ZHOU B, et al. Photoluminescence of fullerenes doped in silica aerogels [J]. Journal of Non-Crystalline Solids, 1998, 225: 315-318.
[115] KIM NK, KIM K, PAYNE DA, et al. Fabrication of hollow silica aerogel spheres by a droplet generation method and sol-gel processing [J]. Journal of Vacuum Science and Technology A, 1989, 7: 1181-1184.
[116] KIM KYK, JANG KY, UPADHYE RS. Hollow silica spheres of controlled size and porosity by sol-gel processing [J]. Journal of the American Ceramic Society, 1991, 74: 1987-1992.
[117] BERNIK DL. Silicon based materials for drug delivery devices and implants [J]. Recent Patents on Nanotechnology, 2007, 1: 186-192.
[118] EMMERLING A, LENHARD W, FRICKE J, et al. Densification behavior of silica aerogels upon isothermal sintering [J]. Journal of Sol-Gel Science and Technology, 1997, 8: 837-842.
[119] OWENS L, TILLOTSON TM, HAIR LM. Characterization of vanadium silica and copper silica aerogel catalysts [J]. Journal of Non-Crystalline Solids, 1995, 186: 177-183.
[120] DANILYUK AF, KRAVCHENKO EA, OKUNEV AG, et al. Synthesis of aerogel tiles with high light scattering length [J]. Nuclear Instruments and Methods A, 1999, 433: 406-407.
[121] TAN CB, FUNG BM, NEWMAN JK, et al. Organic aerogels with very high impact strength [J]. Advanced Materials, 2001, 13: 644-646.
[122] PEKALA RW, ALVISO CT, LU X, et al. New organic aerogels based upon a phenolic-furfural reaction [J].Journal of Non-Crystalline Solids, 1995, 188: 34-40.
[123] PEKALA RW, KONG FM. A synthetic route to organic aerogels-mechanism structure, and properties [J].Journal De Physique, 1989, 50: C433-C440.
[124] THIRUVENGADAM V, VITTA S. Ni-bacterial cellulose nanocomposite; a magnetically active inorganic-organic hybrid gel [J]. RSC Advances, 2013, 3: 12765-12773.
[125] EL KADIB A, BOUSMINA M. Chitosan bio-based organic-inorganic hybrid aerogel microspheres [J].Chemistry, 2012, 18: 8264-8277.
[126] HARRELD JH, DUNN B, NAZAR LF. Design and synthesis of inorganic-organic hybrid microstructures[J]. International Journal of Inorganic Materials, 1999, 1: 135-146.
[127] SANCHEZ C, SOLER-ILLIA GJDAA, RIBOT F, et al. Designed hybrid organic-inorganic nanocomposites from functional nanobuilding blocks [J]. Chemistry of Materials, 2001, 13: 3061-3083.
[128] LOY DA, BEACH JV, BAUGHER BM, et al. Dialkylene carbonate-bridged polysilsesquioxanes: hybrid organic-inorganic sol-gels with a thermally labile bridging group [J]. Chemistry of Materials, 1999, 11:3333-3341.
[129] KANAMORI K, AIZAWA M, NAKANISHI K, et al. Elastic organic-inorganic hybrid aerogels and xerogels [J]. Journal of Sol-Gel Science and Technology, 2008, 48: 172-181.
[130] PARK BW, PHILIPPE B, GUSTAFSSON T, et al. Enhanced crystallinity in organic-inorganic lead halide perovskite on mesoporous TiO2via disorder-order phase transition [J]. Chemistry of Materials, 2014, 26:4466-4471.
[131] SHARP KG. Inorganic/organic hybrid materials [J]. Advanced Materials, 1998, 10: 1243-1248.
[132] WOLDRAB S, SCHONHALS A, GOERING H, et al. Integration of sol-gel derived inorganic nanonetworks into polymers [J]. Polymer Chemistry, 2010, 1: 1226-1236.
[133] NOVAK BM, AUERBACH D, VERRIER C. Low-density, mutually interpenetrating organic-inorganic composite-materials via supercritical drying technology [J]. Chemistry of Materials, 1994, 6: 282-286.
[134] MAMMERI F, BOURHIS EL, ROZES L, et al. Mechanical properties of hybrid organic-inorganic materials [J]. Journal of Materials Chemistry, 2005, 15: 3787-3811.
[135] ALNAIEF M, ALZAITOUN MA, GARCIA-GONZALEZ CA, et al. Preparation of biodegradable nanoporous microspherical aerogel based on alginate [J]. Carbohydrate Polymers, 2011, 84: 1011-1018.
[136] TAMURA H, NAGAHAMA H, TOKURA S. Preparation of chitin hydrogel under mild conditions [J].Cellulose, 2006, 13: 357-364.
[137] LIEW SY, THIELEMANS W, WALSH DA. Electrochemical capacitance of nanocomposite polypyrrole/cellulose films [J]. Journal of Physical Chemistry C, 2010, 114: 17926-17933.
[138] PEKALA RW, ALVISO CT, KONG FM, et al. Aerogels derived from multifunctional organic monomers[J]. Journal of Non-Crystalline Solids, 1992, 145: 90-98.
[139] MULIK S, SOTIRIOU-LEVENTIS C, LEVENTIS N. Time-efficient acid-catalyzed synthesis of resorcinol-formaldehyde aerogels [J]. Chemistry of Materials, 2007, 19: 6138-6144.
[140] SMIRNOVA I, MAMIC J, ARLT W. Adsorption of drugs on silica aerogels [J]. Langmuir, 2003, 19:8521-8525.
[141] SMIRNOVA I, SUTTIRUENGWONG S, ARLT W. Feasibility study of hydrophilic and hydrophobic silica aerogels as drug delivery systems [J]. Journal of Non-Crystalline Solids, 2004, 350: 54-60.
[142] MEHLING T, SMIRNOVA I, GUENTHER U, et al. Polysaccharide-based aerogels as drug carriers [J].Journal of Non-Crystalline Solids, 2009, 355: 2472-2479.
[143] HEINEMANN S, CORADIN T, DESIMONE MF. Bio-inspired silica-collagen materials: applications and perspectives in the medical field [J]. Biomaterials Science, 2013, 1: 688-702.
[144] MOLVINGER K, QUIGNARD F, BRUNEL D, et al. Porous chitosan-silica hybrid microspheres as a potential catalyst [J]. Chemistry of Materials, 2004, 16: 3367-3372.
[145] LU Y, CHEN SC. Micro and nano-fabrication of biodegradable polymers for drug delivery [J]. Advanced Drug Delivery Reviews, 2004, 56: 1621-1633.
[146] ANNABI N, NICHOL JW, ZHONG X, et al. Controlling the porosity and microarchitecture of hydrogels for tissue engineering [J]. Tissue Engineering B, 2010, 16: 371-383.
[147] REVERCHON E, CARDEA S, RAPUANO C. A new supercritical fluid-based process to produce scaffolds for tissue replacement [J]. Journal of Supercritical Fluids, 2008, 45: 365-373.
[148] MALAFAYA PB, SILVA GA, REIS RL. Natural-origin polymers as carriers and scaffolds for biomolecules and cell delivery in tissue engineering applications [J]. Advanced Drug Delivery Reviews,2007, 59: 207-233.
[149] GKIONI K, LEEUWENBURGH SCG, DOUGLAS TEL, et al. Mineralization of hydrogels for bone regeneration [J]. Tissue Engineering B, 2010, 16: 577-585.
[150] LANGER R, VACANTI JP. Tissue Engineering [J]. Science, 1993, 260: 920-926.
[151] CARDEA S, PISANTI P, REVERCHON E. Generation of chitosan nanoporous structures for tissue engineering applications using a supercritical fluid assisted process [J]. Journal of Supercritical Fluids,2010, 54: 290-295.
[152] CHANG C, ZHANG L. Cellulose-based hydrogels: Present status and application prospects [J].Carbohydrate polymers, 2011, 84: 40-53.
[153] SI Y, YU J, TANG X, et al. Ultralight nanofibre-assembled cellular aerogels with superelasticity and multifunctionality [J]. Nature Communications, 2014, 5: 5802-5802.
[154] JIANG F, HSIEH YL. Amphiphilic superabsorbent cellulose nanofiber aerogels [J]. Journal of Materials Chemistry A, 2014, 2: 6337-6342.
[155] KORHONEN JT, KETTUNEN M, RAS RHA, et al. Hydrophobic nanocellulose aerogels as floating,sustainable, reusable, and recyclable oil absorbents [J]. ACS Applied Materials & Interfaces, 2011, 3:1813-1816.
[156] WOOTTON M, BAMUNUARACHCHI A. Application of differential scanning calorimetry to starch gelatination: 2, effect of heating rate and moisture level [J]. Starke, 1979, 31: 262-264.
[157] WHITE RJ, BUDARIN VL, CLARK JH. Tunable mesoporous materials from alpha-D-polysaccharides [J].Chemsuschem, 2008, 1: 408-411.
[158] HOOVER R, VASANTHAN T, SENANAYAKE NJ, et al. The Effects of defeating and heat-moisture treatment on the retrogradation of starch gels from wheat, oat, potato, and lentil [J]. Carbohydrate Research,1994, 261: 13-24.
[159] GLENN GM, KLAMCZYNSKI AP, WOODS DF, et al. Encapsulation of plant oils in porous starch microspheres [J]. Journal of Agricultural and Food Chemistry, 2010, 58: 4180-4184.
[160] SRIAMORNSAK P. Application of pectin in oral drug deliver y[J]. Expert Opinion on Drug Delivery,2011, 8: 1009-1023.
[161] IMESON A. Food stablizers, thickeners and gelling agents [M]. USA, New York: John Wiley & Sons,2009.
[162] BRACCINI I, PEREZ S. Molecular basis of Ca2+-induced gelation in alginates and pectins: the egg-box model revisited [J]. Biomacromolecules, 2001, 2: 1089-1096.
[163] WHITE RJ, BUDARIN VL, CLARK JH. Pectin-derived porous materials [J]. Chemistry, 2010, 16:1326-1335.
[164] ESCUDERO RR, ROBITZER M, DI RENZO F, et al. Alginate aerogels as adsorbents of polar molecules from liquid hydrocarbons: hexanol as probe molecule [J]. Carbohydrate Polymers, 2009, 75: 52-57.
[165] VALENTIN R, HORGA R, BONELLI B, et al. FTIR spectroscopy of NH3on acidic and ionotropic alginate aerogels [J]. Biomacromolecules, 2006, 7: 877-882.
[166] ROBITZER M, DAVID L, ROCHAS C, et al. Nanostructure of calcium alginate aerogels obtained from multistep solvent exchange route [J]. Langmuir, 2008, 24: 12547-12552.
[167] SILVA CM, RIBEIRO AJ, FERREIRA D, et al. Insulin encapsulation in reinforced alginate microspheres prepared by internal gelation [J]. European Journal of Pharmaceutical Sciences, 2006, 29: 148-159.
[168] QUIGNARD F, DI RENZO F.GUIBAL E. From natural polysaccharides to materials for catalysis,adsorption, and remediation [J]. Carbohydrates in Sustainable Development, 2010, 294: 165-197.
[169] WHITE RJ, ANTONIO C, BUDARIN VL, et al. Polysaccharide-derived carbons for polar analyte separations [J]. Advanced Functional Materials, 2010, 20: 1834-1841.
[170] TSIOPTSIAS C, MICHAILOF C, STAUROPOULOS G, et al. Chitin and carbon aerogels from chitin alcogels [J]. Carbohydrate Polymers, 2009, 76: 535-540.
[171] ZAKARIA B, MUDA WMW, ABDULLAH MDP. Chitin and chitosan-versatile environmentally friendly modern materials [D]. Universiti Kebangsaan Malaysia, 1995.
[172] ROBITZER M, DI RENZO F, QUIGNARD F. Natural materials with high surface area: physisorption methods for the characterization of the texture and surface of polysaccharide aerogels [J]. Microporous and Mesoporous Materials, 2011, 140: 9-16.
[173] QUIGNARD F, VALENTIN R, DI RENZO F. Aerogel materials from marine polysaccharides [J]. New Journal of Chemistry, 2008, 32: 1300-1310.
[174] EL KADIB A, MOLVINGER K, CACCIAGUERRA T, et al. Chitosan templated synthesis of porous metal oxide microspheres with filamentary nanostructures [J]. Microporous and Mesoporous Materials,2011, 142: 301-307.
[175] CHANG X, CHEN D, JIAO X. Chitosan-based aerogels with high adsorption performance [J]. Journal of Physical Chemistry B, 2008, 112: 7721-7725.
[176] DIASCORN N, SALLEE H, CALAS S, et al. Mesoporous polyurethane aerogels for thermal superinsulation: textural properties and thermal conductivity [J]. European Physical Journal, 2015, 224:1737-1747.
[177] DIASCORN N, CALAS S, SALLEE H, et al. Polyurethane aerogels synthesis for thermal insulation:textural, thermal and mechanical properties [J]. Journal of Supercritical Fluids, 2015, 106: 76-84.
[178] BIESMANS G, RANDALL D, FRANCAIS E, et al. Polyurethane-based organic aerogels' thermal performance [J]. Journal of Non-Crystalline Solids, 1998, 225: 36-40.
[179] RIGACCI A, MARECHAL JC, REPOUX M, et al. Preparation of polyurethane-based aerogels and xerogels for thermal superinsulation [J]. Journal of Non-Crystalline Solids, 2004, 350: 372-378.
[180] GAVILLON R, BUDTOVA T. Aerocellulose: new highly porous cellulose prepared from cellulose-NaOH aqueous solutions [J]. Biomacromolecules, 2008, 9: 269-277.
[181] AULIN C, NETRVAL J, W GBERG L, et al. Aerogels from nanofibrillated cellulose with tunable oleophobicity [J]. Soft Matter, 2010, 6: 3298-3305.
[182] TINGAUT P, ZIMMERMANN T.SEBE G. Cellulose nanocrystals and microfibrillated cellulose as building blocks for the design of hierarchical functional materials [J]. Journal of Materials Chemistry, 2012,22: 20105-20111.
[183] CARPENTER AW, DE LANNOY CF, WIESNER MR. Cellulose nanomaterials in water treatment technologies [J]. Environmental Science & Technology, 2015, 49: 5277-5287.
[184] YANG X, CRANSTON ED. Chemically cross-linked cellulose nanocrystal aerogels with shape recovery and superabsorbent properties [J]. Chemistry of Materials, 2014, 26: 6016-6025.
[185] VALO H, AROLA S, LAAKSONEN P, et al. Drug release from nanoparticles embedded in four different nanofibrillar cellulose aerogels [J]. European Journal of Pharmaceutical Sciences, 2013, 50: 69-77.
[186] WEI H, RODRIGUEZ K, RENNECKAR S, et al. Environmental science and engineering applications of nanocellulose-based nanocomposites [J]. Environmental Science Nano, 2014, 1: 302-316.
[187] OLSSON RT, SAMIR MASA, SALAZAR-ALVAREZ G, et al. Making flexible magnetic aerogels and stiff magnetic nanopaper using cellulose nanofibrils as templates [J]. Nature Nanotechnology, 2010, 5:584-588.
[188] EL KADIB A, MOLVINGER K, GUIMON C, et al. Design of stable nanoporous hybrid chitosan/titania as cooperative bifunctional catalysts [J]. Chemistry of Materials, 2008, 20: 2198-2204.
[189] LEE EJ, SHIN DS, KIM HE, et al. Membrane of hybrid chitosan-silica xerogel for guided bone regeneration [J]. Biomaterials, 2009, 30: 743-750.
[190] ZHENG Q, CAI Z, GONG S. Green synthesis of polyvinyl alcohol (PVA)-cellulose nanofibril (CNF)hybrid aerogels and their use as superabsorbents [J]. Journal of Materials Chemistry A, 2014, 2:3110-3118.
[191] ZHENG Q, JAVADI A, SABO R, et al. Polyvinyl alcohol (PVA)-cellulose nanofibril (CNF)-multiwalled carbon nanotube (MWCNT) hybrid organic aerogels with superior mechanical properties [J]. RSC Advances, 2013, 3: 20816-20823.
[192] JAVADI A, ZHENG Q, PAYEN F, et al. Polyvinyl alcohol-cellulose nanofibrils-graphene oxide hybrid organic aerogels [J]. ACS Applied Materials & Interfaces, 2013, 5: 5969-5975.
[193] KIM HM, NOH YJ, YU J, et al. Silica aerogel/polyvinyl alcohol (PVA) insulation composites with preserved aerogel pores using interfaces between the superhydrophobic aerogel and hydrophilic PVA solution [J]. Composites A, 2015, 75: 39-45.
[194] DUAN Y, JANA SC,LAMA B, et al. Reinforcement of silica aerogels using silane-end-capped polyurethanes [J]. Langmuir, 2013, 29: 6156-6165.
[195] LI L, YALCIN B, NGUYEN BN, et al. Flexible nanofiber-reinforced aerogel (xerogel) synthesis,manufacture, and characterization [J]. ACS Applied Materials & Interfaces, 2009, 1: 2491-2501.
[196] EICHHORN SJ, DUFRESNE A, ARANGUREN M, et al. Current international research into cellulose nanofibres and nanocomposites [J]. Journal of Materials Science, 2010, 45: 1-33.
[197] SAI H, XING L, XIANG J, et al. Effects of surfactants on the synthesis of silica aerogels prepared by ambient pressure drying [J]. Key Engineering Materials, 2012, 512-515: 1625-1630.
[198] SAI HZ, XING L, XIANG JH, et al. Flexible aerogels with interpenetrating network structure of bacterial cellulose-silica composite from sodium silicate precursor via freeze drying process [J]. RSC Advances,2014, 4: 30453-30461.
[199] SAI H, FU R, XING L, et al. Surface modification of bacterial cellulose aerogels' web-like skeleton for oil/water separation [J]. ACS Applied Materials & Interfaces, 2015, 7: 7373-7381.
[200] BRYNING MB, MILKIE DE, ISLAM MF, et al. Carbon nanotube aerogels [J]. Advanced Materials, 2007,19: 661-664.
[201] ALIEV AE, OH JY, KOZLOV ME, et al. Giant-stroke, superelastic carbon nanotube aerogel muscles [J].Science, 2009, 323: 1575-1578.
[202] WORSLEY MA, KUCHEYEV SO, KUNTZ JD, et al. Stiff and electrically conductive composites of carbon nanotube aerogels and polymers [J]. Journal of Materials Chemistry, 2009, 19: 3370-3372.
[203] WORSLEY MA, KUCHEYEV SO, SATCHER JH, et al. Mechanically robust and electrically conductive carbon nanotube foams [J]. Applied Physics Letters, 2009, 94: 787-781
[204] WORSLEY MA, PAUZAUSKIE PJ, KUCHEYEV SO, et al. Properties of single-walled carbon nanotubebased aerogels as a function of nanotube loading [J]. Acta Materialia, 2009, 57: 5131-5136.
[205] WORSLEY MA, SATCHER JH, JR..BAUMANN TF. Enhanced thermal transport in carbon aerogel nanocomposites containing double-walled carbon nanotubes [J]. Journal of Applied Physics, 2009, 105:845-848.
[206] KIM KH, OH Y, ISLAM MF. Graphene coating makes carbon nanotube aerogels superelastic and resistant to fatigue [J]. Nature Nanotechnology, 2012, 7: 562-566.
[207] WANG J, ELLSWORTH MW. Graphene Aerogels [C] // OBENG Y, DE GENDT Y, SRINIVASAN.Graphene and Emerging Materials for Post-Cmos Applications, Vol. 19. USA, Pennington:Electrochemical Society Inc, 2009: 241-247.
[208] BAE S, KIM H, LEE Y, et al. Roll-to-roll production of 30-inch graphene films for transparent electrodes[J]. Nature Nanotechnology, 2010, 5: 574-578.
[209] ENGLERT JM, DOTZER C, YANG G, et al. Covalent bulk functionalization of graphene [J]. Nature Chemistry, 2011, 3: 279-286.
[210] JIANG X, MA Y, LI J, et al. Self-assembly of reduced graphene oxide into three-dimensional architecture by divalent ion linkage [J]. Journal of Physical Chemistry C, 2010, 114: 22462-22465.
[211] TANG Z, SHEN S, ZHUANG J, et al. Noble-metal-promoted three-dimensional macroassembly of singlelayered graphene oxide [J]. Angewandte Chemie International Edition, 2010, 49: 4603-4607.
[212] XU Y, SHENG K, LI C, et al. Self-assembled graphene hydrogel via a one-step hydrothermal process [J].ACS Nano, 2010, 4: 4324-4330.
[213] BI H, YIN K, XIE X, et al. Low temperature casting of graphene with high compressive strength [J].Advanced Materials, 2012, 24: 5124-5129.
[214] ZHAO J, REN W, CHENG HM. Graphene sponge for efficient and repeatable adsorption and desorption of water contaminations [J]. Journal of Materials Chemistry, 2012, 22: 20197-20202.
[215] ZHAO Y, HU C, HU Y, et al. A versatile, ultralight, nitrogen-doped graphene framework [J]. Angewandte Chemie International Edition, 2012, 51: 11371-11375.
[216] WORSLEY MA, PAUZAUSKIE PJ, OLSON TY, et al. Synthesis of graphene aerogel with high electrical conductivity [J]. Journal of the American Chemical Society, 2010, 132: 14067-14069.
[217] CHEN W, YAN L. In situ self-assembly of mild chemical reduction graphene for three-dimensional architectures [J]. Nanoscale, 2011, 3: 3132-3137.
[218] HAI DINH P, VIET HUNG P, TRAN VIET C, et al. Synthesis of the chemically converted graphene xerogel with superior electrical conductivity [J]. Chemical Communications, 2011, 47: 9672-9674.
[219] ZHANG X, SUI Z, XU B, et al. Mechanically strong and highly conductive graphene aerogel and its use as electrodes for electrochemical power sources [J]. Journal of Materials Chemistry, 2011, 21: 6494-6497.
[220] CHEN K, CHEN L, CHEN Y, et al. Three-dimensional porous graphene-based composite materials:electrochemical synthesis and application [J]. Journal of Materials Chemistry, 2012, 22: 20968-20976.
[221] SHENG K, SUN Y, LI C, et al. Ultrahigh-rate supercapacitors based on eletrochemically reduced graphene oxide for ac line-filtering [J]. Scientific Reports, 2012, 2: 247-250.
[222] LEE SH, KIM HW, HWANG JO, et al. Three-dimensional self-assembly of graphene oxide platelets into mechanically flexible macroporous carbon films [J]. Angewandte Chemie International Edition, 2010, 49:10084-10088.
[223] YIN S, ZHANG Y, KONG J, et al. Assembly of graphene sheets into hierarchical structures for highperformance energy storage [J]. ACS Nano, 2011, 5: 3831-3838.
[224] CHEN Z, REN W, GAO L, et al. Three-dimensional flexible and conductive interconnected graphene networks grown by chemical vapour deposition [J]. Nature Materials, 2011, 10: 424-428.
[225] HU H, ZHAO Z, ZHOU Q, et al. The role of microwave absorption on formation of graphene from graphite oxide [J]. Carbon, 2012, 50: 3267-3273.
[226] QIU L, LIU JZ, CHANG SLY, et al. Biomimetic superelastic graphene-based cellular monoliths [J].Nature Communications, 2012, 3: 1241-1243
[227] YANG F, WANG X, ZHANG D, et al. Chirality-specific growth of single-walled carbon nanotubes on solid alloy catalysts [J]. Nature, 2014, 510: 522-524.
[228] DU R, ZHAO Q, ZHANG N, et al. Macroscopic carbon nanotube-based 3D monoliths [J]. Small, 2015, 11:3263-3289.
[229] GUI X, WEI J, WANG K, et al. Carbon nanotube sponges [J]. Advanced Materials, 2010, 22: 617-621.
[230] XU M, FUTABA DN, YAMADA T, et al. Carbon nanotubes with temperature-invariant viscoelasticity from -196°C to 1000°C [J]. Science, 2010, 330: 1364-1368.
[231] XU M, FUTABA DN, YUMURA M, et al. Carbon nanotubes with temperature-invariant creep and creep-recovery from -190°C to 970°C [J]. Advanced Materials, 2011, 23: 3686-3691.
[232] XU M, FUTABA DN, YUMURA M, et al. Tailoring temperature invariant viscoelasticity of carbon nanotube material [J]. Nano Letters, 2011, 11: 3279-3284.
[233] LIN Z, ZENG Z, GUI X, et al. Carbon nanotube sponges, aerogels, and hierarchical composites: synthesis,properties, and energy applications [J]. Advanced Energy Materials, 2016, 6: No. 1600554.
[234] JIANG F, FANG Y, LIU Y, et al. Paper-like 3-dimensional carbon nanotubes (CNTs)-microfiber hybrid: a promising macroscopic structure of CNTs [J]. Journal of Materials Chemistry, 2009, 19: 3632-3637.
[235] FU Y, CARLBERG B, LINDAHL N, et al. Templated growth of covalently bonded three-dimensional carbon nanotube networks originated from graphene [J]. Advanced Materials, 2012, 24: 1576-1581.
[236] KOHLMEYER RR, LOR M, DENG J, et al. Preparation of stable carbon nanotube aerogels with high electrical conductivity and porosity [J]. Carbon, 2011, 49: 2352-2361.
[237] DONG L, YANG Q, XU C, et al. Facile preparation of carbon nanotube aerogels with controlled hierarchical microstructures and versatile performance [J]. Carbon, 2015, 90: 164-171.
[238] WU ZY, LI C, LIANG HW, et al. Ultralight, flexible, and fire-resistant carbon nanofiber aerogels from bacterial cellulose [J]. Angewandte Chemie International Edition, 2013, 52: 2925-2929.
[239] KIM KH, OH Y, ISLAM MF. Mechanical and thermal management characteristics of ultrahigh surface area single-walled carbon nanotube aerogels [J]. Advanced Functional Materials, 2013, 23: 377-383.
[240] WHITBY RLD, FUKUDA T, MAEKAWA T, et al. Real-time imaging of complex nanoscale mechanical responses of carbon nanotubes in highly compressible porous monoliths [J]. Nanotechnology, 2010, 21:No.075707.
[241] WHITBY RLD, MIKHALOVSKY SV, GUN'KO VM. Mechanical performance of highly compressible multi-walled carbon nanotube columns with hyperboloid geometries [J]. Carbon, 2010, 48: 145-152.
[242] LIU Y, BA H, DINH-LAM N, et al. Synthesis of porous carbon nanotubes foam composites with a high accessible surface area and tunable porosity [J]. Journal of Materials Chemistry A, 2013, 1: 9508-9516.
[243] ZOU J, LIU J, KARAKOTI AS, et al. Ultralight multiwalled carbon nanotube aerogel [J]. ACS Nano,2010, 4: 7293-7302.
[244] SATO Y, OOTSUBO M, YAMAMOTO G, et al. Super-robust, lightweight, conducting carbon nanotube blocks cross-linked by de-fluorination [J]. ACS Nano, 2008, 2: 348-356.
[245] OZDEN S, NARAYANAN TN, TIWARY CS, et al. 3D macroporous solids from chemically cross-linked carbon nanotubes [J]. Small, 2015, 11: 688-693.
[246] DU R, ZHANG N, ZHU J, et al. Nitrogen-doped carbon nanotube aerogels for high-performance ORR catalysts [J]. Small, 2015, 11: 3903-3908.
[247] KIM KH, VURAL M, ISLAM MF. Single-walled carbon nanotube aerogel-based elastic conductors [J].Advanced Materials, 2011, 23: 2865-2869.
[248] JEONG YJ, ISLAM MF. Compressible elastomeric aerogels of hexagonal boron nitride and single-walled carbon nanotubes [J]. Nanoscale, 2015, 7: 12888-12894.
[249] CHEN L, DU R, ZHU J, et al. Three-dimensional nitrogen-doped graphene nanoribbons aerogel as a highly efficient catalyst for the oxygen reduction reaction [J]. Small, 2015, 11: 1423-1429.
[250] WORSLEY MA, OLSON TY, LEE JRI, et al. High surface srea, sp2-cross-linked three-dimensional graphene monoliths [J]. Journal of Physical Chemistry Letters, 2011, 2: 921-925.
[251] HU H, ZHAO Z, WAN W, et al. Ultralight and highly compressible graphene aerogels [J]. Advanced Materials, 2013, 25: 2219-2223.
[252] LIN X, LIU P, WEI Y, et al. Development of an ultra-thin film comprised of a graphene membrane and carbon nanotube vein support [J]. Nature Communications, 2013, 4: 10.1038/ncomms3920.
[253] ZHANG M, ATKINSON KR, BAUGHMAN RH. Multifunctional carbon nanotube yarns by downsizing an ancient technology [J]. Science, 2004, 306: 1358-1361.
[254] ZHANG M, GAO B, CAO X, et al. Synthesis of a multifunctional graphene-carbon nanotube aerogel and its strong adsorption of lead from aqueous solution [J]. RSC Advances, 2013, 3: 2109921105.
[255] XU Z, SUN H, ZHAO X, et al. Ultrastrong fibers assembled from giant graphene oxide sheets [J].Advanced Materials, 2013, 25: 188-193.
[256] SUN H, XU Z, GAO C. Multifunctional, ultra-flyweight, synergistically assembled carbon aerogels [J].Advanced Materials, 2013, 25: 2554-2560.
[257] LI P, KONG C, SHANG Y, et al. Highly deformation-tolerant carbon nanotube sponges as supercapacitor electrodes [J]. Nanoscale, 2013, 5: 8472-8479.
[258] ZHONG J, YANG Z, MUKHERJEE R, et al. Carbon nanotube sponges as conductive networks for supercapacitor devices [J]. Nano Energy, 2013, 2: 1025-1030.
[259] TANG Z, TANG CH, GONG H. A high energy density asymmetric supercapacitor from nanoarchitectured Ni(OH)2/carbon nanotube electrodes [J]. Advanced Functional Materials, 2012, 22:1272-1278.
[260] CHENG X, GUI X, LIN Z, et al. Three-dimensional α-Fe2O3/carbon nanotube sponges as flexible supercapacitor electrodes [J]. Journal of Materials Chemistry A, 2015, 3: 20927-20934.
[261] HU L, WU H, GAO Y, et al. Silicon-carbon nanotube coaxial sponge as Li-ion anodes with high areal capacity [J]. Advanced Energy Materials, 2011, 1: 523-527.
[262] CHEN X, POMERANTSEVA E, BANERJEE P, et al. Ozone-based atomic layer deposition of crystalline V2O5films for high performance electrochemical energy storage [J]. Chemistry of Materials, 2012, 24:1255-1261.
[263] CHEN X, POMERANTSEVA E, GREGORCZYK K, et al. Cathodic ALD V2O5thin films for high-rate electrochemical energy storage [J]. RSC Advances, 2013, 3: 4294-4302.
[264] GREGORCZYK KE, KOZEN AC, CHEN X, et al. Fabrication of 3D core-shell multiwalled carbon nanotube@RuO2lithium-ion battery electrodes through a RuO2atomic layer deposition process [J]. ACS Nano, 2015, 9: 464-473.
[265] SHEN Y, SUN D, YU L, et al. A high-capacity lithium-air battery with Pd modified carbon nanotube sponge cathode working in regular air [J]. Carbon, 2013, 62: 288-295.
[266] WOAN K, PYRGIOTAKIS G, SIGMUND W. Photocatalytic carbon-nanotube-TiO2composites [J].Advanced Materials, 2009, 21: 2233-2239.
[267] LI H, GUI X, JI C, et al. Photocatalytic, recyclable CdS nanoparticle-carbon nanotube hybrid sponges [J].Nano Research, 2012, 5: 265-271.
[268] ALNAIEF M, ANTONYUK S, HENTZSCHEL CM, et al. A novel process for coating of silica aerogel microspheres for controlled drug release applications [J]. Microporous and Mesoporous Materials, 2012,160: 167-173.
[269] YANG KL, YING TY, YIACOUMI S, et al. Electrosorption of ions from aqueous solutions by nanostructured carbon aerogel [J]. Langmuir, 2001, 17: 1961-1969.
[270] GOEL J, KADIRVELU K, RAJAGOPAL C, et al. Removal of mercury(II) from aqueous solution by adsorption on carbon aerogel: Response surface methodological approach [J]. Carbon, 2005, 43: 197-200.[271] BAUMANN TF, WORSLEY MA, HAN TYJ, et al. High surface area carbon aerogel monoliths with hierarchical porosity [J]. Journal of Non-Crystalline Solids, 2008, 354: 3513-3515.
[272] WORSLEY MA, SATCHER JH, JR..BAUMANN TF. Synthesis and characterization of monolithic carbon aerogel nanocomposites containing double-walled carbon nanotubes [J]. Langmuir, 2008, 24: 9763-9766.[273] ZHANG X, LIU J, XU B, et al. Ultralight conducting polymer/carbon nanotube composite aerogels [J].Carbon, 2011, 49: 1884-1893.
[274] SCHIFFRES SN, KIM KH, HU L, et al. Gas diffusion, energy transport, and thermal accommodation in single-walled carbon nanotube aerogels [J]. Advanced Functional Materials, 2012, 22: 5251-5258.
[275] TAPPAN BC, STEINER SA, III.LUTHER EP. Nanoporous metal foams [J]. Angewandte Chemie International Edition, 2010, 49: 4544-4565.
[276] RANMOHOTTI KGS, GAO X, ARACHCHIGE IU. Salt-mediated self-assembly of metal nanoshells into monolithic aerogel frameworks [J]. Chemistry of Materials, 2013, 25: 3528-3534.
[277] GAO X, ESTEVES RJ, LUONG TT, et al. Oxidation-induced self-assembly of Ag nanoshells into transparent and opaque Ag hydrogels and aerogels [J]. Journal of the American Chemical Society, 2014,136: 7993-8002.
[278] PARK JW, SHUMAKER-PARRY JS. Structural study of citrate layers on gold nanoparticles: role of intermolecular interactions in stabilizing nanoparticles [J]. Journal of the American Chemical Society,2014, 136: 1907-1921.
[279] LIU W, HERRMANN AK, GEIGER D, et al. High-performance electrocatalysis on palladium aerogels [J].Angewandte Chemie International Edition, 2012, 51: 5743-5747.
[280] LIU W, RODRIGUEZ P, BORCHARDT L, et al. Bimetallic aerogels: high-performance electrocatalysts for the oxygen reduction reaction [J]. Angewandte Chemie International Edition, 2013, 52: 9849-9852.
[281] PORTER NS, WU H, QUAN ZW, et al. Shape-control and electrocatalytic activity-enhancement of Pt-based bimetallic nanocrystals [J]. Accounts of Chemical Research, 2013, 46: 1867-1877.
[282] WU JB, YANG H. Platinum-based oxygen reduction electrocatalysts [J]. Accounts of Chemical Research,2013, 46: 1848-1857.
[283] PARLETT CMA, WILSON K, LEE AF. Hierarchical porous materials: catalytic applications [J].Chemical Society Reviews, 2013, 42: 3876-3893.
[284] HAYDEN BE. Particle size and support effects in electrocatalysis [J]. Accounts of Chemical Research,2013, 46: 1858-1866.
[285] PEREZ-ALONSO FJ, MCCARTHY DN, NIERHOFF A, et al. The effect of size on the oxygen electroreduction activity of mass-selected platinum nanoparticles [J]. Angewandte Chemie International Edition, 2012, 51: 4641-4643.
[286] RABIS A, RODRIGUEZ P, SCHMIDT TJ. Electrocatalysis for polymer electrolyte fuel cells: recent achievements and future challenges [J]. ACS Catalysis, 2012, 2: 864-890.
[287] CUI CH, YU SH. Engineering interface and surface of noble metal nanoparticle nanotubes toward enhanced catalytic activity for fuel cell applications [J]. Accounts of Chemical Research, 2013, 46:1427-1437.
[288] CHEN ZW, WAJE M, LI WZ, et al. Supportless Pt and PtPd nanotubes as electrocatalysts for oxygenreduction reactions [J]. Angewandte Chemie International Edition, 2007, 46: 4060-4063.
[289] VUKMIROVIC MB, CAI Y, BLIZNAKOV ST, et al. Platinum monolayer electrocatalysts for the oxygen reduction reaction [C] // ZAWODZINSKI T, MUKERJEE S, STRASSER P, Tutorials on Electrocatalysis in Low Temperature Fuel Cells, Vol. 45. ECS Transactions, 2003: 15-23.

第一作者章婷,1991年生,女,浙江金华人,中国科学院大学在读博士研究生。从事气凝胶材料的研究工作,主要集中于金属气凝胶材料的制备及其催化性能的研究。获国家实用新型专利1项。

向军辉,中国科学院大学教授,博士生导师。科研工作主要集中于无机非金属材料领域,涉及先进陶瓷材料、新能源材料、纳米材料、超轻材料等方向。代表性研究论文发表于 Advanced Materials、Langmuir、RSC Advances、Journal of Materials Chemistry A等高影响国际学术期刊。通过双相界面仿生自组装实现柔性衬底上光电材料的精确定位定向制备,在石墨烯透明导电膜、染料敏化太阳电池氧化物光阳极的制备方面取得重要进展。在气凝胶材料的结构优化方面获得突破性成果,提出“多尺度多重网络复合结构气凝胶”的理论模型,并在此基础上开发了自主知识产权的气凝胶非超临界制备技术,推动了气凝胶领域生产方式的变革。

