乳清蛋白-甘油二酯纳米乳液制备及其质量评价
汪慧超 钱 宇 薛秀恒 徐霞红
(安徽农业大学茶与食品科技学院1,合肥 230036) (安徽省农产品加工工程实验室;皖江合肥农产品加工研究院2,合肥 230036)
甘油二酯(diacylglycerol,DG),是一种甘油骨架上只有两个高级脂肪酸的油脂,属于一般公认安全(GRAS)物质[1],在天然油脂中含量很低。1,3-甘油二酯为甘油二酯两种不同异构体中的一种,脂肪酸酰基与甘油骨架中羟基形成间隔酯键。研究表明,1,3-甘油二酯具有降低血脂[2-3]、缓解糖尿病[4]、抗氧化[5]等作用。在美国、日本等国,1,3-甘油二酯已被允许作为烹调用油或食品添加剂使用[6]。但在国内关于1,3-甘油二酯在食品中应用的报道较少,且1,3-甘油二酯极易被氧化,不易贮藏,对其在食品中的应用造成很大的影响。因此,有必要使用特殊的方法,提高1,3-甘油二酯的抗氧化性,保证其在食品中的活性成分不被破坏。
纳米乳液主要是由水、脂溶性芯材、水溶性壁材和乳化剂等组成成分,按一定比例在特定条件下混合形成的分散体系,对于易于氧化水解的功效成分具有良好的保护作用,还可提高其生物利用度。水溶性壁材主要有蛋白质、多糖等,而脂溶性芯材主要有脂溶性维生素、营养素、精油、风味油脂等。纳米乳液的制备可分为高能乳化法和低能乳化法,高能乳化法[7]主要包括高压均质法、高压微射流和超声波法,而低能乳化法[8]主要包括自发乳化法和相转变法。高能乳化法是制备纳米乳液最常用的方法,可用于大规模的工业化生产,且适用于大多数材料,而高压均质法是高能乳化法中使用最普遍的一种。
本研究采用高压均质法,以乳清蛋白为壁材,1,3-甘油二酯为芯材,采用响应面分析法优化乳清蛋白-甘油二酯纳米乳液的制备,并对其表面性质、表征及温度、氧化、贮藏稳定性进行研究,为乳清蛋白-甘油二酯纳米乳液在食品中的应用提供参考。
1 材料与方法
1.1 材料与试剂
乳清蛋白粉:美国唐瑞斯食品物料公司;蔗糖酯SE-11:河南千志商贸有限公司;正己烷(色谱纯)、异丙醇(色谱纯):国药集团化学试剂有限公司;富含1,3-甘油二酯乳脂:实验室自制。
1.2 主要仪器与设备
高速分散器:上海FLUKO有限公司;超高压纳米均质机:德国APV2000公司;Zeta电位及纳米粒度测定仪:英国Malvern公司;OXITEST油脂氧化分析仪:意大利VELP公司;高效液相色谱仪:美国Waters公司。
1.3 方法
1.3.1 乳清蛋白-甘油二酯纳米乳液的制备
采用高压均质法制备纳米乳液。将乳清蛋白粉加入蒸馏水中搅拌至完全溶解,制得乳清蛋白溶液;再将乳脂甘油二酯与乳化剂蔗糖酯混合,在50 ℃水浴中搅拌直至完全溶解,得到混合物;然后将乳清蛋白溶液缓慢倒入混合物中,边倒边搅拌,得到混合乳液;最后将混合乳液2 000 r/min高速分散3 min,并在超高压纳米均质机中进行均质,得到乳清蛋白-甘油二酯纳米乳液。
1.3.2 乳清蛋白-甘油二酯纳米乳液制备的单因素实验
按操作步骤制备乳清蛋白-甘油二酯纳米乳液,以纳米乳液的粒径和包埋率为综合评价指标,分别考察不同壁材浓度(占蒸馏水的百分比:5%、10%、15%、20%、25%)、不同壁芯比(1∶1、2∶1、3∶1、4∶1、5∶1)、不同乳化剂添加量(占总固形物含量的百分比:0,2%、4%、6%、8%)、不同均质压力(30、60、90、120、150 MPa)、不同均质循环次数(2、6、10、14、18)对纳米乳液制备的影响。
1.3.3 乳清蛋白-甘油二酯纳米乳液制备的响应面实验
为确定乳清蛋白-甘油二酯纳米乳液的最佳配方,在单因素实验的基础上,固定高压均质的压力与循环次数,采用Box-Behnken设计,以壁材浓度、壁芯比、乳化剂添加量为因素,以包埋率响应值,进行响应面实验,优化乳清蛋白-甘油二酯纳米乳液制备的工艺参数,因素水平编码如表1所示。

表1 响应面实验因素水平编码表
1.3.4 乳清蛋白-甘油二酯纳米乳液的评价指标1.3.4.1 纳米乳液粒径及Zeta电位的测定
采用Zeta电位及纳米粒度测定仪测定乳清蛋白-甘油二酯纳米乳液的粒径及表面电位。
1.3.4.2 纳米乳液包埋率的测定
采用高效液相色谱仪分别对纳米乳液的表面油及总油进行测定,并按公式计算。

表面油的测定:取制备好的纳米乳液,加入正己烷/异丙醇(15∶1),反复萃取后合并有机相并定容,用高效液相色谱法测定乳脂甘油二酯含量。
总油的测定:将制备好的纳米乳在超声波细胞破碎仪中破乳后,加入正己烷/异丙醇(15∶1),反复萃取后合并有机相并定容,用高效液相色谱测定乳脂甘油二酯含量。
高效液相色谱条件:流动相为正己烷/异丙醇(15∶1),流速1 mL/min,柱温35 ℃,色谱柱为Luna silica C18(5 μm,250×4.6 mm,Phenomenex)。使用示差检测器进行检测,检测器温度35 ℃。实验结果通过峰的峰面积来定量测定。
1.3.5 乳清蛋白-甘油二酯纳米乳液的质量评价1.3.5.1 透射电镜
采用JEM-100SX型透射电镜对纳米乳液的粒径及分布情况进行测定。取一定量的样品滴于干净的铜网表面,经1%磷钨酸染色后自然风干,并利用透射电镜进行观察。
1.3.5.2 红外光谱
采用傅里叶红外光谱仪进行测定,在4 000~400 cm-1范围内进行扫描。
1.3.5.3 温度稳定性
将制备好的纳米乳液分别放置于20、30、40、50、60、70、80、90 ℃水浴锅中加热30 min,然后在室温中静置12 h,测定纳米乳液的粒径和包埋率。
1.3.5.4 氧化稳定性
利用OXITEST油脂氧化分析仪对乳清蛋白-甘油二酯纳米乳液的氧化稳定性进行测定。
1.3.5.5 贮藏稳定性
将制备好的纳米乳液分别放置于4 ℃(冷藏)、25 ℃(常温)、37 ℃(体温)贮藏1个月,每隔5 d取样测定其包埋率,研究不同贮藏温度对纳米乳液稳定性的影响。
1.4 数据分析
利用Design-expert 8.05和Origin Pro 9.0软件对数据进行处理分析。
2 结果与分析
2.1 单因素实验结果
2.1.1 壁材浓度对纳米乳液制备的影响
在固定壁芯比为3∶1,乳化剂添加量为4%,均质压力为90 MPa,均质循环次数为10次时,不同壁材浓度对纳米乳液制备的影响如图1所示。从图1可以看出,随着壁材浓度的升高,纳米乳液的粒径先减小后增大,包埋率先增大后减小,在壁材质量分数为15%时,粒径与包埋率均达到最值。由于乳清蛋白本身具有一定的乳化性,随着壁材浓度的升高,纳米乳液的乳化作用增强,有利于纳米乳液中纳米颗粒的形成,包埋率较高,当壁材浓度过高时,体系黏度过大,不利于分散,导致包埋率降低,粒径增大。因此,选择15%为壁材最佳质量浓度。
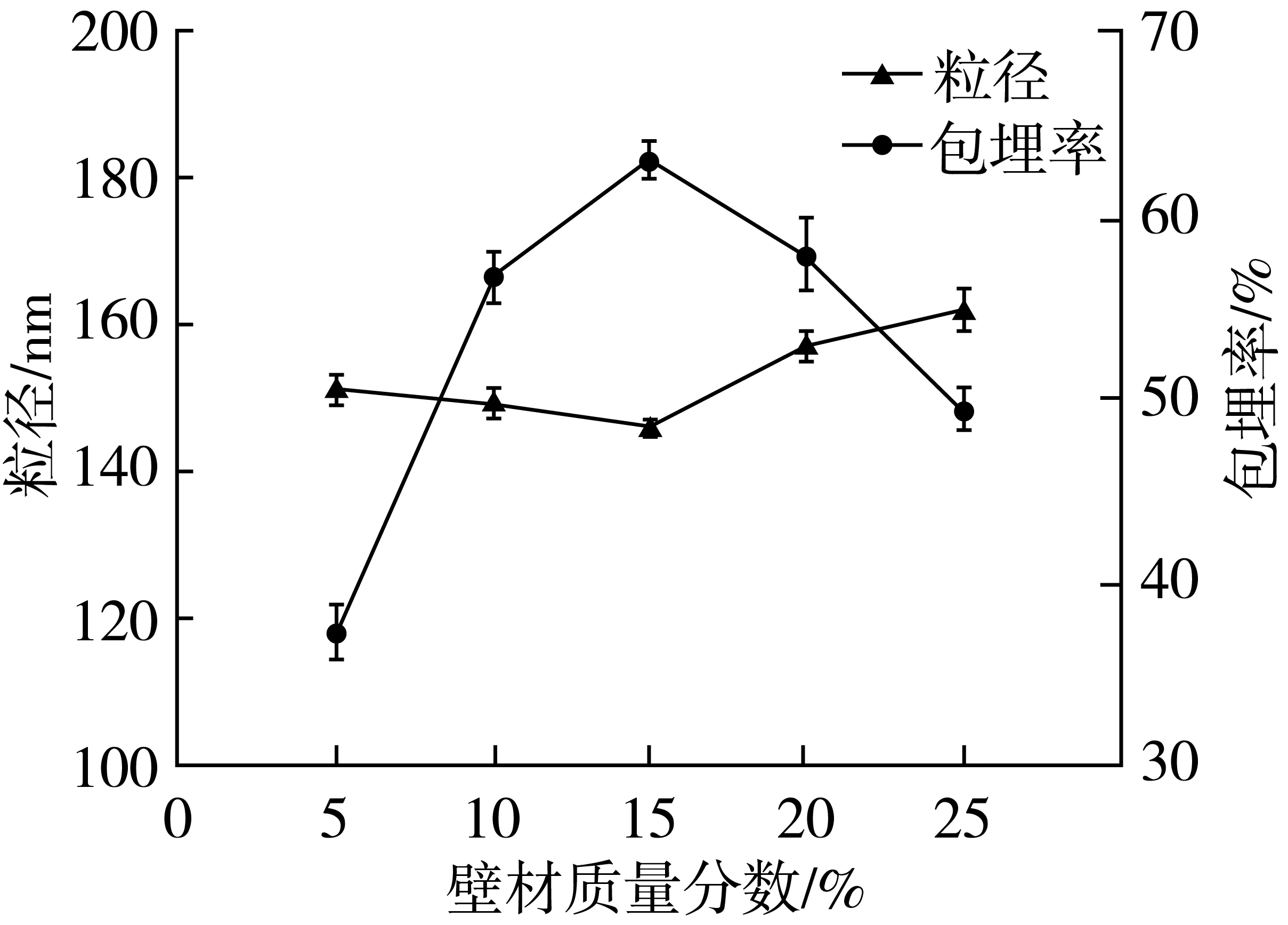
图1 壁材浓度对纳米乳液制备的影响
2.1.2 壁芯比对纳米乳液制备的影响
在选择壁材质量分数为15%的基础上,固定乳化剂添加量为4%,均质压力为90 MPa,均质循环次数为10次时,不同壁芯比对纳米乳液制备的影响如图2所示。从图2可以看出,随着壁芯比的增大,纳米乳液的粒径先迅速减小后缓慢减小,包埋率先增大后减小,在壁芯比为2∶1~4∶1时包埋率增加趋势最大,在壁芯比为4∶1时,包埋率达到最大值。开始时,芯材过多,壁材不足,不能很好的包被乳脂甘油二酯,粒径较大,包埋率较低。随着壁芯比的增大,芯材含量逐渐减少,纳米乳液粒径逐渐减小,包埋率逐渐升高,包被效果较好。但当壁芯比过大时,芯材含量过少,反而导致包埋率的下降。因此,壁芯比为4∶1时,纳米乳液效果最佳。

图2 壁芯比对纳米乳液制备的影响
2.1.3 乳化剂添加量对纳米乳液制备的影响
在选择壁材质量分数为15%、壁芯比为4∶1的基础上,固定均质压力为90 MPa,均质循环次数为10次时,不同乳化剂添加量对纳米乳液制备的影响如图3所示。随着乳化剂的增多,纳米乳液的粒径先减小后增大,包埋率先升高后降低,均在乳化剂添加量为4%时达到最值。添加一定量的乳化剂能提高纳米乳液的乳化性能,有助于纳米乳液中纳米颗粒的形成,但添加量过多时,反而导致粒径增大,包埋率降低。因此以乳化剂添加量4%为最适添加量。

图3 乳化剂添加量对纳米乳液制备的影响
2.1.4 均质压力对纳米乳液制备的影响
在选择壁材质量分数为15%、壁芯比为4∶1、乳化剂添加量4%的基础上,固定均质循环次数为10次时,不同均质压力对纳米乳液制备的影响如图4所示。从图4可以看出,随着均质压力的增大,纳米乳液的粒径先迅速减小,后缓慢增大,在90 MPa时粒径最小。纳米乳液包埋率先升高后降低,也在90 MPa时达到最大值。均质压力的增大,可使纳米乳液在超高压均质过程中混合得更均匀,被分散成更小的颗粒,使纳米乳液粒径减小,包埋率增加。但均质压力过高时,可能会导致纳米乳液被破坏,且部分纳米颗粒会发生聚合,反而导致粒径增大,包埋率降低。因此90 MPa为最佳的均质压力。

图4 均质压力对纳米乳液制备的影响
2.1.5 均质循环次数对纳米乳液制备的影响
在选择壁材质量分数为15%、壁芯比为4∶1、乳化剂添加量4%、均质压力为90 MPa的基础上,不同均质循环次数对纳米乳液制备的影响如图5所示。由图5可知,随着循环次数的增多,纳米乳液的粒径开始时迅速减小,后减小速度极慢,基本保持平衡。包埋率先增加,后逐渐减小,在循环次数为6次时,包埋率最大。高压均质循环一定的次数可使纳米乳液混合更加均匀,粒径分布更加集中,包埋效果更好。但循环次数过多时,机器温度过高,会对纳米乳液造成一定的破坏,导致包埋率迅速降低。综合考虑,最佳高压均质循环次数为6次。

图5 均质循环次数对纳米乳液制备的影响
2.2 响应面实验
2.2.1 响应面实验结果
根据Box-Behnken design实验设计原理,以壁材浓度、壁芯比、乳化剂添加量为自变量,乳清蛋白-甘油二酯纳米乳液的包埋率为因变量,利用响应面分析法优化乳清蛋白-甘油二酯纳米乳液的配方,实验设计及结果见表2。

表2 响应面实验设计及结果
对实验数据进行分析,得到响应面回归模拟方程:
Y=73.94+5.26A-4.35B-2.66C+2.35AB-1.17AC-5BC-11.26A2-3.08B2-25.16C2
由表3可知,模型的P值<0.000 1,说明该模型极显著,失拟项P值为0.068 1>0.05,不显著,说明该模型能很好的拟合实验的真实情况,可以用于乳清蛋白-甘油二酯纳米乳液工艺的优化。通过方差分析结果可知,壁材浓度、壁芯比及乳化剂添加量对纳米乳液包埋率的影响均极显著。而在交互作用中,壁材浓度和壁芯比的交互作用显著,壁芯比及乳化剂添加量的交互作用极显著。

表3 回归方程方差分析表
注:**表示差异极显著;*表示差异显著。
2.2.2 响应面实验因素间交互作用分析
将响应面实验中一个因素设为零水平,其他两个因素交互作用的响应面及等高线图见图6和图7。
图6为壁材浓度和壁芯比交互作用对乳清蛋白-甘油二酯纳米乳液包埋率的影响。当壁材浓度固定时,随着壁芯比的增大,纳米乳液包埋率先升高后降低;当壁芯比保持一定时,随着壁材浓度的增加,纳米乳液包埋率也呈现先升高后降低的趋势。壁材浓度和壁芯比交互作用等高线图呈椭圆形,表明在实验设定的壁材浓度和壁芯比区间内,存在最大交互区间。
图7为壁芯比和乳化剂添加量交互作用对乳清蛋白-甘油二酯纳米乳液包埋率的影响。从图7中可以看出,响应面坡度较陡,壁芯比和乳化剂添加量交互作用极显著。当壁芯比保持一定时,随着乳化剂添加量的增加,纳米乳液包埋率呈先升高后降低的趋势;当壁芯比固定时,随着乳化剂添加量的增大,纳米乳液包埋率也呈现先升高后降低。壁芯比和乳化剂添加量交互作用等高线图也呈椭圆形,表明在实验设定壁芯比和乳化剂添加量区间内,存在最大交互区间。

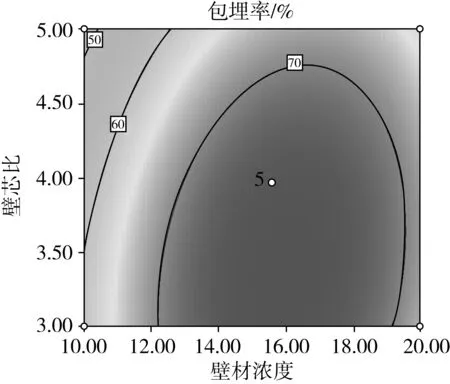
图6 壁材浓度和壁芯比交互作用响应面图及等高线图


图7 壁芯比和乳化剂添加量交互作用响应面图及等高线图
2.2.3 最佳工艺条件的确定及验证
根据模型预测结果,乳清蛋白-甘油二酯纳米乳液的最佳工艺条件为:壁材质量浓度15.83%,壁芯比3.35∶1,乳化剂添加量4.02%。按上述条件制备乳清蛋白-甘油二酯纳米乳液,经3次重复实验,制得的纳米乳液的包埋率为75.5%,与理论值75.776 5%接近,实际测定值与预测的理论值之间相对误差较小,因此,基于响应面法得到的工艺条件是可行的,有实用价值。
2.3 纳米乳液粒径及Zeta电位的测定
通过Zeta电位及纳米粒度测定仪对乳清蛋白-甘油二酯纳米乳液进行测定,其粒径及分布情况如图8所示。由图8可知,纳米乳液粒径呈正态分布,大部分集中在100 nm左右。乳清蛋白-甘油二酯纳米乳液Zeta电位、平均粒径及PDI分散指数见表4。由表4可知,纳米乳液的Zeta电位在-23 mV左右,带负电荷,平均粒径在142 nm左右,PDI指数在0.238左右,表明制得的纳米乳液粒径分布均匀。

图8 乳清蛋白-甘油二酯纳米乳液粒径及分布情况 表4 纳米乳液Zeta电位、平均粒径及PDI分散指数

项目Zeta电位/mV平均粒径/nmPDI1-22.79142.20.2342-23.06140.50.2383-23.70143.70.2394-23.77141.80.2385-23.55142.60.239
2.4 纳米乳液的表征
2.4.1 透射电镜
乳清蛋白及纳米乳液的透射电镜结果如图7所示。从图7中可以看出,经过均质处理后的乳清蛋白粒径较小,仅为几十纳米,形状不规则。乳清蛋白-甘油二酯纳米乳液呈现近似球形,中间芯材甘油二酯部分较亮,粒径为80~200 nm左右,纳米乳液中纳米颗粒具有明显的海岛状壳核结构,表明包被效果较好。

图9 乳清蛋白及纳米乳液的透射电镜图
2.4.2 红外光谱


图10 纳米乳液(a)、乳清蛋白(b)及甘油二酯(c)的红外光谱图
2.5 稳定性实验
2.5.1 温度稳定性
不同温度处理对纳米乳液粒径及包埋率的影响如图11所示。随着处理温度的升高,纳米乳液的粒径略微升高,但是总体基本保持平衡;包埋率逐渐降低,在20~80 ℃下降速度较慢,但在80 ℃之后包埋率下降迅速,可能是由于处理温度较高,对纳米乳液造成一定的破坏,导致包埋率迅速降低。因此,在80 ℃以下,纳米乳液相对较稳定。

图11 不同温度处理对纳米乳液粒径及包埋率的影响
2.5.2 氧化稳定性
纳米乳液的氧化稳定性经OXITEST油脂氧化仪测试结果如图12所示。从图12中可看出,乳脂甘油二酯在较短的时间内急剧氧化,在20 h趋于氧化完全,20 h以后氧压下降极缓慢,基本处于平衡状态。而经超高压纳米均质处理的乳清蛋白-甘油二酯纳米乳液氧化速度则非常缓慢,氧化稳定性较好,经400 h氧化,氧压只下降1.5左右,仍未被氧化完全。因此,乳清蛋白-甘油二酯纳米乳液能提高甘油二酯的氧化稳定性,利于保藏。

图12 纳米乳液的氧化稳定性
2.5.3 贮藏稳定性
不同贮藏温度对纳米乳液包埋率的影响如图13所示。由图13可知,在30 d贮藏时间内,随着时间的延长,纳米乳液包埋率逐渐降低。但温度越高,包埋率下降速度越快,温度较低时,包埋率下降缓慢。说明贮藏温度对纳米乳液品质的影响较大,长期高温贮藏会导致纳米乳液被迅速破坏,包埋率降低,影响纳米乳液的使用及作用效果。因此,该纳米乳液应在4 ℃低温贮藏。

图13 不同贮藏温度对纳米乳液包埋率的影响
3 结论
乳清蛋白-甘油二酯纳米乳液的最佳工艺条件为:壁材质量浓度15.83%,壁芯比3.35∶1,乳化剂添加量4.02%,此时,纳米乳液的包埋率最高,为75.5%。纳米乳液带负电,分布均匀,粒径在142 nm左右,有明显的壳核结构,包被效果较好。纳米乳液在80 ℃以下具有较好的稳定性,且能有效延缓甘油二酯的氧化,最佳贮藏温度为4 ℃。
[1]WATANABE T,SUGIURA M, Sato M, et al. Diacylglycerol production in a packed bed bioreactor[J]. Process Biochemistry, 2005, 40(2):637-643
[2]MURASE T, MIZUNO T, OMACHI T, et al. Dietary diacylglycerol suppresses high fat and high sucrose diet-induced body fat accumulation in C57BL/6J mice[J]. Journal of Lipid Research, 2001, 42(3): 372-378
[3]MAKI K C, DAVIDSON M H, TSUSHIMA R, et al. Consumption of diacylglycerol oil as part of a reduced-energy diet enhances loss of body weight and fat in comparison with consumption of a triacylglycerol control oil[J]. The American journal of clinical nutrition, 2002, 76(6): 1230-1236
[4]李渐鹏, 杜方岭, 闫永恒, 等. 甘油二酯对2型糖尿病肾病大鼠肾脏保护机制[J]. 营养学报,2016,38(2): 147-151 LI J P, DU F L, YAN Y H, et al.The protective effects of diacylglycerol on diabetic nephropathy in type 2 diabetic rats[J]. Journal of nutrition, 2016, 38(2):147-151
[5]闫雪彦. 甘油二酯对大鼠血脂和抗氧化水平影响的实验研究[D].青岛:青岛大学,2011 YAN X Y. Study of diacylglycerol’s effect on the blood fat and antioxidation of rats[D]. Qingdao: Qingdao University, 2011[6]KIMURA H, BURDOCK G A. Chronic study of diacylglycerol oil in rats [J]. Food and Chemical Toxicology, 2001, 39:317-329[7]GUTIERREZ J M, GONZALEZ C, MAESTRO A, et al. Nano-emulsions: new applications and optimization of their preparation[J]. Current Opinion in Colloid & Interface Science, 2008, 13(4):245-251
[8]FERNANDEZ P, ANDRE V, RIEGER J, et al. Nano-emulsion formation by emulsion phase inversion[J]. Colloids and Surfaces A-Physicochemical and Engineering Aspects, 2004, 251(1-3):53-58.

