英夫利昔单抗引起的间质性肺疾病一例
刘泉波 何忠 郑锐
1976年,首次报道炎症性肠病患者出现肺部浸润,考虑可能是炎症性肠病的肠外表现或控制病情的药物而导致的副作用[1-4]。英夫利昔单抗作为一种抗肿瘤坏死因子(抗TNF),已成为炎症性肠病患者的关键治疗药物,虽然有很多关于英夫利昔单抗治疗导致包括肺部感染的文献报道,但迄今为止,大多数英夫利昔单抗所致的非感染性肺部并发症的研究集中在类风湿关节炎患者[5-7]。现报道我科收治的1例炎症性肠病患者应用英夫利昔单抗后出现间质性肺炎,并对英夫利昔单抗治疗引起间质性肺疾病的临床特征进行相关文献复习。
病例资料
患者,男性,73岁。因“间断脓血便3年,气短1个月”于2016年10月20日入院。患者入院3年前无明显诱因出现排暗红色血便,每天排便7~8次,有黏液,脓性分泌物,伴左下腹疼痛,排便后可缓解,于我院肠镜检查提示升结肠、回盲部粘膜炎症改变,诊断炎症性肠病,予强的松、美沙拉嗪治疗后患者症状缓解。此后强的松逐渐减量至停用,美沙拉嗪继续维持治疗。5个月前再次出现脓血便,大便不成形,肠镜示结肠多发溃疡性病变,考虑克罗恩病,停用美沙拉嗪,开始予英夫利昔单抗治疗(5 mg/kg),临床症状缓解,复查肠镜示结肠多发愈合痕,累计应用英夫利昔单抗3次,期间行胸部CT示右肺上叶及左肺下叶结节影,双肺散在多发气肿。1个月前患者无明显诱因出现活动后气短,咳嗽,咳少量白痰,无发热,无胸痛,无关节痛及皮疹,无反复口腔溃疡及雷诺现象,为进一步诊疗就诊我院。患者既往长期吸烟史,有慢性咳嗽咳痰病史。入院查体:体温36.5 ℃,心率80次/min,呼吸频率18次/min,血压118/80 mmHg。双肺呼吸音粗,双肺底可闻及帛裂音,双下肢无浮肿,未见杵状指。实验室检查:白细胞计数4.3×109/L,中性粒细胞百分比8.4%,D-二聚体(D-dimer)212 μg/L(正常),胸部CT示双肺散在大小不等囊性透光影,右肺上叶尖后段,左肺下叶散在结节影,双肺模糊斑片影及索条影,考虑为肺炎,肺气肿,予头孢曲松他唑巴坦抗感染治疗1周,气短不见缓解,停用抗生素,进一步完善检查降钙素原 0.039 ng/ml,C-反应蛋白21.9 mg/L,类风湿因子正常,ANCA阴性,肺炎支原体抗体1︰160,巨细胞病毒-IgM抗体阴性,一般细菌涂片及痰细菌培养阴性,结核菌涂片及结核菌培养阴性,痰真菌培养热带念珠菌生长1次,血气分析:pH 7.467,二氧化碳分压32.1 mmHg,氧分压57.9 mmHg,实际碳酸氢盐22.7 mmol/L,标准碳酸氢盐24.2 mmol/L,动脉血氧饱和度 91.9%。总IgE正常,痰查嗜酸细胞阴性,外周血总T细胞绝对计数515,CD8+T抑制毒细胞绝对计数180,CD4+T辅助细胞绝对计数263,肺功能示混合性通气功能障碍,肺弥散功能下降,见表1。完善胸部HRCT示双下肺近胸膜处网格影,斑片状磨玻璃影,肺气肿,见图1。临床诊断:间质性肺疾病。予莫西沙星片口服,噻托溴铵吸入治疗,醋酸泼尼松片20毫克日一次口服,患者气短症状逐渐缓解,激素治疗1周后复查胸部CT示肺部浸润影较前吸收,见图2。出院半年后随访复查肺功能较前改善,肺部浸润影较前明显吸收。
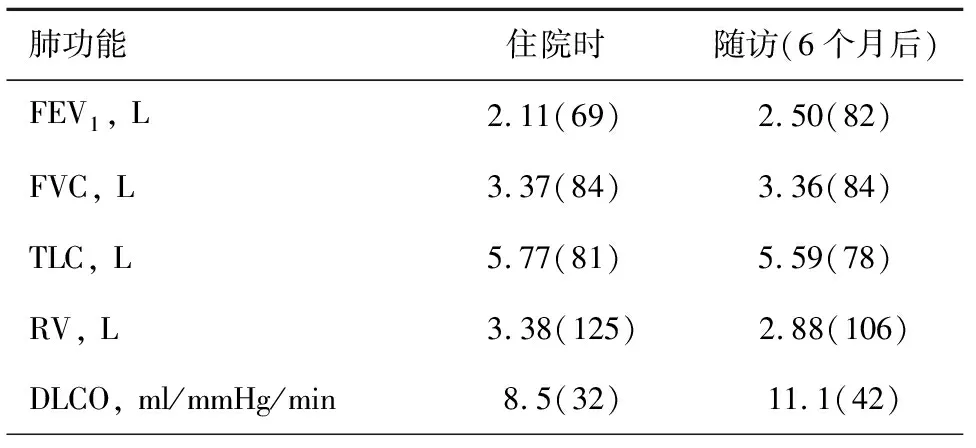
表1 患者肺功能变化趋势(%)
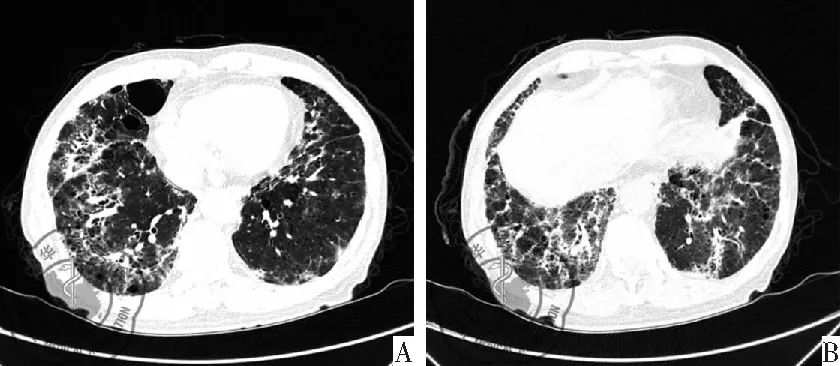
图1 胸部HRCT示双下肺近胸膜下可见网格影,斑片状磨玻璃影

图2 激素治疗1周后复查胸部CT示肺部浸润影较前吸收
讨 论
炎症性肠病(inflammatory bowel disease, IBD)为主要累及回肠、直肠、结肠的一种特发性肠道炎症性疾病,也是一种可以累及全身的异质性疾病,IBD肠外表现发生率较高(20%~40%),其中皮肤损害、虹膜炎、关节炎、硬化性胆管炎等已被普遍认识[8-9]。而IBD合并肺部病变的发生率较低,肺部浸润可以表现为不同的类型[10]。1976年,Kraft等报道6例UC患者出现慢性支气管炎、支气管扩张和慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD),首次提出IBD可累及呼吸系统[11]。此后IBD合并肺部病变的报道见于国内外诸多文献,多数学者发现大部分IBD患者会出现肺功能减退,并能引起如支气管炎、支气管扩张、哮喘、肺实质病变、肺血管疾病等肺部改变[12-13]。部分学者认为肺部病变与IBD治疗用药的不良反应相关,但尚有争议[11-12]。有文献报道美沙拉嗪可引起肺部不良反应,主要表现为嗜酸粒细胞性肺炎,伴有外周血嗜酸性粒细胞增多[14]。自应用美沙拉嗪至出现症状的时间以2~6个月居多,少数病例可达44个月[2,15-16]。本例患者首次出现气短症状时,已应用美沙拉嗪3年余,入院后反复查外周血嗜酸细胞正常,痰嗜酸细胞阴性,所以不考虑美沙拉嗪引起的间质性肺炎。本例患者化验ANA滴度1︰320,抗-nRNP阳性,抗-Sm 弱阳性,但患者无关节症状及皮疹,结合肺部浸润影,需注意结缔组织病肺部并发症,肺部浸润可先于结缔组织病症状出现,但患者明确在应用英夫利昔单抗3次后出现活动后气短,影像学表现为间质性肺炎,考虑为英夫利昔单抗引起的间质性肺炎。
英夫利昔单抗引起间质性肺疾病的具体发生率不详, Perez-Alvarez等[17]研究了10 649例抗TNF剂治疗的RA患者,医生报告的ILD患病率是2.8%。呼吸困难是英夫利昔单抗引起的间质性肺疾病的主要临床表现,大部分为渐进性气短,少部分进展迅速的可表现为急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)[18-19]。部分患者伴有发热,咳嗽,自应用英夫利昔单抗至出现症状的注射次数一般为1~5次,胸部影像学主要表现为磨玻璃影、网格影,少数表现为结节影、实变影等[20-25]。英夫利昔单抗导致间质性肺疾病的机制尚不清楚,已知肿瘤坏死因子(tumor necrosis factor, TNF-α)与白介素1或干扰素可能参与调节成纤维细胞增殖,而英夫利昔单抗对TNF-α的抑制可能导致这些细胞因子的促炎作用增加[26-27]。许多IBD患者同时接受了可能引起药物性肺损伤的5-氨基水杨酸、美沙拉嗪和/或硫唑嘌呤[28-30]。因此,有时难以确定个别药物在肺损伤病因中的作用,也可以认为联合治疗的协同作用可能会进一步增加肺损伤的风险。本例患者和文献报道的病例在停药后临床症状及影像学都有改善,但大部分患者都使用了糖皮质激素,提示激素治疗有效。
英夫利昔单抗临床应用越来越广泛,但仍有一些关于治疗的安全性问题尚未明确,临床医生在应用过程中应提高警惕,尤其是使用后出现渐进性呼吸困难,肺部有新发浸润影时需考虑间质性肺疾病的可能。

