复方丹参注射液辅助治疗小儿过敏性紫癜Meta分析
孙丽平, 王雪姣
过敏性紫癜又称亨-舒综合征(Henoch-Schonlein purpura,HSP),是儿童时期最常见的血管炎之一。作为一种血管变态反应性疾病,以小血管炎为主要病变。临床特点为非血小板减少性紫癜,常伴有关节肿痛或关节炎、腹痛、胃肠道出血、血尿和蛋白尿。多发生于2~6岁,当HSP累及肾脏时,为紫癜性肾炎,是儿科临床最常见的继发性肾炎之一,肾脏的累及程度是影响HSP远期预后的关键[1]。HSP的发病机制目前大多数学者认为各种刺激因子(感染原、过敏原等)作用于具有遗传背景的个体,激发B淋巴细胞多克隆活化,T淋巴细胞和单核细胞CD40配体表达增强,促使B淋巴细胞大量分泌IgA、IgE,IgA、补体C3和纤维蛋白沉积于肾小球系膜、皮肤和肠道毛细血管,使血管内皮细胞受损,血小板活化,血小板黏附性增强,血液呈高凝状态;血管通透性增加,血浆成分渗出,引起皮下组织、黏膜、内脏器官出血、水肿。复方丹参注射液具有扩血管疏通微循环作用,可抑制多种凝血因子,抑制血小板黏附聚集释放,纠正纤溶,降低血液黏度[2]。可加快血流速度,增加肾小球滤过率,此外还有抗炎,抗氧自由基,缓解胃肠道痉挛,还具有调节蛋白代谢和免疫的功能,可阻断HSP病理过程,并进行修复[3]。复方丹参已广泛用于治疗心血管疾病,而临床实践发现也可用于儿科HSP的辅助治疗,但由于临床证据较少,研究样本量不足,复方丹参治疗HSP尚存在争议。本研究通过检索复方丹参注射液治疗HSP的随机对照试验,采用Meta分析的方法,在较大样本的前提下,系统评价在常规使用抗组胺药物治疗的基础上,联合应用复方丹参注射液治疗HSP的有效性及安全性,为HSP的治疗提供科学依据。
1 资料与方法
1.1 纳入标准 (1)复方丹参注射液(丹参、降香)治疗HSP的随机对照试验,无论是否为采用分配隐藏及盲法,仅限中、英文文献;(2)干预措施:对照组接受常规治疗(如维生素C、钙剂、抗组胺药及对症治疗),治疗组在常规治疗基础上静脉滴注复方丹参注射液;(3)临床疗效评价指标:总有效率,皮肤、关节、消化道症状缓解时间及不良反应发生情况。
1.2 排除标准 (1)单纯描述性研究,无对照组;(2)患儿合并其他并发症的文献;(3)非目标干预措施的文献;(4)数据资料无法提取或合并的文献;(5)无本研究关注的结局指标的文献;(6)合并使用其他药物而影响治疗因果关系判断的。
1.3 文献检索 计算机检索Pubmed、WEB OF SCIENCE、The Cochrane Library、CNKI、VIP、WanFangData,筛选复方丹参注射液治疗小儿HSP的国内外文献,检索式为“复方丹参”OR“复方丹参注射液”AND“过敏性紫癜”OR“亨-舒综合征”OR“出血性毛细血管中毒症”;外文检索词为“Salvia”“Compound Danshen”OR“Compound Danshen injection”AND“anaphylactoid purpura”OR“Henoch-Schonlein syndrome”。
1.4 文献质量评价 根据制定好的纳入与排除标准,由两位评价者独立进行文献筛选工作,如遇分歧,由第三方裁定。首先阅读题目和摘要,若为试验性研究则阅读全文,以确定是否符合纳入标准。随机对照试验的质量评价参考改良后的Jadad量表进行评价。盲法:(1)恰当:描述了实施双盲的具体方法并且是恰当的,如采用了完全一致的安慰剂片或类似方法(2分)。(2)不清楚:试验陈述为盲法,但未描述方法(1分)。(3)不恰当:未采用双盲或盲的方法不恰当,如片剂和注射剂比较(0分)。退出与失访:(1)描述了撤出或退出的数目和理由(1分)。(2)未描述撤出或退出的数目或理由(0分)。记分为1~7分(4~7分视为高质量)。
1.5 统计学方法 采用Cochrane协作网提供的RevMan 5.3统计软件进行Meta分析。二分类变量采用相对危险度(RR)为效应分析统计量;连续性变量采用加权均数差(WMD),并给出95%CI。各实验结果的异质性采用χ2检验进行,当各研究间无统计学和临床异质性时(P≥0.10,I2≤50%),则采用固定效应模型进行Meta分析;反之,则采用随机效应模型进行Meta分析。必要时分析其异质性来源并进行亚组分析,若异质性过大或存在明显临床异质性或数据无法合并时,则采用描述性分析,并慎重解释研究结果。采用倒漏斗图判断文献是否存在发表偏倚。
2 结果
2.1 文献筛选结果 根据以上检索策略共初步检出文献377篇(知网158,维普109,万方109篇,The Cochrane Library 1篇),利用Note Express 2去除重复文献74篇,依据文献纳入与排除标准,最后纳入文献10篇,共768例患者,治疗组393例,对照组375例。所有纳入的随机对照试验研究均采用随机、对照的试验设计,明确指出各试验组间的基线情况可比,但均未说明是否实施了分配隐藏,因此可能产生一定的选择性偏倚。纳入文献基本信息与质量评价见表1。
2.2 统计分析结果
2.2.1 两组患儿总有效率的Meta分析 见图1。
7篇研究[4-7,11-13]比较了复方丹参注射液联合常规治疗对比常规治疗的总有效率,各研究间无统计学异质性(P=0.41,I2=2%),采用固定效应模型合并效应量分析,Meta分析结果显示,复方丹参注射液联合常规治疗组总有效率显著高于常规治疗组,差异有统计学意义[RR=1.22,95%CI(1.12,1.33),P<0.000 01]。
2.2.2 两组患儿皮疹消退时间的Meta分析 见图2。
2项研究[9-10]比较了复方丹参注射液联合常规治疗对比常规治疗HSP皮疹消退时间,两项研究间无统计学异质性(P=0.26,I2=21%),采用固定效应模型合并效应量分析,Meta分析结果显示,复方丹参注射液联合常规治疗组皮疹消退时间显著短于常规治疗组,差异有统计学意义[MD=-3.88,95%CI(-4.66,-3.10),P<0.000 01]。

表1 纳入文献基本信息
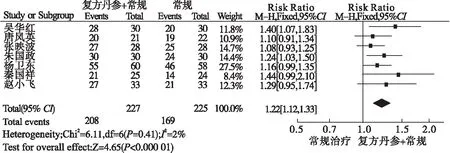
图1 两组患儿总有效率的Meta分析森林图
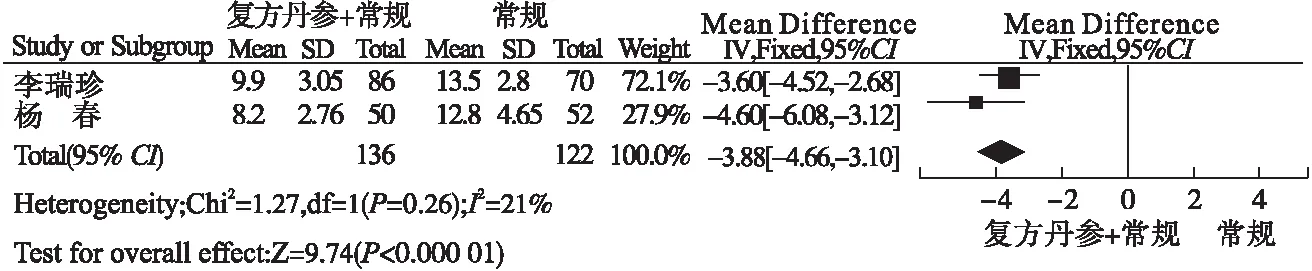
图2 两组患儿皮疹消退时间的Meta分析森林图
2.2.3 两组患儿关节症状缓解时间的Meta分析 见图3。
2项研究[8-9]比较了复方丹参注射液联合常规治疗对比常规治疗HSP关节症状缓解时间,两项研究间无统计学异质性(P=0.45,I2=0%),采用固定效应模型合并效应量分析,Meta分析结果显示,复方丹参注射液联合常规治疗组关节症状缓解时间显著短于常规治疗组,差异有统计学意义[MD=-1.06,95%CI(-1.34,-0.78),P<0.000 01]。
2.2.4 两组患儿消化道症状缓解时间的Meta分析 见图4。
2项研究[8-9]比较了复方丹参注射液联合常规治疗对比常规治疗HSP消化道症状缓解时间,两项研究间无统计学异质性(P=0.83,I2=0%),采用固定效应模型合并效应量分析,Meta分析结果显示,复方丹参注射液联合常规治疗组消化道症状缓解时间显著短于常规治疗组,差异有统计学意义[MD=-1.12,95%CI(-1.48,-0.76),P<0.000 01]。

图3 两组患儿关节症状缓解时间的Meta分析森林图

图4 两组患儿消化道症状缓解时间的Meta分析森林图
2.2.5 不良反应 纳入的10项研究中,有7项研究提到了不良反应的情况,其中1项研究描述了复方丹参注射液的不良反应,秦国祥[12]报道有2例在静脉滴注时出现腹部不适、恶心等表现,经调慢滴速后,症状缓解,未影响治疗。其余均未见明显不良反应。
2.3 发表偏倚分析 见图5。

图5 总有效率的倒漏斗图
选取总有效率为指标,以各效应量的RR值为横坐标、标准误SE[log(RR)]为纵坐标,绘制倒漏斗图,结果,漏斗图左右不对称,提示纳入文献存在发表偏倚。本研究所纳入的患者病情轻重不一,各研究间的治疗组药物用量不完全一致,其中6篇研究复方丹参注射液的药物用量是根据患儿体质量计算,1篇研究是按照患儿年龄换算,其余3篇未给出计算方法。并且给药疗程时间长短不一,这些都是造成观察指标偏倚存在的原因。10篇随机对照研究中,只有3篇有随访记录,因此复方丹参注射液治疗过敏性紫癜的远期疗效,对过敏性紫癜反复发作是否起到预防作用,尚不能得出确切的结论。
3 讨论
HSP是最常见的毛细血管变态反应性疾病,属于中医血证范畴,根据其发病及临床特点,相当于中医古典医籍中所记载的“发斑”“斑毒”“葡萄疫”“肌衄”“血溢”“紫癜风”“紫斑”等病证范畴。近几年HSP的发病率及住院率呈逐年上升趋势,患病率从1.88%逐渐上升至3.43%[14],有45%~65%患儿可出现尿检异常,90%以上患儿可出现肾脏病理改变[15]。而紫癜性肾炎患儿中有1.5%~10%最终发展为慢性肾功能衰竭[16-18]。西医对HSP的治疗主要为去除诱因,应用维生素C、抗生素、抗过敏药、激素和免疫抑制剂等。疗效较显著,但由于不良反应较多,往往导致患者不能耐受,因此亟须探索有效治疗HSP的新方案。中医对于紫癜的治疗,多数学者认为感受外邪、瘀血阻络、正气亏虚为主要病因。瘀既是紫癜病变过程中的病理产物,又作为新的病因进一步加重病情,贯穿于本病的全过程[19]。
复方丹参注射液由丹参、降香二药组成,丹参苦、微寒,有降而行血,血热而滞者宜之,可破宿血、生新血、通经络;降香辛、温,通十二经,可散邪、行气、破滞,能增强丹参的作用。现代试验证明,复方丹参注射液可清除氧自由基;抑制血小板黏附和凝集;降低血液黏稠度;扩张微血管,改善微循环[20]。可加快血流速度,增加肾小球滤过率,此外还有抗炎,抗氧自由基,缓解胃肠道痉挛,还具有调节蛋白代谢和免疫的功能,可阻断HSP病理过程,并进行修复。复方丹参已广泛应用于心血管疾病的治疗,虽然目前临床已尝试将其用于HSP的治疗,但由于各研究样本量有限,质量也良莠不齐,严重影响了临床医生的用药决策。
本文采用Meta分析的方法,在较大样本的前提下,合并了目前评价复方丹参注射液辅助治疗HSP疗效及安全性的所有临床试验,以增强结果的可靠性和客观性,由Meta分析的结果可见,复方丹参注射液联合常规治疗HSP在总有效率、皮疹消退时间、关节症状缓解时间及消化道症状缓解时间,相对于以抗组胺、抗感染、对症治疗为主的常规疗法具明显优势,且差异有统计学意义,表明在常规治疗的基础上辅助应用复方丹参注射液可提高HSP的治疗效果。在不良反应方面,秦国祥报道有2例在静脉滴注时出现腹部不适、恶心等表现,经调慢滴速后,症状缓解,未影响治疗。其余均未见明显不良反应。但本系统评价仍存在以下局限:纳入文献的总体质量较差、未纳入灰色文献、纳入文献数较少,纳入的大部分研究未清楚交代具体的随机方法以及是否采用分配隐藏和盲法。故临床尚需进行大样本、随机、双盲研究,以更好地验证本研究结果。
[1] McCarthy HJ, Tizard EJ.Clinical practice: Diagnosis and management of Henoch-Schonlein purpura[J].Eur J Pediatr,2010,169(6):643-650.
[2] 朱廷富,褚祝飞,李精华.雷公藤多苷联合丹参注射液对过敏性紫癜性肾炎患儿凝血机制的影响[J].中国中药杂志,2016,41(11):2162-2167.
[3] 刘文彬,王太森,刘华君,等.复方丹参、西咪替丁治疗过敏性紫癜疗效及免疫功能变化[J].实用儿科临床杂志,2005,20(5):470-471.
[4] 朱国政,梁全全.复方丹参静脉滴注佐治过敏性紫癜[J].浙江实用医学,2000,5(3):47-48.
[5] 杨卫东,栾春来,丁现超,等.复方丹参治疗儿童过敏性紫癜临床分析[J].慢性病学杂志,2010,12(11):1411-1412.
[6] 唐凤英.复方丹参注射液佐治儿童过敏性紫癜43例疗效观察[J].中国社区医师,2005,21(19):35.
[7] 张映波.复方丹参注射液治疗过敏性紫癜28例[J].浙江中西医结合杂志,2001,11(6):26-27.
[8] 向魏坪,王永霞.复方丹参注射液治疗小儿过敏性紫癜疗效观察[J].河北医药,2003,25(7):500.
[9] 李瑞珍,马新瑜,刘智胜.复方丹参注射液治疗小儿过敏性紫癜的疗效观察[J].中国综合临床,2002,18(9):90.
[10]杨春,康玉梅,王勇.复方丹参注射液辅治小儿过敏性紫癜50例[J].现代中西医结合杂志,2001,10(23):2284.
[11]赵小飞,白青好,关锦玲.复方丹参辅助治疗儿童过敏性紫癜中长期疗效观察[J].国际医药卫生导报,2006,12(21):73-74.
[12]秦国祥.复方丹参注射液防治过敏性紫癜患者肾受累的疗效分析[J].中国医药指南,2008,6(23):425-426.
[13]吴华红,陈松波,蔡锦楠,等.复方丹参注射液治疗过敏性紫癜的疗效观察[J].中国临床医生,2005,33(4):27-28.
[14]张少卿. 过敏性紫癜的随机、双盲、多中心临床研究及阳络伤的免疫失衡机制探讨[D].沈阳:辽宁中医药大学,2015.
[15]张国珍,吴小川,易红,等.儿童紫癜性肾炎临床与病理相关性分析[J].中国当代儿科杂志,2007,49(2):129-132.
[16]Wakaki H, Ishikura K, Hataya H,et al.Henoch-Schonlein purpura nephritis with nephrotic state in children: predictors of poor outcomes[J].Pediatr Nephrol,2011,26(6):921-925.
[17]Narchi H.Risk of long term renal impairment and duration of follow up recommended for Henoch-Schonlein purpura with normal or minimal urinary findings: a systematic review[J].Arch Dis Child,2005,90(9):916-920.
[18]Soylemezoglu O, Ozkaya O, Ozen S,et al.Henoch-Schonlein nephritis: a nationwide study[J].Nephron Clin Pract,2009,112(3):c199-204.
[19]陶宇翔. 小儿过敏性紫癜的“瘀毒”及其治疗[D].南京:南京中医药大学,2009.
[20]郭爱平,蒯文霞.复方丹参注射液联合孟鲁司特钠治疗儿童过敏性紫癜疗效观察[J].儿科药学杂志,2014,20(3):29-31.

