PARADIGM-HF研究设计解读
张宇辉,张健
心力衰竭是心血管病患者住院和死亡的重要病因,随着老龄化进程的加快,患病人群将会持续增加,同时住院率、死亡率也居高不下,给家庭、社会带来沉重负担[1,2]。因此,需要探索能够进一步降低心力衰竭住院率、死亡率的治疗手段就很必要。2014年欧洲心脏病学会(ESC)年会公布的PARADIGM-HF研究结果显示,沙库巴曲缬沙坦(LCZ696)与依那普利相比可以进一步降低心血管死亡或心力衰竭住院风险20%[3]。正是基于PARADIGM-HF研究,欧美指南均对沙库巴曲缬沙坦做出了Ⅰ类推荐。本文就PARADIGM-HF研究的设计和结果进行解读。
1 研究背景
神经内分泌系统参与心力衰竭的发生、发展,肾素-血管紧张素-醛固酮系统(RAAS)和交感神经系统(SNS)持续激活是导致心力衰竭的不利因素。既往治疗通过阻断RAAS和降低SNS活性达到预防、治疗心力衰竭的目的。而在RASS与SNS激活的同时,利钠肽系统也被激活,利钠肽具有促进尿钠排泄、舒张血管、拮抗RAAS等作用,同时也可以降低SNS的活性,重组利钠肽具有血管扩张,改善心力衰竭患者充血症状的作用,我国心力衰竭指南也推荐其用于急性失代偿性心力衰竭患者以改善血液动力学和临床症状[4-6]。因此通过其他方式增加利钠肽水平,也成为另外一个新方向。
利钠肽的代谢主要是通过自身受体介导清除和脑啡肽酶(NEP)的降解两条途径[7,4],所以通过抑制NEP,可以升高心房钠尿肽(ANP)及血浆B型利钠肽(BNP)水平。但是由于NEP的底物具有多样性,单纯的NEP抑制剂(NEPI)对高血压、心力衰竭的患者几乎没有影响,需要与RAAS抑制剂联合应用。奥马曲拉以这样的思路进行了探索,但最终因为奥马曲拉引起血管性水肿风险非常高而被终止研发[8]。分析显示奥马曲拉是因为同时抑制了缓激肽代谢的三个关键酶,即血管紧张素转换酶,NEP,氨基肽酶P[9,10],使活性缓激肽的代谢明显减少,增加了血管性水肿的风险。血管紧张素受体脑啡肽酶抑制剂(ARNI)选择由血管紧张素Ⅱ受体拮抗剂(ARB)和NEPI构成新型复合物沙库巴曲缬沙坦,阻断血管紧张素Ⅱ的1型受体,同时抑制NEP活性,对缓激肽的代谢影响较小,降低不良反应。沙库巴曲缬沙坦具有双系统的作用,PARADIGM-HF研究的主要目的是比较沙库巴曲缬沙坦200 mg bid与依那普利10 mg bid,对心力衰竭患者的心血管死亡和心力衰竭住院的影响[10]。
2 研究设计
PARADIGM-HF试验是随机、双盲、活性药物、平行对照研究。研究分三个阶段(如图1所示):(1)筛选符合入组标准的研究对象;(2)单盲导入期:首先进入依那普利单盲导入期,需要在两周的时间内达到10 mg bid,患者如没有不耐受,则进入沙库巴曲缬沙坦的单盲导入期;经过24 h洗脱期,开始使用沙库巴曲缬沙坦,并且剂量需要在四周达到200 mg bid。(3)双盲期:在经过24 h的洗脱期后,按照1:1随机分配,患者分别接受沙库巴曲缬沙坦治疗或依那普利治疗,同时接受其他推荐的心力衰竭治疗[4,11]。
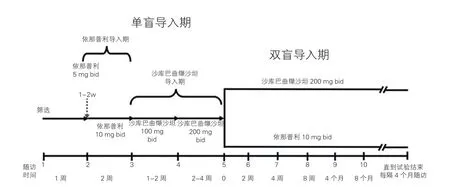
图1 PARADIGM-HF研究设计的三个阶段
3 研究对象
筛选期的纳入标准:年龄≥18岁,纽约心脏协会(NYHA)心功能Ⅱ、Ⅲ或Ⅳ级,左心室射血分数≤40%(2010年12月15日修订方案变更为≤35%),血浆BNP水平≥150 pg/ml或N末端B型利钠肽原(NT-proBNP)水平≥600 pg/ml,如患者在既往12个月内曾因为心力衰竭住院,则BNP≥100 pg/ml(或NT-proBNP≥400 pg/ml)。排除标准:症状性低血压,在筛选时收缩压<100 mmHg(1 mmHg=0.133 kpa)或在随机化时<95 mm Hg,在筛选或随机化时估算肾小球滤过率(eGFR)<30 ml/( min·1.73 m2),或筛选至随机化时eGFR降低>25%(修订为35%),在筛选时血清钾水平>5.2 mmol/L(或在随机化时>5.4 mmol/L),或既往接受血管紧张素转换酶抑制剂(ACEI)或ARB时出现血管性水肿或不可耐受的副作用[11]。
4 统计学
PARADIGM-HF研究设计参考CHARM-Added试验主要终点,估算大约需入组8 000例心力衰竭患者,预计随访34个月。估计沙库巴曲缬沙坦组主要终点风险降低15%。数据和安全性监察委员会指定在事件发生1/3、1/2和2/3时分别进行三次期中分析,并制定了因沙库巴曲缬沙坦获益具有巨大优势而终止试验的统计学要求。因此,在第三次期中分析时沙库巴曲缬沙坦获益达到了终止试验的标准,PARADIGMHF研究在中位数随访27个月时终止研究[4,11]。
5 研究目的
PARADIGM-HF研究设计参考了SOLVD研究及CHARM-Added研究,入组条件与SOLVD研究相同,并且增加了BNP、NT-proBNP水平作为筛选条件。BNP、NT-proBNP在心力衰竭诊断、评估心力衰竭预后方面有重要意义,以此为筛选条件,有助于筛选出高危心力衰竭患者。在选择对照组时,没有选择与安慰剂进行对照,设计成加药试验,而是与活性药物依那普利作为对照,设计为药物替代试验。而且,试验期间,患者需要服用β受体阻滞剂,除非患者不能耐受,最终93%患者使用β受体阻滞剂[12];推荐使用醛固酮受体拮抗剂,即PARADIGM-HF研究入组的患者是在指南推荐的心力衰竭治疗上比较沙库巴曲缬沙坦与依那普利对心力衰竭患者死亡率、住院率的影响。
5.1 血管紧张素转化酶抑制剂的选择
之所以选择依那普利作为对照,是因为依那普利有大量的循证医学证据,而且Val-HeFT、NETWORK、OVERTURE、CARMEN等多项大型的心力衰竭研究中对照组都选择依那普利。PARADIGM-HF研究在剂量选择方面参考了SOLVD研究[13],该研究是ACEI在射血分数降低的心力衰竭(HFrEF)患者的重要试验,试验中依那普利目标剂量就是10 mg bid,而且在至少七项心力衰竭的大型试验中都选择了依那普利10 mg bid作为对照。虽然也有研究将依那普利的目标剂量设定为20 mg或者30 mg bid,但接近一半的患者不能达到这一剂量,所以PARADIGM-HF研究最终把依那普利的对照剂量确定为10 mg bid[11],这也是我国心力衰竭指南推荐HFrEF患者治疗的目标剂量[6]。
5.2 沙库巴曲缬沙坦的剂量
沙库巴曲缬沙坦进入人体后代谢为缬沙坦和沙库巴曲,缬沙坦起到抑制RAAS的作用。而沙库巴曲是NEP抑制剂,其活性代谢产物LBQ657发挥抑制NEP,减少利钠肽代谢的作用。沙库巴曲缬沙坦要实现双系统的抑制作用,一方面要考虑缬沙坦的血药浓度,而同时需要考虑沙库巴曲的抑制程度。缬沙坦在心力衰竭领域的两项研究Val-HeFT和VALIANT,证实缬沙坦160 mg是不劣于ACEI的有效剂量[14,15]。所以,沙库巴曲缬沙坦中缬沙坦的活性剂量需要160 mg。同时,沙库巴曲需要能够达到抑制90%的NEP最大活性的作用,并使环磷酸鸟苷(cGMP)血浆浓度持续增高[10,16]。最终确定沙库巴曲缬沙坦剂量为200 mg,含缬沙坦103 mg(活性剂量相当于160 mg)、沙库巴曲97 mg。该研究中沙库巴曲缬沙坦采用每日两次的给药方式,确保24 h抑制RAAS及NEP活性。
PARADIGM-HF研究作为迄今最大的一项心力衰竭的试验,证实了沙库巴曲缬沙坦可以替代具有基石地位的ACEI,拓宽我们对心力衰竭神经内分泌抑制治疗的思路。多靶点治疗、多系统调节是心力衰竭治疗的新方向。
[1] Mosterd A, Hoes AW. Clinical epidemiology of heart failure[J]. Heart,2007, 93(9): 1137-1146. DOI: 10. 1136/hrt. 2003. 025270.
[2] 陈伟伟, 高润霖, 刘力生, 等. 《中国心血管病报告2017》概要[J].中国循环杂志, 2018, 33(1): 1-8. DOI: 10. 3969/j. issn. 1000-3614.2018. 01. 001.
[3] McMurray JJ, Packer M, Desai AS, et al. Angiotensin-neprilysin inhibition versus enalapril in heart failure[J]. N Engl J Med, 2014,371(11): 993-1004. DOI: 10. 1056/NEJMoa1409077.
[4] Mangiafico S, Costello-Boerrigter LC, Andersen IA, et al. Neutral endopeptidase inhibition and the natriuretic peptide system: an evolving strategy in cardiovascular therapeutics[J]. Eur Heart J, 2013,34(12): 886-893c. DOI: 10. 1093/eurheartj/ehs262.
[5] O'Connor CM, Starling RC, Hernandez AF, et al. Effect of nesiritide in patients with acute decompensated heart failure[J]. N Engl J Med,2011, 365(1): 32-43. DOI: 10. 1056/NEJMoa1100171.
[6] 中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. 中国心力衰竭诊断和治疗指南2014[J]. 中华心血管杂志, 2014, 42(2):98-122. DOI: 10. 3760/cma. j. issn. 0253-3758. 2014. 02. 004.
[7] Potter LR. Natriuretic peptide metabolism, clearance and degradation[J]. FEBS J, 2011, 278(11): 1808-1817. DOI: 10. 1111/j.1742-4658. 2011. 08082. x.
[8] Packer M, Califf RM, Konstam MA, et al. The Omapatrilat Versus Enalapril Randomized Trial of Utility in Reducing Events(OVERTURE) [J]. Circulation, 2002, 106(8): 920-926.
[9] Cruden NL, Fox KA, Ludlam CA, et al. Neutral endopeptidase inhibition augments vascular actions of bradykinin in patients treated with angiotensin-converting enzyme inhibition[J]. Hypertension, 2004,44(6): 913-918. DOI: 10. 1161/01. HYP. 0000146483. 78994. 56.
[10] Gu J, Noe A, Chandra P, et al. Pharmacokinetics and pharmacodynamics of LCZ696, a novel dual-acting angiotensin receptor-neprilysin inhibitor (ARNi) [J]. J Clin Pharmacol, 2010,50(4): 401-414. DOI: 10. 1177/0091270009343932.
[11] McMurray JJ, Packer M, Desai AS, et al. Dual angiotensin receptor and neprilysin inhibition as an alternative to angiotensin-converting enzyme inhibition in patients with chronic systolic heart failure:rationale for and design of the Prospective comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure trial (PARADIGM-HF) [J]. Eur J Heart Fail, 2013, 15(9):1062-1073. DOI: 10. 1093/eurjhf/hft052.
[12] McMurray JJ, Packer M, Desai AS, et al. Baseline characteristics and treatment of patients in prospective comparison of ARNI with ACEI to determine impact on global mortality and morbidity in heart failure trial (PARADIGM-HF) [J]. Eur J Heart Fail, 2014, 16(7): 817-825.DOI: 10. 1002/ejhf. 115.
[13] SOLVD Investigators, Yusuf S, Pitt B, et al. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure[J]. N Engl J Med, 1991, 325(5): 293-302. DOI:10. 1056/NEJM199108013250501.
[14] Cohn JN, Tognoni G. Valsartan heart failure trial investigators. A randomized trial of the angiotensin-receptor blocker valsartan in chronic heart failure[J]. N Engl J Med, 2001, 345(23): 1667-1675.DOI: 10. 1056/NEJMoa010713.
[15] Pfeffer MA, McMurray JJ, Velazquez EJ, et al. Valsartan, captopril,or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both[J]. N Engl J Med, 2003, 349(20):1893-1906. DOI: 10. 1056/NEJMoa032292.
[16] Ruilope LM, Dukat A, Böhm M, et al. Blood-pressure reduction with LCZ696, a novel dual-acting inhibitor of the angiotensin II receptor and neprilysin: a randomised, double-blind, placebo-controlled,active comparator study[J]. Lancet, 2010, 375(922): 1255-1266. DOI:10. 1016/S0140-6736(09)61966-8.

