入院GRACE评分及血管内皮功能对ACS患者PCI术后中远期预后的预测价值
潘文旭,成小凤,何云,王珂,刘婷,范华平,何沛逊,高智春,晋军
急性冠脉综合征(acute coronary syndromes,ACS)早期死亡及再梗死风险较高,但其晚期预后不明确[1-3]。在当前全国范围内建立胸痛中心、倡导尽早恢复血运重建的治疗理念下,新一代药物涂层支架、他汀及双联抗血小板等药物广泛应用,但关于ACS经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)患者术后中远期预后及未来发生死亡及心脏主要不良事件(major adverse cardiac events,MACEs)的风险情况仍不十分清楚[4]。据报道,不同程度的ACS患者在临床表现及预后方面存在较大差异[5]。入院全球注册的急性冠脉事件(global registry of acute coronary events,GRACE)评分主要用于预测ACS患者住院期间死亡发生率,但也有研究表明其用于评估ACS患者长期预后同样具有较好的预测性[6]。Joner等[7]发现,药物涂层支架术后可能存在未来发生晚期支架内血栓的风险,因此入院GRACE评分能否较好地预测术后患者长期预后目前还不清楚,而且缺少中国人群的研究数据。有研究发现,血管内皮功能障碍是动脉粥样硬化性疾病的早期阶段[8],通过检测冠状动脉内皮功能,可为评估ACS患者疾病进展及预后提供重要信息[9-12]。Endo-PAT 2000无创血管内皮功能检测技术是目前检测血管内皮功能的有效方法[13]。通过Endo-PAT 2000检测血管内皮功能可有效预测PCI术后MACEs的发生[14-15]。本研究旨在探讨入院GRACE评分与血管内皮功能对PCI术后患者中远期预后的预测价值。
1 资料与方法
1.1 研究对象 本研究为单中心、观察性、前瞻性临床研究,连续纳入2015年12月-2017年11月陆军军医大学新桥医院的PCI术后患者。排除标准:①住院期间死亡;②恶性肿瘤;③严重心脏功能衰竭,心功能Ⅳ级(NYHA/Killip分级);④严重肝功能衰竭及终末期肾病;⑤仅进行球囊血管成形术而没有植入支架;⑥介入手术术中出现并发症(如冠脉夹层、穿孔等);⑦患有神经/精神障碍,无法配合研究;⑧拒绝行无创内皮功能检测;⑨拒绝入选该研究。本研究符合赫尔辛基宣言,研究前已通过新桥医院伦理审查委员会的审查与批准,所有受试者均已签署知情同意书。根据入院GRACE评分将所有受试者划分为低危组(n=158)、中危组(n=130)和高危组(n=42)。
1.2 基线资料 收集一般人口学及病史资料,包括性别、年龄、体重指数(body mass index,BMI)、收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP)、心率(heart rate,HR)、吸烟史、饮酒史、PCI病史、冠状动脉旁路移植术(cardiac artery bypass graft,CABG)史、高血压史、高脂血症史、外周血管病史、病变血管数量、植入支架数量等。
入院后48h内完善心脏超声(CX50,飞利浦,美国)检查,采取患者空腹(禁食、水12h)静脉血样,进行相关生物化学检测,包括总胆固醇(total cholesterol,TC)、血浆甘油三酯(triglyceride,TG)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、血清肌酐(creatinine,Cr)、D2-聚体(D2-polymer)、脑钠肽(brain natriuretic peptide,BNP)。所有生化检测结果均来自陆军军医大学新桥医院临床实验室血液标本实验室。
1.3 选择性冠状动脉造影及支架植入术 入院后所有受试者均接受血管造影及必要时支架植入治疗,并严格按照中国心脏病学会推荐的急性ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)和非ST段抬高型急性冠脉综合征治疗指南进行[16-17]。
1.4 反应性充血指数(reactive hyperemia index,RHI)的检测 所有受试者在行PCI术后48~72h内完善RHI检测。检测当天患者需禁食、避免锻炼,检查前12h禁止吸烟、饮咖啡或服用其他兴奋剂,长效硝酸酯类药物需停用大于12h,在光线和温度适宜的房间内平卧休息20min以上,在保持安静的情况下进行测试。具体步骤如下:①双上肢放松伸直置于躯干两侧,将PAT探头嵌套于双手的食指末端,通过PAT探头感知双手食指尖的动脉搏动,测定基础PAT信号,测量时间为5min,其中一侧肢体检测血管内皮细胞功能,另一侧肢体作为对照检测全身性血管反应;②将标准袖带束于患者一侧肱动脉上2cm处采集5min血管张力基线数据,随后袖带加压充气至收缩压60mmHg以上或200mmHg阻断肱动脉血流5min并采集数据;③将袖带快速放气,开始测量放气后血管扩张反应,通过Endo-PAT软件进行计算并根据对照侧数据进行修正后,得出RHI。按照国际标准,RHI≥1.67判定为内皮功能正常(normal endothelial function,NEF);RHI<1.67判定为内皮功能障碍(endothelial dysfunction,DEF)。
1.5 入院GRACE评分 入院GRACE评分是根据受试者入院时年龄、HR、SBP、Cr、心肌损伤标志物是否升高、心电图ST段是否有偏移、院前有无心脏停搏以及Killip分级这8项指标来计算积分,各项指标对应相应积分,相加后得到总积分,总积分越高,则危险程度越高。入院GRACE评分≤108分为低危;入院GRACE评分在109~140分为中危;入院GRACE评分>140分为高危[18]。
1.6 随访 出院后所有患者均发放随访手册,详细填写患者的一般信息、手术情况及用药情况。通过门诊、查看住院电子病历或电话3种方式进行随访。本研究将MACEs定义为复合终点事件,包括心源性死亡、急性心肌梗死(acute myocardial infarction,AMI)、缺血性卒中、靶血管血运重建(target vessel revascularization,TVR)和因心脏原因(心力衰竭、心律失常及心绞痛)再次入院(只要发生其中任意一项即代表MACEs发生,当有2次或2次以上MACEs时只记录第一次)。本研究所有受试者随访至2017年11月或出现MACEs即终止随访。
1.7 统计学处理 采用SPSS 19.0进行统计分析。采用K-S法检验连续性变量是否符合正态分布,符合正态分布的连续性变量以表示,组间比较采用单因素方差分析,进一步两两比较采用SNK-q检验;不符合正态分布的连续性变量采用M(Q)表示,组间比较采用Mann-WhitneyU检验。分类变量以例(%)表示,组间比较采用Pearson's 2或Fisher精确概率法。根据入院GRACE评分及RHI值对受试人群进行分组,应用Kaplan-Meier生存分析及Log rank检验比较组间累积MACEs事件发生率的差异。应用单因素及多因素Cox比例风险模型分析发生MACEs事件的独立预测因素,其中将年龄及单因素回归分析中P<0.1的变量纳入多因素Cox比例风险模型分析(采用前向逐步回归分析法)。双侧P<0.05为差异有统计学意义。
2 结 果
2.1 一般临床资料 共纳入330例PCI术后患者,年龄(60.2±9.8)岁,其中STEMI为68例,非ST段抬高型心肌梗死(non ST-segment elevation myocardial infarction,NSTEMI)为22例,不稳定心绞痛(unstable angina,UA)为240例,失访5例,最终随访了325例,中位随访时间为19个月(四分位区间:13~21个月)。根据入院GRACE评分将所有受试者划分为低危组(n=158)、中危组(n=130)及高危组(n=42),其中低危组失访2例,中危组失访1例,高危组失访2例。3组受试人群基线数据在年龄、BMI、入院GRACE评分、心率、舒张压、左室射血分数(left ventricular ejection fraction,LVEF)、BNP、D2-聚体、血管病变数目与诊断STEMI、UA人数上组间差异有统计学意义(P<0.05),而在性别构成、RHI、吸烟史、饮酒史、外周血管疾病史、既往PCI或CABG手术史、高血压史、高脂血症史、收缩压、TC、TG、LDL-C、HDL-C、左室舒张期直径(left ventricular end diastolic dimension,LV)、Cr、诊断NSTEMI人数、药物使用情况[包括血管紧张素转换酶抑制剂(angiotensin converting enzyme inhibitor,ACEI)/血管紧张素受体阻断剂(angiotensin receptor blocker,ARB)、钙通道阻滞剂(calcium-channel blocker,CCB)、β受体阻滞剂、抗血小板聚集药、他汀、硝酸酯类药物(nitric acid lipids)]以及支架植入数量上组间差异无统计学意义(P>0.05,表1)。
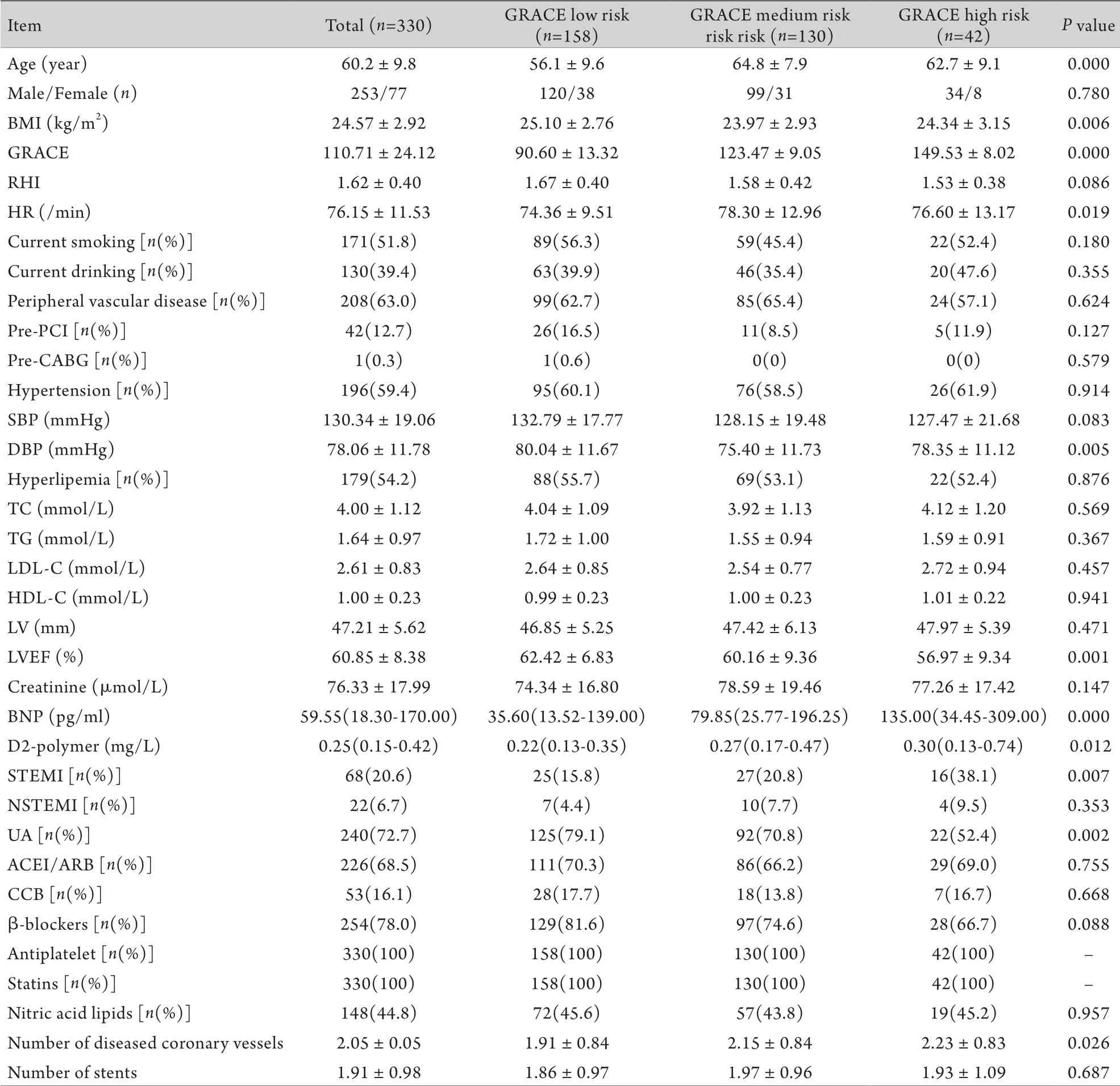
表1 ACS患者PCI术后基线特征Tab.1 Baseline data of the ACS patients after PCI
2.2 不良事件发生情况 在随访期内,共有67例受试者发生了MACEs。其中GRACE低、中、高危三组受试者MACEs发生率(分别为14.7%、22.4%、37.5%)差异有统计学意义(P=0.005);在心源性死亡事件上,三组受试者发生率(分别为0.6%、2.3%、10.0%)差异有统计学意义(P=0.003)。而在MI、TVR、缺血性卒中、因心脏原因再住院事件上,中、高危组人群发生率均普遍高于低危组,但不存在统计学差异(表2)。

表2 ACS患者PCI术后不良事件发生情况[n(%)]Tab.2 Estimated incidence of MACEs in ACS patients after PCI [n(%)]
2.3 Cox比例风险回归模型及生存曲线分析预测价值 单因素Cox比例风险回归模型分析发现,入院GRACE危险分层、RHI、LVEF、BNP,以及病变血管数量与患者发生MACEs有关(P<0.05),将年龄及单因素分析中P<0.1的变量纳入多因素分析发现,入院GRACE危险分层(HR=1.48,95%CI 1.07~2.06,P=0.018)、RHI(HR=0.25,95%CI 0.12~0.52,P=0.000)及病变血管数量(HR=1.51,95%CI 1.10~2.07,P=0.010)是PCI术后患者未来发生MACEs的独立预测因素(表3)。
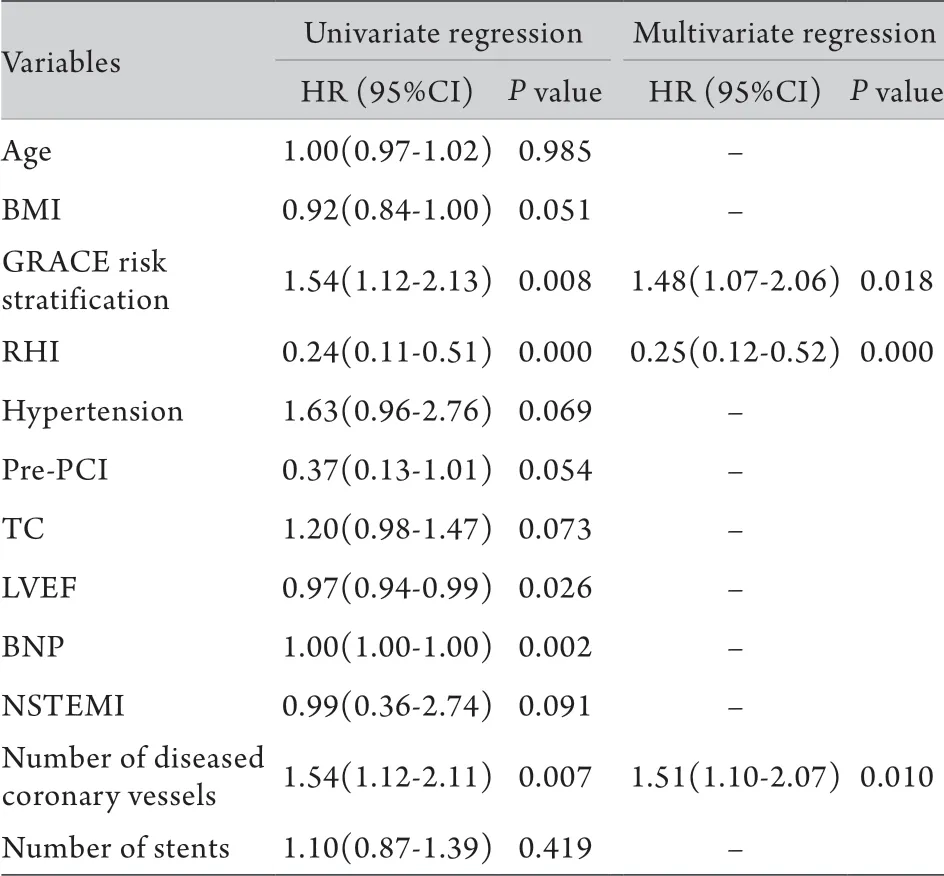
表3 ACS患者PCI术后主要心脏不良事件的Cox比例风险回归分析Tab.3 Regression analysis of Cox proportional comparison hazards for future MACEs in ACS patients after PCI
此外,Kaplan-Meier生存曲线分析显示,GRACE低、中、高危组总体上累积MACEs发生率差异有统计学意义(P=0.021),高危组累积MACEs发生率最高,其次是中危组,低危组累积MACEs发生率最低(图1A)。在GRACE低、中、高危组中,ACS患者PCI术后DEF组累积MACEs发生率较NEF组均明显升高(P=0.026、P=0.038、P=0.046,图1B-D)。
3 讨 论
既往研究发现,由于ACS患者存在个体异质性,导致治疗及预后出现较大差异,因此危险分层在ACS患者的治疗和管理中起着非常重要的作用[19]。入院GRACE评分初始主要用于评估ACS患者住院期间及出院6个月的死亡风险[20-22]。通过对患者进行危险分层,有助于临床医生对ACS患者实行早期管理,指导选择恰当的干预措施,在临床上得到了广泛应用,受到各大指南的推荐[19,23-24]。随后Fox等[6]发现,入院GRACE评分不仅可以评估ACS患者早期死亡及心肌梗死风险,还可用于预测ACS患者长达5年的预后。本研究发现,入院GRACE评分可作为ACS患者PCI术后未来发生MACEs的预测工具。在心源性死亡及心脏主要不良事件上,随着GRACE危险分层增加,心源性死亡及心脏主要不良事件发生率逐渐增加;在急性心肌梗死、靶血管重建、缺血性卒中事件上也呈现出相似的趋势。Cox比例风险回归分析提示,入院GRACE危险分层是未来发生MACEs的独立预测因素。Kaplan-Meier生存曲线分析显示,随着随访的时间延长,入院GRACE危险程度越高,则累积MACEs发生率越高。因此,通过入院GRACE评分将PCI术后患者分为低、中、高危可以作为预测其中远期预后的一个重要危险分层工具。但也有学者认为,入院GRACE评分仍存在不足(如可能会高估低危患者未来发生MACEs的风险等)[25],此外该评分涉及的生物标志物(如心梗标志物、肌酐)较少,不能很好地反映机体的病理状态。因此,有研究人员将一些与ACS病理机制相关的生物标志物(如CRP、血红蛋白、BNP)单独加入GRACE评分体系,发现可以提高其危险分层的价值[25-28]。但这些研究主要关注ACS患者的短期预后,而且这些生物标志物均不能很好地反映冠状动脉的内皮功能状态。本研究通过探讨RHI与入院GRACE评分对PCI术后患者中远期预后的预测价值,发现RHI(为评估冠状动脉血管内皮功能的重要指标)在入院GRACE危险分层基础上,为PCI术后患者提供了传统危险因素以外的重要的预后信息。
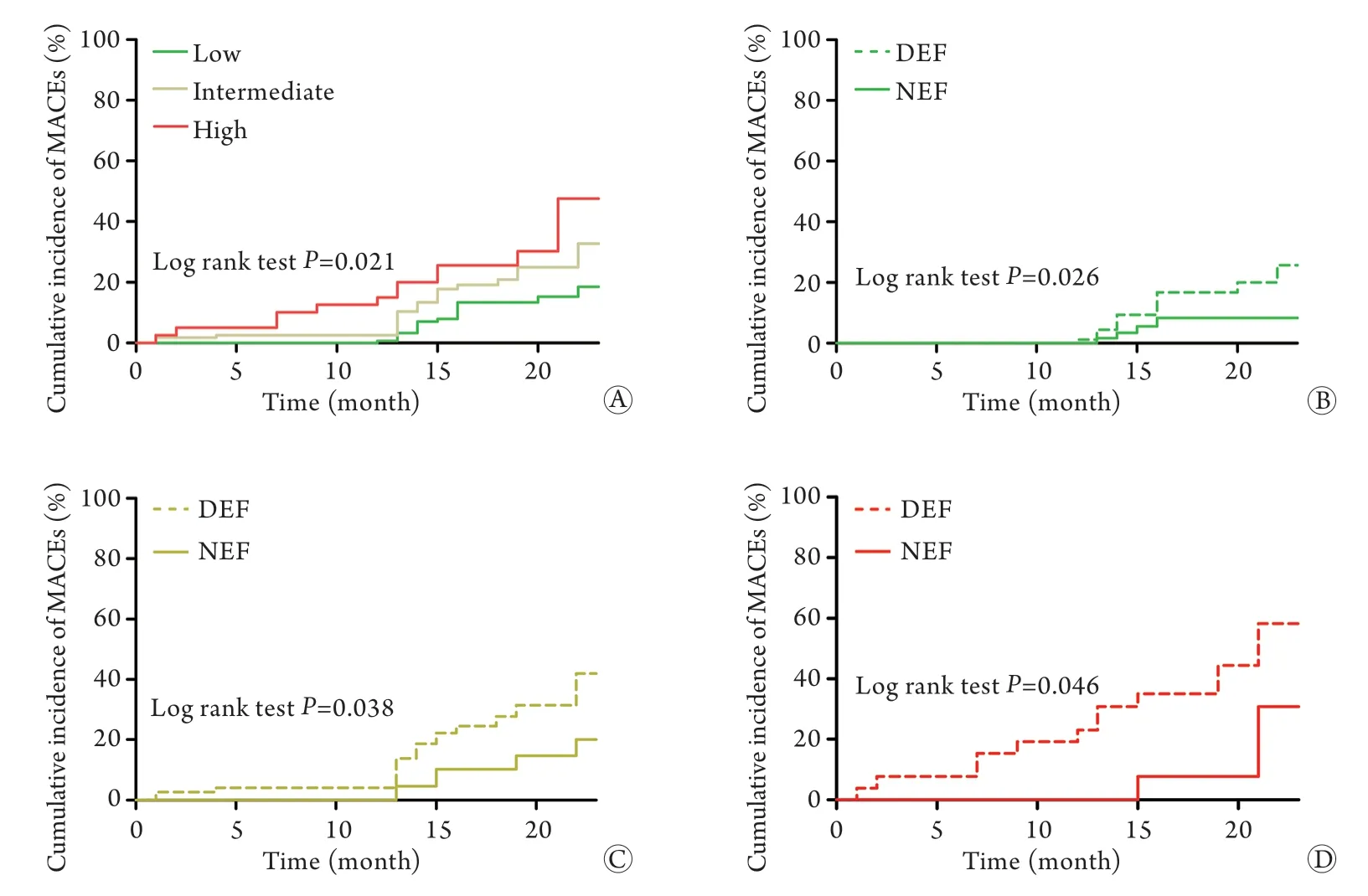
图1 ACS患者PCI术后主要心血管不良事件Kaplan-Meier曲线Fig.1 Kaplan-Meier curves of cumulative incidences of MACEs in ACS patients after PCI
既往研究表明,血管内皮功能障碍是导致动脉粥样硬化的始动因素,在动脉粥样硬化的发生、发展中占有重要地位[29-30]。根据“损伤应答”学说理论,高血脂、高血压、高龄、性激素失衡、氧化应激以及促炎因子等传统心血管疾病危险因素可导致血管内皮细胞损伤,破坏血管内皮机械屏障;同时损伤的内皮细胞可引起血管活性物质合成和分泌功能异常,引起血管局部内皮源性NO合成及效应发生障碍、促进炎症因子激活、TXA2/PGI2平衡失调等,导致单核细胞及脂质不断沉积于内皮下,形成脂纹,同时不断激活血小板聚集并刺激中膜平滑肌细胞增生进展为纤维斑块,最终可导致不稳定斑块形成,引起缺血性或血栓性事件发生[31]。Bonetti等[13]研究表明,与检测冠状动脉血管内皮功能的“金标准”法(即乙酰胆碱诱发试验)相比较,通过外周检测动脉RHI同样能够很好地反映冠状动脉内皮功能状态,因此Endo-PAT 2000可以作为一种无创检测冠状动脉内皮功能障碍的重要方法。同时,RHI与PCI术后支架再狭窄、心绞痛再发及脑卒中的发生密切相关[14,32-33],此外,研究表明,RHI可以作为预测未来发生心血管不良事件的重要指标[15,34]。本研究发现,RHI是ACS患者PCI术后未来发生MACEs的独立预测因素。RHI作为评估冠状动脉内皮功能的重要指标,从整体上可以很好地反映血管内皮的功能状态,并在GRACE危险分层的基础上,可进一步对PCI术后患者再进行危险分层,无论是低、中、高危组患者,DEF组累积MACEs发生率均明显高于NEF组,提高了GRACE危险分层对PCI术后患者中远期预后的预测价值。
此外,本研究还发现,血管病变数量也是PCI术后患者未来发生MACEs的独立预测因素,但与植入支架数量无关,可能提示ACS患者血管病变数量越多,病变越重,PCI术后预后越差,即使植入多个支架尽可能开通阻塞血管,也不能明显改善患者预后,因此应该强调早期诊断,并且早期进行血管再通及药物治疗。
本研究仍存在以下局限性.为单中心的临床研究,样本量有限,后期需要更大样本量的临床研究验证相关结果;由于纳入人群GRACE评分高危组患者数量较少,这可能是MACEs发生率较低的原因。
综上所述,本研究发现,RHI作为反映血管内皮功能状态的重要指标,在入院GRACE危险分层的基础上,可以进一步有效地鉴别出PCI术后患者中远期预后不良的危险人群,针对这些危险人群,进一步加强管理,实施个体化抗栓、降脂及改善内皮功能等治疗,可能有望降低这些患者未来发生MACEs的风险。

