甲烷水合物在不同温度下扩散及其结构的模拟研究
徐鸣彦,李 毅,吴小灵,黄韵卓,冯华杰
(海南师范大学 化学与化工学院,海南 海口 571158)
自20世纪90年代开始,天然气水合物的开采技术一直是重点研究的课题.传统的水合物开采技术主要有注热法、降压法和注化学试剂法,都是通过改变水合物层的环境,使天然气水合物层不稳定,分解并释放出天然气.这些技术破坏水合物地层结构,导致海洋底斜坡灾害,对海洋甚至地球安全造成影响[1, 2].因此,需要进一步研究天然气水合物的性质.
利用分子动力学(Molecular Dynamics, MD)模拟方法可以研究各种体系的扩散行为,并对微观局部结构作深入系统的研究[3-7].由于温度是影响天然气水合物的性质的重要条件,因此本工作拟通过分子动力学模拟方法,在不同温度条件下,从微观水平上研宄甲烷水合物的分子扩散和局部结构.
1 模拟方法
MD模拟采用GROMACS程序包[8],H2O采用SPC力场,CH4采用OPLS-AA力场.自然界中普遍存在的甲烷水合物是sⅠ型水合物[9, 10],即一个sⅠ晶胞包含8个甲烷分子和46个水分子.本工作采用周期性边界条件,模拟3×3×3个sⅠ型水合物晶胞,即甲烷分子个数为216,水分子个数为1 242.范德华作用距离设置为1.4 nm,动力学步长设置为1 fs.采用NpT系综,一共执行了6 000 000动力学步数计算任务,其中前一半动力学步数用于平衡体系研究,后一半动力学步数用于统计分子扩散和结构性质.研究体系的压力都为10 MPa,温度分别为275、285、295和305 K.
2 结果与讨论
2.1 分子扩散系数
根据爱因斯坦的扩散定律[11]分别统计了甲烷分子、水分子的扩散系数D,即:
(1)
其中,r代表的是某个粒子所在的位置
表1列出了模拟得到的甲烷和水的扩散系数.随着温度的升高,甲烷和水的扩散系数均增大.在文献研究的纯甲烷体系中[12],295 K和11 MPa条件下,甲烷的自扩散系数为158×10-9m2·s-1.而从表1可知,295 K和10 MPa条件下,甲烷的扩散系数为9.57×10-9m2·s-1,远远小于纯甲烷体系中甲烷的自扩散系数,表明在甲烷水合物中,水分子之间形成的氢键网络减缓了甲烷分子的扩散.另一方面,也是主要由于水分子之间形成了氢键网络,导致了水分子的扩散系数远远小于甲烷的扩散系数.
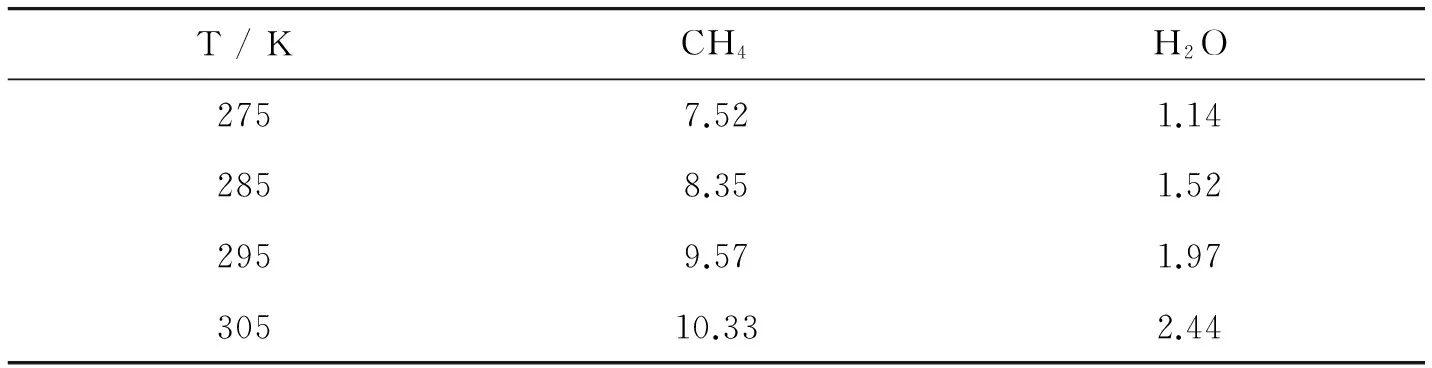
表1 甲烷和水的扩散系数(10-9m2·s-1)
2.2 径向分布函数
为了探讨体系的结构性质,分别研究了不同温度下CH4-CH4、CH4-H2O、H2O-H2O、H2O-CH4的径向分布函数,如图1所示.从图1(a)至(d),当体系温度从275 K升高至305 K,甲烷水合物的各种类型的径向分布函数的第一峰所在位置基本没有变化,分别保持在0.40、0.38、0.27、0.38 nm附近,而第一峰的高度明显随温度上升而下降.其中,CH4-CH4和H2O-H2O的第一峰很强,高度达到4以上,而CH4-H2O和H2O-CH4第一峰很弱,高度仅接近0.5.这表明在甲烷分子附近,其它甲烷分子排列紧密有序,而水分子排列稀疏分散;反之,在水分子附近,其它水分子排列紧密有序,而甲烷分子排列稀疏分散.


图1 温度对CH4-CH4、CH4-H2O、H2O-H2O、H2O-CH4径向分布函数的影响
2.3 配位数
配位数也反映了局部结构性质,它是对径向分布函数积分所得到[13],公式如下:

(2)
式中,ρ0表示数密度,gij表示i和j的径向分布函数.
本文分别对CH4-CH4、CH4-H2O、H2O-H2O、H2O-CH4的径向分布函数的第一个峰积分,即第一溶剂化层,得到的平均配位数列于表2.从表2可知,随着温度的升高,各种类型的平均配位数均减小.很明显,从H2O-CH4的径向分布函数统计得到的配位数远远小于其它类型的配位数,表明了平均每个水分子的第一溶剂化层内的甲烷分子极其少.比较CH4-CH4配位数和CH4-H2O配位数可知,甲烷分子周围出现的其它甲烷分子的数量远多于水分子的数量,也就是说甲烷分子间倾向相互聚集;另一方面,比较H2O-H2O配位数和H2O-CH4配位数可知,水分子周围出现的其它水分子的数量远多于甲烷分子的数量,同理,水分子间倾向相互聚集.

表2 平均配位数
2.4 氢键数
采用了几何标准来计算水分子之间形成的氢键数,即满足以下条件则认为形成氢键:距离O---O小于0.35 nm,角H—O—O小于30°.当温度为275、285、295、305 K时,模拟得到的水的平均氢键数依次为3.65、3.60、3.55、3.50,与文献值中纯水的平均氢键数相近[14].很明显,随着温度的升高,水的平均氢键数减小,即水分子之间形成的氢键网络减弱.
3 结论
采用分子动力学模拟方法,研究了在压力为10 MPa及温度分别为275、285、295、305K的条件下,甲烷水合物的分子扩散和局部结构.总的来说,随着温度的升高,水分子之间形成的氢键网络减弱,各种类型的配位数减小,径向分布函数的第一峰的高度降低,体系的有序性降低,分子的扩散系数增大.水分子之间形成的氢键网络造成水分子的扩散系数小于甲烷分子的扩散系数,而甲烷水合物中甲烷分子的扩散系数远远小于纯甲烷体系中甲烷分子的自扩散系数.在甲烷分子附近,其它甲烷分子排列紧密有序,而水分子排列稀疏分散,即甲烷分子间倾向相互聚集;反之,在水分子附近,其它水分子排列紧密有序,而甲烷分子排列稀疏分散,即水分子间也倾向相互聚集.
[1]Kvenvolden K A. Gas hydrate-geological perspective and global change[J]. Rev Geophys,1993,31(2) :173-187.
[2]徐纯刚,李小森,蔡晶,等.二氧化碳置换法模拟开采天然气水合物的研究进展,化工学报, 2013,64(7):2309-2315.
[3]黎多来,周昌林,李东凯,等.氨的氢键数的分子动力学模拟研究[J].海南师范大学学报(自然科学版), 2012, 25(4): 425-426.
[4]周昌林,黎多来,李东凯,等.氨的局部结构的分子动力学模拟研究[J].海南师范大学学报(自然科学版), 2013, 26(1): 48-50.
[5]冯华杰,聂晶晶,孙振范,等. N-甲基甲酰胺的自扩散和结构性质的分子动力学模拟[J].化工学报, 2015, 66(5): 1683-1689.
[6]徐鸣彦,史娟娟,冯华杰.控温方式对甲烷自扩散和局部结构影响的分子动力学模拟[J].海南师范大学学报(自然科学版), 2016,29(4): 407-410, 417.
[7]Feng H, Gao W, Su L, et al. MD simulation study of the diffusion and local structure of n-alkanes in liquid and supercritical methanol at infinite dilution[J]. J Mol Model, 2017,23(6): 195.
[8]Hess B, Kutzner C, Van Der Spoel D, et al. Gromacs 4: algorithms for highly efficient, load-balanced, and scalable molecular simulation[J]. J Chem Theory Comput, 2008,4(3): 435-447.
[9]Sloan E D, Koh CA. Clathrate hydrates of natural gases[M]. Boca Raton:3rd ed. CRC Press, 2007.
[10]Buffett B A. Clathrate hydrates[J]. Annu Rev Earth Pl Sc, 2000,28(1): 477.
[11]Einstein A. Über die von der molekularkinetischen theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen[J]. Ann Phys, 1905, 17: 549-560.
[12]Greiner-Schmid A, Wappmann S, Has M, et al. Self-diffusion in the compressed fluid lower alkanes: methane, ethane, and propane[J]. J Chem Phys, 1991, 94(8): 5643-5649.
[13]Lengeler B, Eisenberger P. Extended x-ray absorption fine structure analysis of interatomic distances, coordination numbers, and mean relative displacements in disordered alloys[J]. Phys Rev B, 1980, 21(10):4507-4520.
[14]Sit P H L, Bellin C, Barbiellini B, et al. Hydrogen bonding and coordination in normal and supercritical water from x-ray inelastic scattering[J]. Phys Rev B, 2007, 76(24): 245413.

