药师角度对药品不良反应的评价与分析
安胜男,张婉璐,任文静,付桂英(解放军307医院药学部,北京 100073)
药品不良反应(adverse drug reaction,ADR),是指用药后出现与用药目的无关、与预期效果不一致的反应[1]。即使是在合理用药水平较高的美国,也有30%的住院患者发生药品不良反应,严重不良反应发生率约10.9%[2]。世界卫生组织的一项调查表明,全球有1/3的患者死于不合理用药,而不是疾病本身。因发生ADR导致患者入院的比例约占总体住院率的0.6% ~ 36%[3]。由于医学发展的局限性,许多药品的不良反应在审批时难以完全了解,尤其是中药注射剂的广泛使用,不良反应也相对增加[4]。因此在药品上市后,可以根据上报的ADR来及时发现和控制药品安全风险。据CFDA发布数据显示,2016年,我国共收到报告ADR/ADE 143万份,较2015年有所增长,其中,新的和严重的ADR/ADE 42.3万份,仅占报告总量的29.6%。上报的ADR报告中,85.6%来自医疗机构,药品经营企业占12.8%,药品生产企业占1.4%。临床用药过程中ADR的发生较为广泛,及时有效的评价和监测对于保障安全用药至关重要[5]。
本研究根据本院不良反应监测管理系统上报的数据,对所有上报的ADR报告进行回顾性分析,从患者个体差异、药品分类和报告严重程度、转归等角度进行汇总与分析,旨为ADR评价和安全用药提供依据。
1 资料和方法
采用回顾性分析方法,利用我院ADR监测管理系统,收集2012年5月– 2017年5月我院上报的ADR报告,包括门诊和住院的患者。对所发生的ADR进行评价,汇总ADR的分布因素,包括年龄、性别、药物种类、系统损害部位程度和转归等,并从药学角度对新的、严重和中药注射液的ADR进行汇总分析。
2 结果
2.1 基本情况
765例ADR报告中,男性286例,女性479例,年龄大于70岁患者比例高达22.09%,详见表1。全院ADR上报例数最高的科室分别是急诊科(20.05%),呼吸内科(19.66%),药学部(17.30%),肾内科(7.73%)和消化内科(5.37%)。近5年全院ADR上报人职业分布医生共计629例,药师131例,护士5例,其他5例,且药师上报ADR的数量逐年升高,与临床药师密切参与临床工作有关。
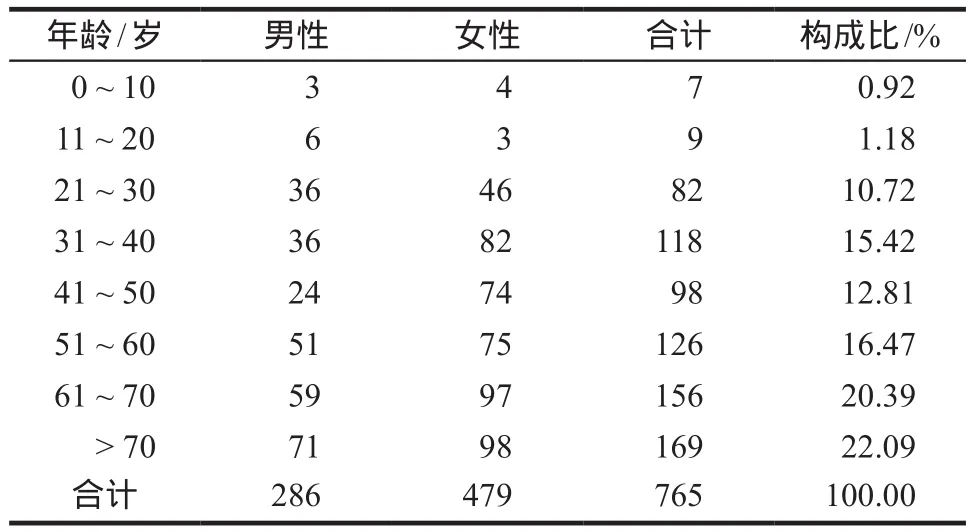
表1 不良反应上报基本情况Tab 1 The basic situation of reporting adverse reactions
2.2 药物分布
全院ADR上报频次最高的药物种类分别是抗生素、人工合成抗菌药、抗肿瘤药、抗真菌药、营养支持用药和肝脏辅助用药,其中抗生素和人工合成抗菌药共计365例(47.71%),排名前5位的药品分别是乳酸左氧氟沙星氯化钠(62例)、盐酸莫西沙星注射液(59例)、盐酸莫西沙星氯化钠注射液(49例)、注射用乳糖酸阿奇霉素(32例)和注射用头孢美唑钠(29例)。抗肿瘤用药共46例(6.01%),包括吉西他滨(8例)、顺铂(7例)和多西他赛(5例);抗真菌用药共计39例(5.10%),主要包括注射用伏立康唑28例;营养支持类药物包括肠内营养乳剂(TPF-T)和结构脂肪乳注射液等共计32例(4.18%);肝脏辅助用药主要是保肝药,涉及注射用复方甘草酸苷、双环醇和异甘草酸镁等共计21例(2.75%)。
另外,本研究关于同一药品出现在不同器官部位的不良反应也进行统计,结果显示,发生ADR涉及部位较多且表现广泛的分别是乳酸左氧氟沙星氯化钠注射液、乳糖酸阿奇霉素、头孢美唑钠、注射用伏立康唑和亚胺培南西司他丁钠。详见表2。
2.3 严重等级和转归
不良反应报告等级为严重的患者共计18例,涉及15种不同的药品。18例患者中男性12例,女性6例,平均年龄57岁,其中有2例不良反应在药品说明书中无记载,包括紫杉醇注射液致溃疡性口炎和注射用兰索拉唑致过敏性休克。其它出现的严重不良反应在说明书或文献中均有报道,具体见表3。

表2 同一药品ADR表现频次较高的信息Tab 2 Information on the higher frequency of ADR performance of the same drug
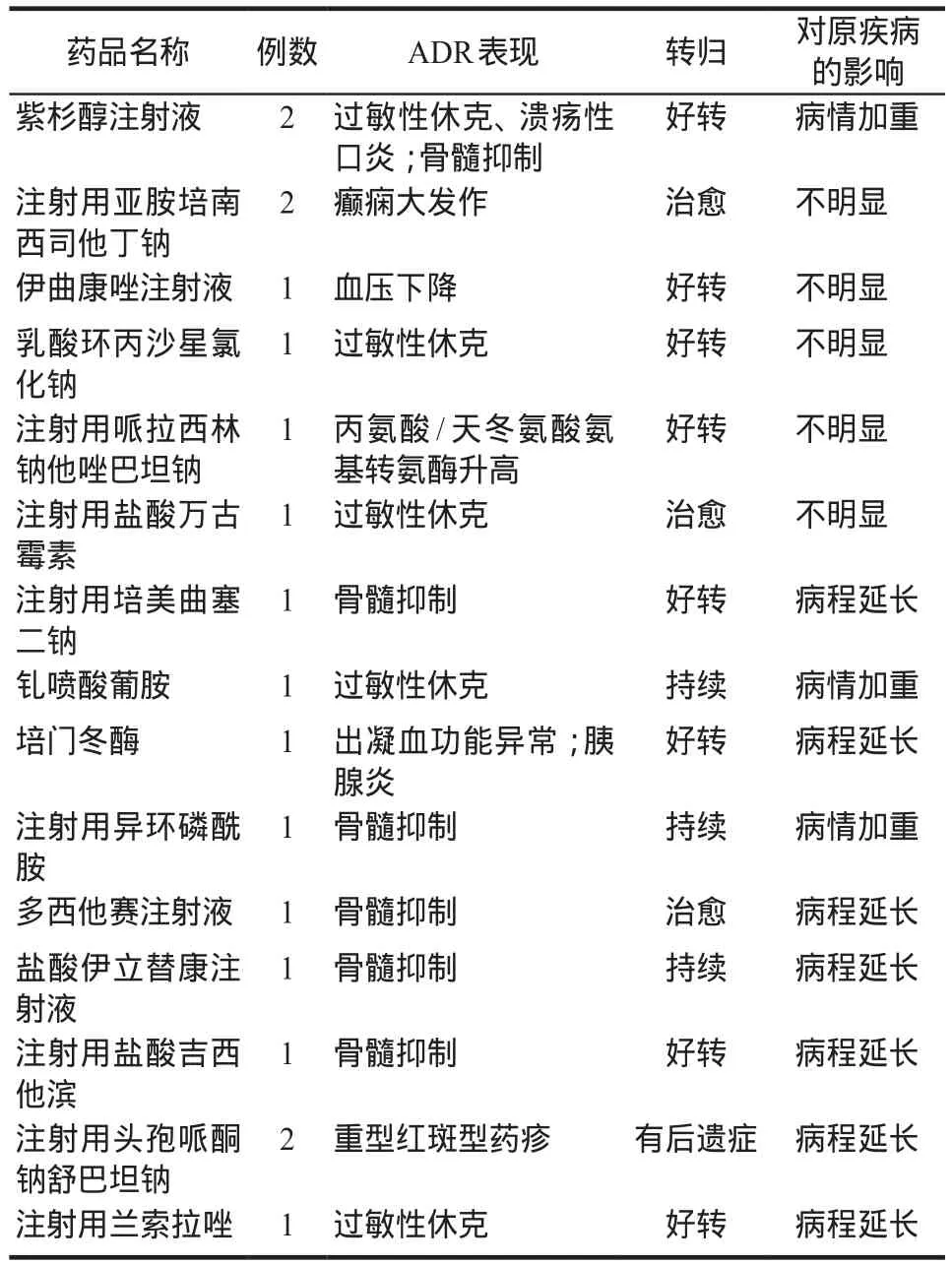
表3 严重不良反应信息分布Tab 3 Information distribution of serious adverse reactions
另本研究发现2例新的一般的不良反应,分别是输注抗人T细胞猪免疫球蛋白后患者出现心前区不适、体重增加、氧饱和度下降,医生对此情况进行停药处理,后好转;除此之外,患者使用注射用奥沙利铂后出现胰腺炎和胰腺外分泌病型糖尿病,医生立即停止输注奥沙利铂并予以盐酸苯海拉明40 mg肌肉注射抗过敏并吸氧,后经治疗好转。
2.4 中药注射剂的不良反应
近年来,中药注射剂的安全性饱受争议,本研究针对中药注射剂的ADR进行统计,结果显示,共计26例患者,男性5例,女性21例,平均年龄54岁。所有患者均采用静脉滴注方式输注,输液后出现ADR的平均时间约153 min,出现ADR后均即刻停药,ADR表现均逐渐减轻或好转,其中4例患者重复应用出现ADR药品后又出现相同的不良反应;剩余22例患者无再次使用此药品记录。具体见表4。
3 讨论
药源性疾病已成为世界范围内的第四位死亡原因,即使是在合理用药水平较高的美国,也有30%的住院患者发生ADR。因此,正确客观的评价药物发生的不良反应及其处理至关重要。本研究收集我院近5年不良反应报告共计765例,近5年ADR上报的总数基本呈下降趋势,分析原因可能与临床对ADR上报的重视程度不够;另外一方面可能与近年来临床药师参加临床查房普及药品知识有关,对过敏体质和用药复杂患者给予合理的用药意见,同时统计结果表明药师上报ADR数量逐年增多。
抗感染药物相关的ADR已逐渐被临床所重视,特别是严重ADR,是除了治疗效果之外,与患者预后情况密切相关的因素之一[6-7]。临床药师对上报频次较高的药物进行统计,涉及种类最多当属抗感染药物,其中乳酸左氧氟沙星氯化钠、盐酸莫西沙星注射液和盐酸莫西沙星氯化钠注射液居多,同时同一种药品发生不良反应涉及的器官居多者是乳酸左氧氟沙星氯化钠注射液、盐酸莫西沙星注射液、盐酸莫西沙星氯化钠注射液。
其次是抗肿瘤药共计46例,包括吉西他滨和多西他赛等,由于抗肿瘤药物本身大多存在治疗窗窄的特点,低剂量使用也会产生ADR,同时肿瘤患者身体状态较差,严重者可能导致患者各个器官出现衰竭[8],因本院是肿瘤专科医院,因此在评价肿瘤药品ADR时应着重区别患者疾病表现和药品引发的ADR。临床药师建议肿瘤患者在药物治疗前应做常规检查,包括血生化和血常规等,以便与化疗后患者指标作比较。
抗真菌药物中的注射用伏立康唑发生ADR的频次也相对较高,除了常见的皮疹外,对视力的影响也较多,包括失明、畏光和飞蝇幻视等,因此对于有原发眼部疾病的患者还应注意使用此药物的剂量和用药后防范措施。营养支持药物包括肠内营养乳剂(TPF-T)和结构脂肪乳注射液共计32例,与营养支持途径(肠内和肠外)无明显比例关系,使用营养支持的患者大多为肿瘤或老年患者,给药速度过快往往会造成患者恶心、胸闷、寒战等[9],出现过敏性休克的患者可能与脂肪乳中含大量大豆蛋白有关[10]。建议临床上使用营养支持类药品时要在控制滴速基础上密切观察患者的反应,缩短用药时间。保肝药主要涉及注射用复方甘草酸苷、双环醇和异甘草酸镁等共计21例,所有不良反应均为非特异性不良事件。
严重不良反应报告数量及比例是影响ADR监测系统敏感度的重要指标[11],本研究共收集18例严重不良反应,涉及15种药品,男性高于女性,所有患者经及时抢救后病情多为好转或治愈,其中注射用头孢哌酮钠舒巴坦钠给患者造成不可逆转的重型红斑型后遗症。由于本院肿瘤患者居多,化疗药物多以静脉给药为主,这也是容易引起严重ADR的原因之一。另出现2例新的不良反应,抗人T细胞猪免疫球蛋白引起心前区不适、体重增加、氧饱和度下降和注射用奥沙利铂后出现胰腺炎和胰腺外分泌病型糖尿病。对于此类ADR,药师应尽早评价,快速上报,并查阅相关药品知识对ADR后续进行处理。
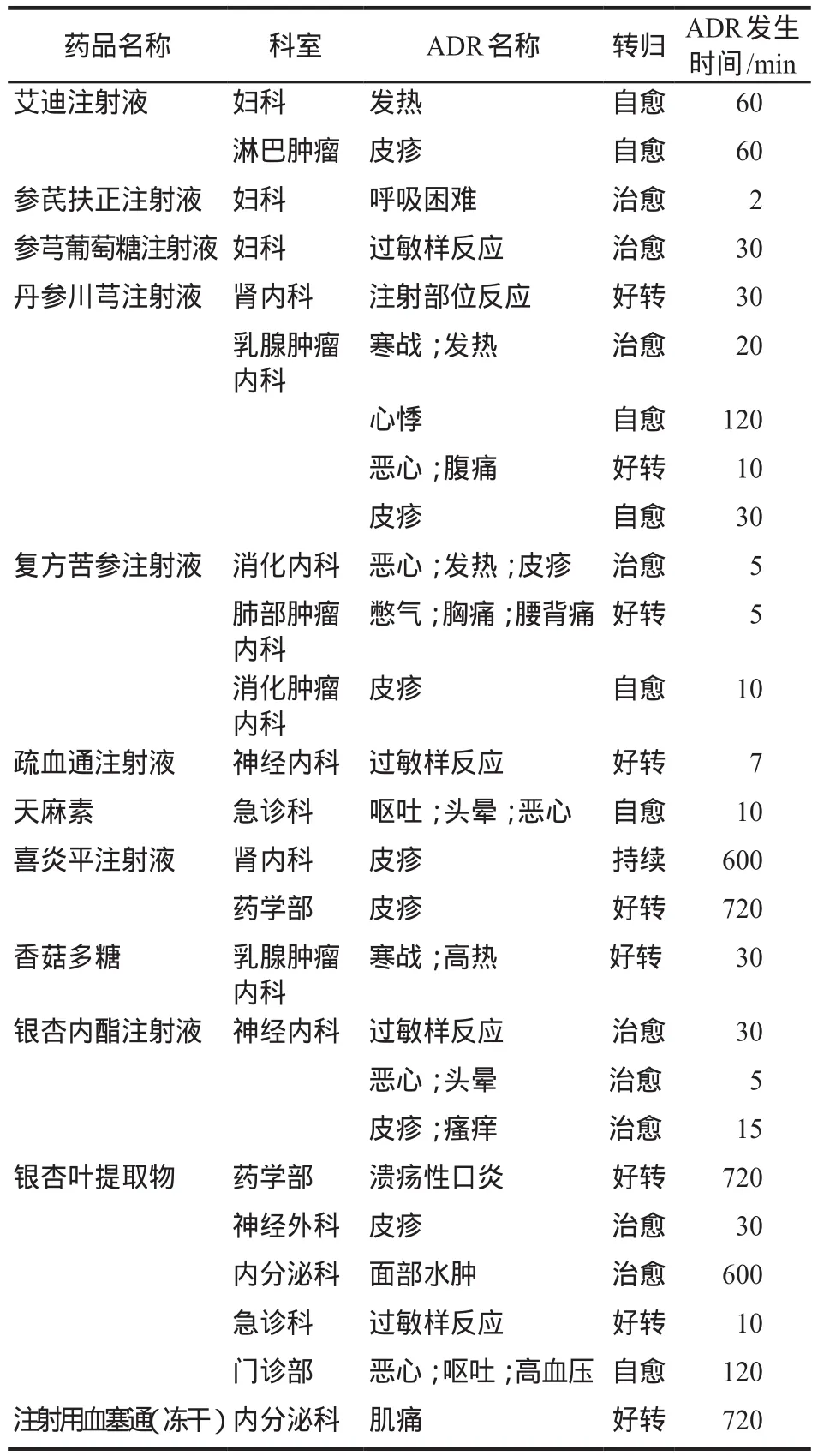
表4 中药注射剂ADR情况Tab 4 The ADR situation of traditional Chinese medicine injection
本研究结果显示,中药注射剂所致ADR发生率女性多于男性,与之前报道结果相近[12-13]。发生ADR的时间基本在1 h之内,发生时间短暂,建议临床密切观察。分析其产生不良反应的原因,药师角度认为中药注射剂本身含有多种成分,含量复杂,有效成分难以定量,在检测的环节很难去界定热源等问题;其次在中药领域中只有确切的标准来检测药物中主要成分,而对附属物例如糖苷等的检测缺乏准确依据;在医疗机构等实际运用的环节可能也出现问题;ADR的发生还与患者个体差异关系密切,过敏体质患者更容易发生ADR[14]。药师建议对于中药注射剂应单独使用,在使用过程中应进行溶解或稀释,谨慎与其他药物混合配伍使用,严格按照药品说明书的要求合理用药。
[1] Inch J, Watson MC, Anakwe-Umeh S,et al. Patient versus healthcare professional spontaneous adverse drug reaction reporting[J]. Drug Saf, 2012, 35(10): 807-818.
[2] Lazarou J, Pomeranz BH, Corey PN. Incidence of adverse drug reactions in hospitalized patients: a meta-analysis of prospective studies[J]. JAMA, 1978, 279(15): 1200-1205.
[3] Ke CH, Chung WH, Wen YH,et al.Cost-effectiveness analysis for genotyping before allopurinol treatment to prevent severe cutaneous adverse drug reactions[J]. J Rheumatol, 2017, 44(6):835-843.
[4] 卞兆祥,商洪才,吴泰相,等.中药注射剂不良反应/不良事件的反思[J].中国循证医学杂志,2010,10(2):116-121.
[5] Alfirevic A, Pirmohamed M. Genomics of adverse drug reactions[J]. Trends Pharmacol Sci, 2017, 38(1): 100-109.
[6] 方静,周学琴.抗感染药物不良反应/事件报告相关因素分析及预防[J].中国抗生素杂志,2012,37(2):141-144.
[7] 祖玉梅.抗菌药物不良反应102例分析[J].临床合理用药,2010,3(6):45-46.
[8] 方文涛,陈勇,张翔宇,等.老年重症开胸手术围术期呼吸循环变化与呼吸并发症的相关性[J].中华胸心血管外科杂志,2006,22(4):245-248.
[9] 闫忠芳,陈丽芳,齐玉梅.97例脂肪乳注射液致不良反应的文献分析[J].中国药房,2010,21(32):3038-3040.
[10] Mirtallo JM, Dasta JF, Kleinschmidt KC,et al. State of the art review: intravenous fat emulsions: current applications, safety profile, and clinical implications[J]. Ann Pharmacother, 2010,44(4): 688-700.
[11] 王文沛,邵蓉.我国新的和严重的药品不良反应报告现状及障碍分析[J].中国药事,2011,25(3):227-230.
[12] 李正伟,原永芳.2013年我院中成药不良反应报告分析[J].中医药导报,2014,21(15):35-36.
[13] Ekor M. The growing use of herbal medicines: issues relating to adverse reactions and challenges in monitoring safety[J]. Front Pharmacol, 2014, 4: 177.
[14] Edwards IR, Aronson JK. Adverse drug reactions: definitions,diagnosis, and management[J]. Lancet, 2000, 356(9237): 1255-1259.
《中国药物应用与监测》杂志2018年征订启事
《中国药物应用与监测》杂志是国内外公开发行的药学类学术性期刊,主要报道范围包括药物在临床研究与应用中的疗效、安全性及经济学评价,药理毒理学研究,药物代谢动力学及生物利用度研究等,主要栏目有专家论坛、临床评价、实验研究、临床药师园地、不良反应监测、药物利用分析、药学进展、案例分析等。本刊为中国科技核心期刊(中国科技论文统计源期刊)。
本刊为双月刊,大16开本,64页,每期定价9.00元(全年54.00元),逢双月25日出刊。邮发代号:80-623,欢迎广大读者通过当地邮局订阅。
联系地址:北京市复兴路28号《中国药物应用与监测》编辑部 邮编:100853
联系电话:(010)66937047
投稿邮箱:zhgywyyyjc@263.net

