多酚原位固化茶渣对水中Cr(Ⅵ)的吸附
龚新怀,戴忠豪,李素琼,张妙君,赵晓杰,郭绍英
(1. 武夷学院 生态与资源工程学院,福建 武夷山 354300;2. 福建省生态产业绿色技术重点实验室,福建 武夷山 354300)
重金属Cr广泛存在于印染纺织、钢铁制造、皮革及电镀行业等排放的废水中,是水污染物的主要成分之一,其中以Cr(Ⅵ)毒性最大[1-2]。目前含Cr(Ⅵ)废水的处理方法主要有絮凝沉淀[3]、膜分离[4]、吸附[2]、电化学[5]等方法,其中吸附法因简便易行而被广泛使用。而利用丰富易得的天然生物质材料或农业废弃物制备低成本生物吸附材料来去除Cr(Ⅵ),更成为当前的研究热点[6-9]。
全球每年的茶叶消耗量超过4500 kt,而在茶叶生产、流通及消费环节中会产生大量的茶渣[10]。茶渣富含纤维素、半纤维素、木质素、多酚、色素等组分,能够有效吸附Cr(Ⅵ),其中的多酚能将吸附的Cr(Ⅵ)部分还原为Cr(Ⅲ)而降低毒性,从而达到去除Cr(Ⅵ)的目的[11-12]。但直接用茶渣吸附Cr(Ⅵ)时,由于茶渣中多酚、色素等组分的溶出,不仅影响了水质外观,增加了有机质新污染物,而且降低了对Cr(Ⅵ)的去除效果[11,13]。将茶渣制成活性炭可提高其吸附性能,但工艺成本较高且回收处理困难[14-15]。
茶渣中富含多酚组分,利用醛类的活性醛基和多酚、色素等的加成、缩合反应[16-19],可将多酚、色素等组分固定在茶渣内部,从而提高茶渣对Cr(Ⅵ)的吸附能力,减少有机质组分的溶出,避免二次污染,还可利用缩聚产物的黏结作用[20]提高茶渣的结构致密性和强度。目前,这方面的研究还鲜见报道。
本工作通过甲醛与茶渣中多酚类组分的反应制备了多酚原位固化茶渣吸附材料,采用FTIR,TG,SEM技术对其进行了表征,并将其用于对水中Cr(Ⅵ)的吸附,研究了吸附影响因素、吸附动力学、吸附热力学等。
1 实验部分
1.1 试剂和材料
茶渣取自当地一家茶叶加工企业,用水冲洗去除杂质,风干后粉碎,并用标准分样筛分取75~180 μm粒径部分。实验所用甲醛、盐酸、硫酸、二苯碳酰二肼、重铬酸钾等均为分析纯,国药试剂。实验用水为去离子水。
1.2 茶渣多酚原位固化的原理及方法
茶渣中的多酚具有间苯二酚或间苯三酚的结构,与甲醛发生酚醛缩合反应的活性比苯酚高[17]。茶渣多酚原位固化反应的示意图见图1。多酚先与甲醛发生加成反应,得到一取代或多取代的羟甲基酚,羟甲基酚可与多酚或羟甲基酚之间发生脱水缩合反应。随着加成与缩合反应的不断进行,多酚之间通过亚甲基连接起来形成交联大分子,使多酚上的活性酚羟基得以保留,有利于茶渣对水溶液中Cr(Ⅵ)的吸附。
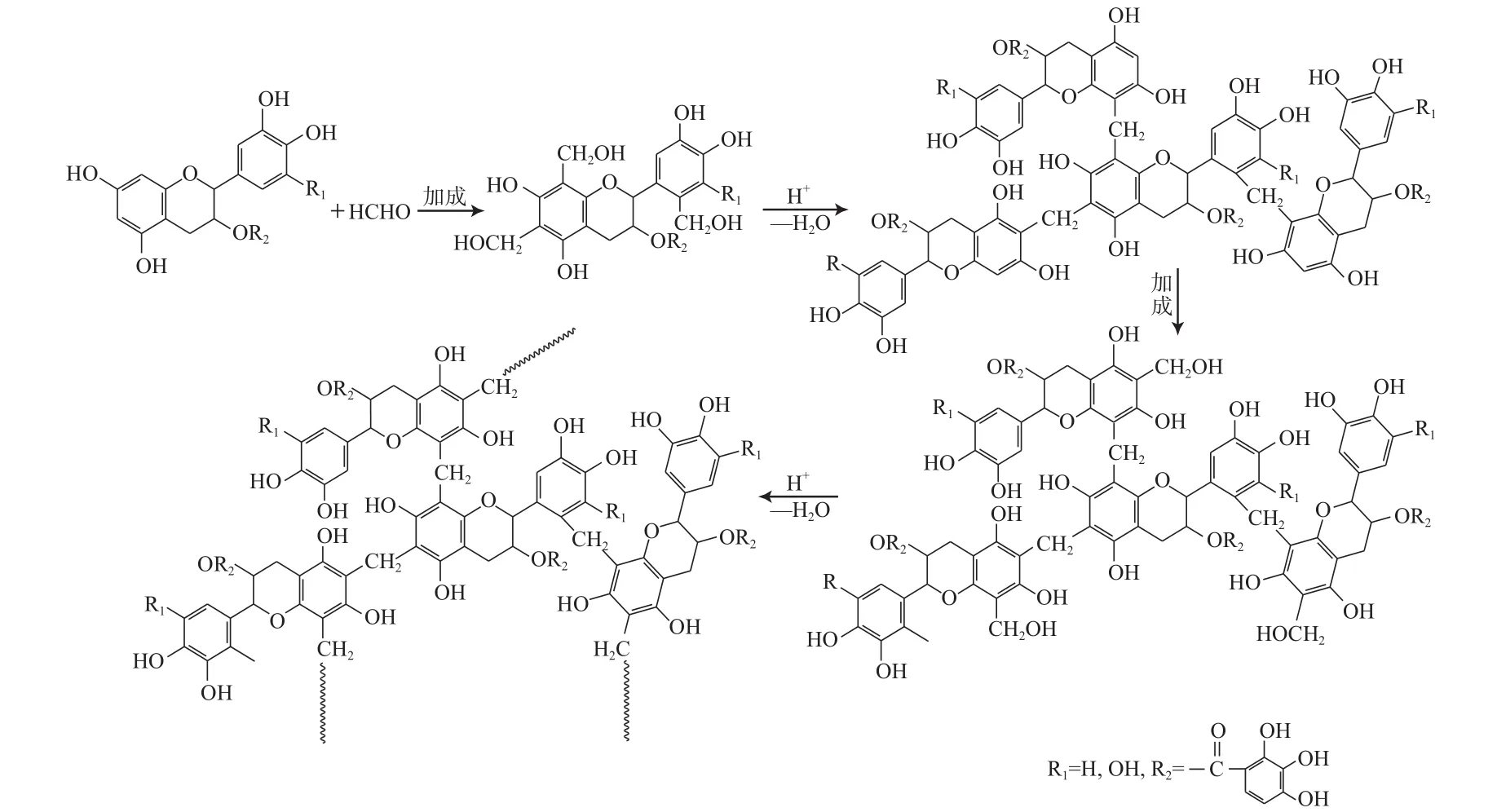
图1 茶渣多酚原位固化反应的示意图
称取5.00 g处理后的茶渣,加入适量去离子水和甲醛于250 mL三口反应瓶中,组装球形冷凝管。加入50 mL 0.5 mol/L的HCl溶液,333 K下搅拌反应2 h。抽滤,洗涤滤渣至滤液pH近中性,转至333 K鼓风干燥箱中干燥24 h,得多酚原位固化茶渣(简称固化茶渣)。
1.3 固化茶渣对Cr(Ⅵ)的吸附
采用静态吸附法考察固化茶渣对Cr(Ⅵ)的吸附性能。取100.00 mL Cr(Ⅵ)溶液,调节pH后,加入0.10 g固化茶渣,转入THZ-82型水浴恒温振荡器(巩义市站街光亚仪器厂)振荡吸附一定时间后,取出静置3~5 min,取上层清液待测。
1.4 分析方法
分别采用AVATAR-330型傅里叶变换红外光谱仪(美国赛默飞世尔科技)、Q600型同步热分析仪(美国TA仪器公司)、S-4800型冷场发射扫描电子显微镜(日本日立公司)对固化前后的茶渣进行表征分析。
采用二苯碳酰二肼分光光度法[17],在UV-2550型紫外-可见分光光度计(日本岛津公司)上测定所取上层清液的吸光度(波长664 nm),得到Cr(Ⅵ)浓度,进而计算其吸附量和去除率。
2 结果与讨论
2.1 表征结果
2.1.1 化学结构分析
茶渣中含有纤维素、木质素、半纤维素、茶多酚及茶多糖等,故其FTIR谱图在整个波数范围几乎都有吸收。茶渣固化前后的FTIR谱图见图2。由图2可见:茶渣经多酚固化后,在2800~3000 cm-1及1463 cm-1处C—H键的吸收峰[21]强度明显增强,表明茶渣改性过程中引入了C—H,这是甲醛反应结合到分子骨架的表现之一[17],说明茶渣的多酚主要是在酚环之间引入—CH2—而交联起来,原位固化成功;3409,3424 cm-1处O—H键的吸收峰几乎未变,这是固化反应前后羟基并未参与反应得以保留所致;苯环骨架吸收峰从1640,1549 cm-1移至1635,1540 cm-1,C—O键的吸收峰从1058 cm-1移至1041 cm-1,这可能是多酚中的酚羟基与甲醛产生了加成及缩合反应,在一定程度上改变了酚环附近取代基的化学环境所致。
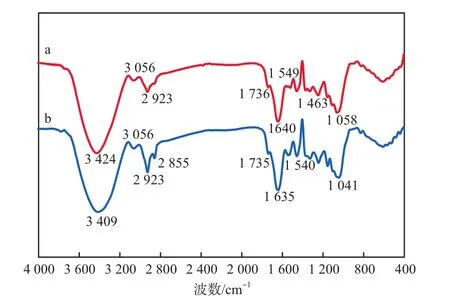
图2 茶渣固化前(a)后(b)的FTIR谱图
2.1.2 热稳定性分析
茶渣固化前后的TG曲线见图3。从室温到200℃的热解失重主要是茶渣中水分及低沸点组分的挥发所致,200~400 ℃是茶渣中纤维素、半纤维素等的热解失重,400 ℃以上是木质素的热解失重。在350 ℃以内茶渣固化前后的热解失重行为接近,其最快纤维素热解失重温度分别为332.2 ℃和332.1℃。但在350 ℃以上固化茶渣表现出更高的热稳定性,在1000 ℃时固化茶渣热解失重83.97%,明显低于茶渣的90.96%。这主要是多酚与甲醛反应形成了类似于木质素结构的交联缩聚产物,且茶渣中可溶性木质素的酚环结构也可与甲醛反应形成交联大分子,这种结构的形成提高了其热稳定性[17],同时再次说明茶渣原位固化成功。
2.1.3 微观形态分析
茶渣固化前后的SEM照片见图4。由图4可见:茶渣粒料截面呈现蜂窝状结构,孔径约在数微米到数十微米间;固化前的茶渣粒料粒径大小不均,存在很多细小碎料、碎片等,截面上附着许多细小碎料,并有少量裂纹、裂缝等,表明茶渣粒料较脆,在外力作用下易脆裂;而固化后的茶渣粒料表面看不到细小碎料,且粒料截面上细小的碎料、碎片以及壁上的裂纹、裂缝也消失不见,截面上似乎涂覆着一些胶质,其中可见一些碎料凸起。这是因为,茶渣中的多酚组分与甲醛反应形成酚醛缩聚物,作为一种单宁基胶黏剂[19],可将碎料相互黏结在一起,同时修补其中的裂纹、裂缝等,对茶渣粒料起到修补增强作用。
2.2 溶液pH对吸附效果的影响
溶液pH可以通过改变吸附剂材料的表面电荷来影响其对Cr(Ⅵ)的吸附效果。在吸附温度303 K、初始Cr(Ⅵ)质量浓度60 mg/L、吸附剂投加量1.0 g/L、吸附时间300 min的条件下,溶液pH对Cr(Ⅵ)吸附效果的影响见图5。
由图5可见:随溶液pH的增大,固化茶渣对Cr(Ⅵ)的吸附量逐渐减小;当pH=2时,固化茶渣对Cr(Ⅵ)吸附量为56.56 mg/g,去除率达94.3%。在较低pH时,固化茶渣表面的羟基等基团会出现较高程度的质子化而带正电荷,与带负电荷的Cr(Ⅵ)形成静电吸附[17]。随pH升高,吸附材料表面的质子化作用降低,且溶液中逐渐增多的OH-会与负电荷的Cr(Ⅵ)产生竞争吸附,导致吸附效果下降。

图4 茶渣固化前(a)后(b)的SEM照片
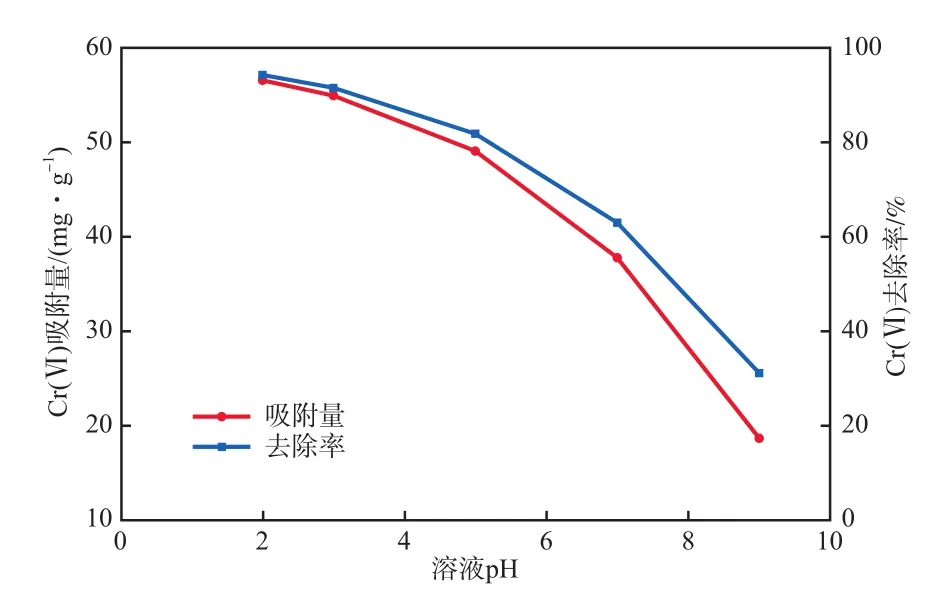
图5 溶液pH对Cr(Ⅵ)吸附效果的影响
2.3 吸附动力学
在吸附温度303 K、吸附剂投加量1.0 g/L、吸附时间300 min、溶液pH 2的条件下,分别采用准一级动力学方程、准二级动力学方程及颗粒内扩散动力学方程(见式(1)~(3))[15]对固化茶渣吸附Cr(Ⅵ)的实验数据进行拟合,结果见表1(ρ0为初始Cr(Ⅵ)质量浓度,mg/L)。由表1可见,准二级动力学方程的拟合结果最优,其相关系数r接近于1,表明颗粒内扩散不是速率控制步骤。

式中:t为吸附时间,min;qt为t时刻的吸附量,mg/g;qe为平衡吸附量,mg/g;k1为准一级速率常数,min-1;k2为准二级速率常数,g/(mg·min);kid为颗粒内扩散速率常数,mg/(g·min1/2);C为常数,mg/g。
2.4 吸附等温式
在初始Cr(Ⅵ)质量浓度60 mg/L、吸附剂投加量1.0 g/L、吸附时间300 min、溶液pH 2的条件下,分别采用Langmuir和Freundlich等温吸附模型(见式(4)和式(5))[15]对固化茶渣吸附Cr(Ⅵ)的实验数据进行拟合,结果见表2。由表2可见:Langmuir和Fredudlich模型拟合得到的r均不低于0.98,表明二者都能较好描述固化茶渣对Cr(Ⅵ)的吸附特性,但相较而言Langmuir模型更为适合;303,318,333 K下利用Langmuir模型求得的饱和吸附量分别为83.26,107.64,129.20 mg/g。。
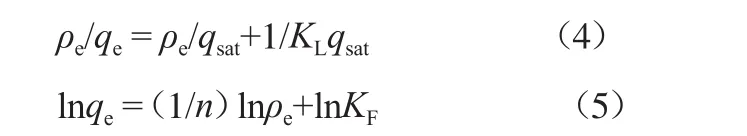
式中:ρe为吸附平衡时的Cr(Ⅵ)质量浓度,mg/L;qsat为饱和吸附量,mg/g;KL为Langmuir吸附常数,L/mg;n和KF为Freundlich吸附常数。
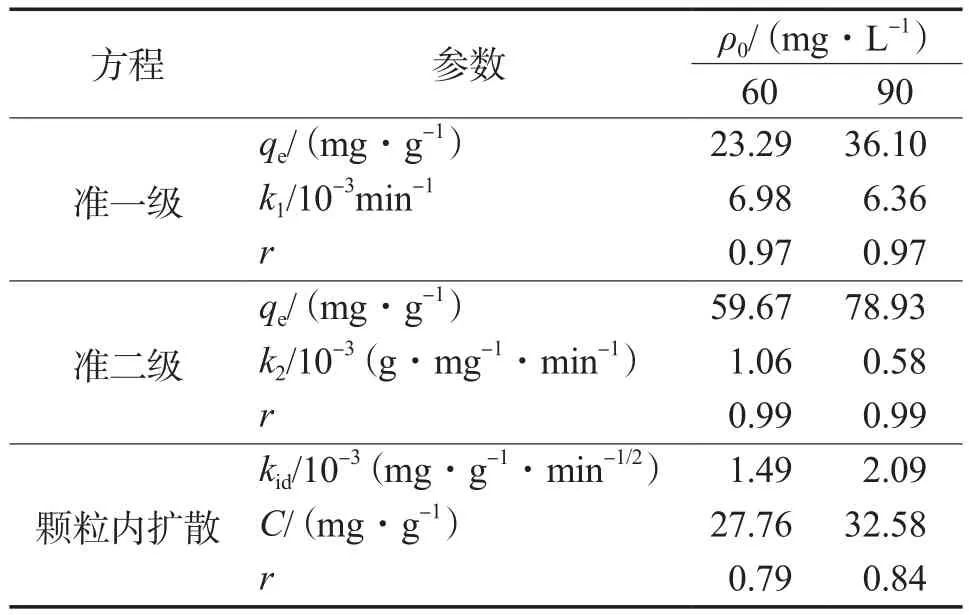
表1 动力学方程的拟合结果

表2 等温吸附模型的拟合结果
2.5 吸附热力学
通过式(6)[5]分析固化茶渣对Cr(Ⅵ)的吸附热力学行为。以ΔG对T作图,通过线性拟合,由直线的斜率和截距可分别得到ΔS和∆H,结果见表3。由表3可见:ΔG为负值,∆H为正值,表明固化茶渣对Cr(Ⅵ)的吸附过程是自发的、吸热过程;ΔS>0,表明在吸附过程中固液界面上分子运动的无序性增加。

式中:∆G为吸附自由能变,J/mol;R为摩尔气体常数,8.314 J/(mol·K);T为吸附温度,K;b为以mol计的KL,L/mol;∆H为吸附焓变,J/mol;ΔS为吸附熵变,J/(mol·K)。
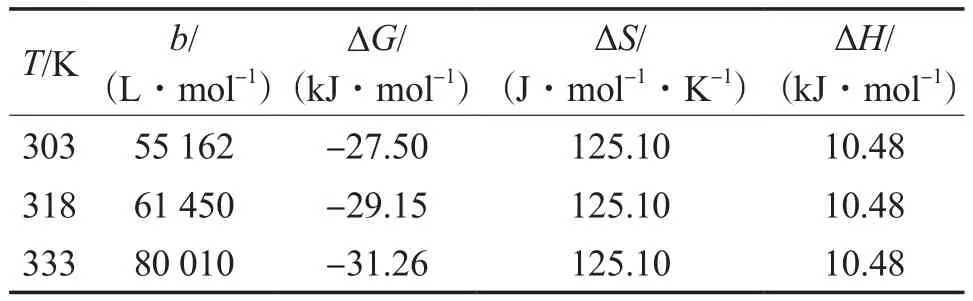
表3 固化茶渣吸附Cr(Ⅵ)的热力学参数
3 结论
a)以甲醛为交联剂,制备了多酚原位固化茶渣。表征结果显示,茶渣多酚的原位固化提高了其热稳定性,同时对茶渣粒料起到了修补增强作用。
b)固化茶渣对Cr(Ⅵ)的吸附量随溶液pH的减小而增大。在吸附温度303 K、初始Cr(Ⅵ)质量浓度60 mg/L、吸附剂投加量1.0 g/L、吸附时间300 min、溶液pH 2的条件下,固化茶渣对Cr(Ⅵ)的吸附量为56.56 mg/g,去除率达94.3%。
c)Langmuir和Fredudlich等温吸附模型均可较好地描述固化茶渣对Cr(Ⅵ)的吸附特性,但相较而言Langmuir模型更为适合,303,318,333 K下的Langmuir饱和吸附量分别为83.26,107.64,129.20 mg/g。准二级动力学方程能较好地描述固化茶渣对Cr(Ⅵ)的吸附动力学过程。热力学分析表明,固化茶渣对Cr(Ⅵ)的吸附是一个自发的、吸热过程。
[1] Gupta V K,Rastogi A,Nayak A. Adsorption studies
on the removal of hexavalent chromium from aqueous solution using a low cost fertilizer industry waste material[J]. J Colloid Interface Sci,2010,342(1):135 -141.
[2] 万晶晶,郭楚玲,涂志红,等. 黄铁矿对水中六价铬的吸附去除[J]. 化工环保,2016,36(5):506 - 510.
[3] Mohan D,Pittman C U,Jr. Activated carbons and low cost adsorbent for remediation of tri-and hexavalent chromium from water[J]. J Hazard Mater,2006,137(2):762 - 811.
[4] Shaalan H F,Sorour M H,Tewfik S R. Simulation and optimization of a membrane system for chromium recovery from tanning wastes[J]. Desalination,2001,141(3):315 - 324.
[5] Qian Ao,Liao Peng,Yuan Songhu,et al. Efficient reduction of Cr(Ⅵ)in ground water by a hybrid electro-Pd process[J]. Water Res,2014,48:326 - 334.
[6] Dakiky M,Khami A ,ManassrA,et al. Selective adsorption of chromium(Ⅵ)in industrial wastewater using low-cost abundantly available adsorbents[J]. Adv Environ Res,2002,6(4):533 - 540.
[7] 刘健,李耀威,王刚,等. 改性废报纸纤维对水中Cr(Ⅵ)的吸附研究[J]. 中国环境科学,2015,35(5):1368 - 1374.
[8] 鲁秀国,段建菊,黄林长,等. 炭化核桃壳对废水中Cr(Ⅵ)的吸附[J]. 化工环保,2016,36(6):611 -616.
[9] Netzahuatl-Muñoz A R,Cristiani-Urbina M C,Cristiani-Urbina E. Chromium biosorption from Cr(Ⅵ)aqueous solutions by Cupressus lusitanica bark:Kinetics,equilibrium and thermodynamic studies[J]. Plos One,2015,10(9):e0137086.
[10] Batiancela M A,Acda M N,Cabangon R J. Particleboard from waste tea leaves and wood particles[J]. J Compos Mater,2014,48(8):911 - 916.
[11] Prabhakaran S K,Vijayaraghavan K,Balasubramanian R. Removal of Cr(Ⅵ)Ions by spent tea and coffee dusts:Reduction to Cr(Ⅲ)and biosorption[J]. Ind Eng Chem Res,2009,48(4):2113 - 2117.
[12] Albadarin A B,Mangwandi C,Walker G M,et al.Influence of solution chemistry on Cr(Ⅵ)reduction and complexation onto date-pits/tea-waste biomaterials[J]. J Environ Manage,2013,114:190 - 201.
[13] Mozumder S I,Khan M R,Islam A. Kinetics and mechanism of Cr(Ⅵ)adsorption onto tea-leaves waste[J]. Asia-Pac J Chem Eng,2008,3(4):452 - 458.
[14] Borah L,Senapati K K,Borgohain C,et al. Preparation of ordered porous carbon from tea by chemical ac-tivation and its use in Cr(Ⅵ)adsorption[J]. J Porous Mater,2012,19(5):767 - 774.
[15] Goswami M,Borah L,Mahanta D,et al. Equilibrium modeling,kinetic and thermodynamic studies on the adsorption of Cr(Ⅵ)using activated carbon derived from matured tea leaves[J]. J Porous Mater,2014,21(6):1025 - 1034.
[16] Chen J P,Yang Lei. Chemical modification of Sargassum sp. for prevention of organic leaching and enhancement of uptake during metal biosorption[J]. Ind Eng Chem Res,2005,44(26):9931 - 9942.
[17] 吴宗华,陈少平,庞燕. 木麻黄树皮的原位固化制备及其对Cr(Ⅵ)的吸附[J]. 应用化学,2010,27(11):1256 - 1259.
[18] 蔡晓红. 茶及茶制品废弃物对甲醛的吸附动力学与环保刨花板开发[D]. 杭州:浙江大学,2010.
[19] Takano Toshiyuki,Murakami Tomomi,Kamitakahara Hiroshi,et al. Mechanism of formaldehyde adsorption of(+)-catechin[J]. J Wood Sci,2008,54(4):329 -331.
[20] Uchiyama Shigehisa,Matsushima Erica,Kitao Nahoko,et al. Effect of natural compounds on reducing formaldehyde emission from plywood[J]. Atmos Environ,2007,41(38):8825 - 8830.
[21] Leong Y W,Abu Bakar M B,Mohd Ishak Z A,et al. Characterization of talc/calcium carbonate filled polypropylene hybrid composites weathered in a natural environment[J]. Polym Degrad Stab,2004,83(3):411 - 422.

