胸腔镜与开胸手术治疗肋骨骨纤维结构不良的临床对照研究*
罗 猛,陈 臣,刘 迪,刘 波,龙 谦,胡 剑,张庆斌,梅 宏
(贵州医科大学附属人民医院胸外科,贵阳 550004)
·经验交流·
胸腔镜与开胸手术治疗肋骨骨纤维结构不良的临床对照研究*
罗 猛,陈 臣,刘 迪,刘 波,龙 谦,胡 剑,张庆斌,梅 宏
(贵州医科大学附属人民医院胸外科,贵阳 550004)
目的比较胸腔镜手术与开胸手术治疗肋骨骨纤维结构不良的疗效,以明确胸腔镜手术的可行性、安全性和有效性。方法回顾性分析该院2000年1月至2015年10月收治的42例肋骨骨纤维结构不良患者的病例资料。根据不同的手术方式分为两组:胸腔镜组16例行胸腔镜肋骨切除术,开胸组26例行开胸肋骨切除术。比较分析两组患者的手术切口总长度、手术时间、术中出血量、术后疼痛时间和程度、术后活动情况、术后胸腔引流时间、术后住院时间、术后并发症及切口满意度。结果胸腔镜组患者的手术切口总长度[(6.2±1.6)vs.(12±2.2)cm,P<0.05]、术后住院时间[(5.4±1.6)vs.(9.3±2.7)d,P<0.05]均明显小于开胸组;胸腔镜组术后第1、2天疼痛视觉模拟评分(VAS)最小值、术后第1~3天及术后第7天VAS最大值均低于开胸组(P<0.05);胸腔镜组术后第1、2天自主下床活动患者百分比及术后切口满意度均高于开胸组(P<0.05);但两组在手术时间、术中出血量、胸腔引流时间和术后并发症总发生率比较,差异均无统计学意义(P>0.05)。结论胸腔镜肋骨骨纤维结构不良切除术安全可行,且与开胸手术相比,具有微创、术后疼痛轻和术后恢复快的优点。
肋骨;骨纤维结构不良;胸腔镜手术;开胸手术
手术切除是治疗原发性肋骨肿瘤的主要手段。近年来,随着腔镜器械的发展,国内外学者逐渐将电视辅助胸腔镜手术(video-assisted thoracic surgery,VATS)用于肋骨病变切除并取得较好疗效。本科室2000年1月至2015年10月收治肋骨骨纤维结构不良42例,其中16例行胸腔镜肋骨骨纤维结构不良切除术。通过回顾性分析42例患者的临床资料及随访结果,比较胸腔镜手术和开胸手术治疗肋骨骨纤维结构不良的疗效,探讨胸腔镜肋骨骨纤维结构不良切除术的安全性及可行性,现报道如下。
1 资料与方法
1.1一般资料 本院胸外科2000年1月至2015年10月共收治肋骨肿瘤患者163例,其中术后病理确诊为肋骨骨纤维结构不良患者44例。纳入标准:(1)无胸部手术史;(2)术前美国麻醉医师协会(ASA)分级Ⅰ~Ⅱ级;(3)行胸腔镜或者开胸肋骨切除术;(4)术后病理诊断确诊为骨纤维结构不良。排除标准:术后因出血等并发症再次手术患者;不满足纳入标准的患者。根据以上条件,最终纳入42例患者资料进行分析,男24例,女18例,其中16例行胸腔镜手术(胸腔镜组),26例行开胸手术(开胸组)。患者临床资料见表1,两组患者在年龄、性别、体质量指数(BMI)、吸烟史、病变长径、症状、并发症等方面比较,差异无统计学意义(P>0.05),具有可比性。随访5个月至15年,无局部复发患者。
1.2方法
1.2.1手术方法 所有患者均采用气管插管全身麻醉,健侧卧位。(1)开胸肋骨切除术:根据胸X线片或胸部CT体表定位画标记线,以病变部位为中心先作5~10 cm皮肤切口,电刀逐层切开皮下及肌层组织,分离显露肋骨,然后酌情根据肋骨病变长度向两端扩大手术切口以充分显露病变部位;于病变部位两端距离病灶3 cm处剪断肋骨,完整切除病变部位送病理检查,腋后线第7肋间置胸腔引流管,逐层缝合手术切口。(2)胸腔镜肋骨切除术:术者站患者腹侧,患侧腋中线第7肋间作2 cm切口作为观察孔,置入胸腔镜。在胸腔镜下可清楚观察第2~10肋骨形态,肋骨病变通常向胸腔内凸起,用注射器针头在距离肋骨病变腹侧端约3 cm处定位,垂直肋骨长轴方向作2~3 cm长皮肤切口作为主操作孔,电凝分离皮下组织达肋骨骨膜,电刀紧贴肋骨向病变方向分离皮下与肋骨间隙作皮下隧道,并紧贴肋骨用电凝切开两侧肋间肌,于肋骨腹侧端距离病变约3 cm处用线锯锯断肋骨。在距病变肋骨下方或上方1个肋间隙肩胛下角线处作1~2 cm切口作为副操作孔。经副操作孔置入卵圆钳或钢丝,将此前离断处的病变肋骨端向下牵拉,充分显露肋骨与皮下组织间隙。经主操作孔用电钩分离胸壁肌层与病变肋骨骨膜,紧贴肋骨离断肋间肌游离病变肋骨,于肋骨背侧端,距离病变3 cm处用线锯再次锯断肋骨,完整切除肋骨病变送病检,肋骨床创面用电凝钩电凝彻底止血。常规于腋中线第7肋间操作孔处置胸腔引流管,逐层缝合手术切口。
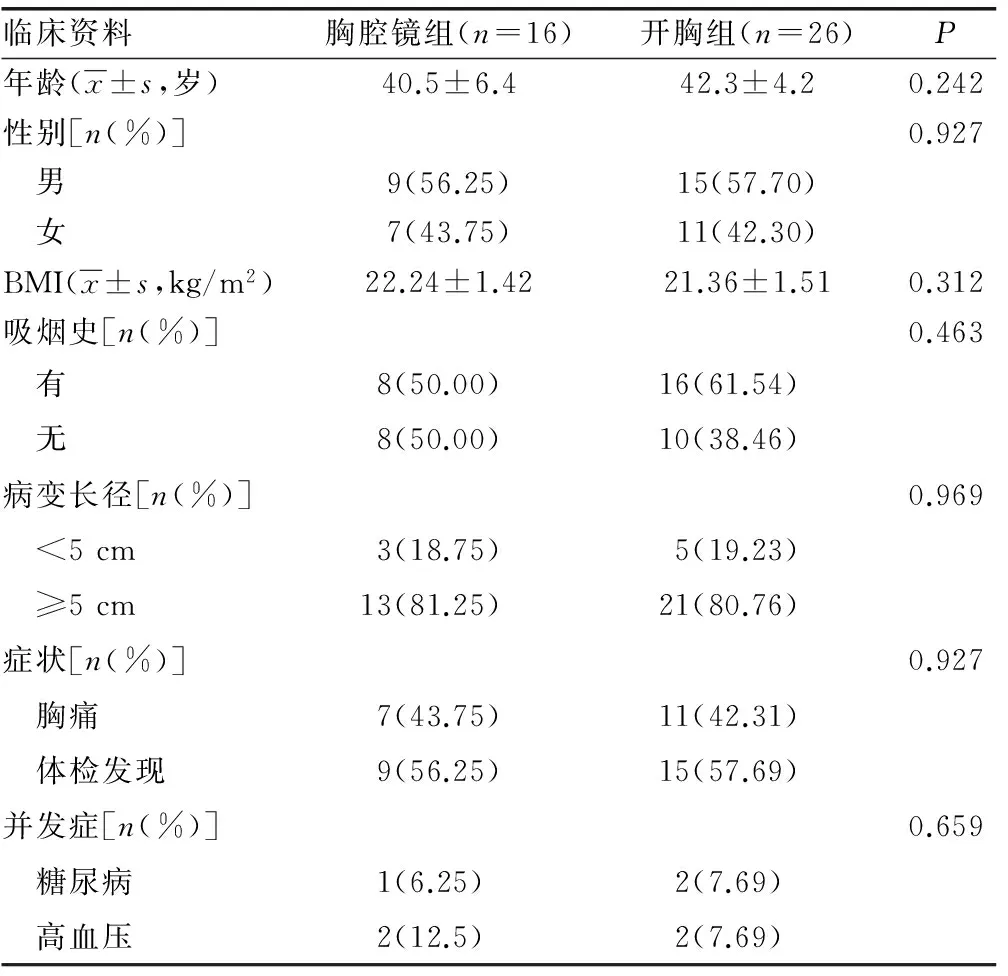
表1 两组患者一般临床资料比较
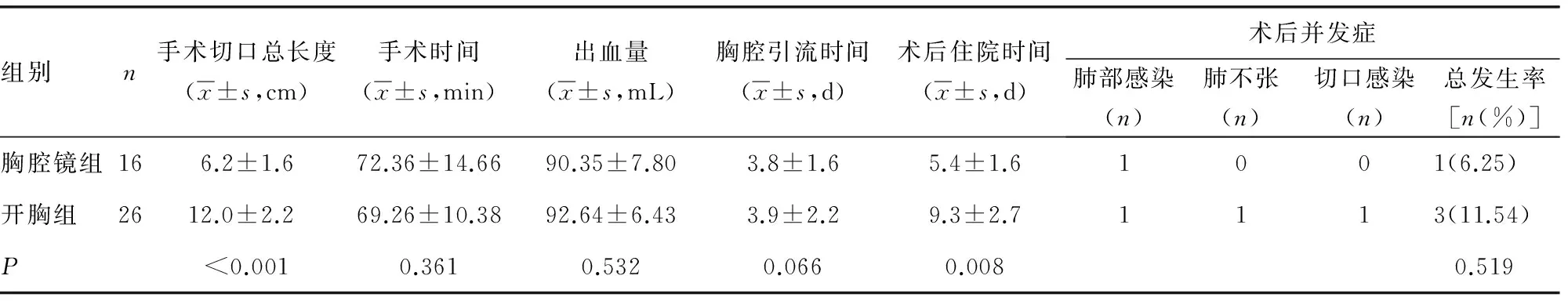
表2 两组手术及术后临床资料比较

表3 两组患者术后疼痛评分比较分)
1.2.2术后处理 所有患者术后入麻醉后恢复室,苏醒拔除气管导管后转至病房。患者术毕经颈内静脉留置导管行静脉自控镇痛(patient controlled intravenous analgesia,PCIA),配方为芬太尼15~25 μg/kg+氟比洛芬酯200 mg,0.9%氯化钠溶液加至100 mL。药物总量为100 mL,基础静脉输注速率为2 mL/h,追加剂量为0.5 mL,锁定时间为15 min。术后48 h停用静脉镇痛泵。术后按胸外科常规处理,鼓励患者早期咳嗽及下床活动。复查胸部X线片提示双侧肺复张良好且胸腔引流管引流量小于或等于200 mL/24 h时拔除引流管。
1.2.3观察指标 观察两组手术切口总长度、手术时间、术中出血量、术后疼痛程度、术后活动度、术后胸腔引流时间、术后住院时间、术后并发症及切口满意度。
1.3评价标准 (1)疼痛观察:采用视觉模拟评分(VAS),赋值0~10分,共分为4级:0分为无痛,1~3分为轻度疼痛,4~6分为中度疼痛,7~10分为重度疼痛;记录患者术后第1~3天及术后第7天疼痛最小值(VASmin)和最大值(VASmax)。(2)术后活动度评估:①不能下床活动,指患者因疼痛或呼吸困难而无法下床活动;②需搀扶下床活动,因各种原因活动时需要人帮助;③自主下床活动,可独立带管活动。(3)将肺部感染、肺不张、心律失常、切口感染4种常见术后并发症纳入统计范畴。
2 结 果
2.1两组手术及术后临床资料比较 两组均无围术期死亡患者。胸腔镜组患者手术切口总长度明显小于开胸组,差异有统计学意义(P<0.05);胸腔镜组患者术后住院时间较开胸组短,差异有统计学意义(P<0.05)。但两组患者手术时间、术中出血量、术后胸腔引流时间及术后并发症总发生率比较,差异均无统计学意义(P>0.05),见表2。
2.2两组术后早期疼痛情况比较 胸腔镜组术后第1、2天VASmin均低于开胸组,差异均有统计学意义(P<0.05),但两组患者术后第3、7天VASmin比较,差异均无统计学意义(P>0.05)。胸腔镜组术后第1~3天及术后第7天VASmax均低于开胸组,差异均有统计学意义(P<0.05),见表3。
2.3两组患者术后活动情况与切口满意度比较 胸腔镜组患者术后第1、2天自主下床活动患者百分比明显高于开胸组,差异均有统计学意义(P<0.05)。胸腔镜组患者切口满意度明显高于开胸组,差异有统计学意义(P<0.05),见表4。
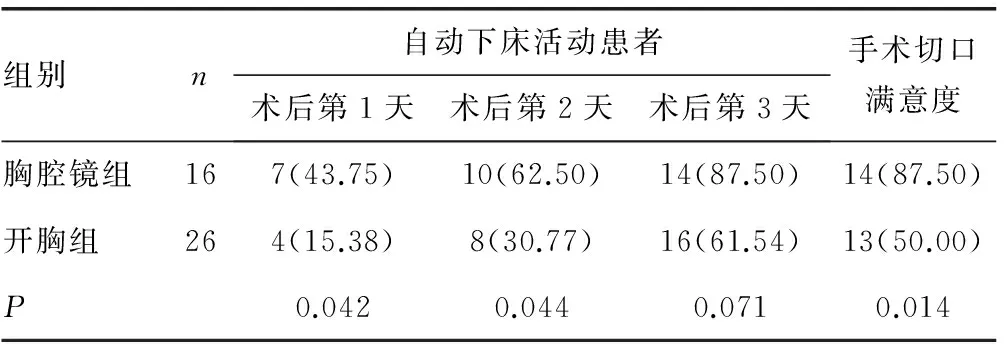
表4 两组患者术后早期活动情况及切口满意度比较[n(%)]
3 讨 论
骨纤维结构不良是一种少见的骨良性病变,可单发或多发于长骨、颅骨或肋骨等部位。约50%的骨纤维结构不良发生于肋骨,且多为单发[1]。骨纤维结构不良恶性转化的发生率为0.4%~4.0%[2]。肋骨的骨纤维结构不良由于具有潜在恶性,并可继续生长压迫肋间神经及肺部,引起胸背部疼痛、呼吸困难等症状[3],一经发现,通常首选手术切除治疗,达到明确诊断与治疗的目的。由于肋骨病变发生部位多变且病变大小不一,肋骨切除手术没有固定的术式。常规开胸肋骨切除手术的手术切口通常比肋骨病变长,由于要切断较多的胸壁肌肉和软组织,导致更多的并发症发生和明显的术后疼痛,降低患者的生活质量。而胸腔镜肋骨骨纤维结构不良切除术只需作1~3个约2 cm长的手术切口,仅切除病变肋骨及其相邻的肋间肌,无需切断其表面的其他胸壁肌肉及皮肤组织,因此术后疼痛明显低于开胸手术。鉴于骨纤维结构不良为良性病变,笔者在用VATS切除肋骨病灶时用电凝钩紧贴肋骨表面分离肋骨,尽可能减少胸壁肌层的损伤。本研究中胸腔镜组患者术后第1、2天的VASmin和VASmax都明显低于开胸组(P<0.05),且胸腔镜组术后第3、7天的VASmax亦低于开胸组(P<0.05)。
胸腔镜手术始于20世纪90年代初,最初主要应用于肺大疱切除术、肺结节楔形切除术及胸膜活检术等简单手术,经过20多年的发展,VATS已经广泛应用于肺癌、食管癌、纵隔肿瘤等胸外科各种疾病的诊断及治疗。与传统开胸手术相比,VATS具有微创及对肩关节功能和呼吸功能影响小等优点[4-5]。近年来,随着腔镜技术的普及和技术的不断提高,VATS第1肋骨切除术已成为治疗胸廓出口综合征的标准术式之一[6]。VATS亦逐渐被用于肋骨病变切除[7]。然而,由于肋骨骨纤维结构不良的发病部位及病变大小不一,肋骨和胸骨的骨性结构限制了胸腔镜的操作空间,可能存在操作距离远,不易游离和离断病变肋骨,进行人工材料重建胸壁难度大等困难。因此,胸腔镜肋骨肿瘤切除术尚处于探索阶段。但有学者通过设计和应用适宜的手术器械,也可以在完全胸腔镜下顺利施行肋骨切除术[8]。
此外,部分肋骨病变经体表不易触及,常规开胸手术不能精准定位。而VATS下可以清楚观察到第2~10肋骨,与传统手术相比能更精确地定位肋骨病变位置[9-10]。笔者通过术前肋骨CT三维重建,明确肋骨病变位置和病变长径与横径最大值;并在VATS观察下,利用注射针头穿刺定位,更有助于选择最佳的操作孔位置。随着经验的不断积累,笔者将三孔VATS肋骨切除术逐渐发展到单孔VATS肋骨切除术,显著减小了手术切口长度和胸壁组织创伤。本研究结果显示,胸腔镜组患者手术切口满意度明显高于开胸组(P<0.05)。由于胸腔镜组患者的术后疼痛较开胸组轻,其术后自主活动恢复明显优于开胸组(P<0.05)。本研究发现,胸腔镜组与开胸组在手术时间、术中出血量、术后胸腔引流时间及术后并发症总发生率比较无明显差异(P>0.05)。
综上所述,VATS肋骨骨纤维结构不良切除术能达到开胸切除术相同的切除效果,且能够保证手术安全性,在降低患者术后疼痛和提高自主活动恢复方面优于开胸手术。与常规开胸手术相比较,VATS肋骨骨纤维结构不良切除术具有以下优势:(1)手术切口总长度明显减小;(2)术中更能精确定位肋骨病变位置;(3)术后疼痛降低;(4)术后住院时间缩短;(5)术后自主活动度恢复快,有利于术后康复。因此,VATS肋骨骨纤维结构不良切除术安全可行,且与开胸手术相比,具有微创、术后疼痛轻和术后恢复快的优点。
[1]O′connor B,Collins FJ.The management of chest wall resection in a patient with polyostotic fibrous dysplasia and respiratory failure[J].J Cardiothorac Vasc Anesth,2009,23(4):518-521.
[2]Dicaprio MR,Dysplasia EF.Pathophysiology,evaluation,and treatment[J].J Bone Joint Surg Am,2005,87(8):1848-1864.
[3]Dixon JL,Smythe WR,Rascoe PA,et al.Surgical resection of giant fibrous dysplasia for near respiratory collapse[J].Ann Thorac Surg,2013,95(6):e135-137.
[4]Demmy TL,Yendamuri S,Hennon MW,et al.Thoracoscopic maneuvers for chest wall resection and Reconstruction[J].J Thorac Cardiovasc Surg,2012,144(3):S52-57.
[5]Li WW,Lee RL,Lee TW,et al.The impact of thoracic surgical access on early shoulder function: video-assisted thoracic surgery versus posterolateral thoracotomy[J].Eur J Cardiothorac Surg,2003,23(3):390-396.
[6]Kara HV,Balderson SS,Tong BC,et al.Video assisted transaxillary first rib resection in treatment of thoracic outlet syndrome (TOS)[J].Ann Cardiothorac Surg,2016,5(1):67-69.
[7]Rocco G,Fazioli F,Martucci N,et al.Video-assisted thoracic surgery rib resection and Reconstruction with Titanium plate[J].Ann Thorac Surg,2011,92(2):744-745.
[8]Nakagiri T,Akashi A,Shigemura N.Thoracoscopic rib resection using a Gigli saw[J].Ann Thorac Surg,2005,80(2):755-756.
[9]Mummaneni PV,Sasso RC.Minimally invasive,endoscopic,internal thoracoplasty for the treatment of scoliotic rib hump deformity: technical note[J].Neurosurgery,2005,56(2 Suppl):E444.
[10]Mcdonald JM,Freeman RK.Thoracoscopic localization of nonpalpable rib tumors for excisional biopsy[J].Ann Thorac Surg,2000,70(1):318-319.
10.3969/j.issn.1671-8348.2017.35.031
贵州省卫生厅科学技术基金资助项目(gzwkj2013-1-149)。
罗猛(1976-),副主任医师,博士,主要从事肺癌的基础与临床研究。
R738
B
1671-8348(2017)35-5000-03
2017-07-17
2017-09-19)

