华蟾素胶囊配合同步放化疗治疗局部晚期食管癌疗效与安全性观察
河南省新乡市第一人民医院肿瘤科 (河南 新乡 453099)
常 伟
华蟾素胶囊配合同步放化疗治疗局部晚期食管癌疗效与安全性观察
河南省新乡市第一人民医院肿瘤科 (河南 新乡 453099)
常 伟
目的观察华蟾素胶囊配合同步放化疗治疗局部晚期食管癌的疗效与安全性。方法将2015年1月-2016年12月入院的84例局部晚期食管癌患者采用随机数表法分为研究组和对照组,每组42例。2组均应用放化疗治疗,研究组加用华蟾素胶囊。对比2组临床疗效及放化疗毒副反应发生情况,评估2组治疗前后免疫功能(T淋巴细胞亚群)的差异性。结果①研究组治疗总有效率高于对照组(P<0.05),放化疗毒副反应发生率则低于对照组(P<0.05);②治疗6w后,2组CD3+、CD4+、CD4+/CD8+水平均较治疗前上升(P<0.05),且研究组增幅较对照组大(P<0.05);CD8+水平治疗前后对比无统计学意义(P>0.05)。结论联合使用华蟾素胶囊能有效降低放化疗毒副反应,且能积极改善患者免疫功能,促使局部晚期食管癌临床疗效提高。
华蟾素胶囊;局部晚期;食管癌;疗效;安全性
随着生活方式转变,全球食管癌发病率均日趋上升,而我国是食管癌高发地区之一[1]。由于此病早期无明显症状,临床确诊患者多已为进展期,死亡率较高,需积极进行治疗以提高患者生存率。放化疗是目前进展期食管癌主要治疗手段之一,能有效延长患者生存期,但其在杀死肿瘤细胞时对机体正常细胞也有较大灭杀作用[2],因此寻求有效且安全的治疗手段成为食管癌治疗相关研究重点。基于此,本研究选取我院收治的局部晚期食管癌患者84例进行研究,以探讨华蟾素胶囊配合同步放化疗治疗局部晚期食管癌疗效与安全性,现报告如下。
1 临床资料
1.1 一般资料选择2015年1月~2016年12月间收治的84例局部晚期食管癌患者为研究对象。纳入标准:经病理检查确诊的局部晚期食管癌患者;年龄18~75岁者;预期生存期>1年;初治者;受试者知情同意。排除标准:严重心肝肾病、恶性肿瘤者;其他原发性消化道疾病者;对本组药物明确禁忌症者。采用随机数表法将84例患者分为研究组和对照组,每组42例。2组各一般资料比较,差异均无统计学意义(P>0.05),如表1所示。
表1 2组患者一般资料[n(%),(±s)]

表1 2组患者一般资料[n(%),(±s)]
组别 n 性别 肿瘤部位 年龄(岁)男性 女性 胸上段及颈 胸中度 胸下段研究组 4 2 3 0(7 1.4 3) 1 2(2 8.5 7) 1 4(3 3.3 3) 1 6(3 8.1 0) 1 2(2 8.5 7) 6 2.6 2±5.0 0对照组 4 2 2 9(6 9.0 5) 1 3(3 0.9 5) 9(2 1.4 3) 1 8(4 2.8 6) 1 5(3 5.7 1) 6 2.8 3±5.7 7
1.2 治疗方法2组患者均同步行放化疗:放疗:使用Novalis Tx型直线加速器(瓦里安医疗系统公司生产)临床靶区纵轴外放3cm,横轴外放1cm,2.00Gy/次,5次/w,持续治疗6w。化疗:d1~5,5-氟尿嘧啶(生产企业:德州德药制药有限公司,规格:0.25g,批准文号:国药准字H20051619)800mg/m2,持续iv.drop;d1,顺铂(生产企业:齐鲁制药有限公司,规格:20mg,批准文号:国药准字H37021357)75mg/m2,iv.drop,持续治疗6w。研究组加用华蟾素胶囊(生产企业:陕西东泰制药有限公司,规格:0.25g/粒,批准文号:国药准字Z20050846)2粒/次,tid,p.o.,持续治疗6w。
1.3 评估方法治疗前后均使用Cube8型流式细胞仪(麦迪生物公司生产)检测患者外周静脉血中CD3+、CD4+、CD8+水平。
1.4 临床疗效评估标准根据实体瘤评价标准[3]将疗效分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)4度,总有效率=(CR+PR)/总例数×100%。
1.5 观察指标对比2组临床疗效及放化疗毒副反应发生情况,评估2组治疗前后免疫功能(T淋巴细胞亚群变化水平)的差异性。
1.6 数据分析采用SPSS19.0软件对原始数据进行统计分析,计量资料用(±s)表示,用t检验;计数资料用百分比表示,采用χ2检验,P<0.05则认为差异有统计学意义。
2 结 果
2.1 2组临床疗效对比治疗6w后,研究组治疗总有效率高于对照组(P<0.05),如表2所示。

表2 2组临床疗效对比[n(%)]
2.2 2组治疗前后免疫功能对比治疗6w后,2组CD3+、CD4+、CD4+/CD8+水平均较治疗前上升(P<0.05),且研究组增幅较对照组大(P<0.05);2组CD8+水平治疗前后对比均无统计学意义(P>0.05),如表3所示。
表3 2组治疗前后免疫功能水平对比(±s)
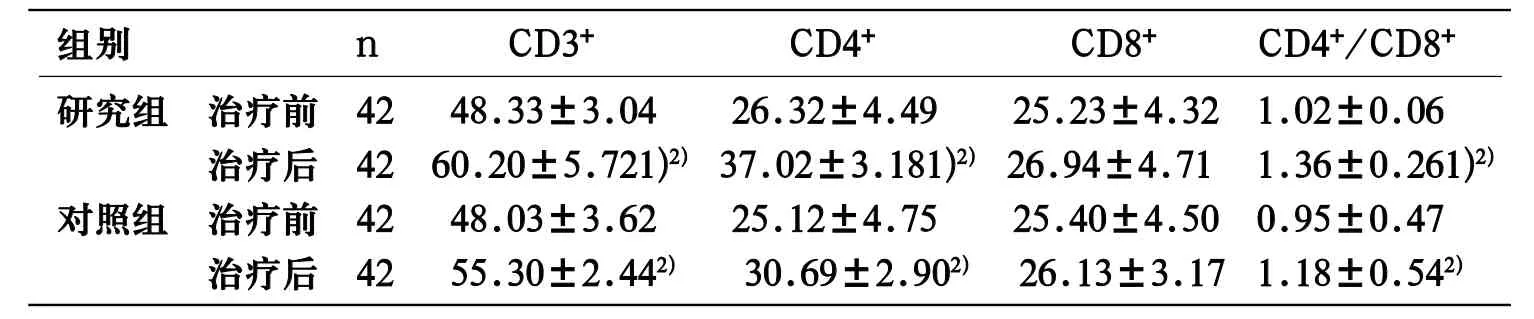
表3 2组治疗前后免疫功能水平对比(±s)
注:1)与同期对照组对比,P<0.05;2)与同组治疗前对比,P<0.05
组别 n C D 3+C D 4+C D 8+C D 4+/C D 8+研究组 治疗前 4 2 4 8.3 3±3.0 4 2 6.3 2±4.4 9 2 5.2 3±4.3 2 1.0 2±0.0 6治疗后 4 2 6 0.2 0±5.7 2 1)3 7.0 2±3.1 8 1)2 6.9 4±4.7 1 1.3 6±0.2 6 1)2)2)2)对照组 治疗前 4 2 4 8.0 3±3.6 2 2 5.1 2±4.7 5 2 5.4 0±4.5 0 0.9 5±0.4 7治疗后 4 2 5 5.3 0±2.4 4 2 6.1 3±3.1 7 1.1 8±0.5 4 2)3 0.6 9±2.9 0 2)2)
2.3 2组放化疗毒副反应发生情况对比治疗6w后,研究组白细胞减少、血小板减少、恶心及食管炎发生率均低于对照组(P<0.05),如表4所示。

表4 2组放化疗毒副反应发生情况对比[n(%)]
3 讨 论
肿瘤根治术联合术后放化疗是现今临床治疗癌症较常用方案,但食管癌由于早期诊断率低,故多数患者确诊时已错失手术时机[3]。放化疗是能延长患者生存期的有效非手术疗法,可通过缩小实体瘤体积和抑制肿瘤细胞转移进程提高患者生存率,但其毒副反应对患者生存质量影响较大,严重者甚至会干扰治疗进程。相关文献指出,中药制剂华蟾素对胃癌、结肠癌等恶性肿瘤均有良好疗效,且能在一定程度上减轻癌痛提高治疗舒适度,为癌症寻求最优治疗方案提供更多选择[4]。
本研究发现,联用华蟾素的研究组治疗有效率高于对照组,这表明华蟾素胶囊对晚期局部食管癌患者疗效良好。华蟾素胶囊主要成分为从蟾蜍皮中提取的华蟾素。蟾皮的主要功效是活血散瘀、拔毒消胀,正对肿瘤癥瘕之症,既能配合放化疗缩小肿瘤体积,又能在治疗后减小毒副作用。现代药理学显示,华蟾素能通过干扰癌细胞核酸代谢来控制肿瘤发展,抑制肿瘤细胞分裂能力并促使其凋亡[6],联合放化疗方案对提高患者近期疗效有利。
研究发现,降低治疗药物毒副作用和提高患者自身免疫力是解决患者对同步放化疗治疗耐受性差的两种途径[5]。本研究结果表明,研究组患者免疫功能改善效果明显优于对照组,猜测可能与华蟾素能调控免疫细胞水平,从而提高对放化疗治疗的耐受性,间接改善临床治疗效果相关。另外,华蟾素可起清热解毒之效,缓和药物毒性,减少因放化疗耗损的机体元气。以上多种效应综合消减放化疗过程中患者出现的副反应,进而提高治疗安全性。本研究也就2组患者放化疗毒副反应发生情况展开分析,发现放化疗配合华蟾素胶囊能降低治疗后白细胞、血小板减少等毒副反应发生率。以上结论与戚诚[6]等学者观点相一致。
本研究限制于样本量和观察时间,未能评估受试者使用华蟾素胶囊后的长期疗效和远期预后,需增加样本量、延长观察时间,以提升结论的科学性和严谨性。
综上所述,华蟾素胶囊能提高临床晚期局部食管癌疗效,也对降低辅助治疗毒副作用、增强免疫功能有积极意义,以综合改善患者治疗耐受性。
[1]舒心,李广欣,朱曦龄,等.自体CIK细胞联合同步放化疗治疗局部晚期食管癌的临床研究[J].现代肿瘤医学,2015,23(10):1376-1380.
[2] 赵丹,王钖,王兰荣,等.周方案紫杉醇联合复方苦参注射液同步放化疗治疗局部晚期老年食管癌临床观察[J].辽宁中医杂志,2017,44(1):89-90.
[3]范瑞华,张铁成,姚榕,等.小剂量TP方案同步放化疗治疗老年人局部晚期食管癌效果观察[J].肿瘤研究与临床,2015,27(10):683-686.
[4] 徐咏梅,刘声.华蟾素胶囊联合化疗对中晚期胃癌的疗效观察[J].世界中医药,2016,11(7):1212-1214.
[5] 杨新波.华蟾素胶囊治疗癌性疼痛的临床疗效观察[J].中国医药导刊,2014,16(3):478-479.
[6]戚诚,赵晓东,刘博,等.华蟾素胶囊联合同步放化疗治疗局部晚期食管癌的疗效分析[J].中国肿瘤临床与康复,2017,24(5):525-528.
Curative Effect and Safety Observation of Huachansu Capsule Combined with Concurrent Chemoradiotherapy in Treatment of Local Advance Esophageal Carcinoma
CHANG Wei. The First People's Hospital of Xinxiang, Xinxiang 453000, Henan Province, China
ObjectiveTo investigate the curative effect and safety of Huachansu capsule combined with concurrent chemoradiotherapy in treatment of local advance esophageal carcinoma.Methods84 cases of local advance esophageal carcinoma in our hospital from January 2015 to December 2016 were selected and divided into observation group and control group, 42 cases in each group. Patients were all given concurrent chemoradiotherapy, and observation group plus Huachansu capsule treatment. Clinic effect, toxicity occurrence condition of chemoradiotherapy of the two groups were compared. Difference of immunological function (T-lymphocyte subsets) of the two groups before and after treatment was evaluated.Results①Total efficiency of observation group was higher than control group (P<0.05),toxic and side effect rate of chemoradiotherapy was lower than control group (P<0.05). ②6w after treatment, CD3+,CD4+, CD4+/CD8+level of the two groups were all increased (P<0.05), growing rate of observation group was larger than control group (P<0.05), the difference of CD8+level before and after treatment had no statistic significance(P>0.05).ConclusionHuachansu capsule combined with concurrent chemoradiotherapy can lower toxicity reaction of chemoradiotherapy, improve immunological function, and promote curative effect of local advance esophageal carcinoma.
Huachansu Capsule; Local Advanced; Esophageal Carcinoma; Curative Effect; Safety
R735.1
A
10.3969/j.issn.1009-3257.2017.06.016
常 伟,女,主治医师,硕士研究生,主要研究方向:食管癌的综合治疗
常 伟
2017-08-13

