XELOX方案一线治疗晚期胃癌的临床效果观察
卞伟钢, 宋 曙, 周小宁, 陈海婷
(江苏省盐城市第一人民医院 肿瘤科, 江苏 盐城, 224002)
XELOX方案一线治疗晚期胃癌的临床效果观察
卞伟钢, 宋 曙, 周小宁, 陈海婷
(江苏省盐城市第一人民医院 肿瘤科, 江苏 盐城, 224002)
XELOX方案一线; 晚期胃癌; 临床效果
胃癌是因胃黏膜上皮组织出现病变导致的,属于恶性肿瘤的一种,是消化道恶性肿瘤的首位并发疾病。因为该病大多数症状无明显或轻微症状,所以大部分患者出现临床较明显症状时,病变期大多数已经到了晚期,错过了最佳的手术治疗时机,只能通过放化疗等综合性手段进行诊治。近几年奥沙利铂与氟尿嘧啶衍生物卡培他滨联合使用XELOX方案在针对消化道恶性肿瘤的放化疗方面得到了较为广泛的运用。现对2010年10月-2013年10月本院收治的晚期胃癌患者给予XELOX方案一线治疗,现报告如下。
1 资料与方法
1.1 一般资料
选取2010年10月—2013年10月间本院收治的晚期胃癌患者48例,其中男30例,女18例,年龄30~74岁,中位年龄60岁。ECOG体能状态评分: PS 0~1分32例, 2分16例。所有患者均经病理组织学验证为胃腺癌患者且ECOG评分≤2; 经影像学检查均可测量病灶; 接受放化疗; 无心脏,肝功能障碍且心电图等常规检查无异常; 均无放化疗病史记录。排除中枢神经流不可控转移患者,肠梗阻无逆转患者以及妊娠或哺乳期妇女等。本研究患者均对此次研究知晓并同意签署知情同意书。
1.2 方 法
本次研究48例患者均采取XELOX3周方案,做法如下。第1天,奥沙利铂以130 mg/m2的剂量连续滴注3 h, 卡培他滨每日2次,每次口服1 000 mg/m2, 连续服用2周,休息以后, 21 d为服用1个周期。
1.3 评价标准
化疗前和化疗2个周期以后,通过CT扫描或MRI增强扫描检查来评价治疗效果,依据实体瘤的治疗效果评价标准(RECIST)来进行,治疗效果分成4个阶段: 完全缓解(CR)、部分缓解(PR)、稳定(SD)和疾病进展(PD)。每例患者至少化疗2个周期,到了疾病进展期后需要换用其他不同的治疗方案进行相关的治疗。通过CR与PR之和来计算有效率(RR),通过CR和PR以及SD 3者之和来计算疾病控制率(DCR)。不良反应情况需要按照WHO所制定的抗癌药物急性和亚急性不良反应评价标准来判定,等级分为0~Ⅳ度。
2 结 果
本研究结果显示,通过2~6周期的XELOX方案化疗, 4周期的中位化疗,患者均可评价疗效。全组48例患者, CR 2例, PR 20例, SD 14例, PD 12例,总有效率为45.8%, 疾病控制率为75%。该病发生的不良反应主要包括消化道症状、骨髓抑制、外周末梢神经毒性以及手足综合征,其中以Ⅰ~Ⅱ级为主。Ⅰ、Ⅱ级中性粒细胞、血小板减少及贫血发生率分别为33.3%、8.4%和25%, Ⅰ、Ⅱ级外周末梢神经毒性发生率为41.7%。Ⅲ~Ⅳ级不良反应主要包括中性粒细胞减少5例和外周末梢神经毒性6例。见表1。
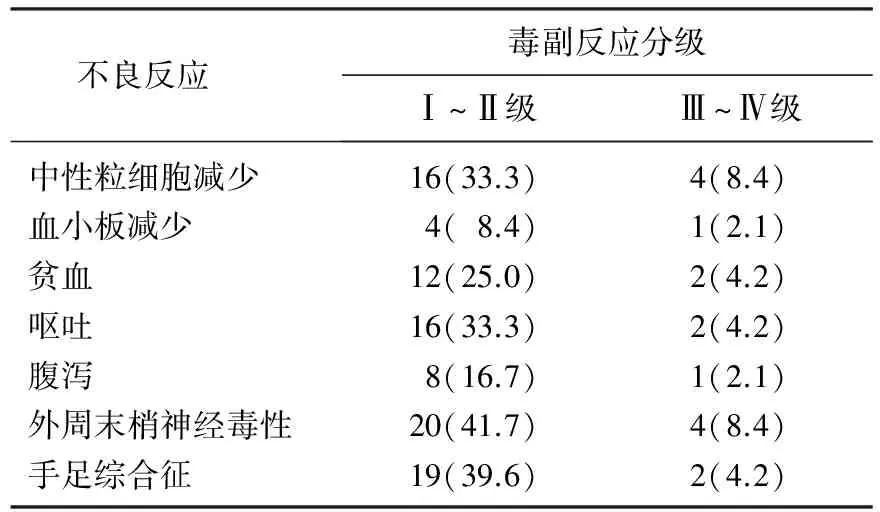
表1 XELOX方案治疗的不良反应[n(%)]
3 讨 论
在大部分西方国家,虽然胃癌的发病率在逐渐下降,但是胃癌仍是导致全世界肿瘤相关死亡率的第2大常见原因[1]。在许多亚洲国家,包括中国、日本、韩国,胃癌仍然保持非常高的发生率和死亡率。尽管胃癌早期诊断手段已取得了进步,但许多患者发现胃癌时已处于不能切除、局部进展或者有转移病灶阶段,预后相对较差。许多晚期胃癌患者即使接受化疗,也仅仅获得6~12个月的中位生存时间[2-5]。
现阶段,对于胃癌晚期患者临床上最为常用的化疗方法为以5-FU和DDP为基础的联合运用方案[6]。然而,除了会导致严重的不良反应外,所有这些方案的管理是不方便的,某些给药方式可能会增加并发症,如静脉血栓形成,偶尔还会发生败血症。在疗效相当的情况下,相比静脉化疗,肿瘤患者一般更倾向于口服化疗药物[7-8]。
卡培他滨作为新型口服氟尿嘧啶氨甲酸酯类抗肿瘤药物之一,服用后药物机体利用其特有的三步酶促反应在肿瘤病变细胞内将其转换为5-氟尿嘧啶(5-Fu)来发挥高度选择性抗癌作用。卡培他滨已经在许多肿瘤中显示出高度的有效性,如乳腺癌、结直肠癌、胃癌。晚期初治的胃癌患者使用单药卡培他滨缓解率可达28.2%[2]。而且,卡培他滨和其他药物联用,如顺铂、奥沙利铂、表柔比星和多西他赛,作为晚期胃癌患者的一线化疗方案,缓解率可达40%~68%[9-11]。奥沙利铂是第3代铂类化疗药,以DNA为靶向作用部位,和卡铂、顺铂作用机制有些不同,该部位不存在交叉耐药,并且能将TP酶活性进行上调,和氟尿嘧啶联合使用能够发挥协同化疗的作用。
多项临床试验结果显示, XELOX方案可用于晚期胃癌的一线治疗。在一项二期的临床研究中,共有74例晚期胃癌患者接受XELOX方案化疗,总缓解率为62.2%, 3例完全缓解, 43例部分缓解,中位进展时间为5.9个月,中位生存时间为10.8个月。最常见的血液学不良反应为1级或2级贫血, 4例患者发生3级中性粒细胞减少症, 1例发生4级中性粒细胞减少症。没有患者发生4级血小板减少症及白细胞减少症。最常见的非血液学毒性是恶心、呕吐、神经病变和腹泻,一般来说反应比较轻[12]。本研究中纳入符合标准的48例晚期胃癌患者,其中CR 2例, PR 20例, SD 14例, PD 12例,总有效率为45.8%, 疾病控制率为75%。该病发生的不良反应主要包括消化道症状、骨髓抑制、外周末梢神经毒性以及手足综合征等,大多数表现为Ⅰ~Ⅱ级。总之,通过对晚期胃癌患者进行XELOX方案一线治疗可获得较高的缓解率,和既往使用的化疗方案相比,这一方案不良反应较轻,克服了耐受性差和不方便的缺点。
[1] Jemal A, Siegel R, Ward E, et al. Cancer statistics[J]. CA Cancer J Clin, 2007, 57: 43-66.
[2] Hong Y S, Song S Y, Cho J Y, et al. A phase Ⅱtrial of capecitabine in previously untreated patients with advanced and/or metastatic gastric cancer[J]. Ann Oncol, 2004, 15: 1344-1347.
[3] Park Y H, Ryoo B Y, Choi S J, et al. A phase Ⅱstudy of capecitabine and docetaxel combination chemotherapy in patients with advanced gastric cancer[J]. Br J Cancer, 2004, 90: 1329-1333.
[4] Thuss-Patience P C, Kretzschmar A, Repp M, et al. Docetaxel and continuous-infusion fluorouracil vs epirubicin, cisplatin and fluorouracil for advanced gastric adenocarcinoma: a randomized phase Ⅱstudy[J]. J Clin Oncol, 2005, 23: 494-501.
[5] Chang H M, Jung K H, Kim TY, et al. A phase Ⅲ randomized trial of 5-fluorouracil, doxorubicin, and mitomycin C versus 5-fluorouracil and mitomycin C versus 5-fluorouracil alone in curatively resected gastric cancer[J]. Ann Oncol, 2002, 13: 1779-1785.
[6] Vanhoefer U, Rougier P, Wilke H, et al. Final results of a randomized phase III trial of sequential high-dose methotrexate, fluorouracil, and doxorubicin versus etoposide, leucovorin, and fluorouracil versus infusional fluorouracil and cisplatin in advanced gastric cancer: a trial of the European Organization for Research and Treatment of Cancer Gastrointestinal Tract Cancer Cooperative Group[J]. J Clin Oncol, 2000, 18: 2648-2657.
[7] Borner M M, Schoffski P, de Wit R, et al. Patient preference and pharmacokinetics of oral modulated UFT versus intravenous fluorouracil and leucovorin: a randomised crossover trial in advanced colorectal cancer[J]. Eur J Cancer, 2002, 38: 349-358.
[8] Hoff P M, Ansari R, Batist G, et al. Comparison of oral capecitabine versus intravenous fluorouracil plus leucovorin as first-line treatment in 605 patients with metastatic colorectal cancer: results of a randomized phase Ⅲ study[J]. J Clin Oncol, 2001, 19: 2282-2292.
[9] Kim T W, Kang Y K, Ahn J H, et al. Phase Ⅱ study of capecitabine plus cisplatin as first-line chemotherapy in advanced gastric cancer[J]. Ann Oncol, 2002, 13: 1893-1898.
[10] Kang Y K, Kim T W, Chang H M, et al. A phase I/II trial of docetaxel, capecitabine, and cisplatin as a first line chemotherapy for advanced gastric cancer [J]. Proc Am Soc Clin Oncol, 2004, 22: s250-7.
[11] Park Y H, Kim B S, Ryoo B Y, et al. A phase Ⅱstudy of capecitabine plus 3-weekly oxaliplatin as first-line therapy for patients with advanced gastric cancer[J]. Br J Cancer, 2006, 94: 959-963.
[12] Yang T, Shen X, Tang X, et al. Phase Ⅱtrial of oxaliplatin plus oral capecitabine as first-line chemotherapy for patients with advanced gastric cancer[J]. Tumori, 2011, 97: 466-472.
2017-07-09
R 735.2
A
1672-2353(2017)21-179-02
10.7619/jcmp.201721072

