不同剂量细辛配伍的小青龙汤对哮喘大鼠肝肾功能的影响
柴茂山,李 鹏,赵 晔,郭智江,邓 亮
(1.山西大同大学医学院,山西大同037009;2.山西省沁水县人民医院,山西晋城048200)
不同剂量细辛配伍的小青龙汤对哮喘大鼠肝肾功能的影响
柴茂山1,李 鹏2,赵 晔1,郭智江1,邓 亮1
(1.山西大同大学医学院,山西大同037009;2.山西省沁水县人民医院,山西晋城048200)
目的成功制备哮喘大鼠模型,用不同剂量细辛配伍的小青龙汤予以治疗,探讨其对哮喘大鼠肝肾功能的影响,从而揭示不同剂量细辛配伍的小青龙汤细辛和整体方剂的安全性,为临床安全使用细辛和小青龙汤提供一定的科学根据。方法84只健康雄性SD大鼠常规饲养1周后,将其随机分为哮喘模型组、正常对照组、0 g、3 g、9 g、15 g、21 g细辛配伍的小青龙汤组,每组12只,造模和治疗同步进行。治疗结束前一天禁食,麻醉后行腹主动脉采血,用全自动生化分析仪检测各组大鼠血清ALT、AST、BUN、SCR的浓度。结果各个不同剂量细辛配伍的小青龙汤治疗组大鼠肝肾功能(ALT、AST、BUN、SCR))与正常组和模型组大鼠比较,均无显著性差异(P>0.05)。结论细辛用量从0 g到21 g,其它药物药量不变,对哮喘大鼠的肝肾功能(ALT、AST、BUN、SCR)无明显影响。
细辛;小青龙汤;哮喘;肝肾功能
小青龙汤出自张仲景的《伤寒杂病论》,是治疗外寒内饮咳喘的经典名方,由麻黄、桂枝、干姜、芍药、五味子、半夏、细辛、炙甘草组成。其治疗冷哮的疗效与细辛的用量有一定关系,本人在30多年的临床上发现细辛用9g时对冷哮的疗效较3g有明显提高。许多医家在临床上也有类似的临床经验,如周德生等[1]医家建议在治疗外感伤寒时,细辛用3~5 g;当治疗风寒束肺咳喘时候,细辛应与干姜、五味子同用,构成温肺化饮的常用组合,用量应达到8~10 g;当治疗脉络痹阻之各种痛症时,细辛用量应达到15 g及其以上。但是细辛历代有不过钱之说,这样就限制了细辛治疗效果的发挥,我国2015版药典也明确规定细辛在煎剂中的用量为1~3 g,致使细辛在临床上的使用受到了很大限制。基于以上观点,制备哮喘大鼠动物模型,通过检测哮喘大鼠肝肾功能,来探讨不同剂量细辛配伍的小青龙汤对哮喘大鼠肝肾功能的影响。从而揭示不同剂量细辛配伍的小青龙汤中细辛和整体方剂的安全性,为临床安全使用细辛和小青龙汤提供一定的科学根据。
1 材料
1.1 药品与试剂
1.1.1 药品
小青龙汤中的药物麻黄、芍药、细辛、干姜、炙甘草、桂枝、半夏、五味子由同仁堂药店提供。
1.1.2 主要试剂
卵白蛋白(OVA)干粉(美国Sigma公司,批号A5378),氢氧化铝粉末(天津市光复精细化工研究所,批号CNAB 035-Q),0.9%氯化钠注射液(湖北天药药业股分有限公司,批号20140321),戊巴比妥钠(美国sigma公司,批号P3761)。
1.2 主要仪器
大鼠雾化箱(60cm×50cm×50cm),超声雾化器(江苏鱼跃医疗设备股份有限公司,402A型),BS 224S万分之一天平(德国赛多利斯),HC-2062高速离心机(安徽中科中佳科学仪器有限公司),-80℃超低温冰箱(日本SANYO公司,MD⁃FU-281型),全自动生化分析仪(日本东芝公司)。
2 实验方法
2.1 动物分组
将SPF级健康雄性SD大鼠(7~8周龄,180±30 g)84只常规饲养1周,称重后,随机分为7组,分别为正常组、模型组、0 g细辛配伍的小青龙汤组(复方0 g组)、3 g细辛配伍的小青龙汤组(复方3 g组)、9 g细辛配伍的小青龙汤组(复方9 g组)、15 g细辛配伍的小青龙汤组(复方15 g组)、21 g细辛配伍的小青龙汤组(复方21 g组)。
2.2 药物制备
按《伤寒杂病论》原书的剂量换算为现代剂量:麻黄9 g、芍药9 g、细辛3 g、干姜9 g、炙甘草9 g、桂枝9 g、半夏9 g、五味子9 g,此剂量称为复方3 g组;细辛药量变为0、9、15、21 g,则分别为复方0、9、15、21 g组。
中药给药剂量按人与大鼠体表面积换算法的有关公式进行换算。计算方法:成人每日服用量为X克,大鼠每日所需药量为Xg×0.018/0.2 kg=0.09Xg∕kg,0.018是依据《中药药理实验方法学》中人与大鼠按体表面积换算药量时的转换系数,0.2 kg为大鼠的标准体重。除细辛外其它生药量63 g,复方0、3、9、15 g,21 g组小青龙汤生药量分别为 63、66、72、78、84 g,服用量分别为5.67、5.94、5.9、6.48、7.02、7.56 g∕kg。
将上述各组中药用500 mL水浸泡30 min后,第1次煎煮30 min,过滤。再次向药锅中加入300 mL水,煎煮20 min,过滤,将2次过滤出的药液合并,于60℃恒温水浴分别浓缩为0.567、0.594、0.648、0.702、0.756 g∕mL的煎液,那么各剂量组大鼠每日服用的药量为相应浓度的煎液1 mL∕100 g,经120℃高温灭菌后冷藏备用。
2.3 哮喘大鼠动物模型的制备
参照文献[2-3]的造模方法:模型组和复方治疗组大鼠采用致敏和激发两步法制备哮喘大鼠模型。具体方法为①致敏阶段:分别于实验的第1天和第8天分2点向除正常组以外的各组大鼠腹腔内注射抗原液1 mL(含卵蛋白OVA 100 mg和氢氧化铝100 mg)使致敏,正常对照组用同样方法注射1 mL生理盐水来代替。②激发阶段:在大鼠致敏15 d后,各个复方治疗组大鼠用不同剂量细辛配伍的小青龙汤灌胃治疗,正常组和模型组用生理盐水代替,灌胃1 h后将大鼠放入自己制作的未完全密闭的透明雾化箱(60 cm×50 cm×50 cm)内,每次12只,随后向超声雾化器内倒入1%卵蛋白生理盐水150 mL,启动雾化器让模型组和复方治疗组大鼠每日自行吸入20 min左右,每天在相同时间重复激发1次,连续进行上述操作14 d,正常组仅吸入不含OVA的生理盐水。
造模成功的标志:在激发过程中大鼠出现咳嗽、节律性收腹样喘促、点头运动、连续打喷嚏、搔鼻、烦躁、紫绀等症状说明大鼠模型制备成功。
2.4 给药方法
各组从造模成功后(激发的第1天)开始给药,连续给药2周至实验结束,每日激发前1 h给药,每日1次;给药剂量和方式:复方治疗组分别按相应浓度的水煎液1mL∕100 g的标准来进行灌胃,正常组和模型组每次用1 mL∕100 g的生理盐水灌胃。
2.5 待测样本的制备和指标检测
2.5.1 待测样本的制备
连续灌胃给药2周,末次激发大鼠哮喘后,停水停食,第2日称重后用提前配制的10%的水合氯醛(3 mL∕kg)腹腔注射麻醉大鼠,将大鼠仰卧固定于实验操作台上,在腹部做一“V”字形切口,显露腹主动脉,持采血针在腹主动脉下方分叉处进针,待针尖刺入血管后,立即将采血针的另一端插入负压的真空采血管中,用红色的普通采血管采血5 mL,在室温静置2 h,3 500 r∕min,离心10 min后分离血清,吸取血清置于2 mL的离心管中,冻存于-80℃的冰箱待检测。
2.5.2 指标的检测
用全自动生化分析仪检测大鼠血清中ALT、AST、BUN、SCR的浓度。
2.6 统计学方法
采用SPSS 18.0软件进行统计分析,计量资料以均数±标准差(±s)表示,采用单因素方差分析组间显著性差异,以P<0.05为具有统计学意义。
3 实验结果
3.1 不同剂量细辛配伍的小青龙汤对哮喘大鼠肝功能(ALT、AST)的影响
各组大鼠肝功能检测结果显示:各个不同剂量细辛配伍的小青龙汤治疗组大鼠肝功能(ALT、AST)与正常组和模型组大鼠比较,均无明显显著性差异(P>0.05),见表1,图1、2。
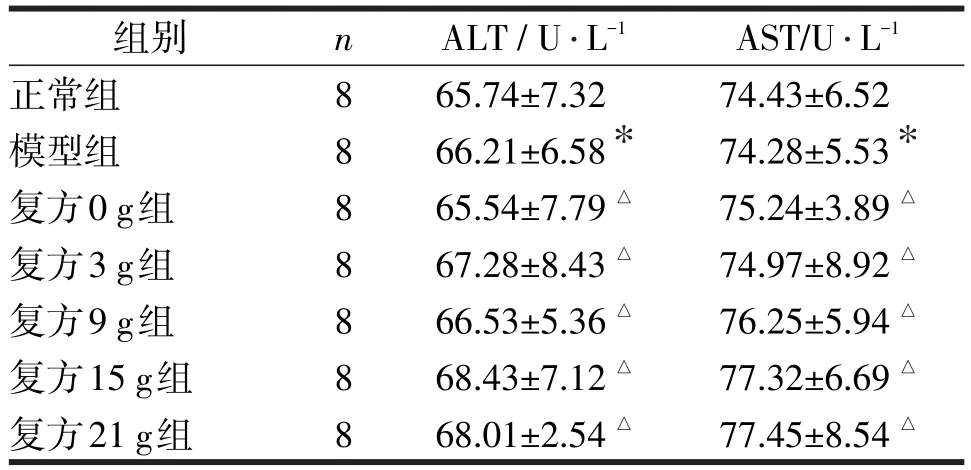
表1 不同剂量细辛的小青龙汤对哮喘大鼠肝功能的影响
图1 不同剂量细辛的小青龙汤对哮喘大鼠ALT浓度的影响

图2 不同剂量细辛的小青龙汤对哮喘大鼠AST浓度的影响
3.2 不同剂量细辛配伍的小青龙汤对哮喘大鼠肾功能(BUN、SCR)的影响
各组大鼠肾功能检测结果显示:各个不同剂量细辛配伍的小青龙汤治疗组大鼠肾功能(BUN、SCR)与正常组和模型组大鼠比较,均无明显显著性差异(P>0.05)。
结果见表2,图3、4。
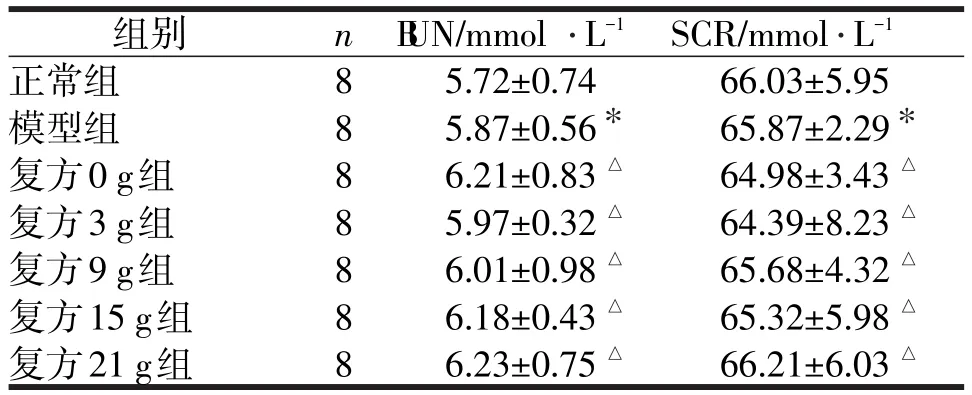
表2 不同剂量细辛的小青龙汤对哮喘大鼠肾功能的影响

图3 不同剂量细辛的小青龙汤对哮喘大鼠BUN浓度的影响
图4 不同剂量细辛的小青龙汤对哮喘大鼠SCR浓度的影响
4 讨论
4.1 开展中药肝肾毒性研究的重要性
随着国家对药品的毒副反应越来越重视,关于中药不良反应的报道也日益增多,中药安全性的问题已经引起了广大医务工作者的广泛关注。汤浩通过对6 903例药物性肝损害文献分析发现,中药是引起药源性肝损坏的首要因素,比例占到28.57%[4]。据研究,可以引起肝损害的中草药有100多种,中成药有30多种,比如中药川楝子、山慈姑,以及中成药六神丸、首乌片等均可引起药物性肝中毒或肝损害[5],中药引起的肾损害也非常常见。药物性肾损害疾病的发生一般都非常迅速,一旦损伤,肾脏的功能很难恢复,往往在较短的时间内就会进展到肾功能衰竭[6]。由于中药引起肾功能损害主要是由于某些中药内含有较高毒性的马兜铃酸,所以有时我们也将中药引起的肾病称为马兜铃酸肾病。细辛与马兜铃、关木通一样同属于马兜铃科多年生草本植物,关木通由于其肾毒性已经不再作为中药继续使用,细辛也因此受到牵连,在临床上的使用受到了很大限制,细辛[7]化学成分主要含有萜类(挥发油的主要成分)、苯丙基及其苷类(如甲基丁香酚、黄樟醚等)、木脂素类(如细辛脂素)、生物碱及酰胺类(如马兜铃内酰胺)、有机酸类及其酯类(如马兜铃酸)等。其中细辛挥发油中的甲基丁香酚、黄樟醚具有较强的毒副作用,其代谢产物具有抑制呼吸和致癌的作用,非挥发性成分中的马究铃酸具有较强的的肾毒性。
4.2 实验指标的选择及意义
4.2.1 肝功能测定的指标
本实验主要研究药物的肝损害,因此选择了反映肝实质损害的指标ALT、AST。
ALT(丙氨酸氨基转移酶)主要分布于肝细胞浆中,而血清中ALT的含量很低,肝脏中ALT的浓度是血中的1 000~5 000倍。ALT是肝细胞受损非常敏感的指标,并且与肝细胞受损的严重程度成正相关[5],当药物性肝损害发生时,ALT可超过正常值的5~20倍,因此目前将ALT作为评价药物性肝损害的指标之一。
AST是天门冬氨酸氨基转移酶的简称,主要分布于肝细胞线粒体中,肝细胞浆中仅占20%。当肝细胞发生轻微的损害时,血中AST的浓度一般不会升高,只有当肝细胞严重病变使肝细胞线粒体遭到严重破坏时,AST才从肝细胞的线粒体和细胞浆中释放到血液,使血清AST浓度升高,其敏感性不如ALT高。
4.2.2 肾功能测定的指标
BUN和SCR是反映肾小球功能好坏的重要指标,是评价药物性肾损害的检查指标之一。正常情况下,BUN和SCR主要均从肾小球滤过后随尿排出,当肾实质受损使肾小球的排泄功能受到障碍时,血BUN和SCR就会增加。
BUN是指血清尿素氮,是蛋白质分解代谢的终产物,其90%以上是通过肾脏排泄,仅有一小部分通过肠道和皮肤排出,当肾实质受损使肾小球的滤过功能受到障碍时,BUN就会升高,是评价肾功能的重要指标之一。BUN增高主要见于各种肾实质性病变,如肾小球肾炎、急慢性肾功能衰竭、肾内占位性病变和肾外因素引起的各种病变。肾功能轻度受损时,BUN可在正常范围,只有当肾单位受损大于50%时,BUN浓度才开始增加[6]。所以BUN不能作为肾功能早期损害的特异性指标,其对肾脏病早期损害的敏感性不高。
SCR是血清肌酐的英文简称,是肌酸的代谢产物。当每天摄入的蛋白量和运动相对稳定时,肌酐的生成量就比较恒定。由于SCR在肾小球滤过后,肾小管基本不重吸收,所以测定SCR浓度即可以反映肾小球的滤过能力,其敏感性优于BUN,是临床上评价肾功能损坏的重要指标。
5 结论
在本实验中复方治疗组大鼠ALT、AST、BUN、SCR与正常组和模型组大鼠比较,均无明显显著性差异(P>0.05),提示复方配伍中的细辛经过煎煮后,对肝肾功能没有影响,同时也提示小青龙汤整体煎剂对肝肾功能没有影响。
这样从一个侧面证实了小青龙汤中细辛和整体方剂的安全性,为临床安全使用细辛和青龙汤提供了一定的科学根据。细辛在复方煎剂中可以突破不过钱这一传统说法,以在临床上发挥其应有的治疗效果。
[1]周德生,黄仁忠.常用中药特殊配伍精要[M].太原:山西科学技术出版社.2007.
[2]吕国平,崔德健,郭英江,等.介绍一种建立大鼠哮喘模型的实验方法[J].中华结核和呼吸杂志,1995,18(6):377-378.
[3]崔龙平,杨永清,陈汉平,等.过敏性哮喘大鼠模型的制备[J].上海实验动物科学,2000,20(22):69.
[4]汤浩,杨晶露,李磊.6903例药物性肝损害文献分析[J].华南国防医学杂志,2014,28(9):172-173.
[5]黄道林,向娟,刘晓东,等.药源性肝损伤中药的研究进展[J].海峡医学,2012,24(10):13-15.
[6]刘平.中草药的肝损伤的问题[J].中华肝脏病杂志,2004,12(4):243.
[7]吕崇山.中药的肾毒性和肾保护浅谈[J].中医药学报,2003,31(3):24.
〔责任编辑 杨德兵〕
Study the Effects of Asarum Dosage Conversion of Xiaoqinglong Decoctionon on Asthma Rat Liver and Kidney Function
CHAI Mao-Shan1,LI Peng2,ZHAO Ye1,GUO Zhi-Jiang1,DENG Liang1
(1.School of Medicine,Shanxi Datong University,Datong Shanxi,037009;2.The People's Hospital of Qingshui,Jincheng Shanxi,048200)
ObjectiveBased on the replication of rat model of asthma,we investigate its effect on the liver and renal function in asthmatic rats by treating with different dosage of Asarum compatibility of Xiaoqinglong Decoction,to reveal the different dosage of Asa⁃rum compatibility of Xiaoqinglong Decoction whether there is a dose-response relationship,to reveal the safety of the Asarum and Xiao⁃qinglong Decoction,which provides a scientific basis for the clinical safe and efficient use of Asarum.Method84 healthy male SD rats are fed one week after routine and divided into model group,0 grams of Asarum compatibility of Xiaoqinglong Decoction group,3 grams Asarum compatibility of Xiaoqinglong Decoction group,9 grams of Asarum compatibility of Xiaoqinglong Decoction group,15 grams of Asarum compatibility of Xiaoqinglong Decoction group,21 grams of Asarum compatibility of Xiaoqinglong Decoction group,normal group,with 12 rats in each group.The modeling and treatment are carried out simultaneously.After the treatment,all rats are fasted for one night,collect blood samples from abdominal aorta.Measure ALT,AST,BUN,SCR content with automatic biochemistry ana⁃lyzer.ResultsCompared with the normal group and model group,there is no significant difference in the ALT、AST、BUN 、SCR serum content of each compound treatment group(P>0.05);ConclusionIn accordance with the fifth edition of prescriptions dose of Xiaoqin⁃glong Decoction,when Asarum uses from 0 g to 21 grams and other medication unchanged,Xiaoqinglong Decoction has no obvious ef⁃fect on liver and kidney function(ALT,AST,BUN,SCR)of asthmatic rats.
asarum;xiaoqinglong decoction;asthma;liver and renal function
R285.5
A
1674-0874(2017)05-0042-05
2017-05-16
大同市科技攻关项目[2015097]
柴茂山(1962-),男,山西怀仁人,硕士,教授,研究方向:方剂学。

