秋水仙素对北柴胡生长的影响
, , , , (西南科技大学生命科学与工程学院, 四川 绵阳 621010)
·研究报告·
秋水仙素对北柴胡生长的影响
刘宏伟,唐志康,余马,舒晓燕,侯大斌
(西南科技大学生命科学与工程学院, 四川 绵阳 621010)
[目的]以北柴胡新品种川北柴1号为材料,研究秋水仙素处理对柴胡生长的影响。[方法]对北柴胡审定品种川北柴1号采用生长点滴定和浸泡2种处理方法,0.1%~0.5% 5个处理浓度,3~5 h 3个处理时间、1叶期及5叶期2个处理时期进行诱导。[结果]生长点滴定法对柴胡幼苗生长影响不显著。浸泡法中秋水仙素浓度、浸泡时间、处理浓度和浸泡时间协同作用对北柴胡存活率、植株变异率及叶绿素含量有显著影响。此外,赤霉素添加对北柴胡诱导效果及生长发育也有显著影响。[结论]本研究对创制柴胡新材料具有重要意义。
北柴胡; 川北柴1号; 秋水仙素; 方差分析
北柴胡(BupleurumchineseDC.)为伞形科(Umbellifetae)多年生草本植物,其根为常用大宗药材之一。药理研究表明,柴胡具有解热、抗病毒、降血脂、保肝、抗炎、抗肿瘤等功效[1-2]。目前柴胡的使用量在所有中药中位列前3名,年用量逾1万t,且随柴胡为主要原料的药品不断开发上市而快速递增。但由于近年来野生柴胡资源逐渐枯竭和产地生态环境持续恶化,采挖量逐年减少,加之出口量也不断增加,而国内又没有较大规模且持续量产的柴胡规范化种植基地,导致柴胡的供应日趋紧张。
柴胡主要药用部位(主根)较小,单株产量低(≤1 g)[3],严重制约了柴胡产业化发展效率。多倍体育种具有增大植物营养器官的特点,在保留原有药用成分的基础上获取较正常植株大的营养器官,从而获取新的种质资源[4-5]。通过秋水仙素诱导桔梗[6]、黄芩[7]、金银花[8]、刺果甘草[9]等药用植物上成功获得多倍体植株。本试验采用秋水仙素诱导柴胡获得药用植物新材料,探讨秋水仙素诱导对柴胡生长的影响,为加速柴胡产业化进程提供新的资源。

图1 秋水仙素处理单株DHcbc 11与空白组长势对照
1 材料与方法
1.1 材 料
供试柴胡为北柴胡审定品种川北柴1号。该品种由西南科技大学、四川德培源中药科技开发有限公司及中国药科院药用植物研究所等多家单位共同选育。
1.2 方 法
本研究均在幼苗长出第1片真叶时移栽培育,待所有幼苗成活后选取相同生长时期进行分组处理。所有实验在环境可控的加代温室内(25 ℃)进行,设3次重复。
表1 浸泡法实验处理条件
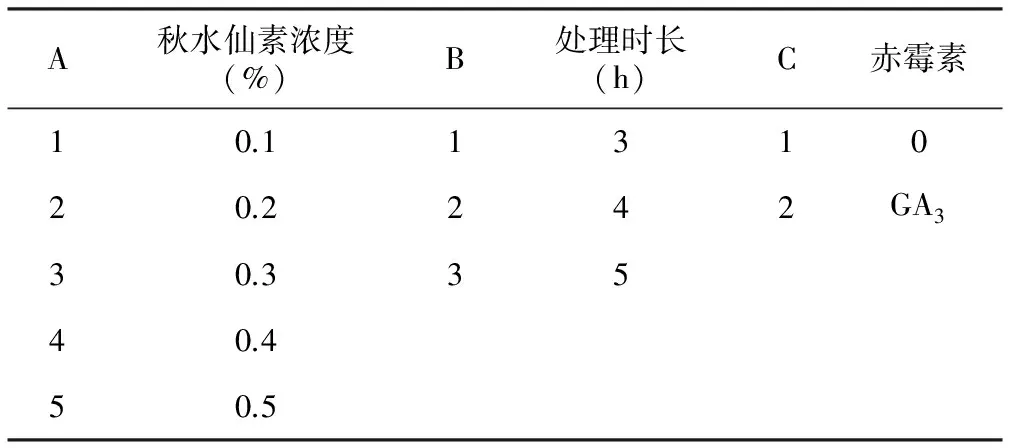
A秋水仙素浓度(%)B处理时长(h)C赤霉素10.1131020.2242GA330.33540.450.5
1.2.1 生长点滴定法诱导北柴胡幼苗
当供试材料生长时期处于1叶期、5叶期时,分别用蘸有0.1%、0.2%、0.3%、0.4%、0.5%秋水仙素的棉球,放置于柴胡的生长点处,并且每6 h补充滴加,以保持药液浓度,处理24 h,每盆5棵,每个处理15株,处理后将棉球移除,并充分洗净植株上残存药液,待进一步生长后,进行观察和鉴定。
1.2.2 浸泡法诱导北柴胡幼苗
以30棵正常植株为空白对照,当供试材料生长时期处于1叶期时,用水将根部的土洗去,设置包括秋水仙素浓度、浸泡时间及是否添加赤霉素的30个处理的完全随机组合实验(表1)。将处理后的柴胡幼苗用小水流浸泡冲洗,每12 h后换1次水,至24 h后倒掉水。将柴胡幼苗移栽至1加仑育苗盆中,每盆4棵,每个处理12株,待对照植株进入拔节期时进行观察和鉴定。
1.2.3 存活率的测定
对用秋水仙素处理后的幼苗生长情况进行定期观察,直至不再死亡。
存活率(%)=存活株数/处理株数×100%。
1.2.4 植株突变率的统计
以处理后植株生长缓慢、叶色浓绿、叶片变大变宽作为形态变异指标,统计变异率。
变异率(%)=变异株数/处理株数×100%。
1.2.5 植株叶绿素含量(SPAD)的测定
使用SPAD-502叶绿素仪,选取每株植株倒5叶,在距叶尖1/3处测量SPAD值,测量5次,取平均值。以该植株倒5叶距叶尖1/3处测定值的平均值作为该植株叶片叶绿素含量。
1.3 数据统计
统计分析采用SPSS 16.0软件(Ver.16.0 developed by IBM,USA.)进行计算。
2 结果与分析
2.1 生长点滴定法对柴胡幼苗诱导的效果
采用生长点滴定法诱导的川北柴1号幼苗,1叶期和5叶期的植株存活率达到了100%。植株变异率为60%,但与对照相比,发生变异的部位仅限于接触棉球的叶片,后期生长出的叶片未有变异的性状,因此该方法对柴胡后期生长不会造成显著影响。
2.2 浸泡法诱导对柴胡幼苗存活率、变异率和叶绿素含量的影响
与对照植株相比,采用浸泡法处理柴胡幼苗后,部分柴胡植株在幼苗期及成株期生长产生显著差异,如植株矮化、叶片变厚、叶绿素含量增加等(图1,图2)。
2.2.1 不同处理条件对植株的存活率、变异率和叶绿素含量的影响
不同处理条件对植株的存活率、变异率和叶绿素含量的影响不同(表2)。从表2可看出,随着处理浓度(A)的升高,植株存活率呈逐步降低趋势,变异率先升高后降低。随着处理时间(B)的延长,植株存活率降低,变异率提高。随着处理浓度(A)的升高和处理时间(B)的延长,植株叶绿素含量呈逐步升高趋势。
表2 不同处理条件下的植株存活率、变异率和叶绿素含量
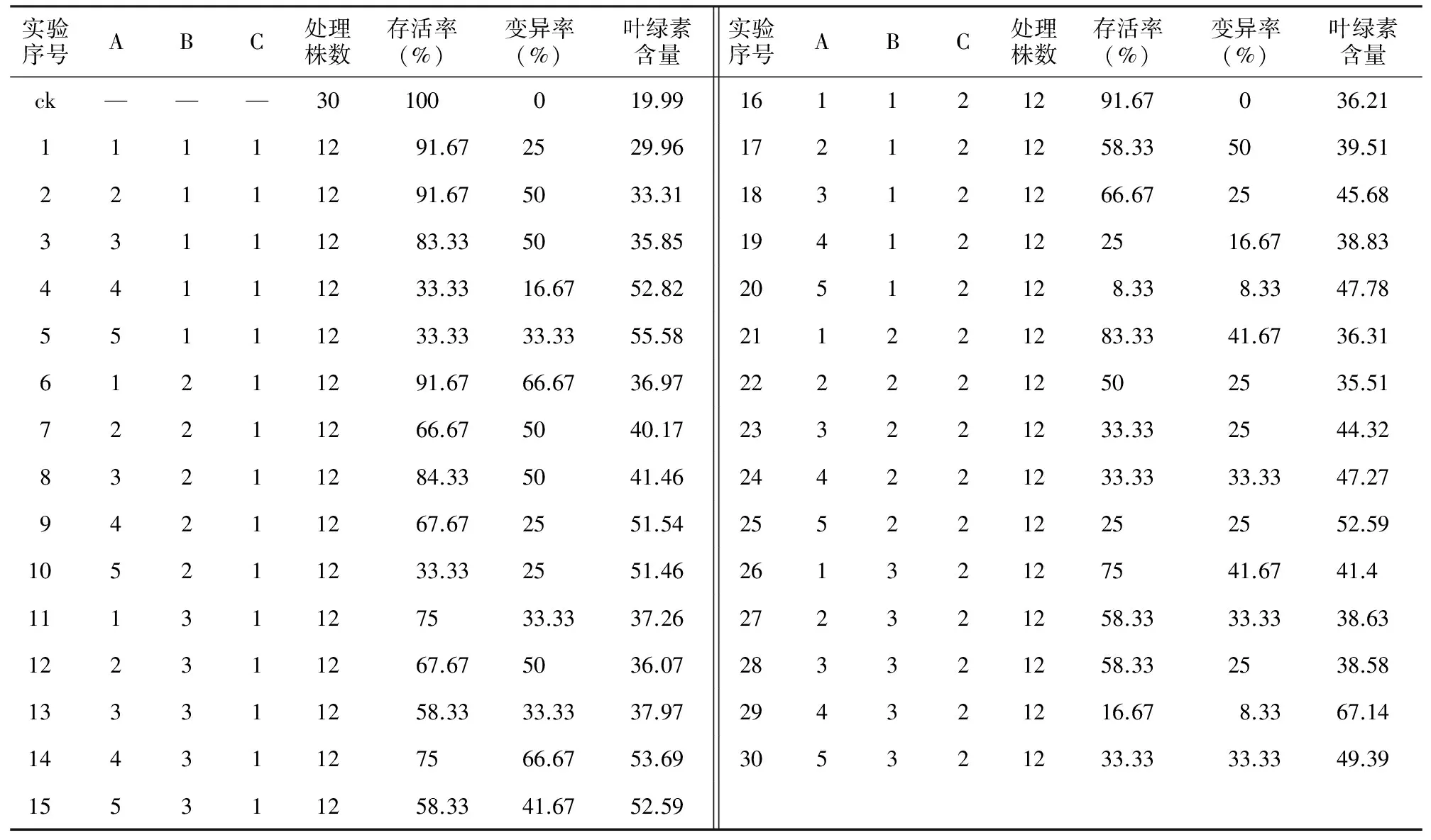
实验序号ABC处理株数存活率(%)变异率(%)叶绿素含量实验序号ABC处理株数存活率(%)变异率(%)叶绿素含量ck———30100019.99161121291.67036.2111111291.672529.96172121258.335039.5122111291.675033.31183121266.672545.6833111283.335035.8519412122516.6738.8344111233.3316.6752.8220512128.338.3347.7855111233.3333.3355.58211221283.3341.6736.3161211291.6766.6736.972222212502535.5172211266.675040.17233221233.332544.3283211284.335041.46244221233.3333.3347.2794211267.672551.542552212252552.59105211233.332551.4626132127541.6741.411131127533.3337.26272321258.3333.3338.63122311267.675036.07283321258.332538.58133311258.3333.3337.97294321216.678.3367.1414431127566.6753.69305321233.3333.3349.39155311258.3341.6752.59
注:A(处理浓度)中,1、2、3、4、5分别代表0.1%、0.2%、0.3%、0.4%、0.5%;B(处理时间)中,1、2、3分别代表3 h、4 h、5 h;C(添加赤霉素)中,1代表未添加赤霉素,2代表添加赤霉素。

注:DHcbc 1502为处理组植株,株高46 cm,ck为对照组植株,株高103 cm。图2 秋水仙素处理柴胡与空白组株高对照
对秋水仙素浓度、处理时间的两因素进行方差分析(表3),可以看出,处理浓度对柴胡幼苗存活率影响极显著(plt;0.01),处理时间及其两者交互作用对柴胡幼苗存活率影响不显著(pgt;0.05);处理浓度、处理时间对柴胡幼苗变异率影响不显著(pgt;0.05),但其交互作用对柴胡幼苗变异率影响显著(plt;0.05);处理浓度对柴胡幼苗叶绿素含量影响极显著(plt;0.01),处理时间及处理浓度和处理时间的交互作用对柴胡幼苗叶绿素含量影响不显著(pgt;0.05)。
从诱变效果看,0.1%~0.5%的秋水仙素对柴胡的诱导均有效果,植株的存活率和变异率受秋水仙素浓度和处理时间2个因素影响,其中A1B2C1和A4B3C1(0.1%的秋水仙素处理4 h和0.4%的秋水仙素处理5 h)组合变异率最高,为66.67%。综合考虑植株存活率、变异率、实验成本以及时间等因素,采用0.1%处理4 h的组合进行柴胡多倍体诱导效果最佳。
2.2.2添加赤霉素后不同处理条件对植株的存活率、变异率和叶绿素含量的影响
添加赤霉素后,不同处理条件对植株的存活率、变异率和叶绿素含量的影响不同(表2)。从表2可看出,随着处理浓度(A)的升高,植株存活率呈逐步降低趋势,变异率先升高后降低。随着处理时间(B)的延长,植株存活率先降低后升高,变异率先升高后降低。随着处理浓度(A)的升高和处理时间(B)的延长,植株叶绿素含量皆呈逐步升高趋势。

注:DHcbc 1601为处理组植株,ck为对照组植株。图3 秋水仙素处理柴胡与空白组倒七叶叶片形态对照
对添加赤霉素后秋水仙素浓度、处理时间的两因素进行方差分析(表4),可以看出,处理浓度对柴胡幼苗存活率影响极显著(plt;0.01),处理时间及其两者交互作用对柴胡幼苗存活率影响不显著(pgt;0.05);秋水仙素浓度、处理时间及其交互作用对柴胡幼苗变异率影响皆不显著(pgt;0.05);处理浓度对柴胡幼苗叶绿素含量影响极显著(plt;0.01)处理时间对柴胡幼苗叶绿素含量影响不显著(pgt;0.05),其两者的交互作用对柴胡幼苗叶绿素含量影响显著(plt;0.05)。
表3 不同处理浓度和时间对柴胡幼苗的两因素方差分析
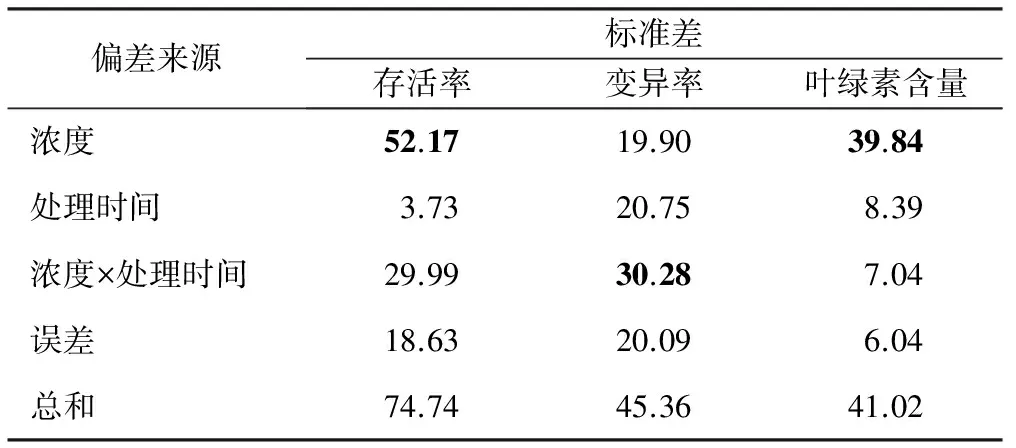
偏差来源标准差存活率变异率叶绿素含量浓度52.1719.9039.84处理时间3.7320.758.39浓度×处理时间29.9930.287.04误差18.6320.096.04总和74.7445.3641.02
注:加粗字体表示该因素差异显著(plt;0.05)。下同。
以植株存活率与变异率为指标,添加赤霉素后秋水仙素溶液的最佳诱导浓度和时间为0.2%和3 h。在最优诱导条件下,较未添加赤霉素的处理,存活率由91.67%降为58.33%,减少36.37%;变异率由66.67%降为50%,减少25%。结果表明,添加赤霉素未对秋水仙素诱导结果起促进作用。
表4 添加赤霉素后不同处理浓度和时间对柴胡幼苗的两因素方差分析
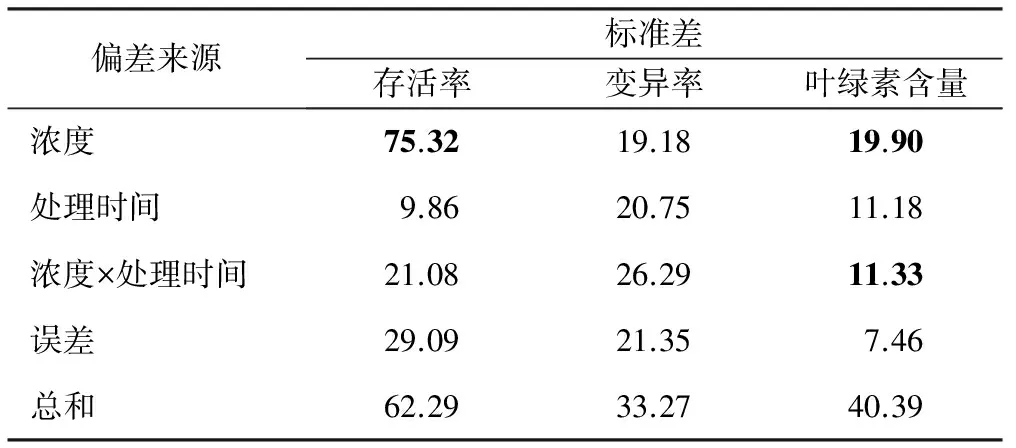
偏差来源标准差存活率变异率叶绿素含量浓度75.3219.1819.90处理时间9.8620.7511.18浓度×处理时间21.0826.2911.33误差29.0921.357.46总和62.2933.2740.39
以植株叶绿素含量为指标,未添加赤霉素的最优处理组合为A5B1C1(条件为秋水仙素浓度0.5%,处理3 h);添加赤霉素的最佳组合为A4B3C2(条件为秋水仙素浓度0.4%,处理5 h)。同在最适诱导条件下处理,植株叶片叶绿素含量较未添加赤霉素处理的含量增加20.80%。结果表明,添加赤霉素的秋水仙素溶液有助于提高柴胡叶片的叶绿素含量。
3 讨论与结论
秋水仙碱的浓度和处理时间是影响染色体加倍的最重要的外在条件。用秋水仙碱处理时,植物种类不同,其浓度和处理时间的最佳组合不同[10]。由于秋水仙素对外植体有毒害作用,若处理不当,会造成材料在处理过程中死亡,影响成苗率,但不同作物、品种或器官对秋水仙素的敏感性不同[11]。研究表明,石斛兰[12]、非洲菊[13]均随秋水仙素处理浓度的增加或时间的延长,而受害程度加重,成活率降低。Martin B等的研究发现,赤霉素加入秋水仙素溶液可使玉米花药诱导产生二倍体的比率由20%提升至52%[14]。本研究结果显示,秋水仙素处理的幼苗的存活率的影响显著不同,存活率随秋水仙素处理浓度升高及时间延长而显著降低。而赤霉素加入秋水仙素溶液对浸泡法诱导柴胡有一定的抑制作用。因此,柴胡多倍化材料创制过程中不宜添加赤霉素。
秋水仙素处理浓度和时间不仅影响存活率,也是诱导植物产生多倍体的关键。番茄幼苗茎尖在含8 mmol/L秋水仙素的液体培养基中处理96 h,其四倍体诱导率达11.11%[15]。本研究结果表明,不同秋水仙素处理时间和浓度对幼苗变异率影响显著不同,变异率随处理时间延长不断上升,随处理浓度升高先上升后降低。
叶绿素是植物进行光合作用的重要物质,其含量的多少对光合速率有直接影响,是反映植物叶片光合能力的一个重要指标,以说明某种措施或环境条件对植物产生的影响[16]。另有研究表明,叶片叶绿素含量增加,PBP羧化酶活性增强,净光合速率提高,这不仅可以增大苗期地上部生长所需的有机营养,而且也可保证根系生长所需要的营养物质,因而苗期植株得以健壮生长,促进壮苗[17]。本研究结果表明,秋水仙素浓度的升高以及处理时间的延长,柴胡植株叶绿素含量皆呈逐步升高趋势,添加赤霉素有利于植物叶片叶绿素含量的增加。
植物体细胞染色体加倍后,分化生成的多倍体植株,通常表现出巨大性,如茎变粗短、叶片变厚,有时比较粗糙或生皱纹、多毛,花朵、果实和种子变大,生育期延长,整个植株变成巨型,这些特征都可作为判别多倍体的根据[18]。柴胡的变异主要表现为茎秆变粗,节间距、株高变短(图1,图2),叶片的形状改变(卷曲、变宽、变厚,图3),这在正常的植株中是没有的。本研究结果表明,不同秋水仙素处理时间和浓度对叶片叶绿素含量影响显著,叶绿素含量均随秋水仙素处理浓度升高及时间延长而显著增加。
[1]武振华,牛炳韬,王新宇.药用植物染色体加倍的研究进展[J].西北植物学报,2005,25(12):2 569-2 574.
[2]杜晓华.园林植物遗传育种学[M].北京:中国水利水电出版社,2013:170-223.
[3]郑亭亭,隋春,魏建和,等.北柴胡二代新品种“中柴2号”和“中柴3号”的选育研究[J].中国中药杂志,2010,35(15):1 931-1 934.
[4]乔永刚,赵晓明.药用植物的多倍体育种[J].世界科学技术——中医药现代化,2007,9(5):77-82.
[5]张海凤,郑辉,陈新华,等.药用植物多倍体研究进展[J].河北林果研究,2008,23(2):169-172.
[6]Yuxiang Wu,Fuhong Yang,Xiaoming Zhao,et al.Identification of tetraploid mutants of Platycodon grandiflorus by colchicine induction[J].Caryologia-Firenze,2014,64(3):343-349.
[7]乔永刚,赵晓明,宋芸.秋水仙素诱导黄芩多倍体的研究[J].中国医药生物技术,2008,3(5):389-390.
[8]王惠利,赵晓明.金银花多倍体诱变及早期形态鉴定[J].山西农业科学,2012,40(12):1 240-1 242.
[9]吴玉香,贺润丽,高建平,等.刺果甘草多倍体诱变育种的研究[J].山西农业大学学报(自然科学版),2004,24(2):116-117.
[10]赵阳,黄韬.秋水仙素在园艺植物多倍体育种中的应用研究进展[J].上海蔬菜,2010(2):29-31.
[11]孔素萍,曹齐卫,孙敬强,等.秋水仙素对大蒜茎尖试管苗四倍体的诱导[J].中国农业科学,2014,47(15):3 025-3 033.
[12]Sarathum S,Hegele M,Tantiviwat S,et al.Effect of concentration and duration of colchicine treatment on polyploidy induction inDendrobiumscabrilingueL.[J].European Journal of Horticultural Science,2010,75(3):123-127.
[13]Gantait S,Mandal N.Induction and identification of tetraploids using in vitro colchicine treatment of Gerbera jamesonii Bolus cv.Sciella[J].Plant Cell,Tissue and Organ Culture (PCTOC),2011,24(3):218-230.
[14]Martin B,Widholm J M.Ploidy of small individual embryo-like structures from maize anther cultures treated with chromosome doubling agents and calli derived from them.[J].Plant Cell Reports,1996,15(10):781-785.
[15]Praça,M.M,Carvalho,C.R,et al.A practical and reliable procedure for in vitro induction of tetraploid tomato[J].Scientia Horticulturae,2009,122(3):501-505.
[16]高福元,张吉立,刘振平,等.盐胁迫对树锦鸡儿叶绿素含量和根系活力的影响[J].贵州农业科学,2010,38(5):46-48.
[17]张慧玲.植物生长物质对柴胡产量及品质的影响[D].河南农业大学,2006.
[18]詹忠根,徐程.秋水仙素诱导铁皮石斛多倍体研究[J].浙江大学学报(理学版),2011,38(3):321-325.
The Influence of Colchicine on Growth ofBupleurumchinenseDC
LIUHongwei,TANGZhikang,YUMa,SHUXiaoyan,HOUDabin
(School of Life Science and Engineering,Southwest University of Science and Technology,Mianyang Sichuan 621010,China)
[Objective]Identify the influence of colchicine on growth ofBupleurumchinenseDC by used of new commercial variety of Chuanbeichai No.1.[Method] the seedlings of Chuanbeichai No.1 were induced by treating the shoot tip meristem and soaking method (whole plant with colchicine).In addition,the effects of colchicine concentrations (0.1%-0.5%),treatment times(3-5 hour),and treatment period (one leaf and five leaf period stages) were also studied.[Results]The effect of colchicine treating on shoot tip meristem was insignificant toB.chinenseDC.The colchicine concentrations,treatment times and their interactions showed significant effects on survival rate,mutational rate, and chlorophyll content ofB.chinenseDC with soaking method.In addition,it also showed significant effects on the mutagenic effect and growth and development ofB.chinenseDC while adding gibberellin in colchicine.[Conclusion]The colchicine induction procedure is very important to creation of mutation inB.chinenseDC.
BupleurumchinenseDC; Chuanbeichai No.1; colchicine; ANOVA
2017-02-17
国家自然科学基金(81603223);四川省“十三五”科技育种攻关项目(2016 NYZ 0036-4-2)。
刘宏伟(1988—),男,学士,在读硕士研究生,研究方向:药用植物育种;E-mail:eric531959109@126.com。
侯大斌,男,博士,教授,研究方向:天然产物;E-mail:dbhou@126.com。
10.16590/j.cnki.1001-4705.2017.05.001
S 567
A
1001-4705(2017)05-0001-05

