N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺的合成
于宏伟,杜林楠,苏苗苗,关胜琴,孙佳玥,侯腾硕,刘 磊
(石家庄学院 化工学院,河北 石家庄 050035)
N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺的合成
于宏伟,杜林楠,苏苗苗,关胜琴,孙佳玥,侯腾硕,刘 磊
(石家庄学院 化工学院,河北 石家庄 050035)
乙酸(1-二茂铁基乙基)酯1与二甲胺反应制备出N,N-二甲基-1-二茂铁乙胺2,收率74%.在正丁基锂/乙醚的反应体系中,化合物2进一步与二苯基氯化磷反应,制备出N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3,收率18%.化合物3的结构经1H NMR 和31P NMR 进行了表征,并进一步研究了其合成机理.
乙酸(1-二茂铁基乙基)酯;N,N-二甲基-1-二茂铁乙胺;N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺;合成;表征;机理
0 引言
N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3是一类重要的金属有机化合物,由于其具有P-N双齿配体结构,因此作为配体可以高活性地促进Pd催化溴代芳烃与芳胺(脂肪胺)的Buchwald Hartwig C-N偶联反应[1].此外,N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3的结构还可进一步修饰,作为配体可促进Pd催化Suzuki-Miyaura C-C偶联反应[2-7].N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺 3价格昂贵,主要是因为其含有三价磷的结构,对空气敏感,制备困难.笔者参考相关文献报道[8-12],从乙酸(1-二茂铁基乙基)酯出发,通过两步反应,制备出N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3(图1),通过1H NMR 和31P NMR 对其结构进行了表征,并进一步研究了其合成机理.
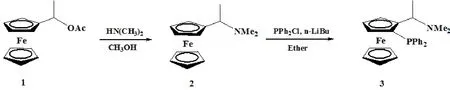
图1 N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3的合成
1 实验部分
1.1 仪器与试剂
核磁共振波谱仪(Bruker Drx 400 MHz型,瑞士Bruker公司),电子天平(AR 1140型,上海奥毫斯国际贸易有限公司).
乙酸(1-二茂铁基乙基)酯,按照文献方法合成[10,11].正丁基锂,二苯基氯化磷(Aldrich公司),其他试剂均为市售分析纯试剂.催化反应中的所有试剂均按照Schlenk标准技术,进行严格的脱气及干燥处理.
1.2 合成方法
1.2.1 N,N-二甲基-1-二茂铁乙胺2的合成
乙酸(1-二茂铁基乙基)酯1(52.2 g,192 mmol),溶于600 mL甲醇后,加入80 mL的33%的二甲胺水溶液,室温搅拌反应12 h后,TCL检测反应.反应结束后,减压蒸馏除去溶剂,残留物用8.5%的磷酸水溶液溶解,调节pH<7,酸溶液用乙醚萃取(100 mL×3),萃取后的水溶液在剧烈搅拌的条件下,分批加入无水碳酸钾,调节pH=10,二氯甲烷萃取水相(100 mL×3),合并有机相,饱和食盐水洗涤(100 mL×3)有机相,无水碳酸钾干燥有机相,过滤,减压蒸馏除去溶剂,得到红色粘稠状液体36.4 g,产率74%,不需要提纯,直接进行下一步反应.
1.2.2 N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3的合成
高纯氮气下,N,N-二甲基-1-二茂铁乙胺2(36.4 g,142 mmol)溶于400 mL无水脱气乙醚中,在室温条件下,1 h内缓慢滴加59 mL的正丁基锂的正己烷溶液(C=2.89 mol/L,171 mmol),继续搅拌反应1 h后,缓慢加热至微沸,在1 h内缓慢滴加二苯基氯化磷(62.9 g,284 mmol)的50 mL乙醚溶液,加热回流4 h,冷却至0℃,缓慢加入100 mL饱和碳酸氢钠水溶液,室温搅拌反应10 min,乙醚萃取水相(100 mL×3),合并有机相,饱和食盐水洗涤有机相(50 mL×3),无水硫酸钠干燥24 h,减压蒸除乙醚,得到红色粘稠液体,脱气无水乙醇重结晶,得到红色固体11.6 g,收率18%.
2 结果讨论
2.1 N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3合成方法研究
在第一步反应中,乙酸(1-二茂铁基乙基)酯1首先与二甲胺反应制备出N,N-二甲基-1-二茂铁乙胺 2.这是一个室温下的二甲胺的亲核取代反应,反应很容易进行,室温搅拌反应12 h,收率较高可达到74%.而第二步反应,则是整个合成反应的关键.首先,在乙醚溶液中,N,N-二甲基-1-二茂铁乙胺2首先与强碱正丁基锂反应,原位生成二茂铁-锂金属化合物后,二苯基氯化磷进一步与其发生亲电取代反应,生成粗产品,经过简单的重结晶分离,就可以得到高纯度的目标产物.由于正丁基锂和二苯基氯磷对于水和氧气非常敏感,因此第二步反应必须严格采用Schlenk标准技术,可以有效地避免水及空气中的氧气对于反应的影响.
2.2 N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3的结构表征
2.2.1 N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3的31P NMR谱解析
通过31P NMR对化合物3的结构进行表征.结果见图2.
其中δ22.1是化合物分子中磷原子化学位移,说明化合物3中含有的磷原子处于三价态,并没有发生氧化现象.
2.2.2 N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3的1H NMR谱解析
通过1H NMR对化合物3的结构进行表征,结果见图3.
其中δ1.20(3个氢原子)是与手性碳原子相连的甲基上的的化学位移;δ1.70(6个氢原子)归属于N原子相连的两个甲基上氢原子的化学位移;δ3.80(1个氢原子),δ3.85(5个氢原子),δ4.18(1个氢原子)和 δ4.30(1个氢原子)则归属于二茂铁基团上8个氢原子的化学位移;δ4.10(1个氢原子)则归属于手性碳上氢原子的化学位移;δ7.10(5个氢原子),δ7.27(3个氢原子)和δ7.51(2个氢原子)则归属于苯环上10个氢原子的化学位移.经过分析,所合成化合物结构正确,为目标产物N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3.
3 结论
制备出N,N-二甲基-1-(2-二苯膦基)二茂铁乙胺3,通过1H NMR和31P NMR对其结构进行表征,并进一步研究了二甲胺的亲核取代反应及二苯基氯化磷亲电取代反应机理,本研究未见相关文献报道,具有一定的理论研究价值.
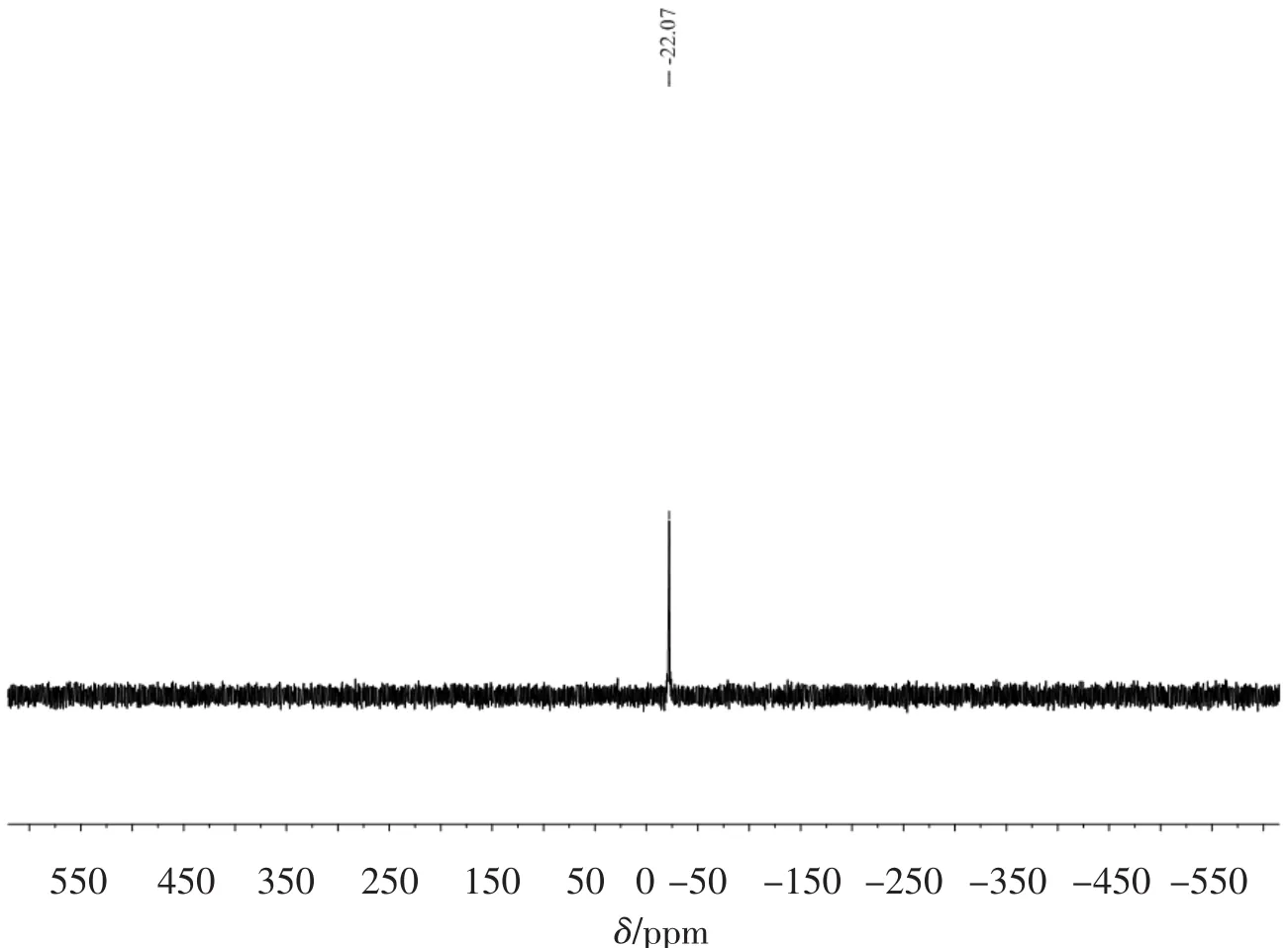
图 2 化合物3 的31P NMR谱图(CDCl3,161 MHz)
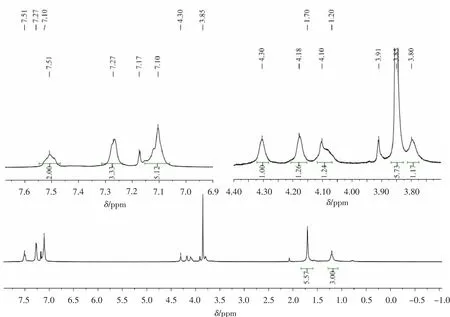
图 3 化合物3 的 1H NMR谱图(CDCl3,400 MHz,TMS)
[1]MARCOUX J,WAGAW S,BUCHWALD S L.Palladium-catalyzed Amination of Aryl Bromides:Use of Phosphinoether Ligands for the Efficient Couplingof Acyclic Secondary Amines[J].Journal of Organic Chemistry,1997,62(6):1568-1569.
[2]LITTKE A F,DAI C Y,FU G C.Versatile Catalysts for the Suzuki Cross-coupling of Arylboronic Acids with Aryl and Vinyl Halides and Triflates under Mild Conditions[J].JAmChemSoc,2000,122(17):4020-4028.
[3]WOLFEJP,BUCHWALDSL.A highly Active Catalyst for the Room-temperature Amination and Suzuki Coupling of Aryl Chlorides[J].Angew ChemInt Ed,1999,38(16):2413-2416.
[4]Arduengo IIIAJ,Harlow RL,Kline M.A Stable Crystalline Carbene[J].JAmChemSoc,1991,113(1):361-363.
[5]ALTENHOFF G,GODDARD R,LEHMANN C W,et al.An N-heterocyclic Carbene Ligand with Flexible Steric Bulk Allows Suzuki Cross-coupling of Sterically Hindered Aryl Chloridesat Room Temperature[J].Angew Chem Int Ed,2003,42(31):3690-3693.
[6]贾莉,于宏伟,童庆松,等.氧官能化的膦配体在钯催化的Suzuki-Miyaura反应中的应用[J].有机化学,2008,28(6):1115-1118.
[7]于宏伟,童庆松,贾莉,等.聚乙二醇(PEG)桥连的新型双N-杂环卡宾-膦的合成及其在水相Suzuki反应中的应用[J].有机化学,2011,31(5):742-746.
[8]HAYASHI T,KUMDA M.Asymmetric Synthesis Catalyzed by Transition-metal Complexes with Functionalized Chiral Ferrocenylphosphine Ligands[J].Acc ChemRes,1982,15:395-401.
[9]GISCHIGS,TOGNIA.Synthesisand Coordination Chemistryofa New Chiral Tridentate PCPN-Heterocyclic Carbene Ligand Based ona FerroceneBackbone[J].Organometallics,2004,23(10):2479-2487.
[10]吴晶,于宏伟,段书德,等.1-(1-二茂铁基乙基)-3-金刚基-1-咪唑碘盐配体的制备及结构表征[J].石家庄学院学报,2008,10(6):55-58.
[11]于宏伟.二茂铁膦、卡宾配体合成及其在Pd催化Suzuki反应的研究[D].大连:大连理工大学,2007.
[12]周向东,陈迎春,蒲泽佳,等.锦纶用耐久性阻燃剂的合成与应用[J].成都纺织高等专科学校学报,2016,33(1):37-41.
Synthesis of N,N-Dimethyl-1-[2-(diphenylphosphino)ferrocenyl]Ethylamine
YU Hong-wei,DU Lin-nan,SU Miao-miao,GUAN Sheng-qin,SUN Jia-yue,HOU Teng-shuo,LIU Lei
(School of Chemical Engineering,Shijiazhuang University,Shijiazhuang,Hebei 050035,China)
N,N-dimethyl-1-[2-ferrocenyl]ethylamine 2 is synthesized by acetic acid(1-ferrocene ethyl)ester 1 and dimethylamine,the yield is 74%.N,N-dimethyl-1-[2-(diphenylphosphino)ferrocenyl]ethylamine 3 is prepared by compound 2 and chlorodiphenyl phosphine in the solution of butyl lithium/ether.The yield is 18%and the structure is characterized by1H NMR and31P NMR.The synthesis mechanism is studied also.
acetic acid (1-ferrocene ethyl)ester;N,N-dimethyl-1-[2-ferrocenyl]ethylamine;N,N-dimethyl-1-[2-(diphenylphosphino)ferrocenyl]ethylamine;synthesis;characterization;mechanism
O623
A
1673-1972(2017)06-0005-04
2017-08-10
石家庄市科学技术研究与发展计划(171501232A);石家庄学院化工制药实验教学示范中心本科生科技创新基金(2017-5X)
于宏伟(1979-),男,黑龙江哈尔滨人,副教授,博士,主要从事精细石油化工研究.
(责任编辑 王颖莉)

