无锂助熔剂B2O3对Li1.3Al0.3Ti1.7(P∗O4)3固体电解质离子电导率的影响
史茂雷 刘磊 田芳慧 王鹏飞 李嘉俊 马蕾
(河北大学电子信息工程学院,保定 071002)
无锂助熔剂B2O3对Li1.3Al0.3Ti1.7(P∗O4)3固体电解质离子电导率的影响
史茂雷 刘磊†田芳慧 王鹏飞 李嘉俊 马蕾
(河北大学电子信息工程学院,保定 071002)
固体电解质,Li1.3Al0.3Ti1.7(PO4)3,助熔剂,固相烧结法
采用固相法制备锂离子电池用固体电解质磷酸钛锂铝Li1.3Al0.3Ti1.7(PO4)3(LATP),研究了不同烧结温度以及助熔剂对LATP固体电解质离子电导率的影响.采用X射线衍射、能谱分析、扫描电镜和交流阻抗等方法,研究样品的结构特征、元素含量、形貌特征以及离子导电性能.结果表明,在900°C烧结可以获得结构致密、离子电导率较高的纯相LATP陶瓷固体电解质.与添加助熔剂LiBO2的样品进行对比实验发现,采用B2O3代替LiBO2作为助熔剂也可以提高烧结样品的离子电导率,并且电解质的离子电导率随助熔剂添加量的增大,先增大后减小,其中添加质量百分比为2%的B2O3的样品具有最高的室温离子电导率,为1.61×10−3S/cm.
1 引 言
解决锂离子电池的安全问题一直是规模化储能和便携式储能的研究重点,使用惰性的无机固体电解质替换易燃易爆的液体电解质,是改善锂离子电池安全问题的重要途径[1−3].锂离子无机固体电解质主要分为陶瓷电解质(晶态)和玻璃电解质(非晶态)两大类[4].玻璃态电解质虽然室温下离子电导率较高,已知最高可以达到1.3×10−3S/cm[5],但玻璃是亚稳态结构,高温下性能不稳定[6].陶瓷和微晶陶瓷固体电解质电导率相对较低,但由于其结构稳定,制备成本低,是固体电解质的研究热点之一[7].目前无机固体电解质中,NASICON型结构的铝掺杂磷酸钛锂LiTi2(PO4)3(LTP)陶瓷材料,由于其结构稳定、电导率较高,受到国内外研究人员的广泛关注[8−11].
研究表明,LTP具有与锂离子半径匹配的孔道结构,使得锂离子可以顺畅传输[13].制备LTP常用的方法主要有溶胶凝胶法[13,14]、流延法[15]、喷雾干燥法[16]和固相法等.其中固相法相对简单,可控性较高.Chen[17]通过高温固相烧结得到的LTP,其室温离子电导率为2×10−6S/cm.通过烧结所得到的LTP的离子电导率较低,主要原因在于单纯烧结得到样品的空隙率较高.而使用阳离子(Fe,Al,Cr,Ga等)对Ti位进行替位式掺杂可以提高电解质的电导率[18],其中,铝掺杂的磷酸钛铝锂Li1.3Al0.3Ti1.7(PO4)3(LATP)在室温下电导率相对较高[19].这是因为,根据电荷平衡,铝掺杂会导致锂浓度增大(即Ti4+→Al3++Li+),从而使电导率增大.Hosono等研究发现,磷酸钛铝锂(LATP)电导率相较于LTP的提高主要是因为提高了晶体的致密度,导致晶界导电活化能减小,而非改善锂离子的迁移率[20].吴显明[21]在LATP制备中使用了助熔剂LiBO2,结果显示在加入助熔剂后样品致密度提高,电导率也有所提高.以上研究表明,在烧结前粉体中加入适量的助熔剂LiBO2可以改善烧结质量,增加样品致密度,提高电导率.然而,电导率的提高是否是助熔剂中引入锂源所致并未确认,是否使用无锂的助熔剂也可以提高电导率也尚未明确.
本文以碳酸锂(Li2CO3),三氧化二铝(Al2O3),二氧化钛(TiO2)和磷酸二氢铵(NH4H2PO4)为前驱物,通过固相烧结法制备了LATP固体电解质,并研究了B2O3和LiBO2两种助熔剂的加入对LATP样品离子电导率的影响.通过X射线衍射(XRD)图谱、能谱分析仪(EDS)、交流阻抗(EIS)图谱以及扫描电镜(SEM)观察,分析了两种助熔剂对固体电解质离子电导率的影响及其原因.
2 实验方法
将Li2CO3,Al2O3,TiO2和NH3H2PO4按照Li1.3Al0.3Ti1.7(PO4)3化学计量比进行称量混合,置入球磨罐,加入少量无水乙醇作为分散剂,在行星球磨机中以每分钟280转的速度球磨2 h.球磨后所得粉末在干燥箱中80°C干燥10 h,使乙醇挥发完全.干燥后的粉末置入石英舟中,于烧结炉中氩气氛围400°C煅烧2 h.所得物质再次球磨后在30 mPa压力下压制成直径为16 mm、厚度为1 mm的圆片,圆片分别在600,800,900,1000°C下烧结4 h,对比样品衍射图谱和离子电导率,确定最优烧结温度.于粉末中按照质量百分比1 wt.%—3 wt.%分别混合加入助熔剂氧化硼和偏硼酸锂,再次球磨使粉末混合均匀后按照同样方式压片,在最优烧结温度下烧结4 h,得到不同的样品烧结片.
对粉末与样品烧结片采用XRD图谱和EDS能谱分析,其结构特征与元素含量;对样品烧结片经过喷金处理后进行SEM形貌观察;通过阿基米德原理测试材料密度;利用电化学工作站对烧结样品进交流阻抗测试,分析其离子导电性能.交流阻抗测试前将样品烧结片两面使用800目金相砂纸打磨后,均匀涂抹导电银浆.样品置于铝箔中在120°C干燥箱中干燥2 h.所有测试均在25°C室温条件下进行.
3 实验结果与分析
3.1 XRD与EDS分析
通过XRD对样品的物相进行了分析,扫描角度为10°—80°.图1(a)为在不同温度下烧结的样品的XRD图谱.由图1(a)可以知,600°C时仍有中间物质AlO(OH)和Ti2O3的 (012),(120),(031)晶面衍射峰(图1(a)中*号已标出);随着温度升高到800°C,LATP结晶程度升高,中间物质AlO(OH)和Ti2O3的衍射峰完全消失,形成纯相的LATP;温度进一步升高到900和1000°C,没有新的衍射峰出现,表明无新物质生成,物相保持稳定.与LiTi2(PO4)3(LTP)的标准卡(PDF#04-006-8821)对比发现衍射峰位整体发生右移.根据布拉格方程

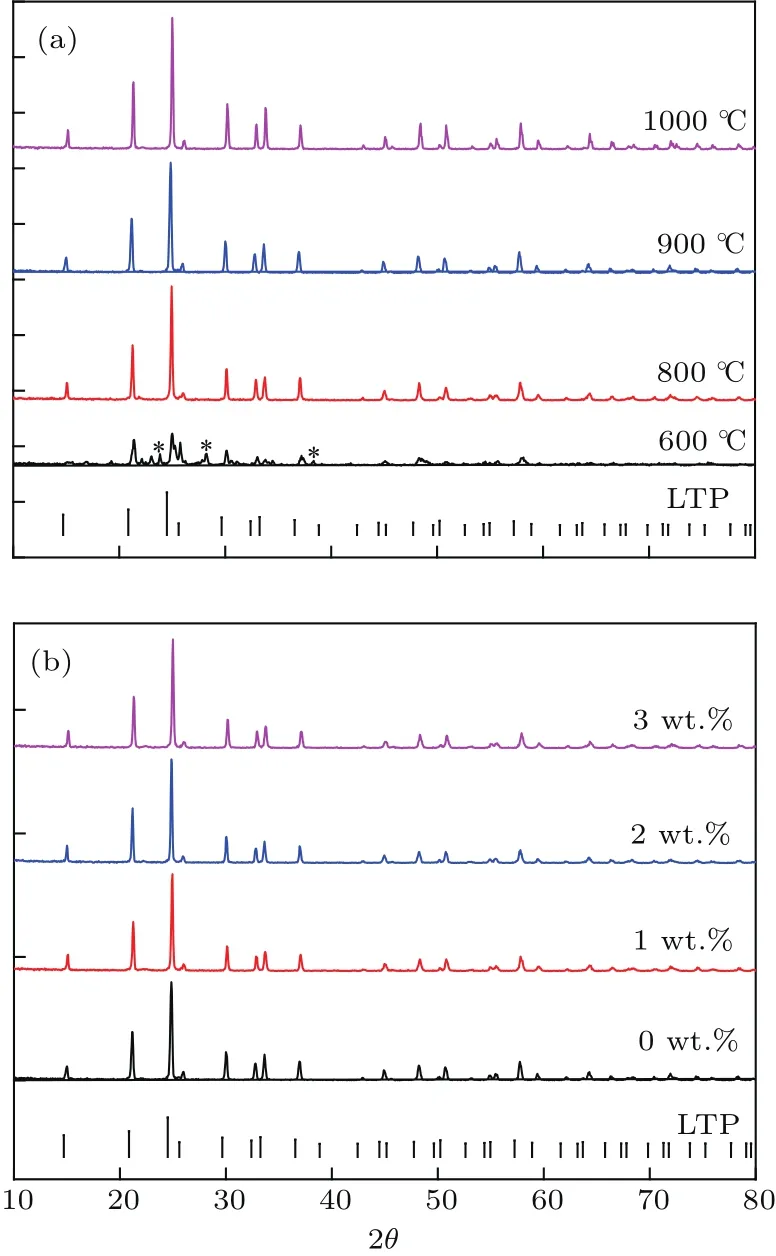
图1 XRD图谱 (a)在不同温度下(600—1000°C)烧结4 h得到的LATP样品;(b)添加不同质量百分比(0—3%)助熔剂氧化硼900°C烧结所得样品Fig.1.X-ray di ff raction pattern:(a)Sintered at various temperatures(600–1000 °C)for 4 h;(b)different percentages(0–3%)of fl ux were added then sintered at temperature 900°C for 4 h.
分析可知,XRD峰位发生右移表明Al掺杂后形成的LATP的晶面间距小于LiTi2(PO4)3的晶面间距,即晶格参数减小.这是由于进行替位式掺杂的Al离子半径小于Ti离子半径,因此造成面间距等晶格参数减小.这也从侧面说明掺杂的Al成功替换了LiTi2(PO4)3晶格中的Ti离子,从而形成了Li1.3Al0.3Ti1.7(PO4)3,这一结果与Best等[22]和Birke等[23]的研究结果一致.XRD分析进一步表明,加入适量的助熔剂氧化硼(B2O3)不会对LATP的物相产生明显影响.图1(b)为加入重量百分比为1%—3%的氧化硼、900°C烧结的LATP样品的XRD图,衍射图谱与未添加助熔剂在900°C烧结所得LATP的衍射图谱基本一致,没有出现新的衍射峰.这表明加入重量比为3%以内的氧化硼(B2O3)能够保证LATP的物相稳定.对烧结温度为900°C的样品进行EDS分析,如图2所示,可知铝、钛、磷、氧的元素比基本符合Li1.3Al0.3Ti1.7(PO4)3中的元素比值,该结果与XRD图谱结果一致,同样说明生成的物质为LATP.
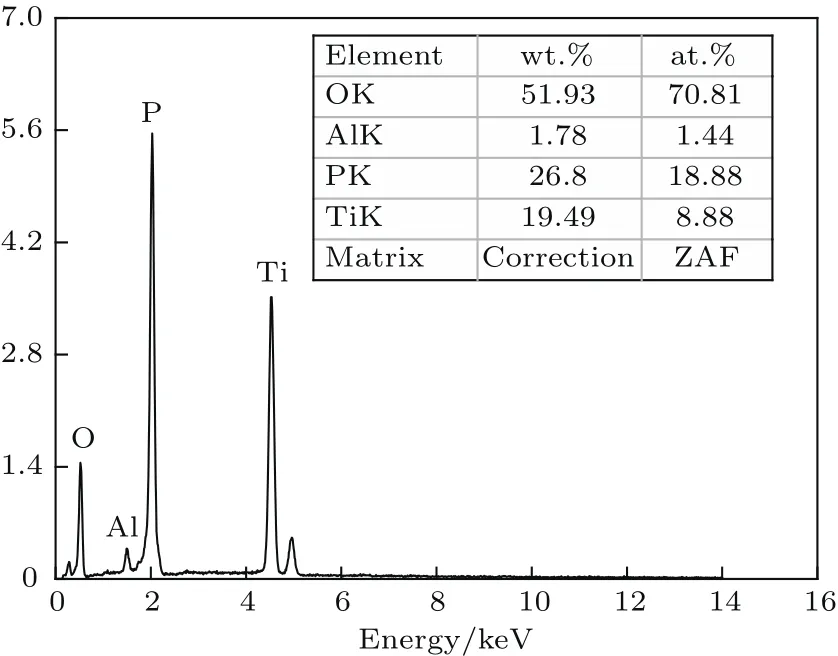
图2 烧结温度为900°C的LATP样品的EDS能谱分析Fig.2.EDS of LATP sintered at temperature 900°C.
3.2 SEM分析
采用SEM对添加助熔剂氧化硼前后的LATP烧结样品进行了形貌观察和分析.图3(a)为未添加助熔剂的LATP样品的SEM图片;图3(b)—3(d)分别为添加助熔剂质量百分比为1%—3%的LATP烧结样品的SEM图片,图中所有样品烧结温度均为900°C.由SEM图可知,四种烧结样品的颗粒大小较为均匀,平均粒径约为1µm.从图3(a)中可以观察到未添加助熔剂的样品颗粒之间存在明显的间隙,材料空隙率较高;由图3(b)可以发现,助熔剂B2O3的加入,使得样品颗粒之间间隙减小,空隙率降低,改善了材料的致密性;随着助熔剂B2O3添加量达到2%,颗粒之间已无明显的空隙,如图3(c)所示;当添加B2O3质量百分比达到3%时,颗粒边界变得模糊.这是由于助熔剂B2O3为无定形态,在450°C时会完全融化,远低于烧结温度900°C,在烧结过程中B2O3会融化形成液相促进烧结,并填充于颗粒间隙之中.降温冷却过程中,融化的B2O3有部分会依附在样品表面,形成非晶态薄膜层,这与吴显明等[21]添加助熔剂LiBO2的实验结果类似.表明助熔剂B2O3的加入,填充了粒间空隙,从而降低了材料空隙率,改善了LATP固体电解质的致密性.

图3 烧结温度为900°C的LATP样品的SEM图片 (a)未添加助熔剂;(b)氧化硼质量分数1%;(c)氧化硼质量分数2%;(d)氧化硼质量分数3%Fig.3.Scanning electron microscope(SEM)microphotographs of LATP thick fi lms sintered at temperature 900°C:(a)Fluxless;(b)1 wt.%B2O3;(c)2 wt.%B2O3;(d)3 wt.%B2O3.
3.3 EIS分析
使用电化学工作站(ParStat4000)对添加助熔剂前后的LATP烧结样品进行了交流阻抗测试.图4为未添加助熔剂时LATP在不同温度下(600—1000°C)烧结的样品的交流阻抗图谱,测试温度为25°C.EIS图谱都是由高频部分一个近似的半圆和低频部分一条斜线组成的,半圆表示电子与锂离子在导电结合处的电荷传输过程,斜线则与锂离子在活性材料内部固体扩散过程相关.高频时,半圆左侧截距为电解质和电极夹等的系统电阻;而随着频率降低,电解质界面层间电容对电流的阻碍作用越来越大,直至停止导电,这时半圆右侧截距即为材料电阻,由电荷传递阻抗与系统电阻串联组成[24].根据半圆右侧截距R和公式[16,25]

其中σ为离子电导率,L为样品片厚度,R为电阻,S为有效面积,计算后发现离子电导率随着烧结温度的增大先增大再减小,并且在烧结温度为900°C时,烧结样品具有最高离子电导率,为4.16×10−4S/cm.这一结果与Arbi等[27]与Morimoto等[28]报道的数据具有相同的数量级.结合XRD图谱对材料样品的晶粒尺寸进行计算,根据Scherrer公式
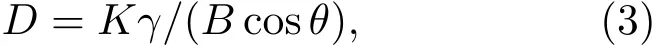
其中K为Scherrer常数,γ为X射线波长,B为衍射峰半高宽,θ为衍射角,D为晶粒垂直于晶面方向的平均厚度,计算得到烧结温度600,800,900,1000°C的样品平均晶粒尺寸分别为33.1,75.4,78.5,90.4 nm.可见随烧结温度上升,晶粒尺寸呈持续增大趋势.图5为不同温度下烧结的样品与添加助熔剂并900°C烧结的样品的密度.由图可见,样品的密度随着烧结温度的升高而增大,这与晶粒生长相符合.这一结果与何海亮[28]与朱宇豪等[29]研究烧结温度对LATP颗粒尺寸影响的结果一致.烧结温度较低时(600,800°C),晶粒未生长成熟,密度较低,导致LATP中晶界阻抗较大,离子电导率较低;当温度升高到900°C,晶粒熔融生长,促进了晶粒之间的良好衔接,晶体密度增大,LATP中的晶界阻抗变小,离子电导率升高;当烧结温度高于900°C时,晶粒继续熔融生长,大晶粒数量增多而小晶粒数量减少,虽然密度继续增大,但粒间总接触面积减小,导致LATP晶界阻抗再次变大,离子电导率降低.
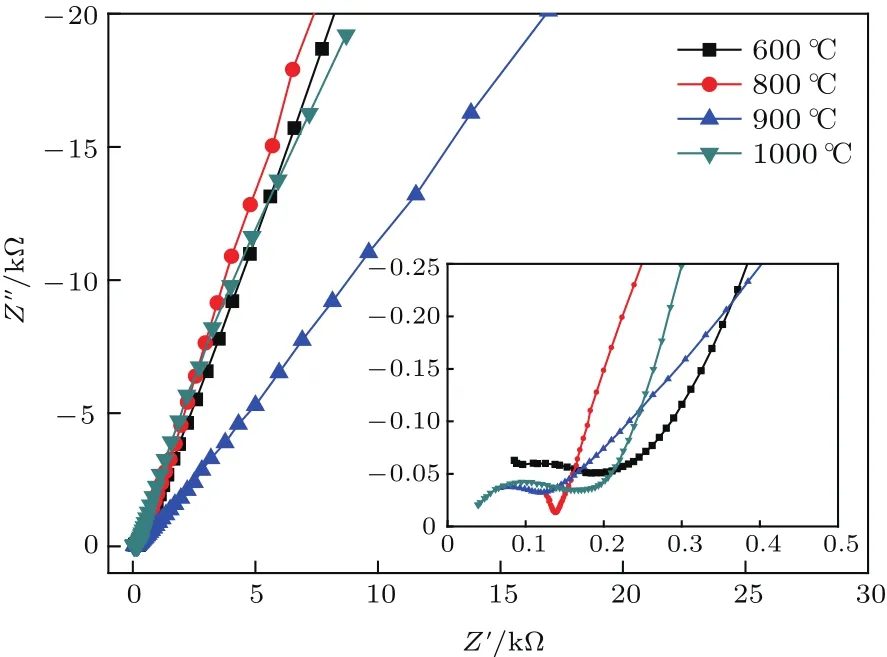
图4 (网刊彩色)不同温度(600—1000°C)下烧结4 h样品的交流阻抗图谱Fig.4. (color online)Alternating-current impedance spectra of samples sintered at different temperatures(600–1000 °C)for 4 h.
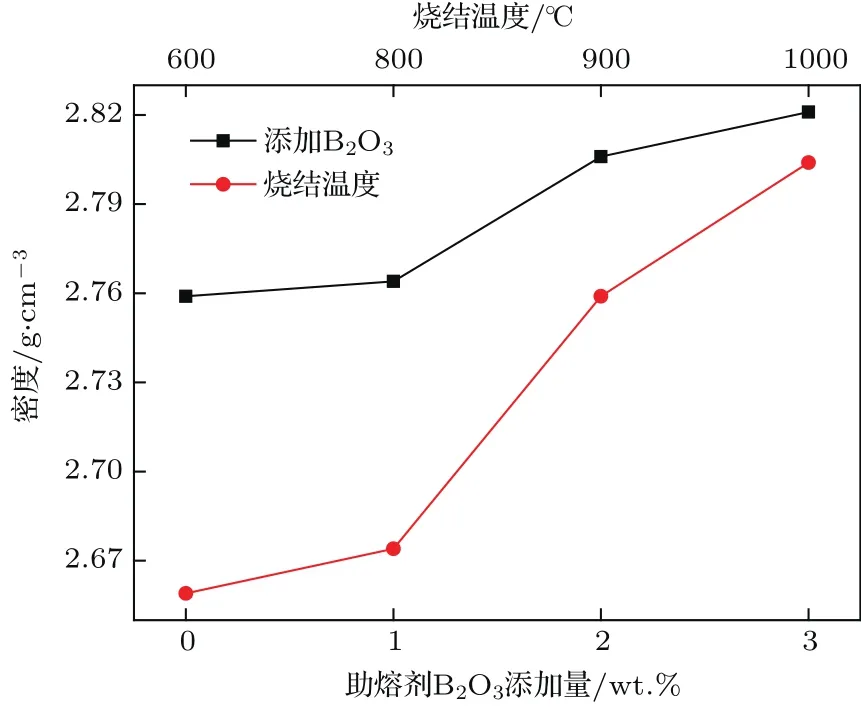
图5 不同烧结温度的LATP和900°C烧结的含氧化硼的LATP的密度Fig.5.Density of LATP obtained at different sintering temperatures and LATP sintered at 900°C with added fl ux B2O3.
图6为添加助熔剂B2O3与LiBO2前后900°C烧结样品的交流阻抗图谱.对比数据发现,添加助熔剂后样品的EIS曲线中半圆与斜线的连接点左移,电阻R减小,根据(2)式可知材料的离子电导率有所增加.图7为添加助熔剂B2O3和LiBO2前后LATP烧结样品的离子电导率.由图可知,在添加两种助熔剂后,LATP样品的离子电导率都有所提高,并均在助熔剂添加量为2 wt.%时达到最大值,其中添加助熔剂B2O3的样品离子电导率最高可达1.61×10−3S/cm.结合图5和图7可知,助熔剂添加量增大到3 wt.%时,虽然样品密度仍然有所提升,但样品的离子电导率则开始下降,这是因为过量的加入助熔剂会使样品内部粒间间隙中非晶物质和表面非晶层厚度持续增加,而形成的非晶层会阻碍锂离子在电解质中的传输,从而降低样品的电导率.对比图7中数据可知,相比于添加助熔剂偏硼酸锂的样品,添加氧化硼的样品具有更高的离子电导率,可见不含锂的助熔剂B2O3的加入同样可以改善LATP样品的致密性,提高LATP离子电导率.
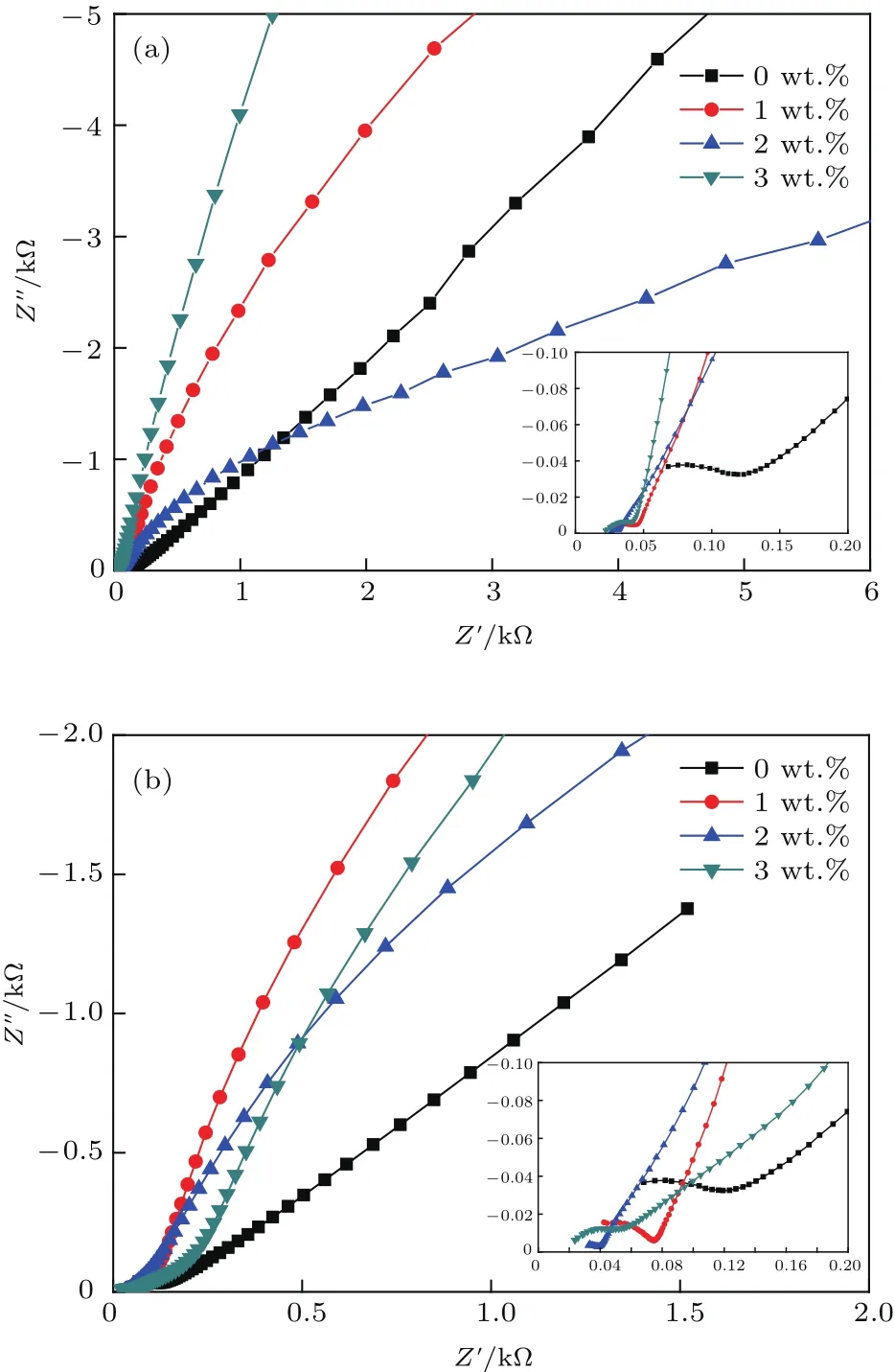
图6 LATP烧结片在室温下的交流阻抗图谱 (a)添加不同质量分数的B2O3;(b)添加不同质量分数的LiBO2Fig.6.Alternating–current impedance spectra at room temperature for thick fi lms:(a)With different mass fraction B2O3added;(b)with different mass fraction LiBO2 added.
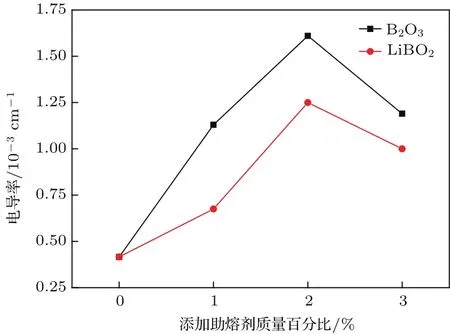
图7 添加不同质量百分比的助熔剂B2O3与LiBO2的样品的电导率Fig.7. Conductivity of the samples with different mass percent fl uxes of B2O3and LiBO2added.
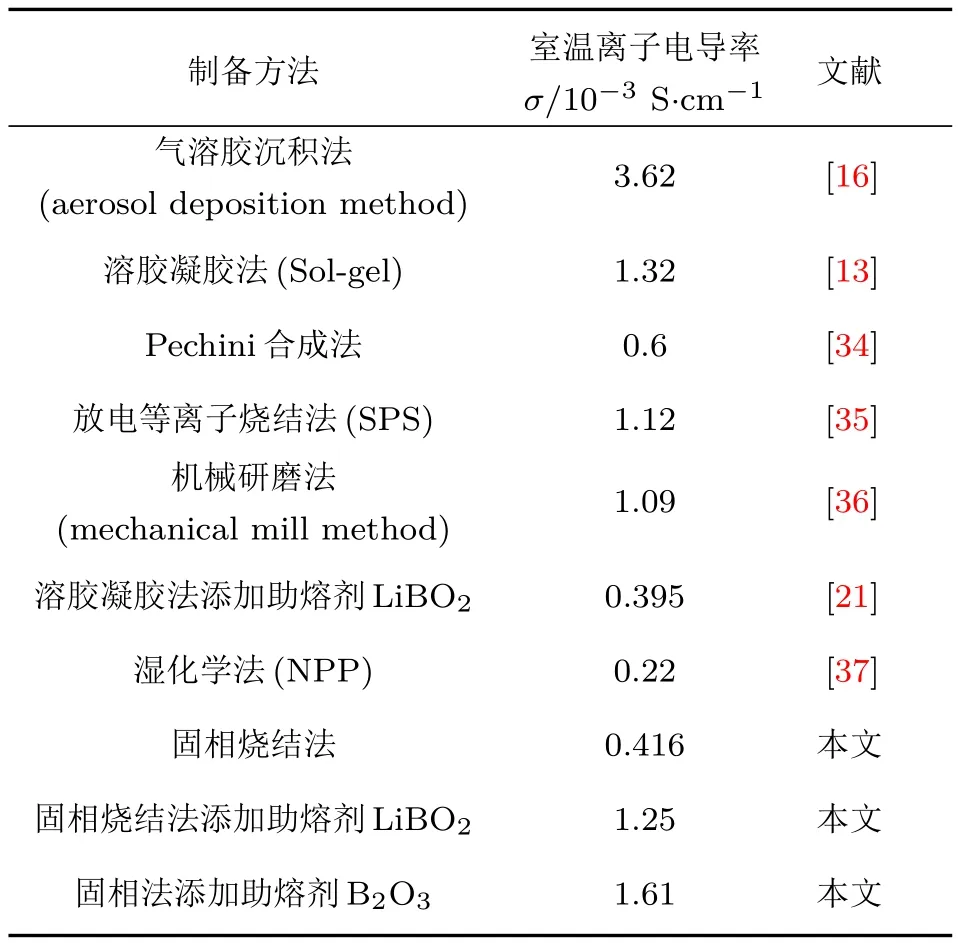
表1 不同方法制备的LAPT的离子电导率Table 1.Ion conductivity of LATP prepared by different methods.
采用固相法制备LATP固体电解质,发现在烧结时添加适量无锂助熔剂B2O3可以提高LATP样品的离子电导率,最高可达1.61×10−3S/cm.总结了近年来采用不同方法制备的LATP样品的离子电导率,如表1所列.其中Popovici等[30]与本文工作中的LATP样品离子电导率均达到10−3S/cm数量级,这一电导率基本满足了锂离子电池对固体电解质离子电导率的要求.但是机械研磨时间较长,气溶胶沉积与放电等离子烧结工艺要求高、可控性较低,与之相比本文采用的固相法较为简单,可控性较高,且同样可以制备出离子电导率较高的LATP固体电解质.LATP是目前所知的固体电解质中较为适合制作锂空气电池与全固态锂离子电池的一种.同时性能优越的正负极材料层出不穷,这为LATP组成全固态锂离子电池与锂空气电池提供了更多的电极选择[31−33].虽然LATP固体电解质离子电导率较高,但是较高的烧结温度降低了其工艺适配性.而且在电池制作过程中,由于LATP容易与金属锂反应,并且与电极接触时界面阻抗较大[1],目前难以实现良好的界面稳定性.如何防止LATP中钛离子与电极材料中锂金属接触时反应[35],以及减小电极材料和LATP固体电解质之间的界面阻抗,提高其工艺适配性是后续工作中需要进一步解决的问题.
4 结 论
在600—1000°C温度下采用固相烧结法制备了LATP固体电解质,样品颗粒均匀,物相稳定,离子电导率最高可达4.16×10−4S/cm.添加含锂助熔剂LiBO2或不含锂助熔剂B2O3后LATP样品离子电导率均得到改善,其中以B2O3为助熔剂的LATP样品具有更高的离子电导率.此外,LATP样品的离子电导率随助熔剂含量的增加先增大后减小,并且添加2 wt.%的B2O3的样品离子电导率高达1.61×10−3S/cm,显著改善了LATP的Li离子输运性能.不含锂助熔剂B2O3的使用进一步表明助熔剂的加入对LATP固体电解质离子电导率的改善,主要原因是改善了电解质的致密度,降低了电解质的晶界阻抗.
[1]Han F,Gao T,Zhu Y,Gaskell K J,Wang C 2015Adv.Mater.27 3473
[2]Ma Q,Xu Q,Tsai C L,Tietz F,Guillon O 2016J.Am.Ceram.Soc.99 410
[3]MonchakM,HupferT,SenyshynA,BoysenH,Chernyshov D,Hansen T,Schell K G,Bucharsky E C,Ho ff mann M J,Ehrenberg H 2016Inorg.Chem.55 6
[4]Zheng H H,Qu Q T,Liu Y W,Xu Z Y 2007Chin.J.Power Sources31 349(in Chinese)[郑洪河,曲群婷,刘云伟,徐仲榆2007电源技术31 349]
[5]Fu J 1997Solid State Ionics96 195
[6]Matsuo T,Shibasaki M,Katsumata T 2002Solid State Ionics154 759
[7]Guo W H,Xiao H,Men C L 2015Acta Phys.Sin.64 077302(in Chinese)[郭文昊,肖惠,门传玲2015物理学报64 077302]
[8]Shimonishi Y,Tao Z,Imanishi N,Im D,Dong J L,Hirano A,Takeda Y,Yamamoto O,Sammes N 2011J.Power Sources196 5128
[9]Bucharsky E C,Schell K G,Hintennach A,Ho ff mann M J 2015Solid State Ionics274 77
[10]Kotobuki M,Koishi M,Kato Y 2013Ionics19 1945
[11]Schroeder M,Glatthaar S,Binder J R 2011Solid State Ionics201 49
[12]Wang C Z 2000Solid Electrolyte and Chemical Sensors(Beijing:Metallurgical Industry Press)p138(in Chinese)[王常珍 2000固体电解质和化学传感器 (北京:冶金工业出版社)第138页]
[13]Sun M R,Wang Z X,Li X H,Guo H J,Peng W J 2013Chin.J.Nonferrous Met.2 469(in Chinese)[苏明如,王志兴,李新海,郭华军,彭文杰 2013中国有色金属学报2 469]
[14]Ma Q,Xu Q,Tsai C L,Tietz F,Guillon O 2016J.Am.Ceram.Soc.99 410
[15]Jiménez R,Campo A D,Calzada M L,Sanz J,Kobylianska S D,Solopan S O,Belous A G 2016J.Electrochem.Soc.163 1653
[16]Popovici D,Nagai H,Fujishima S,Akedo J 2011J.Am.Ceram.Soc.94 3847
[17]Chen H,Tao H,Wu Q,Zhao X 2013J.Am.Ceram.Soc.96 801
[18]Kothari D H,Kanchan D K 2016Physica B:Condens.Matter501 90
[19]Zhu Y M,Ren X F,Li N 2010Chem.Bull.73 1073(in Chinese)[朱永明,任雪峰,李宁 2010化学通报 73 1073]
[20]Hosono H,Tsuchitani F,Imai K,Maeda Y A M 1994J.Mater.Res.9 755
[21]Wu X M,Xiao Z B,Ma M Y,Chen S 2011J.Chin.Ceram.Soc.39 329(in Chinese)[吴显明,肖卓炳,麻明友,陈上2011硅酸盐学报39 329]
[22]Best A S,Forsyth M,Macfarlane D R 2000Solid State Ionics136–137 339
[23]Birke P,Salam F,Döring S,Weppner W 1999Solid State Ionics118 149
[24]Churikov A V,Gamayunova I M,Shirokov A V 2000J.Solid State Electrochem.4 216
[25]Thevenin J 1985J.Power Sources14 45
[26]Arbi K,Bucheli W,Jiménez R,Sanz J 2015J.Eur.Ceram.Soc.35 1477
[27]Morimoto H,Hirukawa M,Matsumoto A,Kurahayashi T,Ito N,Tobishima S I 2014Electrochem.82 870
[28]He H L,Wu X M,Chen S,Ding Q C,Chen S B 2015J.Synth.Cryst.44 1(in Chinese)[何海亮,吴显明,陈上,丁其晨,陈守彬2015人工晶体学报44 1]
[29]Zhu Y H,Wang H,Zheng C M 2016Guangzhou Chem.Ind.44 15(in Chinese)[朱宇豪,王珲,郑春满 2016广州化工44 15]
[30]Zhou C,Li H Q,Qiao K,Zhang J,Tang Q 2014Adv.Mater.Ind.3 40(in Chinese)[周矗,李合琴,乔恺,张静,唐琼2014新材料产业3 40]
[31]Li J,Ru Q,Hu S J,Guo L Y 2014Acta Phys.Sin.63 168201(in Chinese)[李娟,汝强,胡社军,郭凌云 2014物理学报63 168201]
[32]Bai X J 2014Acta Phys.-Chim.Sin.33 337(in Chinese)[白雪君2014物理化学学报33 337]
[33]Ma H,Liu L,Lu X S,Liu S P,Shi J Y 2015Acta Phys.Sin.64 248201(in Chinese)[马昊,刘磊,路雪森,刘素平,师建英2015物理学报64 248201]
[34]Liu P,Ma Q,Fang Z,Ma J,Hu Y S,Zhou Z B,Li H,Huang X J,Chen L Q 2016Chin.Phys.B25 97
[35]Zhao E,Ma F,Jin Y,Kanamura K 2016J.Alloys Compd.680 646
[36]Xu X,Wen Z,Yang X,Chen L 2008Mater.Res.Bull.43 2334
[37]Xu X,Wen Z,Yang X,Zhang J,Gu Z 2006Solid State Ionics177 2611
[38]Liu Y L,Zhang H,Xue D,Cui B,Li Z C 2012Chin.J.Nonferrous Met.22 144(in Chinese)[刘玉龙,张鸿,薛丹,崔彬,李志成2012中国有色金属学报22 144]
E ff ect of lithium-free fl ux B2O3on the ion conductivity of Li1.3Al0.3Ti1.7(PO4)3solid electrolyte∗
Shi Mao-LeiLiu Lei†Tian Fang-HuiWang Peng-FeiLi Jia-Jun Ma Lei
(College of Electronic and Information Engineering,Hebei University,Baoding 071002,China)
3 March 2017;revised manuscript
9 June 2017)
Using solid electrolyte instead of liquid electrolyte is regarded as an important measure to solve the safety problems of lithium ion batteries,and has attracted wide attention of researchers.Among many solid electrolytes,Li1.3Al0.3Ti1.7(PO4)3(LATP)is considered to be one of the most commercially available solid electrolytes for its high ionic conductivity.However,as a replacement substitute of for liquid electrolyte,the LATP solid electrolyte has an ionic transport property of LATP solid electrolyte that still needs to be improved.In this paper,LATP solid electrolyte used for lithium ion batteries is successfully prepared by solid reaction process,and the in fl uences of different sintering temperatures and addition of fl ux B2O3and or LiBO2on the ionic conductivity of LATP solid electrolyte are discussed.The structures,element content,morphologies,and ionic conductivities of the sintered samples are investigated at room temperature by X-ray di ff raction,energy dispersive spectrometer,electrochemical impedance spectrum and scanning electron microscopy.It is found that pure phase LATP ceramic solid electrolyte can be obtained at the sintering temperatures between 800 and 1000°C.And the ionic conductivities of the samples fi rst increase fi rst and then decrease with the increasing sintering temperatures increasing.The sample with a highest ionic conductivity of 4.16×10−4S/cm can be obtained at the a sintering temperature of 900°C.Further research shows that the ionic conductivities of the sintered samples can also be e ff ectively improved by using B2O3instead of LiBO2as fl ux.Moreover,the ionic conductivities of the samples fi rst increase fi rst and then decrease with the increasing amount of the fl ux increasing.And the highest ionic conductivity of 1.61×10−3S/cm is obtained with the sampleby adding B2O3with a mass fraction of 2%into the sample.The results indicate that the elevating of sintering temperature and the adding of fl ux B2O3and or LiBO2can both decreasing reducing the grain boundary impedances of the LATP samples,so as to thereby improve improving their ionic conductivities.However,when the sintering temperature is higher than 900°C or the amount of fl ux B2O3and or LiBO2exceeds the mass percentage of 2%,the ionic conductivities of the LATP samples will drop.In addition,the ionic conductivities of the samples used using B2O3as fl ux are higher than that those of the samples used LiBO2as fl ux.These results also indicate that the increases of ionic conductivities of LATP samples with fl ux is are closely related to their densities density and compactness,and is irrespective of no matter whether or not the fl ux contains lithium ion.
solid electrolyte,Li1.3Al0.3Ti1.7(PO4)3, fl ux,solid state sintered technology.
(2017年3月3日收到;2017年6月9日收到修改稿)
10.7498/aps.66.208201
∗国家自然科学基金(批准号:61204079)、河北省自然科学基金(批准号:F2017201130)和河北省青年拔尖人才计划资助的课题.
†通信作者.E-mail:thesisliu@163.com
©2017中国物理学会Chinese Physical Society
http://wulixb.iphy.ac.cn
PACS:82.47.Aa,66.30.–h,82.45.GjDOI:10.7498/aps.66.208201
*Project supported by the National Natural Science Foundation of China(Grant No.61204079),the Natural Science Foundation of Hebei Province,China(Grant No.F2017201130),and the Youth Outstanding Talent Project of Hebei Province,China
†Corresponding author.E-mail:thesisliu@163.com

