蝉花、蛹虫草和冬虫夏草药材中脂肪酸含量的比较研究Δ
卞智慧,于瑞莲,魏思敏,蒋文,邵佳蔚,喻振,许金国,吕高虹(南京中医药大学药学院,南京210023)
蝉花、蛹虫草和冬虫夏草药材中脂肪酸含量的比较研究Δ
卞智慧*,于瑞莲#,魏思敏,蒋文,邵佳蔚,喻振,许金国,吕高虹(南京中医药大学药学院,南京210023)
目的:建立同时测定蝉花、蛹虫草和冬虫夏草药材中脂肪酸含量的方法,并比较上述药材中脂肪酸含量的差异。方法:采用气相色谱-质谱法。色谱条件:色谱柱为TG-5MS毛细管柱,载气为氮气,流速为1.2 mL/min,进样口温度为290℃,不分流进样,开阀时间为1 min,进样量为1µL;质谱条件:离子源为电喷雾电离源,离子源温度/传输线温度为280℃,色谱柱初始温度为80℃(程序升温),电离电压为70 eV,溶剂延迟时间为5 min,扫描质量范围为m/z 30~400。结果:十四烷酸、十五烷酸、软脂酸、棕榈油酸、十七碳酸、十七碳烯酸、十八烷酸、油酸甲酯、亚油酸、花生酸、花生一烯酸、花生二烯酸、二十碳三烯酸、二十一碳酸、山萮酸、二十三碳酸、木焦油酸检测质量浓度线性范围分别为1.400~44.520µg/mL(r=0.999 8)、2.091~93.721µg/mL(r=0.999 7)、3.146~85.856µg/mL(r=0.998 2)、1.664~61.444µg/mL(r=0.998 7)、1.773~64.983µg/mL(r=0.999 5)、1.781~68.421µg/mL(r=0.999 7)、1.706~55.606µg/mL(r=0.999 8)、1.439~47.989µg/mL(r=0.999 6)、1.738~66.908µg/mL(r=0.999 6)、2.086~94.206µg/mL(r=0.999 5)、1.356~44.966µg/mL(r=0.999 4)、1.444~56.814µg/mL(r=0.999 7)、1.375~52.335µg/mL(r=0.999 8)、1.512~60.312µg/mL(r=0.999 5)、1.450~59.760µg/mL(r=0.999 7)、1.427~58.757µg/mL(r=0.999 1)、1.269~58.109µg/mL(r=0.999 3);定量限≤1 764.71 ng/mL,检测限≤529.42 ng/mL;精密度、稳定性、重复性试验的RSD<2.0%;加样回收率为84.87%~108.93%(RSD为0.19%~2.23%,n=6)。蝉花、蛹虫草和冬虫夏草药材中分别含有17、16、16种脂肪酸,上述药材中不饱和脂肪酸含量均高于饱和脂肪酸含量;其中人工栽培蝉花药材样品中各种脂肪酸含量大多高于其他药材样品。结论:该方法操作简单,精密度、稳定性、重复性较好,可用于蝉花、蛹虫草和冬虫夏草药材中脂肪酸含量的同时测定;从脂肪酸含量角度讲,上述3种药材中人工栽培蝉花药材品质较优。
蝉花;蛹虫草;冬虫夏草;脂肪酸;气相色谱-质谱法
蝉花Isaria cicadae、蛹虫草Cordyceps militaris和冬虫夏草C.sinensis同属麦角菌科虫草类中药材。蝉花是我国传统的一种名贵药材,又名蝉草、蝉茸和胡蝉等,其药用部位是子座及寄主昆虫的尸体(菌核)[1],野外采摘时,去掉表面泥土,晒干研成粉末即可药用。蝉花在我国主要分布于云南、江苏、浙江、福建、四川等省区,也见于南亚、欧洲、北美等地[2],作为古籍中记载的唯一可以替代冬虫夏草的药材,有着较高的药用价值和广阔的市场前景[3]。蝉花含有腺苷、虫草酸、脂肪酸、麦角甾醇等有效成分[4-5]。脂肪酸是部分已知虫草类中药材中的重要活性成分之一,根据其碳氢主链上碳氢键饱和与否可以分为三类,即饱和脂肪酸、单不饱和脂肪酸、多不饱和脂肪酸[6-7]。饱和脂肪酸包括软脂酸、硬脂酸、花生酸等,不饱和脂肪酸包括油酸、亚油酸、亚麻酸等。
目前,对脂肪酸的分析方法主要有气相色谱-火焰离子化检测法、气相色谱-质谱法(GC-MS)等。GC-MS法具有快速、准确等优点,已广泛用于药物分析、油脂化学成分分析等方面[8-9]。本试验建立GC-MS法同时测定蝉花、蛹虫草、冬虫夏草药材中十四烷酸(C14.0)、十五烷酸(C15.0)、软脂酸(C16.0)、棕榈油酸(C16.1)、十七碳酸(C17.0)、十七碳烯酸(C17.1)、十八烷酸(C18.0)、油酸甲酯(C18.1N9C)、亚油酸(C18.2N6C)、花生酸(C20.0)、花生一烯酸(C20.1)、花生二烯酸(C20.2)、二十碳三烯酸(C20.3N6)、二十一碳酸(C21.0)、山萮酸(C22.0)、二十三碳酸(C23.0)、木焦油酸(C24.0)的含量,并对上述药材中脂肪酸含量的差异进行比较,以期为虫草类中药材的质量控制提供技术支持[10]。
1 材料
1.1 仪器
1310 ISQ型GC-MS仪(美国Thermo Finniga公司);RE-200型旋转蒸发仪(上海亚荣生化仪器厂);AG135型精密电子天平(瑞士Mettler-Toledo公司)。
1.2 试剂
脂肪酸甲酯混合对照品(批号:CDAA-251019M,纯度:>99%)、十九烷酸甲酯对照品(批号:S2257B21589,纯度:>99%)均购自美国Nu-Chek公司;甲醇为色谱纯,正己烷、氯仿、盐酸均为分析纯,水为纯化水。
1.3 药材
人工栽培蝉花药材由南京中医药大学于瑞莲副教授提供;野生蝉花药材、蛹虫草药材、冬虫夏草药材购自南京文德大药房,均经南京中医药大学于瑞莲副教授鉴定为真品。
2 方法与结果
2.1 试验条件与系统适用性考察
2.1.1色谱条件色谱柱:TG-5MS毛细管柱(30 m×0.25 mm×0.25 μm);载气:氮气;流速:1.2 mL/min;进样口温度:290℃;不分流进样;开阀时间:1 min;进样体积:1µL。
2.1.2 质谱条件离子源:电喷雾电离源;离子源温度/传输线温度:280℃;色谱柱温度:初始温度80℃,程序升温(80℃保持1 min,以10℃/min的速率升温至200℃;以5℃/min的速率升温至250℃;以2℃/min的速率升温至270℃,保持3 min);电离电压:70 eV;溶剂延迟时间:5 min;扫描质量范围:m/z 30~400。
在上述试验条件下,理论板数以C17.0峰计>5 000;各待测峰之间分离良好,详见图1。
2.2 溶液的制备
2.2.1 混合对照品溶液取脂肪酸甲酯混合对照品25 mg,一次性加正己烷溶解制成脂肪酸甲酯质量浓度为500µg/mL的混合对照品母液,冻存;精密量取上述混合对照品母液2 mL,置于10 mL量瓶中,加正己烷溶解并定容,制成脂肪酸甲酯质量浓度为100µg/mL的混合对照品溶液。
2.2.2 供试品溶液取药材样品适量,60℃烘干,粉碎,过60目筛,取样品粗粉80~100 mg,置于15 mL离心管中,加5%盐酸溶液-甲醇(1∶1,V/V)2 mL、氯仿-甲醇3 mL、十九烷酸甲酯对照品溶液(内标液,10µg/mL)100µL,置于85℃水浴锅中水浴加热1 h;加热完成后,待温度降至室温,再加正己烷1 mL,振荡萃取2 min,静置1 h;取上清液100µL,置于1 mL量瓶中,加正己烷定容;经0.45µm微孔滤膜滤过,取续滤液,4℃下密封贮藏,即得。
2.3 线性关系考察
分别精密量取“2.2.1”项下混合对照品母液适量,置于10 mL量瓶中,加正己烷稀释,制成脂肪酸甲酯质量浓度分别为10、50、100、300、500µg/mL的系列混合对照品溶液,均加入“2.2.2”项下内标液100µL。精密量取上述系列混合对照品溶液各1 μL,按“2.1”项下试验条件进样测定,记录离子信号相对强度。以脂肪酸甲酯质量浓度(x,μg/mL)为横坐标、离子信号相对强度(y)为纵坐标进行线性回归。回归方程与线性范围见表1。
2.4 定量限与检测限考察
分别精密量取“2.2.1”项下混合对照品溶液适量,倍比稀释,并按“2.1”项下试验条件进样测定,当信噪比为10∶1时,得定量限;当信噪比为3∶1时,得检测限,详见表1。
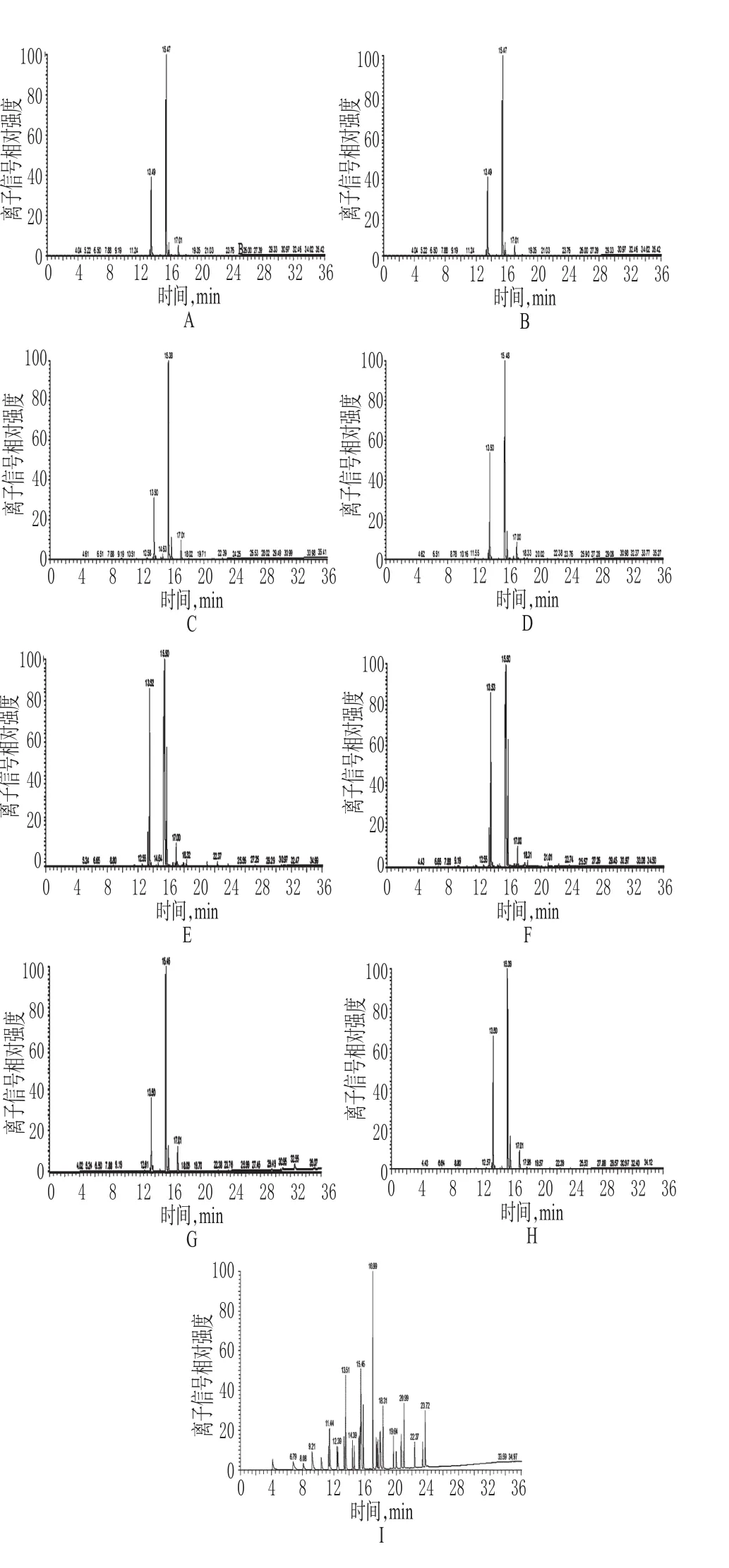
图1 提取离子流图Fig 1 Chromatograms of extraction ion flow
2.5 精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下试验条件连续进样测定6次,记录离子信号相对强度。结果,各脂肪酸甲酯成分与内标离子信号相对强度比值的RSD均<2.0%(n=6),表明仪器精密度良好。
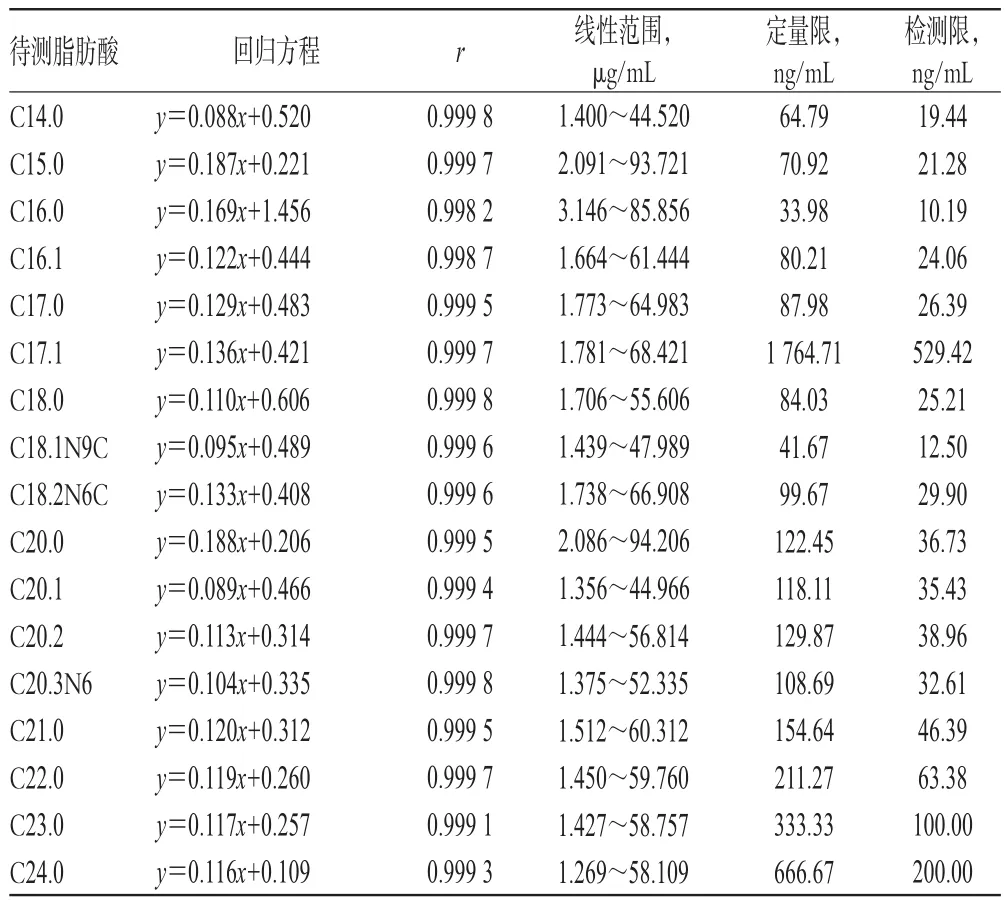
表1 回归方程、线性范围与定量限、检测限Tab 1 Regression equations,linear ranges,limits ofquantification and limits of detection
2.6 稳定性试验
取“2.2.2”项下蛹虫草药材供试品溶液适量,分别于室温下放置0、1、2、4、6、8 h时按“2.1”项下试验条件进样测定,记录离子信号相对强度。结果,各脂肪酸甲酯成分与内标离子信号相对强度比值的RSD均<2.0%(n=6),表明供试品溶液室温放置8 h内基本稳定。
2.7 重复性试验
精密称取同一批蛹虫草药材样品适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下试验条件进样测定,记录离子信号相对强度。结果,各脂肪酸甲酯成分与内标离子信号相对强度比值的RSD均<2.0%(n=6),表明本方法重复性良好。
2.8 加样回收率试验
取蛹虫草药材样品粉末6份,每份50 mg,分别加入一定质量的混合对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下试验条件进样测定,记录离子信号相对强度并计算加样回收率,结果见表2。

续表2Continued Tab 2
2.9 药材样品中脂肪酸含量的测定
取药材样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下试验条件进样测定,记录离子信号相对强度并计算样品含量,结果见表3(表中“0”为低于定量限)。
由表3可知,各虫草类中药材中C18.1N9C的含量最高,其次为C18.2N6C。蝉花药材中含有17种脂肪酸,蛹虫草和冬虫夏草药材中各含有16种脂肪酸,其中,C20.3N6为蝉花药材所特有,可以用于与蛹虫草和冬虫夏草进行区分。

表3 药材样品中脂肪酸含量的测定结果(n=3,g/kg)Tab 3 Results of content determination of fatty acid in samples(n=3,g/kg)
3 讨论
本试验优选出的GC-MS法,对几种虫草类中药材及其不同部位中的脂肪酸(测定脂肪酸甲酯换算得脂肪酸)含量进行了定量分析,并进行了方法学考察。结果显示,17种脂肪酸的加样回收率为84.87%~108.93%,RSD为0.19%~2.23%(n=6),检测质量浓度线性范围为1.400~94.206 ng/mL(r>0.999)。
GC-MS分析表明,蝉花、蛹虫草和冬虫夏草药材中所含的脂肪酸均以不饱和脂肪酸(油酸和亚油酸)为主。人工栽培蝉花药材中各脂肪酸(尤其是油酸和亚油酸)含量较野生品及蛹虫草、冬虫夏草药材高。
综上所述,本方法操作简单,精密度、稳定性、重复性较好,可用于蝉花、蛹虫草和冬虫夏草药材中的脂肪酸含量的同时测定;从脂肪酸含量角度讲,上述3种药材中人工栽培蝉花药材品质较优。
[1] 李冰岚.蝉药的本草学考证[J].现代应用药学,1993,10(2):22.
[2] 刘波.中国药用真菌[M].2版.太原:山西人民出版社,1978:27.
[3] 陈万群,陈古荣.冬虫夏草代用品研究进展[J].中草药,1994,25(5):269.
[4] 刘肖肖,李淑林,陆瑞利,等.液相色谱-电喷雾飞行时间质谱法同时测定虫生真菌菌丝中16种游离氨基酸[J].食品与发酵工业,2013,39(1):181-186.
[5] 贺亮,马素云,程俊文,等.药用真菌蝉拟青霉生物活性物质的研究进展[J].食品与生物技术学报,2012(1):8-16.
[6] Akira H,Takafumi H,Atsuhiko I,et al.Free fatty acid receptors and their physiological role in metabolic regulation[J].Yakngaku Zasshi,2011,131(12):1683-1689.
[7] Guo LX,Xiao MX,Wu CF,et al.Fatty acid composition of liquids in wild Cordyceps sinensis from major habitats in China[J].Biomed Prev Nutr,2012,2(1):42-50.
[8] 吴健,孙东东,李祥,等.板蓝根脂溶性成分的GC-MS分析[J].中国药房,2008,19(30):2354-2356.
[9] Yang FQ,Feng K,Zhao J,et al.Analysis of sterols and fatty acids in natural and cultured Cordyceps by one-stepderivatization followed with gas chromatography-massspectrometry[J].J Pharm Biomed Anal,2009,49(5):1172-1178.
[10] Cui HY,Li TH,Song B,et al.GC-MS Analysis of fatty acids from Cordyceps guang dongensis[J].J Edib Fungi,2012,2(1):89-92.
Comparative Study on the Contents of Fatty Acids in Isaria cicadae,Cordyceps militaris and Cordyceps sinensis
BIAN Zhihui,YU Ruilian,WEI Simin,JIANG Wen,SHAO Jiawei,YU Zhen,XU Jinguo,LYU Gaohong(College of Pharmacy,Nanjing University of TCM,Nanjing 210023,China)
OBJECTIVE:To establish a method for simultaneous determination of fatty acids in Isaria cicadae,Cordyceps militaris and C.sinensis,and to compare the difference of the contents of fatty acids among above medicinal herbs.METHODS:GCMS method was adopted.Chromatographic condition:the determination was performed on TG-5MS gas phase capillary column with carrier gas of nitrogen at the flow rate of 1.2 mL/min.The inlet temperature was 290℃by splitless sampling;valve opening time was 1 min,and volume of sample was 1µL.Mass spectrometry condition:the ion source is an electrospray ionization source.The temperatures of ion source and transmission line were 280℃,the initial temperature of the chromatographic column was 80℃(gradient elution),ionization voltage was 70 eV.Solvent delay time was 5 min,and scan mass range was m/z 30-400.RESULTS:The linear ranges of tetradecanoic acid,pentadecanoic acid,palmitic acid,palmitoleic acid,heptadecanoic acid,heptadecenoic acid,docosahexaenoic acid,methyl oleate,linoleic acid,arachidonic acid,eicosenoic acid,diolefinic acid,eicosatrienoic acid,heneicosanoic acid,behenic acid,tricosanoic acid,lignoceric acid were 1.400-44.520µg/mL(r=0.999 8),2.091-93.721µg/mL(r=0.999 7),3.146-85.856µg/mL(r=0.998 2),1.664-61.444µg/mL(r=0.998 7),1.773-64.983µg/mL(r=0.999 5),1.781-68.421µg/mL(r=0.999 7),1.706-55.606µg/mL(r=0.999 8),1.439-47.989µg/mL(r=0.999 6),1.738-66.908µg/mL(r=0.999 6),2.086-94.206µg/mL(r=0.999 5),1.356-44.966µg/mL(r=0.999 4),1.444-56.814µg/mL(r=0.999 7),1.375-52.335µg/mL(r=0.999 8),1.512-60.312µg/mL(r=0.999 5),1.450-59.760µg/mL(r=0.999 7),1.427-58.757µg/mL(r=0.999 1),1.269-58.109µg/mL(r=0.999 3),respectively.The limit of quantitation was no more than 1 764.71µg/mL,and the limit of detection was no more than 529.42µg/mL.RSDs of precision,stability and reproducibility tests were all lower than 2.0%.The recoveries were 84.87%-108.93%(RSD ranged 0.19%-2.23%,n=6).There were 17 fatty acids in C.militaris,16 fatty acids in I.cicadae and 16 fatty acids in C.sinensis.The contents of unsaturated fatty acids in above medicinal herbs were higher than that of saturated fatty acids.The content of fatty acids in artificial cultivated I.cicadae was mostly higher than other medicinal herbs.COCLUSIONS:The method is simple,accurate,stable and reproducible.It can be used for simultaneous determination of fatty acids in I.cicadae,C.militaris and C.sinensis.Above 3 kinds of medicinal materials.From the perspective of fatty acid content,the quality of artificial cultivated I.cicadae is best.
Isaria cicadae;Cordyceps militaris;Cordyceps sinensis;Fatty acid;GC-MS
R932
A
1001-0408(2017)30-4252-05
DOI10.6039/j.issn.1001-0408.2017.30.20
国家自然科学基金资助项目(No.81673918);江苏省普通高校专业学位研究生创新计划项目(No.SJZZ15-0122);江苏省科技项目(No.BY2015008-03);江苏高校优势学科建设工程项目(No.2011ZYX6-006)
*硕士研究生。研究方向:中药新药开发。E-mail:343793122@qq.com。
#通信作者:副教授,硕士生导师,博士。研究方向:中药新药开发。E-mail:yu3ruilian@126.com
2016-12-03
2017-02-05)
(编辑:张静)

