生育酚的薄层色谱快速定性分析
张 翼,郭永红,胡志雄*,齐玉堂
1.武汉中学 (武汉 430061)2.武汉轻工大学食品科学与工程学院 (武汉 430023)
2017-08-21
张 翼,男,1999年出生。
*通讯作者:胡志雄,男,1971年出生,副教授,博士,主要研究领域为色谱分析。
生育酚的薄层色谱快速定性分析
张 翼1,郭永红2,胡志雄2*,齐玉堂2
1.武汉中学 (武汉 430061)2.武汉轻工大学食品科学与工程学院 (武汉 430023)
建立了一种快速、简单的生育酚单体(α-,γ-和δ-生育酚)的薄层色谱定性分析方法。以硅胶为分离介质,系统考察了由4种溶剂为基础溶剂(环己烷、二氯甲烷、石油醚和氯仿)共38种溶剂体系为展开剂的分离效果。实验结果表明:当采用100%二氯甲烷、二氯甲烷-乙醚(98∶2,v/v)、二氯甲烷-乙酸乙酯(98∶2,v/v)、100%氯仿、氯仿-乙酸乙酯(98∶2,v/v)、氯仿-乙醚(98∶2和95∶5,v/v)为展开剂时,均能分离3种生育酚单体。其中100%二氯甲烷因具有展开时间短和操作简单的优点,成为最适宜建立快速、简单薄层色谱分离的展开剂。在此分离体系条件下,分离展开时间仅需7 min,α-, γ-和δ-生育酚的比移值分别为0.69,0.55和0.43。
生育酚;维生素E;薄层色谱;定性分析
生育酚是维生素E的重要组成成分,进一步可分为α-,β-,γ-和δ-生育酚。它具有抗不育、清除体内自由基、抗癌、抗心血管疾病、提高免疫力和抗衰老等作用[1],近两年的科学研究表明它还具有调节细胞信号和基因表达的非抗氧化作用[2-3]。4种生育酚虽然具有相似的结构但它们的功能性存在着差异。δ-生育酚的抗氧化能力最强,作为抗氧化剂已广泛用于食品行业。α-生育酚的生理活性最高,能有效清除体内氧自由基;γ-生育酚具有一些特殊的作用,能有效地清除体内过量的NO和NO2自由基,阻止它们对蛋白质、肽和各种器官造成的损害[4]。油料及坚果类植物如大豆、花生、核桃、榛子、葵花籽等生育酚的含量较多。天然生育酚通常是从油脂精练厂的脱臭馏出物中制备。随着生育酚单体的生理功能不断被人们所认识,医药、化妆品及保健品等行业对生育酚单体的需求量在不断增大,人们想了解食品中生育酚单体组成的要求也愈发强烈。因此,建立一种简便、快捷的分析检测方法以满足人们的需要显得迫在眉睫。
目前常用的生育酚单体分析检测方法有薄层色谱、气相色谱和高效液相色谱等。后两种方法准确性好,但分析成本较高,适合于生育酚的定量分析;薄层色谱虽然准确性较差,但操作简单、成本低适合于进行快速定性分析。虽然已有薄层色谱分析生育酚的报道[5-6],但缺少系统的研究。本文选取硅胶为吸附介质,系统的考察了多种淋洗剂体系的分离效果,旨在建立一种高效、快捷的薄层色谱分析方法。
1 材料与方法
1.1原材料及试剂
α-生育酚标样(95%),SIGMA-ALDRICH Inc.;γ-,δ-生育酚标样,SUPELCO USA;维生素E粗品,由大豆脱臭馏出物浓缩得到,含混合维生素E 31.27%;2.5 cm×7.5 cm载玻片;薄层层析用硅胶G,化学纯,青岛海洋化工有限公司;氯仿,天津市天力化学试剂有限公司;二氯甲烷、乙酸乙酯,均为天津市福晨化学试剂厂;石油醚,天津市纵横兴工贸有限公司化工试剂分公司;环已烷,天津市东丽区天大化学试剂厂;无水乙醇、乙醚,均为天津市津沽工商实业公司;甲醇,天津市科密欧化学试剂开发中心;羧甲基纤维素钠,湘大化学工试剂有限公司;碘(颗粒)。以上试剂均为分析纯。
1.2方法
1.2.1薄层色谱板的制备
称取适量硅胶G,用0.3%的羧甲基纤维素钠(CMC)溶液调成均匀浆状,均匀地涂布在载玻片上形成0.25 mm厚度左右的薄层。将铺好的硅胶板室温下凉干后移入烘箱,在110 ℃的温度下活化30 min后置于干燥器中备用。
1.2.2薄层色谱操作过程
点样处距载玻片下边缘1.5 cm,溶剂展开终点距载玻片上边缘1.0 cm,展开距离为5.0 cm。在起始线上用毛细管点混合标样,挥干后倾斜置于有展开剂的烧杯中上行展开(展开剂高度为0.5 cm),记录展开时间。展开结束后取出硅胶板,挥发掉溶剂并置于充满碘蒸气的烧杯中显色1~2 min,α-,γ-和δ-生育酚斑点显黄色。显色后,立刻用铅笔将斑点描画出来,计算出比移值(Rf)和相对比移值(ΔRf)。
比移值是化合物样点移动的距离与展开剂前沿移动的距离的比值,即:
Rf=a/b
式中:a为斑点中心到起始线的距离;b为溶剂前沿到起始线的距离。相对比移值考察α-生育酚,γ-生育酚和δ-生育酚间分离的程度,计算公式如下:
ΔRf1=Rf1-Rf2
ΔRf2=Rf2-Rf3
式中:Rf1、Rf2、Rf3,分别为α-生育酚,γ-生育酚和δ-生育酚的比移值;ΔRf1为α-生育酚与γ-生育酚的比移值之差;ΔRf2为γ-生育酚与δ-生育酚的比移值之差。
2 结果与讨论
2.1展开剂的选择
考察的展开剂组成见表1。根据上述方法在薄层色谱板上点上3种生育酚标准混合液并进行展开,计算出不同展开剂条件的Rf和ΔRf1、ΔRf2及展开时间。
表1展开剂组成

表2环己烷为基础溶剂的展开结果

展开剂组成/(v/v)Rfα-生育酚γ-生育酚δ-生育酚展开时间/min100%环已烷----环已烷-甲醇99.5∶0.5----99∶1----98∶2----环已烷-乙醇99.5∶0.5----99∶1----98∶2----环已烷-乙醚90∶100.290.220.161280∶200.510.430.3511环已烷-乙酸乙酯90∶100.470.390.311580∶200.650.590.5414

表3 二氯甲烷为基础溶剂的展开结果
100%环已烷、环已烷-甲醇(99.5∶0.5、99∶1,v/v)、环已烷-乙醇(99.5∶0.5,v/v)只能使混合标样在薄层板的起始线上显1个斑点,不能将混合标样中的α-, γ- 和 δ-生育酚分离开。环已烷-甲醇(98∶2,v/v)、环已烷-乙醇(99∶1、98∶2,v/v)这3种混合溶剂展开的效果是一条直线或出现拖尾,分离效果不理想。环已烷-乙醚(90∶10、80∶20,v/v)和环已烷-乙酸乙酯(90∶10、80∶20,v/v)能将α-,γ-和 δ-生育酚完全分开,其比移值见表2。
由表3可知,100%二氯甲烷能将3种生育酚完全分离。随着二氯甲烷中乙醇的加入和乙醇量的增加,得到的斑点越来越不清晰,拖尾现象严重而无法判断比移值。二氯甲烷-乙酸乙酯(98∶2,v/v)为展开剂能将3种标样分离开,但随着乙酸乙酯量加大,分离效果变差,至95∶5(v/v)时无法分离,仅在溶剂前沿显1个斑点。用二氯甲烷-乙醚(90∶10、95∶5、98∶2,v/v)为展开剂均能将α-,γ-和δ-生育酚分离(见表3)。

表4 石油醚为基础溶剂的展开结果
100%石油醚的溶剂强度较弱,不能将标样中各组分展开,在起始线上显现1个斑点。石油醚-乙酸乙酯(80∶20,v/v)的溶剂强度太强,只在靠近溶剂前沿处显现1个斑点。石油醚-甲醇(99∶1、95∶5、90∶10,v/v)和石油醚-乙醇(99∶1、95∶5、90∶10,v/v)作展开剂的展开效果不理想,均不能得到清晰的3个斑点。石油醚-乙酸乙酯(90∶10,v/v)、石油醚-乙醚(70∶30、80∶20、90∶10,v/v)、石油醚-氯仿(50∶50,v/v)的分离效果较好,其比移值见表4。
100%氯仿、氯仿-乙酸乙酯(98∶2,95∶5,90∶10,v/v)、氯仿-乙醚(98∶2,95∶5,90∶10,v/v)为展开剂时均能将α-,γ-和 δ-生育酚分离,比移值见表5。

表5 氯仿为基础溶剂的展开结果
2.2最佳展开剂的选择
分别计算出能分离3种生育酚的21种展开剂的ΔRf1和ΔRf2值,并作图(见图1)。
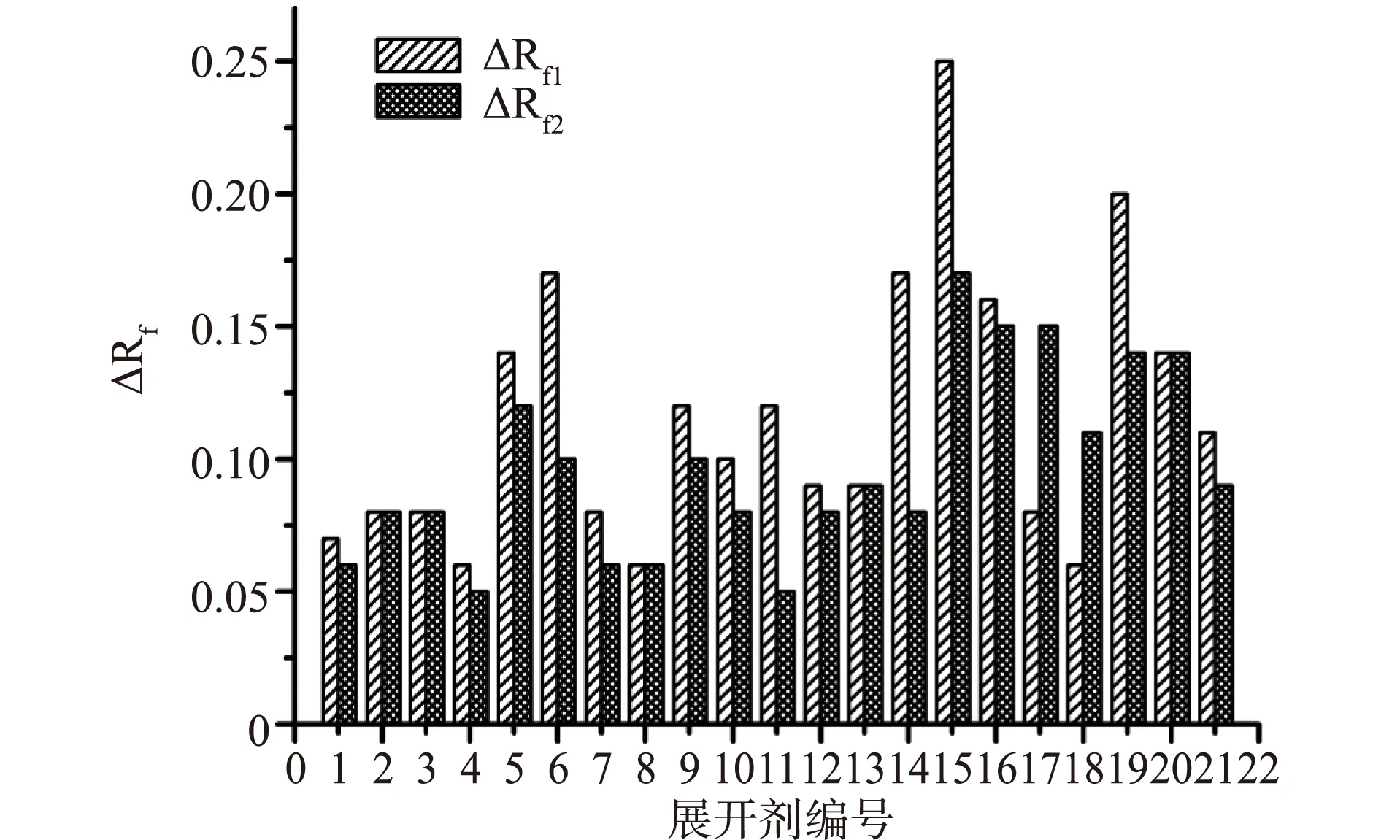
注: 1、2分别为环己烷-乙醚(90∶10, v/v)和(80∶20, v/v);3、4分别为环己烷-乙酸乙酯(90∶10, v/v)和(80∶20, v/v);5为100%二氯甲烷;6、7、8分别为二氯甲烷-乙醚(98∶2, v/v)、(95∶5, v/v)和(90∶10, v/v);9为二氯甲烷-乙酸乙酯(98∶2, v/v);10为石油醚-乙酸乙酯(90∶10, v/v);11、12、13分别为石油醚-乙醚(90∶10, v/v)、(80∶20, v/v)和(70∶30, v/v);14为石油醚-氯仿(50∶50, v/v);15为100%氯仿;16、17、18分别为(98∶2, v/v)、(95∶5, v/v)和(90∶10, v/v);19、20、21分别为氯仿-乙醚(98∶2, v/v)、(95∶5, v/v)和(90∶10, v/v)。图1 不同展开剂的分离效果
当ΔRf>0.1时,可认为相邻两种生育酚基本分开;ΔRf越大说明分离越好。由图1可知,ΔRf1和ΔRf2值均在0.1以上的展开剂编号为5、6、9、15、16、19和20(为二氯甲烷和氯仿为基础溶剂的展开剂),展开时间分别为7.0 min、6.5 min、6.0 min、9.0 min、8.0 min、8.0和8.5 min。虽然氯仿为基础溶剂的分离效果好于二氯甲烷为基础溶剂的,其中分离效果最好的为100%氯仿,但耗时相对较长,不利于快速分离。因此,在建立快速分析方法时选择后者较为合适。在以二氯甲烷为基础溶剂的展开剂中,100%二氯甲烷的时间略长于二氯甲烷-乙醚(98∶2, v/v)和二氯甲烷-乙酸乙酯(98∶2, v/v),但由于后两种为混合溶剂导致测量的重复性相对单一溶剂差,所以选择100%二氯甲烷为展开剂最佳(展开结果见图2)。

图2 100%二氯甲烷展开维生素E粗品
3 结论
以100%二氯甲烷为展开剂的硅胶薄层色谱能将α-,γ-和 δ-生育酚完全分离开。不仅耗时少(7 min),而且重现性较好,适合于生育酚单体的快速定性检测。
[1] 陈仁惇.营养保健食品[M].北京:中国轻工业出版社,2001.
[2] Paul Pfluger, Dirk Kluth, Nico Landes, et al. Vitamin E: Underestimated as an antioxidant[J].Redox Report,2004,9(5):249-254.
[3] Jean Marc Zingg, Angelo Azzi. Non-antioxidant activities of Vitamin E [J].Current Medicinal Chemistry,2004,11(9):1113-1133.
[4] Yoshiko Nagata, Yohta Matsumoto, Hideko Kanazawa. Products of the reaction between α- or γ-tocopherol and nitrogen oxides analyzed by high-performance liquid chromatography with UV-visible and atmospheric pressure chemical ionization mass spectrometric detection[J]. Journal of Chromatography A,2004,1036:177-182.
[5] B Kivak, S Akay.Quantitative determination of α-tocopherol in Pistacia lentiscus, Pistacia lentiscus var. chia, and Pistacia terebinthus by TLC-densitometry and colorimetry [J]. Fitoterapia,2005,76:62-66.
[6] B Kivak, T Mert.Quantitative determination of α-tocopherol in Arbutus unedo by TLC-densitometry and colorimetry [J]. Fitoterapia,2001,72: 656-661.
Fastqualitativeanalysisoftocopherolwiththin-layerchromatography
Zhang Yi1, Guo Yonghong2, Hu Zhixiong2*, Qi Yutang2
1.Wuhan High School (Wuhan 430061)2.College of Food Science and Engineering, Wuhan Polytechnic University (Wuhan 430023)
A fast and simple qualitative analysis of individual tocopherol (α-, γ- and δ-tocopherol) by using thin-layer chromatography (TLC) was established. Silica was used as absorbant and four types of solvent system (cyclohexane, dichloromethane, petroleum ehther and chloroform used as basic solvents), total 38 solvent systems, were investigated to separate three tocopherols. Results show that three tocopherols can be separated when using 100% dichloromethane, dichloromethane-ether (98∶2, v/v), dichloromethane-ethyl acetate (98∶2, v/v), 100% chloroform, chloroform-ethyl acetate (98∶2,v/v), chloroform-ether (98∶2 and 95∶5, v/v) as developers. 100% dichloromethane is the optimum developer for establishing a fast and simple TLC analytical method owing to having some advantages such as short developing time and easy operation. Using this TLC method,Rfof α-, γ- and δ-tocopherol are 0.69, 0.55 and 0.43, respectively, and developing time is 7 min.
tocopherol; vitamin E; TLC; qualitative analysis
TS227
A
1672-5026(2017)05-009-04

