热重分析法测定大米中淀粉含量
崔丽伟 展海军 张佳佳 胡怡洁
(河南牧业经济学院食品工程学院1,郑州 450046)(河南工业大学化学化工学院2,郑州 450001)
热重分析法测定大米中淀粉含量
崔丽伟1展海军2张佳佳2胡怡洁2
(河南牧业经济学院食品工程学院1,郑州 450046)(河南工业大学化学化工学院2,郑州 450001)
本研究采用红外和热重分析技术,在250~330 ℃区间建立了热重分析法测定大米淀粉含量的2个模型。1)纯品大米淀粉含量与失重率所建相关性方程为:Y=0.539 7X+3.598,r=0.999。2)大米样品中淀粉含量与失重率相关性方程为:Y=0.523 4X+4.683,r=0.999。通过与国标方法结果对比,2种模型方法所测结果相对误差范围分别为0.53%~0.99%和0.04%~0.33%。在相同试验条件下,所建模型均可用于籼米、糯米和粳米淀粉含量的测定。该方法具有样品基底影响小、前处理简单,测定快速等优点。
热重分析 大米 淀粉 红外吸收光谱
中国是世界上最大的稻米生产国,全国大部分地区以大米为主食,大米的品质与营养结构与人们的健康息息相关。在3种大米(籼米、糯米和粳米)中,淀粉都是其主要成分,质量分数达80%以上,作为大米的主成分,淀粉因其独特的性能,在食品、化工、医药等工业中具有广泛的应用价值。因此,准确快速测定大米中淀粉含量意义重大。
粮食中淀粉含量常采用国家标准方法进行测定,该方法虽测定结果准确,但操作比较繁琐,使用试剂较多,分析速度慢。此外,测定淀粉含量的方法还有酶催化法[1]、色谱法[2]、近红外光谱法[3]等,但这些方法由于繁琐的过程而受到一定限制。本研究通过热重分析与红外吸收光谱法对大米淀粉热分解特征的研究,建立了一种快速测定大米淀粉含量的新方法。
1 材料与方法
1.1 试验试剂
大米淀粉标准品:美国 Sigma 公司;碘化钾、碘、淀粉酶、无水乙醇、甲基红、无水乙醚、盐酸、硫酸铜、亚甲蓝、酒石酸钾钠、氢氧化钠、亚铁氰化钾、乙酸锌、冰乙酸、葡萄糖,以上试剂均为分析纯。
1.2 试验仪器
Linens SAT PT 1600 型同步热分析仪:德国林赛斯国际公司。
1.3 样品来源与处理
选取来源于河南省、湖南省、广东省、黑龙江省、泰国等地不同品种的30种大米,按照品种不同依次命名为糯米1~10号,粳米1~10号、籼米1~10号。用密封袋保存好。选取具有代表性的样品经粉碎机粉碎后依据需求过一定目数的筛网,采用四分法称取样品。
1.4 试验方法
1.4.1 大米中淀粉含量测定
依据GB/T 5009.7—2008[4]和GB/T 5514—2008[5]对大米中淀粉含量进行平行测定2次,取其平均值。
1.4.2 热重分析法
精准称取10 mg样品于刚玉坩埚中,空坩埚为参比样,在空气氛围下以10 ℃·min-1的升温速率从25 ℃升至600 ℃,得到热重-微商热重(TG-DTG)谱图。
1.4.3 红外吸收光谱法
分别将大米淀粉及分解后的残渣进行红外吸收光谱仪扫描。FTIR采用KBr压片法制备,扫描次数为16 次,分辨率为4 cm-1,结果用Oringin 8.0软件进行合并。
1.4.4 统计分析
运用Linseis Platinum Software进行失重率的计算;SPSS16.0进行方差分析、线性回归模型的建立;对结果进行F检验和t检验,置信区间为90%。
2 结果与分析
为探究大米和大米淀粉的热分解过程,对不同品种的大米、大米淀粉用 Linseis SAT PT 1600型同步热分析仪进行热重分析。结果表明不同品种间的大米热重图谱相差不大,选取大米淀粉标准品和9号粳米作为样品,按照1.4.2中分析方法得到其TG-DTG曲线图,分别如图1、图2所示。
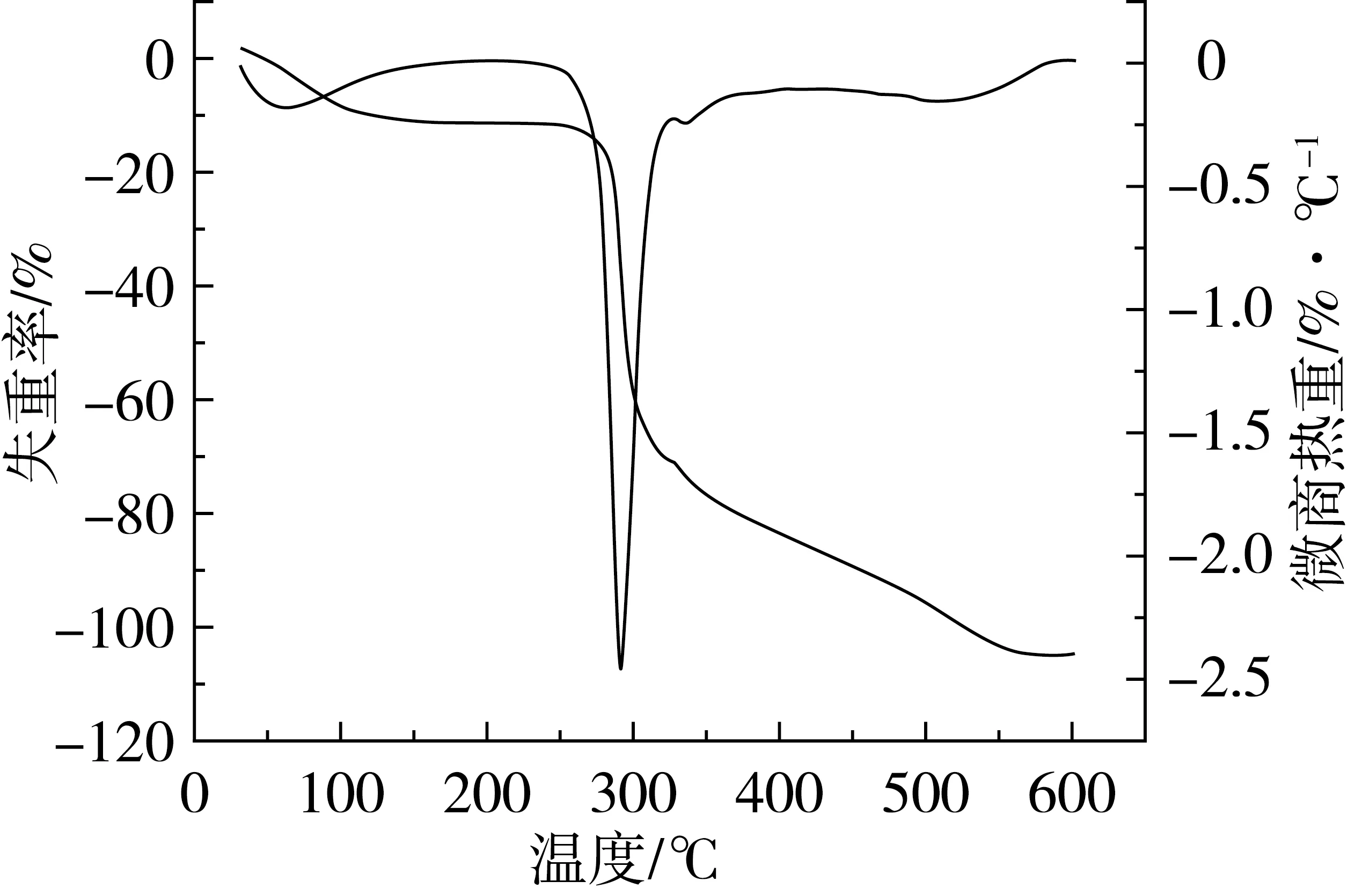
图1 大米淀粉标准品的TG-DTG曲线图

图2 粳米9号的TG-DTG曲线图
图1和图2显示,粳米9号及大米淀粉受热失重的过程可分为3个阶段:第1阶段(T≤140 ℃)此阶段热重平台清晰,这主要是由于易挥发物质的蒸发所致,其中水分为主要成分;第2阶段(250 ℃≤T≤330 ℃)此阶段失重明显,失重速率达到最大值。这一阶段葡萄糖环羟基的快速脱水和分解形成水分子[6],C-C-H、C-O和C-C键发生断裂,主链也发生了断裂。主要的分解产物是H2O、CO、CO2和一些类似CH4和C2H4的化合物,质量损失是由于淀粉分解所致。此阶段可能是单一反应或者是多重反应的合并[7];第3阶段(T>330 ℃)质量损失是由于发生了碳化,这可能是由于淀粉分解后中间产物完全分解所致。从大米淀粉的TG-DTG曲线图中得知,当T≥550 ℃淀粉已完全失重。图谱信息表明:淀粉的特征分解温度区间为250~330 ℃,289 ℃时分解速率最大,当温度升至550 ℃时,淀粉已完全分解。
2.2 红外吸收光谱分析
将大米淀粉及其在250和330 ℃灼烧后的残渣粉碎、过60 目筛后,按照1.4.3法得到其红外吸收光谱图,如图3所示。
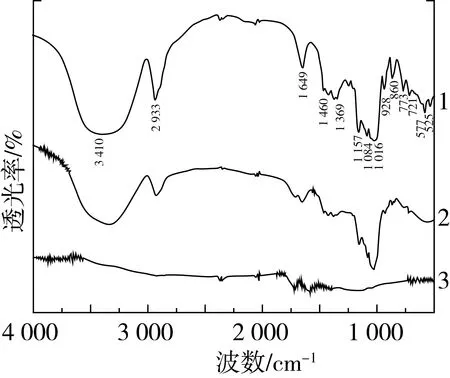
图3 大米淀粉分解前后红外光谱对照图
图3中曲线1是大米淀粉的红外光谱图,曲线2为大米淀粉在经过250 ℃灼烧后残渣的红外光谱图,曲线3为大米淀粉在经过330 ℃灼烧后残渣的红外光谱图。通过对比可以得知,淀粉在升至250 ℃发生分解之前的FTIR谱图峰形及峰位与原淀粉基本相同;当温度升至330 ℃发生分解之后淀粉的特征吸收峰基本消失,证明此时淀粉已经被完全分解。进一步证明了大米淀粉的特征分解温度区间为250~330 ℃,与热重分析的试验结果相一致。
2.3 大米淀粉测定模型1的建立与验证
2.3.1 纯品淀粉含量与失重率相关关系
用Al2O3粉末配制浓度分别为20%、40%、60%、80%、100%的大米淀粉浓度梯度系列,然后准确称取10 mg待测样品于陶瓷坩埚中,在空气氛围下用Al2O3作参比,以10 ℃·min-1的升温速率从25 ℃升到600 ℃。记录TG曲线中在250~330 ℃区间淀粉失重率。平行测定2次取其淀粉失重率均值并与大米淀粉含量做相关关系曲线,如图4所示,线性方程为:Y=0.539 6X+3.599,r=0.999,其中X表示大米淀粉浓度,Y表示大米淀粉在250~330 ℃区间的失重率。由此可以得出:用失重率大小来评价淀粉含量高低这个方法可行,且相关性较好。
爸爸不停地哄她,又是“宝贝”又是“买布丁果冻”,每一句都像蜜糖般能够抚慰心肺,声音像风吹过麦浪似的轻柔,生怕惊着果果。从我记事以来,父亲就这么对果果说话,就好像她是永远长不大的孩子。想着想着,卧室的门就被踹开了,爸爸拖起躺在床上的我,“你小子想干什么!果果怎么惹着你了,惹着你又怎样,什么时候轮到你去训她……”山洪暴发般的声音回荡在我不太小的房间里,在我的大脑里穿行。倚在门框边的果果火上浇油:“就是,什么时候轮到你教训我了?”她的洋腔怪调,傲慢不堪的神色彻底惹怒我了,我握紧拳头大声叫嚷:“她有什么权力翻我的书包!说翻情书,我高三了,每天像牛一样忙,还要给她做午饭,哪有他妈的时间去谈恋爱!”
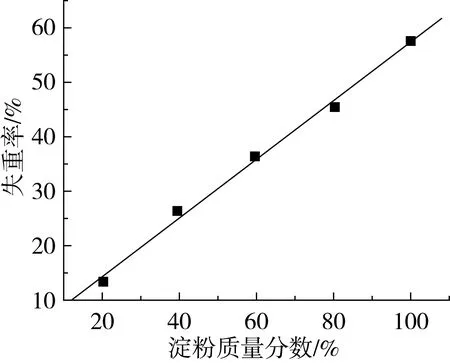
图4 大米淀粉质量分数与失重率相关度曲线
2.3.2 大米淀粉含量测定模型1的验证
分别采用 TG法与国家标准法对同一大米样品(籼米7号)中淀粉的含量进行测定,平行测定5次,根据大米淀粉测定模型1得出淀粉含量,2种方法的测定值对照结果如表1所示。

表1 国标法与TG法测定结果对照表
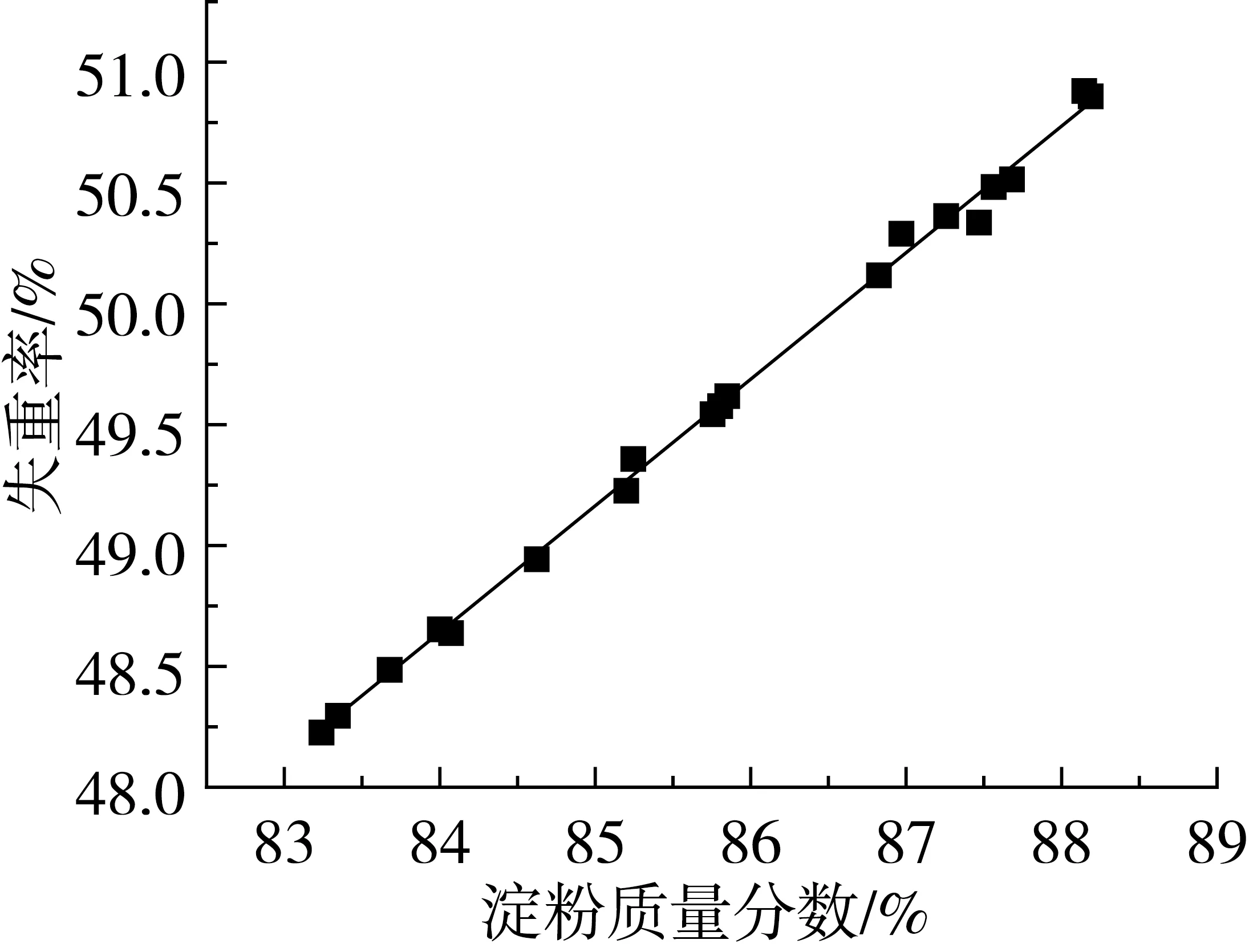
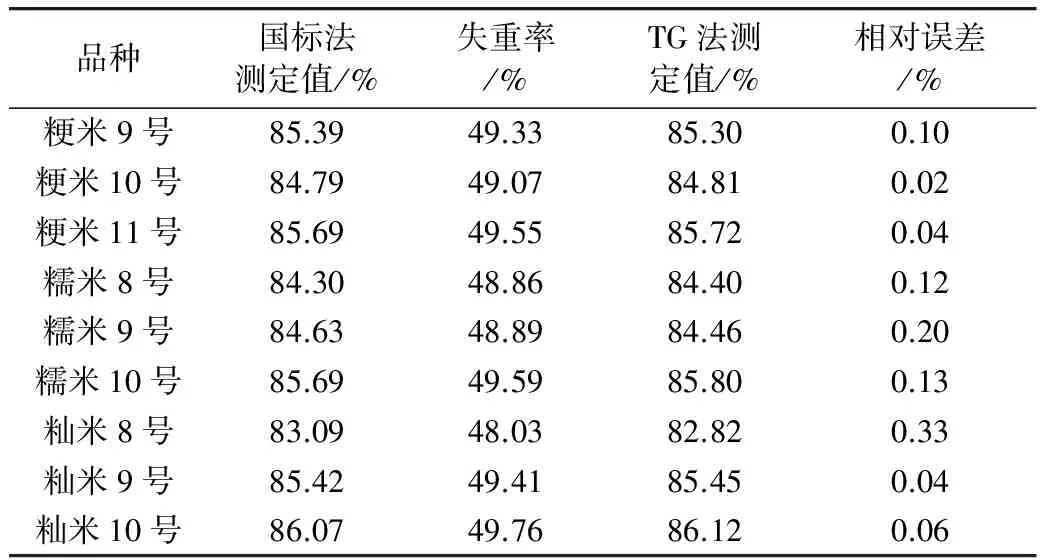
为了检验TG法的精密度和准确度,需要对试验结果进行F检验和t检验。F=2.25,当P=0.90时,F4,4=6.39;F 表2 不同品种大米淀粉含量的测定结果 2.4 大米淀粉含量测定模型2的建立 2.4.1 样品淀粉含量与失重率相关关系 将30种不同品种不同产地的大米样品按1.4.1中的国家标准方法对大米中淀粉含量进行测定,平行测定2次取其平均值。同时对这30种大米样品进行热重分析。平行测定2次取其250~330 ℃区间失重率均值,随机选取20种样品将其在250~330 ℃区间的失重率与国家标准方法所测得淀粉含量做相关关系曲线,如图5所示,大米淀粉含量与TG曲线相应温度区间(250~330 ℃)的失重率呈正相关,且相关性较好。线性方程为:Y=0.523 4X+4.683,r=0.999。 图5 淀粉质量分数与TG谱图中特征区间(250~330℃)失重率相关性曲线 2.4.2 大米淀粉含量测定模型2的验证 分别采用所建大米淀粉含量测定模型2与国家标准法对同一大米(籼米7号)中淀粉的含量进行测定,平行测定5 次,2种方法的测定值对照结果如表3所示。 表3 国标法与 TG 法精密度试验结果对照表 为了检验测定模型2的精密度和准确度,需要对试验结果进行F检验和t检验。F=2.25,当P=0.90时,F4,4=6.39;F 分别采用国家标准法和大米淀粉含量测定模型2法对9种不同品种的大米样品进行淀粉含量测定,结果如表4所示。从表中可以看出,用模型2得出的大米淀粉含量与国家标准法测定值之间的相对误差均小于0.5%,结果令人满意。说明该模型适用于不同品种大米的淀粉含量测定。 表4 国家标准法与TG法准确度试验结果对照表 通过测定热重图谱中250~330 ℃温度区间样品的失重率,建立了淀粉含量与失重率之间的相关关系。纯品淀粉含量与失重率所建相关性方程(模型1)为:Y=0.539 7X+3.598,r=0.999;国家标准方法所测大米样品淀粉含量与失重率相关性方程(模型2)为:Y=0.523 4X+4.683,r=0.999;用2种模型测定不同类型的大米淀粉含量时,3种类型的大米之间无显著性差异。通过对比表2和表4,可以得出,模型2准确度更高,这可能是由于模型2考虑了样品背景的干扰。故在相同试验条件下,无论是籼米、糯米或粳米都可根据TG曲线淀粉在特征区间(250~330 ℃)的失重率,用同一个方程Y=0.523 4X+4.683计算大米的淀粉含量。本方法准确、快速,具有较好的实用性。 [1]McCleary B V,Solah V,Gibson T S. Quantitative measurement of total starch in cereal flours and products[J]. Cereal Science,1994,20(1):51-58 [2]AOAC International. Official methods of analysis of AOAC International[M]. AOAC International, 2005 [3]Zeng W,Zhang H Z,Lee T C. Direct determination of the starch content in gravy by near-infrared spectroscopy[J]. Agricultural Food Chemistry,1996,44(6):1460-1463 [4]GB/T 5009.7—2008 食品中还原糖的测定[S] GB/T 5009.7—2008 Determination of reducing sugar in foods[S] [5]GB/T 5514—2008 粮油检验粮食、油料中淀粉含量测定[S] GB/T 5514—2008 Inspection of grain and oils-Determination of starch content in grain and oilseeds [S] [6]Gómez P P,Coral D F,Rivera D R,et al. Thermo-alkaline treatment. A process that changes the thermal properties of corn starch[J]. Procedia Food Science,2011, 1:370-378 [7]Opfermann J. Kinetic analysis using multivariate non-linear regression[J]. Thermal Analysis and Calorimetry,2000,60(2):641-658. Determination of Starch Content in Rice by Thermogravimetric Analysis Cui Liwei1Zhan Haijun2Zhang Jiajia2Hu Yijie2 In this paper, two models of thermogravimetric analysis of rice starch content were established in the range of 250~330 ℃ by infrared and thermogravimetric analysis. (1) The correlation equation of pure rice starch content and weight loss rate was:Y=0.539 7X+3.598,r=0.999. The correlation equation of starch content and weight loss rate in rice sample was:Y=0.523 4X+4.683,r=0.999. Comparing with GB method, the relative error ranges of the two models were 0.53%~0.99% and 0.04%~ 0.33%, respectively. Under the same experimental conditions, the model can be used for the determination of starch content in indica rice, glutinous rice and japonica rice. The method had the advantages of small sample base, simple pretreatment and rapid determination. thermogravimetric analysis, rice, starch, infrared absorption spectrum O657 A 1003-0174(2017)08-0167-04 2016-07-21 崔丽伟,女,1987年出生,助教,粮油食品分析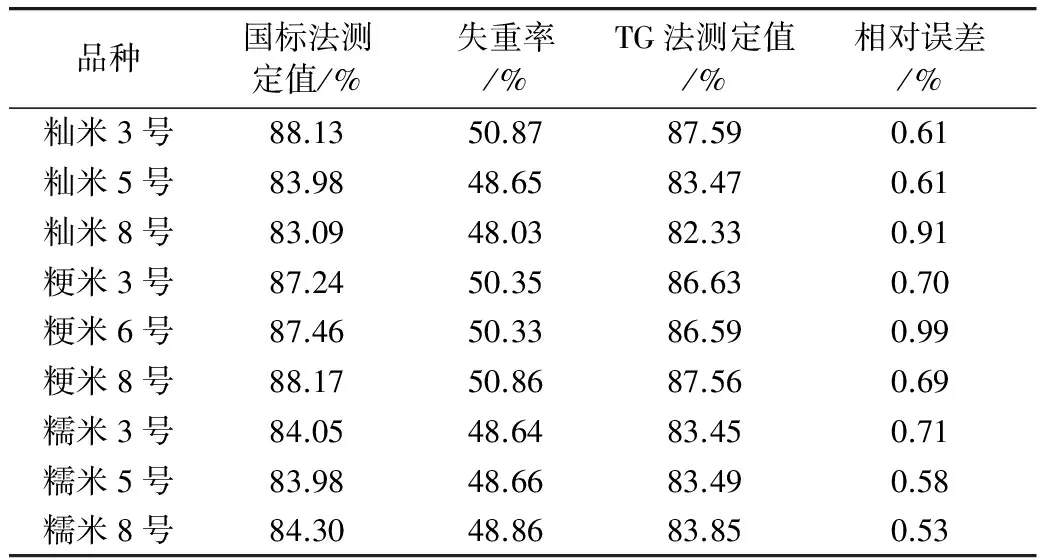

3 结论
(School of Food Engineering, Henan University of Animal Husbandry and Economy1, Zhengzhou 450046)(School of Chemistry and Chemical Engineering, Henan University of Technology2, Zhengzhou 450001)

