阿帕替尼治疗晚期肺恶性肿瘤疗效观察并文献复习
沈旦 冯薇 杨雯 黄建安
阿帕替尼治疗晚期肺恶性肿瘤疗效观察并文献复习
沈旦 冯薇 杨雯 黄建安
目的探讨阿帕替尼在晚期肺恶性肿瘤中的疗效。方法分析2017年3月至4月在苏州大学附属第一医院呼吸与危重症医学科经病理证实的晚期肺恶性肿瘤患者3例,均至少接受过2种静脉系统化疗而无法控制病情,通过观察肺部病灶的变化评价阿帕替尼疗效,并观察不良反应。结果3例患者中,男性2例,女性1例,年龄61-74岁。其中小细胞肺癌(small cell lung cancer,SCLC)1例,肺腺癌1例,子宫内膜癌肺转移1例。3例患者中,2例病灶部分缓解(partial response,PR),1例病灶稳定(stable disease,SD)。不良反应主要为口腔溃疡(2/3);食欲下降(2/3);低钠血症(2/3);手足综合症(1/3);低钾血症(1/3);肝功能异常(1/3);白细胞下降(1/3),心包积液(1/3),蛋白尿(1/3)。结论阿帕替尼治疗晚期肺恶性肿瘤效果良好,减量口服可耐受不良反应,但仍需要大样本证实。
阿帕替尼;晚期肺恶性肿瘤;疗效;不良反应
肺癌是我国常见的恶性肿瘤之一,无论是原发性还是转移性肺癌,预后均不理想[1]。对于晚期肺恶性肿瘤,化疗和分子靶向治疗是目前的主要治疗手段,然而总体效果并不满意。阿帕替尼是小分子血管内皮生长因子受体2(vascular endothelial growth factor receptor 2,VEGFR-2)酪氨酸激酶抑制剂,可强效抑制肿瘤血管生成,已推荐用于晚期胃癌的治疗[2]。然而,在肺恶性肿瘤的治疗中,阿帕替尼的报道不多,现分析我院近期收治的3例晚期肺恶性肿瘤患者口服阿帕替尼的疗效及不良反应,以提高对阿帕替尼在晚期肺恶性肿瘤治疗中的认识。
资料与方法
一、临床资料
1 病例1,患者男性,61岁,2016年1月30日因“干咳一月余,胸闷伴气喘十余天”入院,查胸部CT示左肺多发结节,纵隔淋巴结肿大融合,双肺大疱,行支气管镜纵隔淋巴结穿刺病理示小细胞肺癌,诊断SCLC(广泛期)。3月14日行依托泊苷单药化疗1周期, 4月6日行依托泊苷联合卡铂化疗1周期,5月9日查胸部CT左肺病灶PD,于5月10日、6月2日调整方案为多西他赛联合卡铂化疗2周期。6月22日查胸部CT左肺病灶继续PD。6月28日起调整方案为伊立替康单药化疗5周期,末次化疗时间2016年12月20日,期间查胸部CT左肺病灶仍缓慢PD。住院期间曾出现自发性气胸2次,予以胸腔闭式引流治疗后肺复张,2017年2月28日因上腔静脉综合征行上腔静脉支架置入术。3月2日开始每日口服阿帕替尼250mg,三天后加至每日500mg,后因双手、双足部位的皮肤开裂、溃疡而减量至每日250mg,4月24日(治疗54天)查胸部CT,左肺病灶PR(图1),但出现心包积液,检查发现异型细胞,予以引流后心包腔内局部注入顺铂及重组人血管内皮抑制素。4月25日查生化全套:谷丙转氨酶(ALT)明显升高。5月17日复查胸部CT,左肺病灶较前稍缩小,心包积液较前减少。5月28日因病情突然恶化死亡。
2 病例2,患者男性,74岁,2016年11月05日因“体检发现右下肺肿块一月余”入院,既往6年前曾行冠状动脉、左肾动脉植入术。入院查胸部CT示:右下肺软组织肿块影,行经皮肺穿刺检查病理提示腺癌,表皮生长因子受体(Epidermal growth factor receptor,EGFR)和间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)融合基因检测均阴性。PET-CT检查示右肺癌伴淋巴结多发转移,骶骨转移,诊断右肺腺癌IV期(T1N2M1b),11月12日起予培美曲塞单药方案化疗4周期,末次化疗时间为2017年1月1日,期间查胸部CT病灶SD。2月15日查胸部CT示右肺病灶PD。2月16日、3月14日调整方案为多西他赛单药化疗2周期。4月10日查胸部 CT:右肺病灶继续PD,右侧胸腔积液。行胸腔闭式引流,并局部注入顺铂,4月16日开始每日口服阿帕替尼250mg,三天后加量至每日500mg,后因口腔粘膜破溃、食欲下降而改为每日250mg/500mg交替。5月12日(治疗27天)复查胸部CT,右肺病灶SD(图2)。
3 病例3,患者女性,70岁,2014年5月14日因“绝经后阴道出血一月余”入外院,妇科检查明确为子宫内膜腺癌。于6月19日行“经腹次广泛全子宫切除术+双附件切除术+腹主动脉旁及盆腔淋巴结清扫术”,术后病理:(全子宫)内膜低分化腺癌,侵及肌壁全层,腹主动脉旁(1/5)见癌转移,腹水见核大细胞。术后行多西他赛联合卡铂静脉化疗6周期,2周期后曾行全盆腔放疗,45Gy/25F,过程顺利,末次化疗时间12月15日,期间评估病情SD。2015年7月出现明显胸闷气急,查胸部CT示左侧大量胸腔积液伴胸膜结节状软组织影,为进一步治疗入住我科,胸水检查见癌细胞,结合免疫组织化学染色考虑来源于子宫内膜,明确为肺转移性腺癌,诊断:① 子宫内膜癌术后,② 肺转移性癌。8月13日起继续予多西他赛联合卡铂化疗6周期,过程顺利,末次化疗时间12月16日,期间评估病情SD。2016年1月起予多西他赛单药维持4周期,末次化疗时间5月24日,期间评估病情SD。7月15日入院查胸部CT,见双肺、胸膜、纵隔多发结节,评估病情PD,调整化疗方案为吉西他滨单药,化疗4周期,期间评估病情SD,末次化疗时间2017年1月12日。3月22日复查胸部CT双肺结节较前明显增多、增大,并出现椎体破坏,肝脏转移,评估病情PD。3月23日起每日口服阿帕替尼250mg,三天后加至每日500mg,后因食欲下降、口腔溃疡改为每日250mg。5月10日(治疗49天)复查胸部CT,双肺病变PR(图3)。
二、方法
1 所有患者均行血常规、生化全套、胸部CT检查,并详细询问病史及体格检查,观察不良反应。
2 阿帕替尼起始剂量每日为250mg,第4天起每日500mg,如不能耐受不良反应,则减量。
3 肺部病灶参考实体瘤的疗效评价标准(RECIST)[3],不良反应参考世界卫生组织发布的抗癌药物常见毒副反应分级标准。
结 果
所有患者均因不良反应而减量口服阿帕替尼,其主要不良反应包括:口腔溃疡2例(Ⅱ级),食欲明显下降2例,低钠血症2例,手足综合症1例(Ⅲ级),低钾血症1例,肝功能异常1例(Ⅲ级),白细胞下降1例(Ⅰ级),心包积液1例(Ⅲ级),蛋白尿1例。肺部病灶疗效评价:2例PR(图1,3),1例SD(图2);相关血常规及生化指标(见表1,2)。
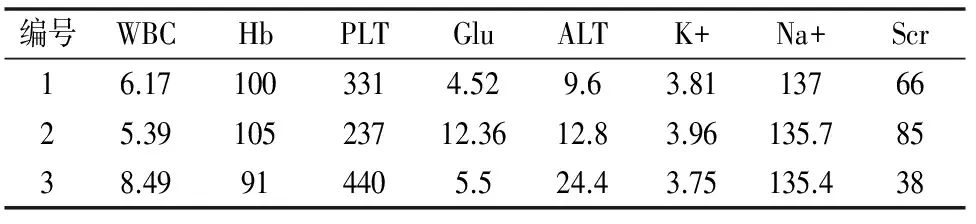
表1 治疗前血常规及相关生化指标

表2 治疗后血常规及相关生化指标
注:WBC:白细胞;Hb:血红蛋白;PLT:血小板;Glu:血糖;K+:血钾离子;Na+:血钠离子;Scr:血肌酐

图1 SCLC患者治疗前后胸部CT对比
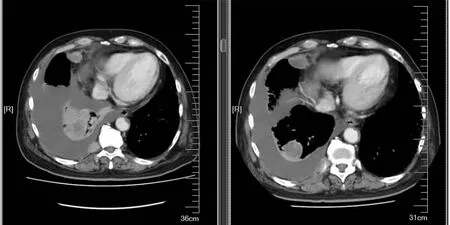
图2 肺腺癌患者治疗前后胸部CT对比

图3 子宫内膜癌肺转移患者治疗前后胸部CT对比
讨 论
晚期肺恶性肿瘤的疗效目前并不理想。对于广泛期SCLC,主要采用化疗为主的综合治疗;对于非小细胞肺癌(non small cell lung cancer,NSCLC),存在EGFR敏感突变的患者推荐EGFR-酪氨酸激酶抑制剂(tyrosine kinase inhibitors,TKIs)口服,而存在ALK融合基因阳性患者则推荐口服克唑替尼;对于无上述敏感基因突变的NSCLC,含铂双药方案的全身化疗仍是目前治疗的基石[4]。对于局部或区域转移的III期子宫内膜癌,主要选择手术治疗,完整切除所有转移病灶,术后加盆腔外照射和(或)化疗;对于有远处转移的IV期患者,通常使用以铂类为基础的化疗[5]。
肿瘤的生长依赖于周围微环境,血管生成在肿瘤形成及转移过程中发挥重要作用,微血管密度增高与肿瘤生长及不良预后关系密切[6]。血管内皮生长因子(vascular endothelial growth factor,VEGF)及VEGFR介导的信号传导通路可调控肿瘤血管的生成过程[7]。VEGFR-2表达于内皮细胞,可调节细胞分裂、血管生成及增强VEGF的作用,与肿瘤血管的生成关系密切[8]。有研究显示,VEGF的单克隆抗体贝伐单抗,可显著改善晚期非鳞NSCLC患者的总生存期(overall survival,OS)[9],故理论上抑制VEGFR-2的表达同样可减少血管的生成,从而抑制肿瘤的生长。阿帕替尼作为小分子抗血管生成制剂,可结合并抑制VEGFR-2,在晚期胃癌的治疗中,取得了积极的疗效[10],但在晚期肺恶性肿瘤的治疗中,报道并不多见。
本组3例患者中,均进行了以化疗为主的综合治疗,然而病灶仍不断进展。在SCLC患者,化疗几乎无效,肿块持续增大;在NSCLC患者,因其年龄较大,基础疾病较多,故采用了单药化疗,但效果不佳;子宫内膜癌肺转移患者,经过综合治疗后,原发病灶未见复发,但肺转移病灶持续增大。3例患者口服阿帕替尼治疗以后,胸部病灶评估疗效均达到SD以上,效果良好。其中SCLC及子宫内膜癌肺转移患者肿瘤均明显缩小,病灶得到PR,而NSCLC患者肿瘤缩小并不明显,病情评估SD,然而该例患者服用阿帕替尼时间较前两例均短,延长治疗时间是否有益于疗效的发挥,仍需要进一步观察。有研究[11]入组135例晚期非鳞NSCLC患者,口服阿帕替尼与安慰剂对照。结果发现阿帕替尼组中位无疾病进展生存期(progression free survival,PFS)较安慰剂组明显延长(4.7月vs.1.9月,P<0.001)。Song[12]等研究42例NSCLC患者每日口服阿帕替尼500mg,其中腺癌30例,鳞癌12例,发现疾病控制率为61.9%,平均PFS和OS分别为4.2个月和6个月;Fang[13]等报道3例EGFR及ALK融合基因均阴性的晚期腺癌患者每日口服阿帕替尼500mg,病灶均达到PR,PFS为2.8个月、5.8个月和6个月;Ding[14]等报道两例NSCLC患者,其中腺癌、鳞癌各1例,均无EGFR及ALK融合基因突变,口服阿帕替尼每日850mg,PFS为4.6个月和6个月。涂燕等[15]发现阿帕替尼在直肠癌肺转移的治疗中,同样有效。而使用阿帕替尼治疗晚期子宫内膜癌,目前国内外报道甚少。本组病例中,SCLC患者的OS为2.9个月,腺癌患者的PFS目前为2.2个月,而子宫内膜癌肺转移患者PFS已达3个月,目前仍在继续随访中。
阿帕替尼的常见不良反应包括血液学毒性和非血液学毒性。血液学毒性包括白细胞、粒细胞、血小板减少等;非血液学毒性包括高血压、蛋白尿、手足皮肤反应、乏力、腹泻等[10]。文献报道阿帕替尼治疗NSCLC的主要不良反应为:高血压[12-14]、蛋白尿[12-13]、手足综合症[12-14],肝功能异常[12],乏力[12],恶心呕吐[12],中性粒细胞减少伴发热[12],贫血[12]。本组患者中,2例患者出现口腔溃疡,包括舌部,严重时影响进食;2例出现食欲明显下降,均见于口腔病变者,推测与口腔内破损、溃疡所致的疼痛不适有关;3例患者出现电解质紊乱,均为轻度,其中低钠血症2例,低钾血症1例,推测与食欲下降进食量较少所致;1例患者出现手足综合症;1例患者出现蛋白尿;1例患者出现肝功能异常,但此例患者同时合并有大量心包积液,不排除由于心包填塞肝脏淤血所致,入院后行心包穿刺闭式引流及加强保肝治疗后好转;1例患者出现白细胞下降,予以重组人集落刺激因子皮下注射后白细胞上升。本组3例患者均因不良反应而减量口服,但症状在阿帕替尼减量并对症处理后均能耐受,提示阿帕替尼的安全性尚可,其不良反应的发生率及严重程度是否存在剂量依赖性,有待于大样本研究观察。
值得注意的是,3例患者均在剂量减量并小剂量维持的情况下,复查胸部CT病灶都能达到SD及以上,提示阿帕替尼在晚期肺恶性肿瘤的治疗中,其疗效尚可,但其最佳治疗剂量及最小维持剂量仍有待于进一步研究探索。
[1] Zhi XY,Zou XN,Hu M,et al.Increased lung cancer mortality rates in the Chinese population from 1973-1975 to 2004-2005: An adverse health effect from exposure to smoking[J].Cancer,2015,121(Suppl 17):3107-3112.
[2] Ajani JA,D'Amico TA,Almhanna K,et al.Gastric Cancer, Version 3.2016, NCCN Clinical Practice Guidelines in Oncology[J].J Natl Compr Canc Netw,2016,14(10):1286-1312.
[3] Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours: Revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[4] 石远凯,孙燕,于金明,等.中国晚期原发性肺癌诊治专家共识(2016年版)[S].中国肺癌杂志,2016,19(1):1-15.
[5] Colombo N,Creutzberg C,Amant F,et al.ESMO-ESGO-ESTRO Consensus Conference on Endometrial Cancer: diagnosis, treatment and follow-up[J].Ann Oncol,2016,27(1):16-41.
[6] Jayson GC,Kerbel R,Ellis LM,et al.Antiangiogenic therapy in oncology: current status and future directions[J].Lancet,2016,388(10043):518-529.
[7] Matsumoto T,Mugishima H.Signal transduction via vascular endothelial growth factor (VEGF) receptors and their roles in atherogenesis[J].J Atheroscler Thromb,2006,13(3):130-135.
[8] Guo S,Colbert LS,Fuller M,et al.Vascular endothelial growth factor receptor-2 in breast cancer[J].Biochim Biophys Acta,2010,1806(1):108-121.
[9] Reck M,von Pawel J,Zatloukal P,et al.Phase III trial of cisplatin plus gemcitabine with either placebo or bevacizumab as first-line therapy for nonsquamous non-small-cell lung cancer: AVAil[J].J Clin Oncol, 2009,27(8):1227-1234.
[10] 秦叔逵,李进.阿帕替尼治疗胃癌的临床应用专家共识[S].临床肿瘤学杂志,2015,20(9):841-847.
[11] 涂艳,彭枫.阿帕替尼治疗恶性肿瘤的临床研究进展[J].中国肿瘤临床,2016,43(12):545-548.
[12] Song ZB,Yu XM,Lou GY,et al.Salvage treatment with apatinib for advanced non-small-cell lung cancer[J].Onco Targets Ther,2017,10:1821-1825.
[13] Fang SC,Zhang HT,Zhang YM,et al.Apatinib as post second-line therapy in EGFR wild-type and ALK-negative advanced lung adenocarcinoma[J].Onco Targets Ther,2017,10:447-452.
[14] Ding L,Li QJ,You KY,et al.The Use of Apatinib in Treating Nonsmall-Cell Lung Cancer: Case Report and Review of Literature[J].Medicine,2016,95(20):e3598.
[15] 涂艳,彭枫,罗德云.阿帕替尼治疗直肠癌肺转移有效1例报告[J]. 四川大学学报(医学版),2016,47(5):818.
EfficacyofApatinibintreatmentofadvancedlungcancer
SHENDan,FENGWei,YANGWen,HUANGJian-an
DepartmentofRespiratoryandCriticalCareMedicine,theFirstAffiliatedHospitalofSoochowUniversity,Suzhou,Jiangsu215000,China
ObjectiveTo investigate the efficacy of Apatinib in treatment of advanced malignant tumors in lung.MethodsThe clinical features of 3 patients with advanced malignant tumors in lung from March to April 2017 were selected, and all of them
at least two kinds of chemotherapy before and their tumors were still making progress. After treating with Apatinib, their pulmonary CT scans and side effects were observed.ResultsIn these patients, 2 cases were male and 1 case was female. The mean age of the subjects was 68.3 years old. The pathology patterns were small cell lung cancer, adenocarcinoma and metastatic adenocarcinoma from endometrium. The tumors were partial response in 2 cases and stable disease in 1 case. The main side effects were aphthous ulcer (2/3), loss of appetite (2/3), hyponatremia (2/3), hand-foot syndrome (1/3), hypokalemia (1/3), elevated liver enzymes (1/3), leukocyte decrease (1/3), pericardial effusion (1/3), and proteinuria (1/3).ConclusionApatinib has good effect in advanced malignant tumors in lung, and the side effects are tolerated by reducing the doses. But all these results still need a large sample to verify.
Apatinib; advanced lung cancer; efficacy; side effect
2017-06-22]
10.3969/j.issn.1009-6663.2017.11.035
215000 江苏 苏州,苏州大学附属第一医院呼吸与危重症医学科
黄建安,E-mail:huang_jian_an@163.com
——评《卵巢恶性肿瘤诊疗手册》

