利拉鲁肽治疗2型糖尿病合并肥胖患者对胰岛素抵抗的影响
潘润洪 梁志群 黄丽儿 向四国 丘文干 黄敏旋 谢锦智
广东省东莞市企石医院内二科,广东东莞 523500
利拉鲁肽治疗2型糖尿病合并肥胖患者对胰岛素抵抗的影响
潘润洪 梁志群 黄丽儿 向四国 丘文干 黄敏旋 谢锦智
广东省东莞市企石医院内二科,广东东莞 523500
目的观察利拉鲁肽及胰岛素治疗2型糖尿病合并肥胖患者对胰岛素抵抗的影响。方法将本研究中70例2型糖尿病合并肥胖患者随机分为试验组和对照组各35例,试验组在利拉鲁肽治疗下和对照组在胰岛素治疗下,通过增加利拉鲁肽的使用量及胰岛素的使用量使两组患者在1个月内血糖控制达标,继续治疗6个月时为观察点1(即治疗6个月时),停试验组利拉鲁肽治疗,若患者血糖仍高,仍继续利拉鲁肽治疗,对照组持续胰岛素治疗1年后为观察终点(即治疗1.5年时)。对比治疗6个月时﹑1.5年后两组患者胰岛素抵抗的差异。观察指标有:HOMA-IR﹑HOMA-β﹑FINS ﹑FBG﹑2hPG﹑HbA1C﹑BMI﹑TG﹑LDL-C。结果试验组在治疗6个月后﹑1.5年后HOMA-IR水平较治疗前下降(P<0.05)。对照组在治疗6个月后﹑1.5年后HOMA-IR水平较治疗前无统计学意义(P>0.05)。试验组在治疗6个月后﹑1.5年后HOMA-IR水平差值较对照组变化显著(P<0.05)。结论利拉鲁肽治疗2型糖尿病合并肥胖患者对胰岛素抵抗减轻明显,减轻体重,改善BMI﹑血糖﹑血脂,不发生低血糖风险。
2型糖尿病合并肥胖;利拉鲁肽;胰岛素;胰岛素抵抗
据最近调查显示我国成人糖尿病患病率已上升达11.6%,糖尿病整体防治现状令人担忧,连续四年的调查结果显示,我国患者HbA1C的达标率分别为35.28%﹑32.33%﹑31.77%﹑30.15%[1],同时 2 型糖尿病合并肥胖患者显著增多[2]。2型糖尿病发病和病情进展的主要原因是胰岛β细胞功能缺陷和胰岛素抵抗,而2型糖尿病合并肥胖患者胰岛素抵抗严重[3-5],减轻体重能减轻胰岛素抵抗,高血糖能得到控制[6]。GLP-1类似物(代表药:利拉鲁肽)以葡萄糖浓度依赖性地促进胰岛素的合成及分泌的同时,抑制胰高血糖素分泌,刺激β细胞增殖及新生并抑制β细胞凋亡[7],发挥其高效降糖作用,同时促进心肌﹑骨骼肌和脂肪细胞的葡萄糖摄入,增加肝糖原贮积,还具有延缓胃排空,抑制食欲,减轻患者体重,改善血脂等多种胰外作用[8]。胰岛素的副作用之一是增加患者体重,增加胰岛素抵抗,血糖渐难控制。本研究以胰岛素抵抗为切入点,对比此二类药物在治疗2型糖尿病合并肥胖患者的地位。具体报道如下。
1 资料与方法
1.1 一般资料
选取我院2015年03~10月门诊70例2型糖尿病合并肥胖患者,随机分为利拉鲁肽治疗组(试验组)35例,胰岛素治疗组(对照组)35例。试验组有6例受试者中途退出,对照组也有6例受试者中途退出,后又各增加6例2型糖尿病合并肥胖患者进行试验,共70例受试者完成试验。试验组35例(男17例,女18例),年龄(49.7±1.5)岁,BMI(31.9±0.3)kg/m2,病程(1.1±0.4)年。对照组35例(男18例,女17例),年龄(47.8±1.3)岁,BMI(31.5±0.3)kg/m2,病程(1.1±0.3)年。比较两组受试者年龄﹑病程﹑BMI﹑HbA1C等一般情况,差异无统计学意义(P>0.05),具有可比性。
1.2 纳入及排除标准
纳入标准:(1)全部受试者均来自东莞市企石医院门诊;(2)年龄18~60岁,男女不限;(3)血糖控制不达标者(FBG>7.0mmol/L或2h PG>11.1mmol/L 且 HbA1C > 7%);(4)BMI> 28kg/m2;(5)肝肾心功能正常。排除标准:(1)对研究药物不耐受或过敏或有禁忌症;(2)半年内使用过噻唑烷二酮(PZD)类降糖药﹑GLP-1类似物及胰岛素者;(3)严重糖尿病急慢性并发症和其他内分泌相关肿瘤或炎症;(4)1年内曾参与药物或手术减肥项目;(5)需接受长期激素治疗。
1.3 方法
所有受试者均由科研人员教导糖尿病饮食方面知识﹑运动方面知识﹑注射利拉鲁肽的技术﹑注射胰岛素的技术﹑监测指尖血糖的技术,可能出现的不良反应的知识及与科研人员报告处理追踪访问。试验组开始予利拉鲁肽(丹麦诺和诺德公司,J20110026)0.6mg/d,早餐前皮下注射,每4~7天监测血糖,若空腹指尖血糖(FPG)>7.0mmol/L或餐后2小时指尖血糖(2hPG)>11.1mmol/L,利拉鲁肽每次加量0.6mg,直到血糖控制达标。最大剂量3.0mg/d。对照组开始予体重×0.7为胰岛素总量,分1/2量为睡前皮下注射的长效胰岛素(甘精胰岛素,来得时,法国赛诺菲安万特公司,J20140054),剩下的1/2量再等分为3份,为三餐前皮下注射的速效胰岛素(赖脯胰岛素,优泌乐,美国礼来公司,J20140152),每4-5天监测血糖,若空腹指尖血糖(FPG)>7.0mmol/L或餐后2小时指尖血糖(2hPG)>11.1mmol/L,胰岛素个体化加量2 ~ 8U,直到血糖控制达标。
1.4 观察指标
两组受试者治疗前测量身高﹑体重﹑计算BMI;抽取静脉血测量 FINS﹑FBG﹑2hPG﹑HbA1C﹑TG﹑LDL-C,并计算稳态模型评估的胰岛素抵抗指数(HOMA-IR=FINS×FBG/22.5)﹑胰岛β细胞基础功能(HOMA-β=20×FINS/(FPG-3.5))。到观察点1及观察终点时重复上述操作。
1.5 不良反应处理
试验期间出现便秘﹑腹泻﹑恶心﹑呕吐﹑皮疹﹑心悸﹑胸闷﹑胸痛﹑乏力等症状或出现一般低血糖反应予及时处理并记录,肝肾心功能异常且进行性升高或反复低血糖反应,且不能缓解,予退出试验并记录。
1.6 统计学处理
采用统计学软件SPSS19.0版对数据进行统计分析,计量资料采用()表示,配对t检验比较组内治疗前后,独立样本t检验比较组间治疗前后。P<0.05为差异有统计学意义。
2 结果
2.1 利拉鲁肽治疗组(试验组)治疗前后治疗效果比较
试验组在治疗6个月后﹑1.5年后BMI﹑HbA1C﹑FBG﹑2hPG﹑TG﹑LDL-C﹑FINS水平较治疗前下降(P<0.05);HOMA-β水平较治疗前上升(P<0.05);HOMA-IR水平较治疗前下降(P<0.05)。见表1~2。
2.2 胰岛素治疗组(对照组)治疗前后治疗效果比较
对照组在治疗6个月后﹑1.5年后HbA1C﹑FBG﹑2hPG 水平较治疗前下降(P< 0.05);FINS﹑HOMA-β水平较治疗前上升(P<0.05);HOMAIR水平较治疗前无统计学意义(P>0.05)。1.5年后BMI水平较治疗前上升(P<0.05)。见表3 ~ 4。
2.3 两组治疗效果差值比较
试 验 组 在 治 疗 6个 月 后 BMI﹑FBG﹑TG﹑LDL-C﹑FINS﹑HOMA-β﹑HOMA-IR 水平差值较对照组变化显著(P< 0.05),HbA1C﹑2hPG 水平差值两组变化不显著(P>0.05),见表5;试验组在治疗 1.5年后 BMI﹑HbA1C﹑FBG﹑TG﹑LDL-C ﹑FINS﹑HOMA-β﹑HOMA-IR水平差值较对照组变化差异有统计学意义(P<0.05),2hPG水平差值两组变化无统计学意义(P>0.05),见表6。
表1 利拉鲁肽治疗组在观察点1时治疗前后各项指标比较( ± s)
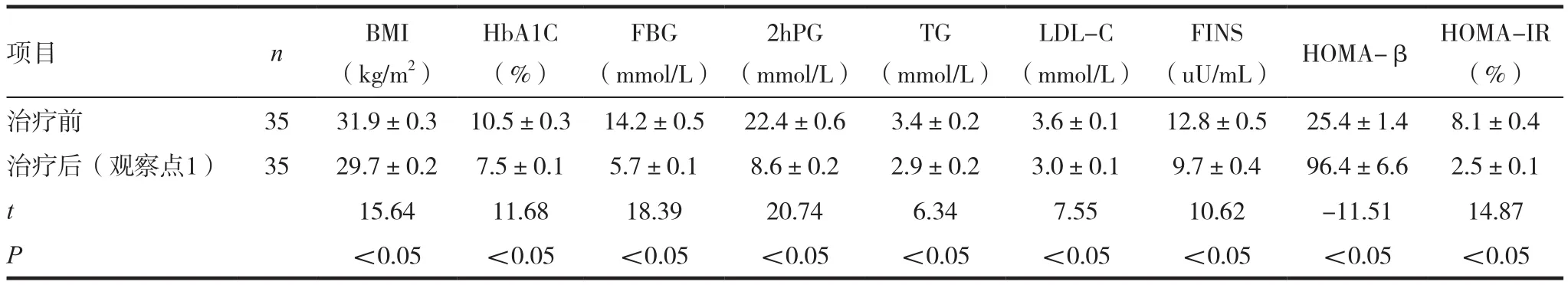
表1 利拉鲁肽治疗组在观察点1时治疗前后各项指标比较( ± s)
(uU/mL) HOMA-β HOMA-IR(%)治疗前 35 31.9±0.3 10.5±0.3 14.2±0.5 22.4±0.6 3.4±0.2 3.6±0.1 12.8±0.5 25.4±1.4 8.1±0.4治疗后(观察点1) 35 29.7±0.2 7.5±0.1 5.7±0.1 8.6±0.2 2.9±0.2 3.0±0.1 9.7±0.4 96.4±6.6 2.5±0.1 t 15.64 11.68 18.39 20.74 6.34 7.55 10.62 -11.51 14.87 P<0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05项目 n BMI(kg/m2)HbA1C(%)FBG(mmol/L)2hPG(mmol/L)TG(mmol/L)LDL-C(mmol/L)FINS
表2 利拉鲁肽治疗组在观察终点时治疗前后各项指标比较(± s)
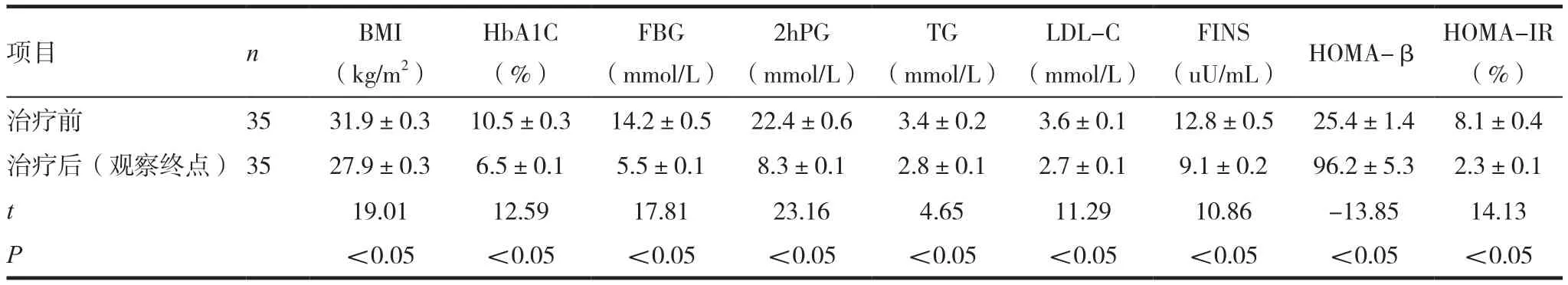
表2 利拉鲁肽治疗组在观察终点时治疗前后各项指标比较(± s)
(uU/mL) HOMA-β HOMA-IR(%)治疗前 35 31.9±0.3 10.5±0.3 14.2±0.5 22.4±0.6 3.4±0.2 3.6±0.1 12.8±0.5 25.4±1.4 8.1±0.4治疗后(观察终点) 35 27.9±0.3 6.5±0.1 5.5±0.1 8.3±0.1 2.8±0.1 2.7±0.1 9.1±0.2 96.2±5.3 2.3±0.1 t 19.01 12.59 17.81 23.16 4.65 11.29 10.86 -13.85 14.13 P<0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05项目 n BMI(kg/m2)HbA1C(%)FBG(mmol/L)2hPG(mmol/L)TG(mmol/L)LDL-C(mmol/L)FINS
表3 胰岛素治疗组在观察点1时治疗前后各项指标比较( ± s)
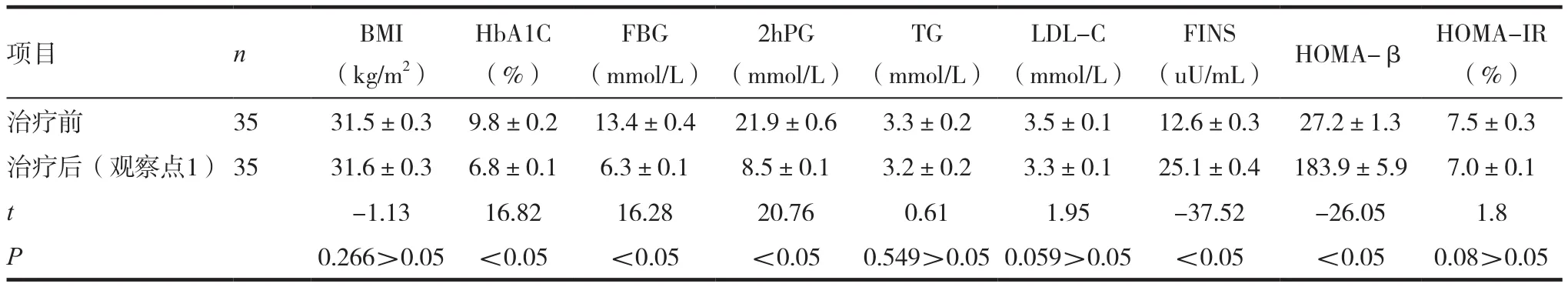
表3 胰岛素治疗组在观察点1时治疗前后各项指标比较( ± s)
(uU/mL) HOMA-β HOMA-IR(%)治疗前 35 31.5±0.3 9.8±0.2 13.4±0.4 21.9±0.6 3.3±0.2 3.5±0.1 12.6±0.3 27.2±1.3 7.5±0.3治疗后(观察点1) 35 31.6±0.3 6.8±0.1 6.3±0.1 8.5±0.1 3.2±0.2 3.3±0.1 25.1±0.4 183.9±5.9 7.0±0.1 t-1.13 16.82 16.28 20.76 0.61 1.95 -37.52 -26.05 1.8 P 0.266>0.05 <0.05 <0.05 <0.05 0.549>0.05 0.059>0.05 <0.05 <0.05 0.08>0.05项目 n BMI(kg/m2)HbA1C(%)FBG(mmol/L)2hPG(mmol/L)TG(mmol/L)LDL-C(mmol/L)FINS
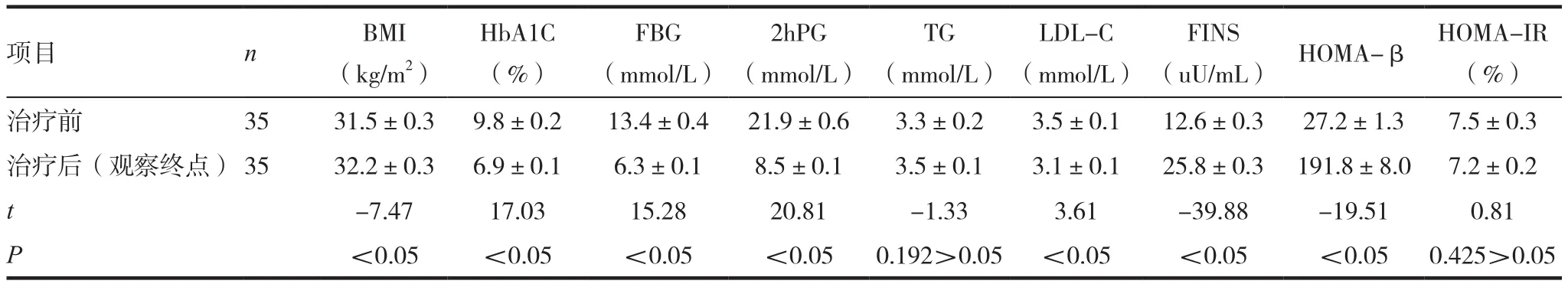
表4 胰岛素治疗组在观察终点时治疗前后各项指标比较(x ± s)
2.4 伴随事件
试验组治疗初期有14例患者感恶心﹑腹胀,能耐受,治疗2~4周症状消失,能继续治疗,全部患者无发生低血糖事件,有6例中途退出,原因主要是药物价格高,难以继续治疗;对照组出现4例一般性低血糖,及时进食纠正,未出现严重低血糖,有6例中途退出,原因有搬家﹑注射胰岛素次数多拒绝继续治疗等。
3 讨论
世界各地糖尿病患病率均在急剧上升,糖尿病已成为目前最主要的内分泌代谢疾病,是引起代谢综合征的重要因素[9],严重影响人们的身体健康,是全球范围的公共健康问题。糖尿病主要致病机制是胰岛β细胞功能缺陷或胰岛素抵抗,而2型糖尿病合并肥胖患者胰岛素抵抗为主要原因,PZD类药对胰岛素抵抗有一定的效果,但近年来研究发现该类药的副作用[10](如增加心力衰竭风险等)限制了其应用。利拉鲁肽是胰高血糖素样肽-1的一种人工合成类似物,Drab[11]和Vilsboll[12]研究后发现,利拉鲁肽能促进胰岛素的合成及分泌,抑制胰高血糖素分泌,刺激β细胞增殖及新生并抑制β细胞凋亡,同时能延缓胃排空,抑制食欲,减轻患者体重,使胰岛素抵抗好转,从而发挥其高效降糖作用,还有调血脂等作用,其不良反应轻微,作为一种新上市的降糖药物,其临床应用前景优异。
表5 两组在观察点1时治疗前后各项指标差值比较( ± s)
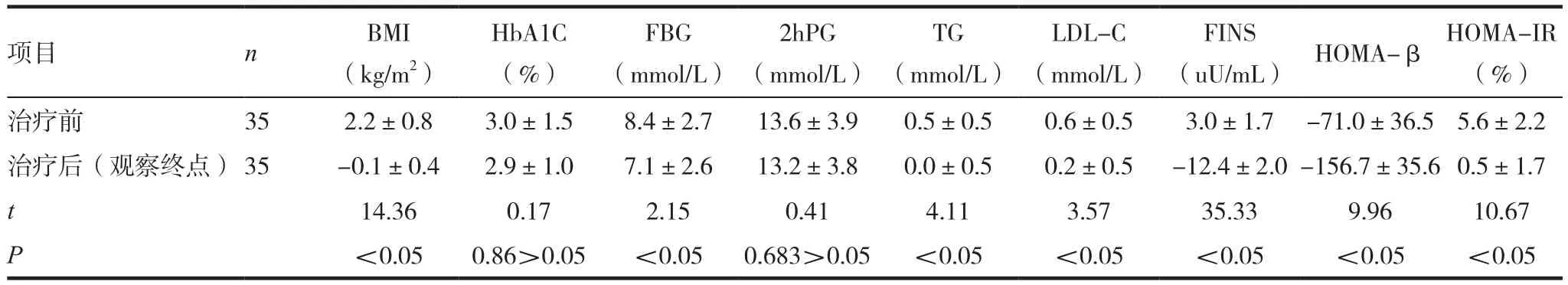
表5 两组在观察点1时治疗前后各项指标差值比较( ± s)
项目 n BMI(kg/m2)(uU/mL) HOMA-β HOMA-IR(%)治疗前 35 2.2±0.8 3.0±1.5 8.4±2.7 13.6±3.9 0.5±0.5 0.6±0.5 3.0±1.7 -71.0±36.5 5.6±2.2治疗后(观察终点)35 -0.1±0.4 2.9±1.0 7.1±2.6 13.2±3.8 0.0±0.5 0.2±0.5 -12.4±2.0-156.7±35.6 0.5±1.7 t 14.36 0.17 2.15 0.41 4.11 3.57 35.33 9.96 10.67 P<0.05 0.86>0.05 <0.05 0.683>0.05 <0.05 <0.05 <0.05 <0.05 <0.05 HbA1C(%)FBG(mmol/L)2hPG(mmol/L)TG(mmol/L)LDL-C(mmol/L)FINS
表6 两组在观察终点时治疗前后各项指标差值比较( ± s)
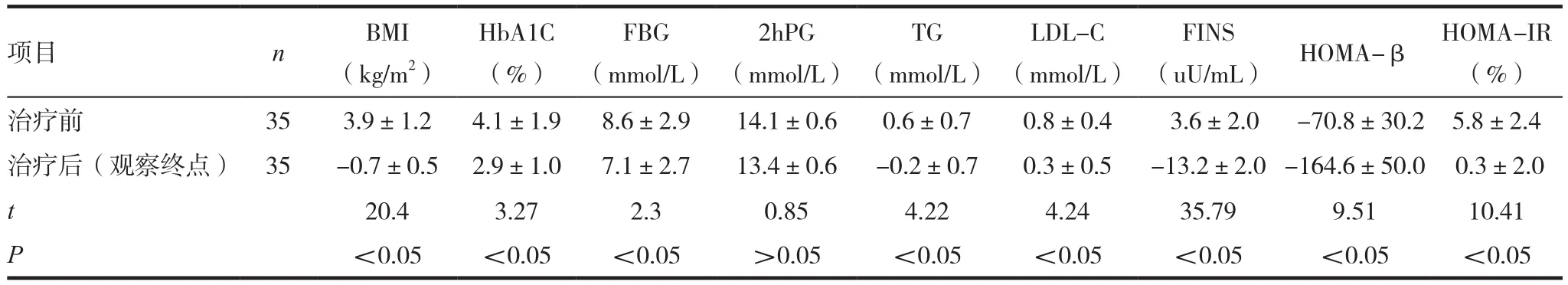
表6 两组在观察终点时治疗前后各项指标差值比较( ± s)
项目 n BMI(kg/m2)(uU/mL) HOMA-β HOMA-IR(%)治疗前 35 3.9±1.2 4.1±1.9 8.6±2.9 14.1±0.6 0.6±0.7 0.8±0.4 3.6±2.0 -70.8±30.2 5.8±2.4治疗后(观察终点) 35 -0.7±0.5 2.9±1.0 7.1±2.7 13.4±0.6 -0.2±0.7 0.3±0.5 -13.2±2.0-164.6±50.0 0.3±2.0 t 20.4 3.27 2.3 0.85 4.22 4.24 35.79 9.51 10.41 P<0.05 <0.05 <0.05 >0.05 <0.05 <0.05 <0.05 <0.05 <0.05 HbA1C(%)FBG(mmol/L)2hPG(mmol/L)TG(mmol/L)LDL-C(mmol/L)FINS
2型糖尿病合并肥胖患者的血糖需控制良好,减轻胰岛素抵抗是关键[13],HOMA-IR是胰岛素抵抗严重程度的评价指标[14],胰岛素抵抗程度越严重该值越高,胰岛素抵抗程度减轻该值下降。本研究表明,试验组治疗6个月后﹑1.5年后HOMA-IR与治疗前比较及与对照组比较均显著下降,提示受试者的胰岛素抵抗能被利拉鲁肽减轻,且体重也减轻,部分受试者血糖得到蜜月期缓解(本次试验组中有5例患者达到蜜月期缓解);而对照组HOMA-IR较治疗前反而增加,提示胰岛素虽然能控制2型糖尿病合并肥胖患者的血糖,但胰岛素抵抗加重,胰岛素使用量也渐增加,患者体重渐增加;两组治疗前后各项指标差值比较,提示利拉鲁肽治疗2型糖尿病合并肥胖患者效果明显,且利拉鲁肽以葡萄糖浓度依赖性地起降糖作用,极少引起低血糖[15],本研究中试验组的患者均未发生低血糖,故利拉鲁肽可作为今后治疗该类患者的优先选择,而胰岛素在治疗该类患者作为次要选择。
本研究是受试者在血糖控制达标的情况下评估使用利拉鲁肽后及使用胰岛素后受试者胰岛素抵抗在不同的时间点是否有减轻,因利拉鲁肽固有的药物特性在治疗后患者可能减量或暂停使用该药时血糖仍能控制达标,或血糖达标时仍使用该药也不会引起低血糖,故本研究人为规定6个月内都必须使用该药,而6个月后到1.5年内根据血糖是否达标来决定是否继续使用利拉鲁肽,不能使用其他降糖药物来干扰研究。而胰岛素在2型糖尿病合并肥胖这类患者中是必须使用才能血糖控制达标的,停用血糖肯定升高,故方案中患者是一直使用胰岛素的。
综上所述,胰高血糖素样肽-1类似物利拉鲁肽治疗2型糖尿病合并肥胖患者效果优异,不良反应轻微,具有很好的临床应用前景,但目前该药价格高昂,希望逐渐下调药价,使更多患者能优先选择该药治疗,从而获益更多。
[1] 高雷莉,纪立农,陆菊明,等.2009~2012年我国2型糖尿病患者药物治疗与血糖控制状况调查[J].中华糖尿病杂志,2014,22(7):594-598.
[2] 杨泽,郑宏,史晓红,等.超重﹑肥胖及其与糖尿病的患病风险分析[J].中华内分泌代谢杂志,2003,19(3):177-180.
[3] 杨凌辉,邹大进.肥胖致胰岛素抵抗的机制[J].中华内分泌代谢杂志,2002,18(3):244-246.
[4] 邹大进,吴鸿.腹型肥胖致胰岛素抵抗的机制及治疗展望 [J].中国糖尿病杂志,2006,14(4):309-312.
[5] 王秋月,张秀斌,张凌云,等.2型糖尿病血浆抵抗素水平与胰岛素敏感性相关因素的研究[J].中国糖尿病杂志,2006,14(5):338-339.
[6] 张致丹,李志军.减重治疗对胰岛功能的改善[J].中华医学写作杂志,2004,11(15):1294-1295.
[7] 郭晓蕙.利拉鲁肽对β细胞的保护和早期获益[J].药品评价,2014,11(15):38-42.
[8] 郭晓蕙,利拉鲁肽LEAD-6及后续研究结果浅析[J].药品评价,2010,7(15):30-31.
[9] 潘长玉.代谢综合征认识和防治的新进展--评《国际糖尿病联盟关于代谢综合征定义的全球共识》[J].中华内分泌代谢杂志,2005.21(4).298-300.
[10] 杨兴华,李婧楠,曾勍婕.吡格列酮不良反应国内外研究现状 [J].药品评价,2012,9(23):6-9.
[11] Drab SR.Clinical studies of liraglutide,a novel,oncedaily human glucagon-like peptide-1 analog for improved management of type 2 diabetes mellitus[J].Pharmacotherapy,2009,29(12):43-54.
[12] Vilsboll T.The effects of glucagon-like peptide-1 on the beta cell[J].Diabetes Obes Metab,2009,11(3):238-240.
[13] 马存花,王小春,艾比拜,等.利拉鲁肽对2型糖尿病患者胰岛素抵抗的影响[J].国际检验医学杂志,2016,37(17):2398-2400.
[14] 张家庆.HOMA-IR是个较好的胰岛素抵抗指数[J].中华内分泌代谢杂志,2005,21(4):304-305.
[15] 潘长玉.长效人胰升血糖素样肽-1类似物利拉鲁肽的安全性回顾[J].中国糖尿病杂志,2011,19(7):555-558.
Effect of liraglutide on insulin resistance in patients with type 2 diabetes mellitus combined with obesity
PAN Runhong LIANG Zhiqun HUANG Lier XIANG Siguo QIU Wengan HUANG Minxuan XIE Jinzhi
Second Division of Neurology,Qishi Hospital of Dongguan City,Dongguan 523500,China
ObjectiveTo observe the effect of liraglutide and insulin on insulin resistance in patients with type 2 diabetes mellitus combined with obesity.MethodsSeventy patients with type 2 diabetes mellitus combined with obesity were randomly divided into two groups of 35 patients.The patients in experimental group were treated with liraglutide and the patients in control group were treated with insulin.By increasing the use of liraglutide and the use of insulin,the blood glucose control of the two groups reached the standard within 1 month.To continue treatment for 6 months was observation point 1 (6 months of treatment),the experimental group stopped the treatment of liraglutide therapy,if the patient's blood glucose remained high, continued to be treated with liraglutide.The control group continued insulin treatment 1 year later was the end point of observation (1.5 years).The differences in insulin resistance in 2 groups after 6 months and 1.5 years were compared.The observation indicators were HOMAIR﹑HOMA-β﹑FINS ﹑FBG﹑2hPG﹑HbA1C﹑BMI﹑TG﹑LDL-C.ResultsAfter the treatment of 6 months and 1.5 years,the HOMA-IR level decreased (P<0.05).In the control group,HOMA-IR levels was not statistically significant after 6 months and 1.5 years of treatment(P>0.05).The difference of HOMA-IR between experimental group and the control group was significant(P<0.05) after 6 months and 1.5 years of treatment.ConclusionLiraglutide which treatment in patients with type 2 diabetes mellitus combined with obesity can reduce insulin resistance,reduce weight,improve BMI blood lipid, and no hypoglycemia risk.
Type 2 diabetes mellitus combined with obesity;Liraglutide;Insulin;Insulin resistance
R587.1
A
2095-0616(2017)19-61-05
广东省东莞市科技计划医疗卫生类科研项目(2015105101163)。
2017-06-21)

