《化学工艺学》教学实践与探讨
史瑞欣
摘要:本文以天然气蒸气转化制合成气的生产工艺为典型案例,对《化学工艺学》教学过程中,教师如何充分运用案例式、启发式教学方法使学生在学习本课程时,对化工产品生产工艺流程形成清晰的设计思路,建立科学的思维方法进行了探讨。
关键词:《化学工艺学》;典型案例;设计思路
中图分类号:G642.0 文献标志码:A 文章编号:1674-9324(2017)40-0158-02
《化学工艺学》是化学工程与工艺专业的一门重要的专业基础课程,是高等化工教育的核心内容之一。该课程将学生所学的化学与化工基础知识运用到产品工业化的实践中,在化工专业课程体系中,具有承前启后和知识集大成的特点。
化学工艺是以过程为研究目的,重点解决整个生产过程的组织、优化;将各单项化学工程技术在以产品为目标的前提下集成,解决各单元间的匹配、链接;在确保产品质量的条件下,实现全系统的能量、物料及安全污染诸因素的优化[1]。因此,在化工工程项目中,化学工艺承担着核心作用。只有根据工艺的要求,才能合理利用化学工程、工业催化、化工机械和系统控制等学科的最新成就,提供所需设备,组织合成出最先进的流程,其他诸如土建工程、公用工程、安全与环保等均围绕着如何满足工艺要求而实施[2]。因此,《化学工艺学》课程在培养具有创新精神和工程实践能力的高水平化学工业科技人才中,占有举足轻重的地位。
《化学工艺学》课程内容涉及面广,涵盖了无机化工、有机化工、高分子化工、精细化工和生物化工等领域,综合性强,工艺纷繁,流程复杂。为了使学生在有限的教学学时内对《化学工艺学》有深入的理解和清晰的学习思路,笔者就自身在教学实践中的教学体会,提出应通过选取典型案例,使学生明晰工艺开发思路,从而实现上述的教学目标。
为了使学生在学习工艺学课程时能够建立清晰的学习思路,了解化工产品生产工艺开发的主要过程,使学生在学习过程中不是被动地接受教师对一个又一个化工产品的工艺路线简单、枯燥的介绍,而是能够与教师在课堂上一起针对一个产品,按照“反应原理—热力学—动力学—工艺条件—反应设备—工艺流程”这样一条逻辑主线,完成对该产品工艺路线的学习,不仅“知其然”,更“知其所以然”,两种学习效果的差别自是不言而喻。下面,将以“天然气蒸气转化制合成气”为例,介绍如何在教学过程中,通过典型案例向学生介绍化工产品工艺开发的基本思路与主要步骤。
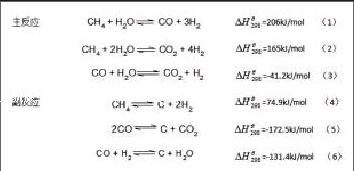
首先,向学生介绍甲烷水蒸气转化过程的主、副反应,如(图)式(1)—(6)所示,这是化工产品生产过程的核心,也是产品生产工艺设计的入手点。
从上述的主、副反应出发,教师首先与学生一起对反应式进行观察,总结反应特点。甲烷蒸气转化制合成气的反应特点可以归纳为以下三点:①主、副反应均为可逆反应;②主反应(1)、(2)为强吸热反应,副反应(4)为吸热反应,其余均为放热反应;③若操作条件不适当,副产物大量产生,将发生析碳现象,应特别注意防止。这些信息虽然并不复杂,但教师应该使学生学会从上述几方面,即反应是否可逆,主、副反应的热效应如何,主、副产物是否影响催化剂的催化活性,等等来观察反应式,获取对热力学、动力学分析有用的信息。这种对问题思考方式的培养,实际上都是在日常教学过程中逐渐实现的。接下来,教师将带领学生一起分析该生产过程的热力学特点,讨论温度、水碳比和压力对化学平衡的影响。首先是对温度的分析。为了方便学生分析问题,教师可以一边与学生回忆,一边在黑板上把温度对化学平衡影响的规律简要地列出来,利用这个规律学生可以看出,甲烷与水蒸气反应生成CO和H2是吸热的可逆反应,因此升高反应温度将使产物CO和H2的平衡产率提高,原料CH4的平衡含量降低。同时,由于一氧化碳变换反应是放热的可逆反应,高温不利于该反应的进行,可以减少二氧化碳的生成,并且高温还会抑制一氧化碳歧化和还原析碳这两个放热型的副反应,但温度过高将有利于甲烷的裂解。这些结论都是将温度对反应平衡的影响规律应用于甲烷蒸气转化过程并根据主、副反应的热效应分析得到的,在思维逻辑上并不复杂,学生从这里着手,不会产生畏难情绪。为了增强学生的感性认识,当学生跟随教师的思路完成上述的分析过程后,教师可以将主、副反应平衡常数随温度变化的实验数据呈现给学生,使学生更加直观地体会到,他们通过科学地分析所得到的结论是能够经得住实践检验的。
采用与上述教学过程相似的组织方法和教法,教师继续与学生完成对水碳比和压力的分析,从而得到下述结论,即从反应平衡的角度考虑,甲烷蒸气转化过程应该采用适当的高温、稍低的压力和高水碳比。
在现代化工生产中,近90%的化学反应需使用催化剂,因此学生应对重要反应类型所使用的催化剂有所了解,并对催化剂在化工生产中的影响引起足够重视。甲烷水蒸气转化过程也是在催化剂的催化作用下,实现在较低的反应温度获得理想的反应速率,从而使该过程具备了工业生产价值。在对其反应动力学进行分析时,依据的是催化条件下的动力学方程。首先,讨论温度的影响。当温度升高时,反应速率常数增大,由相关的动力学方程可知,反应速率也增大。其次,讨论压力的影响。如果提高总压,则各组分压也相应有了提高,对反应初期速率提高很有利。最后,讨论组分的影响。水碳比过高,虽然水蒸气分压高,但甲烷分压过低,反应速率不一定高,反之亦然,因此水碳比要适当。
教师在引领学生完成上述热力学与动力学特征分析后,以此为理论依据,对工艺条件进行选择。本文仅以操作压力为例,对教师的教学过程进行介绍。从热力学特征来看,低压有利于转化反应进行。从动力学特征看,反应初期,加压使反应速率加快,但当反应接近平衡时,由于产物浓度高,此时加压反而会降低反应速率。因此,从化学角度看,压力不宜过高。但实际生产过程还需从工程角度考虑,由于甲烷转化制合成气的主反应是吸热反应,需要外部供热使反应在一定温度下顺利进行,而大的给热系数是强化传热的前提,提高压力能够有效提高给热系数,因此提高操作压力对传热有利,并且加压还可以减小设备、管道的体积,提高设备的生产强度。从上述化学、工程角度进行综合考虑,确定甲烷蒸气转化过程的操作压力为3MPa左右。在3MPa的压力下,若使反应器出口残余甲烷含量低至0.3%(干基),反应温度需达到1000℃,但反应器的材质经受不了这么高的温度,因此甲烷蒸气转化制合成气的生产工艺要求将转化过程分为两段进行。从一段、二段转化炉对反应温度的要求为出发点,教师引导学生从反应器的结构特点、反应器的材质要求、不同温位的余热回收等方面进行分析,进而对合成气生产工艺流程和典型设备进行学习。
通过上述内容的学习,学生对天然气蒸气转化制合成气这个气固相催化反应过程的工艺特点有了较为深入的了解,当学生再接触类似的生产过程时,将能够按照这种对相关问题的思考方式进行正确的分析,这正是我们的教学目的所在。正所谓“授之以鱼不如授之以渔”,通过对工艺学的学习,使学生逐步建立总体观念、系统观念,不仅有解决局部问题的本领,更具备统领全局,建立以产品为目标的全系统优化合成的理念[2],这正是《化学工艺学》课程的精髓所在。
参考文献:
[1]米镇濤.化学工艺学[M].北京:化学工业出版社,2012.
[2]米镇涛,张香文,王苙.当代“化学工艺学”的地位与展望[J].化学工业与工程,2005,(22):75-77.endprint

