聚硅氧烷离子液体用于快速气相色谱固定相的研究
叶晓雨, 孙晓杰,2, 赵晓洁, 张 娜, 张 茜, 柳 杨, 邢 钧*
(1.生物医学分析化学教育部重点实验室,武汉大学化学与分子科学学院,湖北武汉 430072;2.中国水产科学研究院黄海水产研究所,山东青岛 266071;3.武汉轻工大学食品工程学院,湖北武汉 430023)
近年来,随着单个样品分析成本的增加,如何提高色谱分析速度逐渐成为研究者们非常感兴趣的课题。快速气相色谱(Fast GC)不仅可以极大提高分析效率并节约分析成本,还能提高分析的灵敏度和准确性,可广泛应用于现场及在线分析。1961年,Desty等[1]对快速气相色谱进行了论证,但面临实验操作和样品制备等许多问题,其优势难以发挥。例如:早在十几年前就可以实现九种物质在0.7 s内的分离[2],却不能用同样的速度分析多氯联苯的上百种异构体[3]。因此,很多科研工作都致力于研究实际应用中有效地快速气相色谱分离[4 - 5]。方法大致可分为三种:分离度最小化、提高色谱系统的选择性和在保证分离度恒定的条件下缩短分离时间。缩短柱长、减小内径是目前最常用的手段,但会严重影响柱效和分离度,而解决该问题最佳手段就是提高色谱固定相的分离选择性。
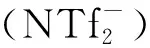
1 实验部分
1.1 主要仪器与试剂
Agilent 6890N气相色谱仪(美国,Agilent公司),配有FID检测器;SETSYS 16TG 热重分析仪(法国,AETARAM公司);Milli-Q超纯水装置(美国,Millipore公司);弹性石英毛细管柱(75 μm i.d.,河北永年光纤维厂),从商用DB-1色谱柱(30 m×0.32 mm×0.25 μm,美国Agilent公司)截取8 m用于对比,用萘测得柱效为3 635N/m。
1-甲基咪唑(99%,分析纯,Fluka公司);二(三氟甲基磺酸酰)亚胺锂(98%,分析纯,Acros公司);氯丙基甲基二乙氧基硅烷、六甲基二硅氧烷和二甲基二乙氧基硅烷(98%,化学纯,武大有机硅公司);二氯甲烷、甲醇(分析纯,上海国药化学试剂有限公司);其它所有测试药品均为分析纯(上海国药化学试剂有限公司)。
1.2 快速气相色谱柱的制备
1.2.1毛细管的预处理石英毛细管柱(3 m×75 μm i.d.) 和石英毛细管柱(8 m×0.25 mm i.d.) 均分别用5 mL甲醇和5 mL二氯甲烷冲洗后,在300 ℃下通氮气高温处理4 h,备用。
1.2.2聚硅氧烷离子液体的制备首先合成侧链为卤代烷烃的聚硅氧烷,然后通过季铵盐反应将甲基咪唑键合到聚硅氧烷链上,制得聚硅氧烷键合的离子液体([PSOMIM][Cl],A)[10],最后通过阴离子交换反应制得另一聚硅氧烷键合的离子液体([PSOMIM][NTf2],B)[12]。合成路线见图1。
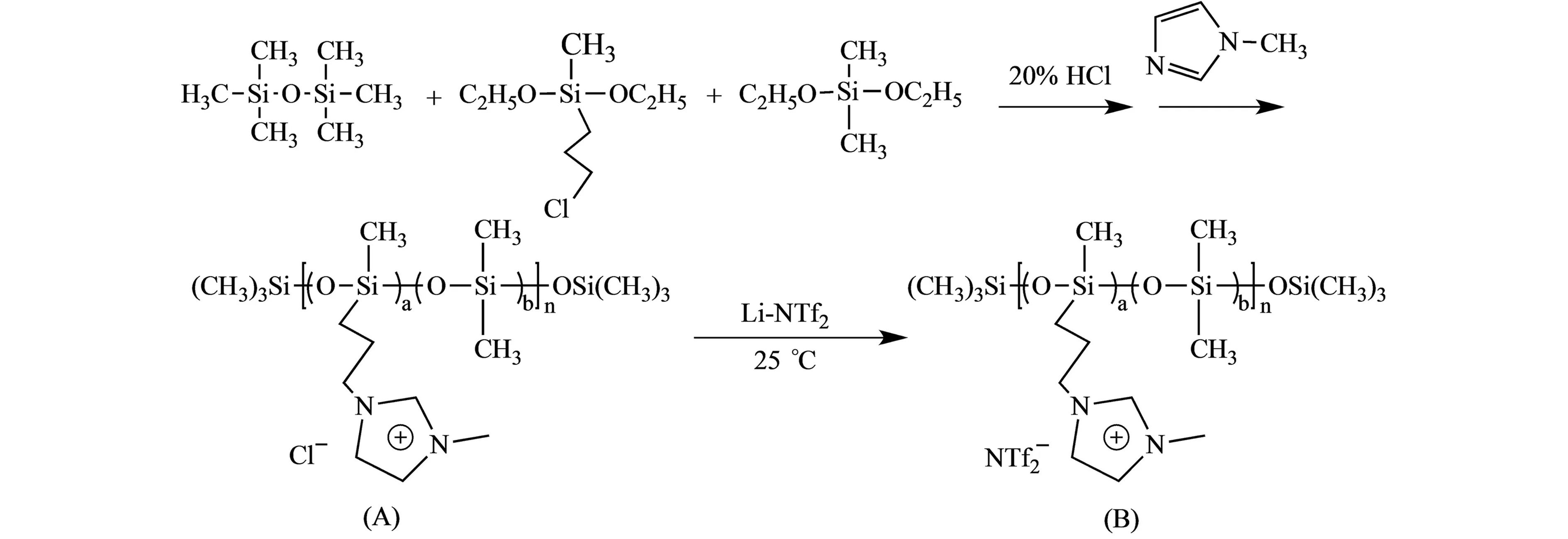
图1 [PSOMIM][NTf2]的合成路线Fig.1 Synthetic route of compound [PSOMIM][NTf2]
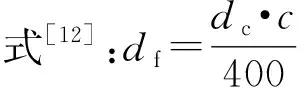
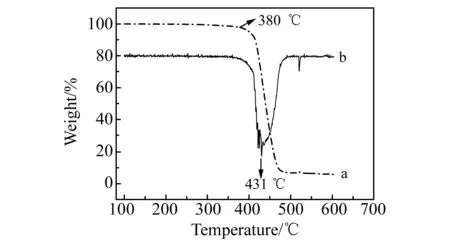
图2 [PSOMIM][NTf2]的热重(a) 和差热分析(b)图(以10 ℃/min 的速率从100 ℃升到600 ℃)Fig.2 Thermogravimetric analysis(a) and differential thermal analysis (b) of [PSOMIM][NTf2](Temperature programmed from 100 ℃ to 600 ℃ at a heating rate of 10 ℃/min)
2 结果与讨论
2.1 聚硅氧烷离子液体的表征
聚硅氧烷离子液体[PSOMIM][NTf2]的核磁表征结果为:1H NMR(CD3OD; 300 MHz):δ(ppm)8.82(s,1H,NCHN),7.56(t,2H,NCHCN),4.19(t,2H,NCH2C),3.92(s,3H,NCH3),1.92(m,2H,CH2CN),0.57(t,2H,CH2CCN)。离子液体[PSOMIM][NTf2]中咪唑单元的含量,可以通过δ8.82 ppm与δ0.093 ppm位移处积分面积的比值计算,约占30%。
为了评价制备的聚硅氧烷离子液体的热稳定性,本文通过热重和差热分析测试了材料的热分解温度。图2是聚硅氧烷离子液体[PSOMIM][NTf2]的热重和差热分析图。由图可知,样品在380 ℃才开始出现缓慢分解,400 ℃以后才出现显著分解,这可以证明[PSOMIM][NTf2]具有较好的热稳定性。
2.2 快速柱的分离性能
2.2.1快速柱的柱效及对Grob试剂的分离性能为了得到制备的色谱柱的柱效,在一定柱温下,用萘测试了色谱柱的理论塔板数,结果见表1。由表1可知,快速柱A的柱效接近8 000N/m,柱效是常规柱C柱效的近两倍。为了更好地评价所制备色谱柱的涂渍效果、分离效率、吸附活性等方面的综合性能,我们用快速柱A和常规柱C对Grob试剂进行分离,图3为其分离谱图。由图3可见,各种组分在快速柱和常规柱上均能很好的分离且峰的对称性较好。此外,十几种组分在2 min左右就能在快速柱上分开,相对于常规柱的4 min提高了约一倍,色谱峰形也得到了较好的改善。因此,当[PSOMIM][NTf2]作为固定相时,同时缩短色谱柱柱长和减小涂层的厚度不会对色谱柱柱效造成损失。

表1 色谱柱的柱效

图3 Grob试剂在快速柱A(A)和常规柱C(B) 上的分离谱图Fig.3 Chromatograms of Grob reagents on the fast column A (A) and fast column B (B).1.n-decane;2.n-undecane;3.n-dodecane;4.nonanal;5.n-octanal;6.2,3-butanediol;7.methyl decanoate;8.methyl undecanoate;9.2,6-dimethylphenol;10.methyl dodecanoate;11.2,6-dimethylaniline,Conditions:(A) 60 ℃ for 0.5 min,60 ℃/min to 180 ℃,Linear velocity:16 cm/s;(B) 80 ℃ for 1 min,35 ℃/min to 180 ℃,Linear velocity:15 cm/min.
2.2.2对异构体的分离性能本文选取一些代表性的芳香位置异构体作为分析对象,考察了快速柱A、常规柱C以及商用DB-1柱对于异构体的分离选择性能,表2列出了这些异构体在上述色谱柱上的保留因子及分离因子。从表中可以看出,不管是对于弱极性的(二甲苯、甲基萘)还是极性的(甲基酚)亦或是高沸点的异构体(硝基苯胺),快速柱和常规柱的分离度是相当的,且都好于商用柱。[PSOMIM][NTf2]作为固定相可以提高色谱柱的选择性,即使缩短了色谱柱的柱长,大部分的异构体仍然可以被有效地分离。
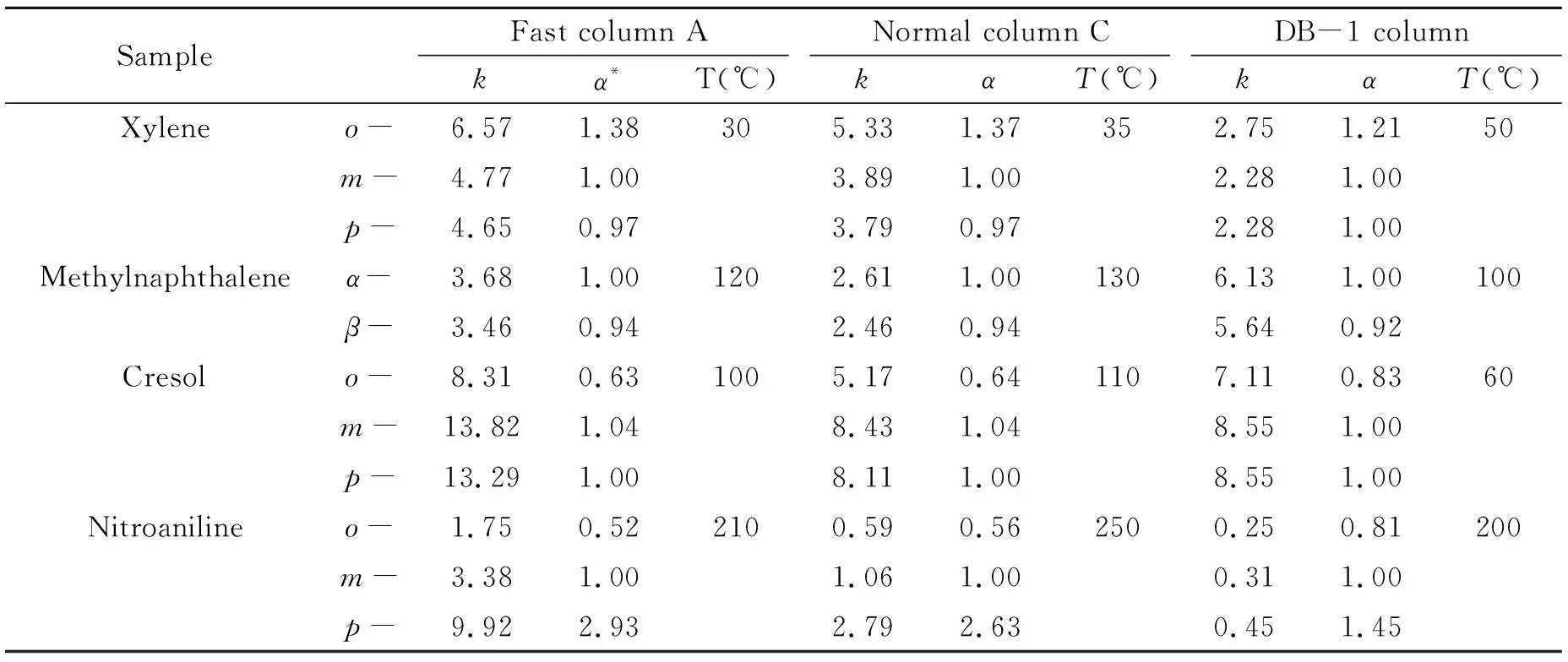
表2 异构体在快速柱A、常规柱C和商用柱DB-1上的保留因子(k) 和分离因子(α)
*αis the relative retention,which is the ratio ofkof each isomer to the second largestkamong isomers.
2.2.3对同系物的分离性能由于离子液体具有特殊的“两性”选择性,因此本文用所制备的色谱柱对极性同系物进行分离以考察其分离性能。图4为邻苯二甲酸酯类化合物分别在快速柱A和常规柱C上的分离谱图。很明显6种邻苯二甲酸酯类在1 min内就能用快速柱全部分离,且分离度分离度良好,与常规柱6 min的分离时间相比,分离速度提高了6倍左右。由此可知,[PSOMIM][NTf2]固定相能保证快速柱的两性选择性同时有效提高检测速度。
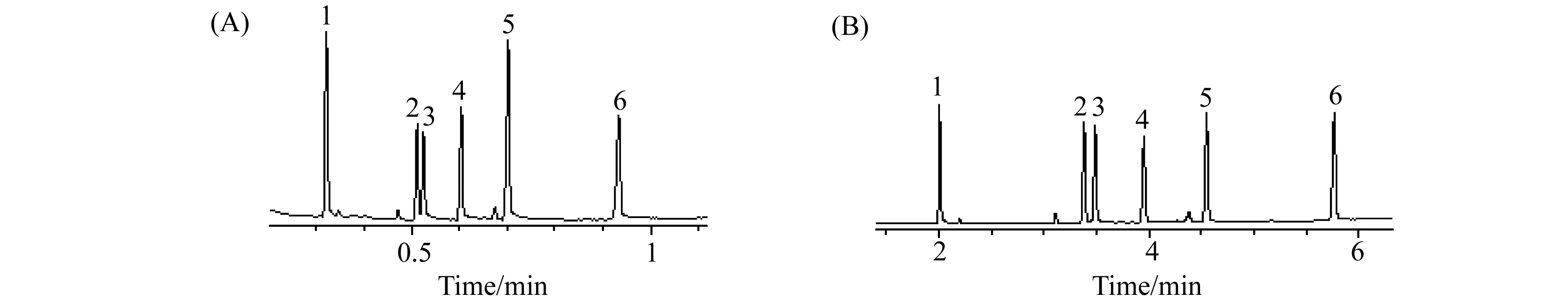
图4 邻苯二甲酸酯类化合物在快速柱A(A)和常规柱C(B)上的分离色谱图Fig.4 Chromatograms of the phthalic acid esters on fast column A (A) and normal column C (B)1.mono-n-butyl phthalate;2.dihexyl phthalate;3.diisooctyl phthalate;4.diisononyl phthalate;5.di-n-octyl phthalate;6.di-n-decyl phthalate,Conditions:(A) Temperature programmed from 220 ℃ to 260 ℃ at 50 ℃/min,linear velocity:31 cm/s;(B) Temperature programmed from 200 ℃ to 260 ℃ at 10 ℃/min,linear velocity:23 cm/s.
2.3 固定相厚度对分离效率的影响
为了研究涂层厚度对分离速度和分离选择性的影响,我们用所制备的两根长度和内径都相同,而膜厚不同的色谱柱A(膜厚0.056 μm) 和色谱柱B(膜厚0.075 μm)对几组同族化合物进行分离。图5、图6分别为9种酚类和11种醇类化合物在柱A和柱B上的分离色谱图。由图可知,在分离酚类化合物时,涂层较薄的快速柱A的分离时间为1 min左右,是涂层较厚的快速柱B的4倍;在分离醇类化合物时,柱A的分离时间大约为2 min,是柱B的两倍左右,同时色谱峰的分离度都没有较大的差异。这一结果说明,在使用[PSOMIN][NTf2]作为固定相时,可以通过减小涂层膜厚实现快速分离。
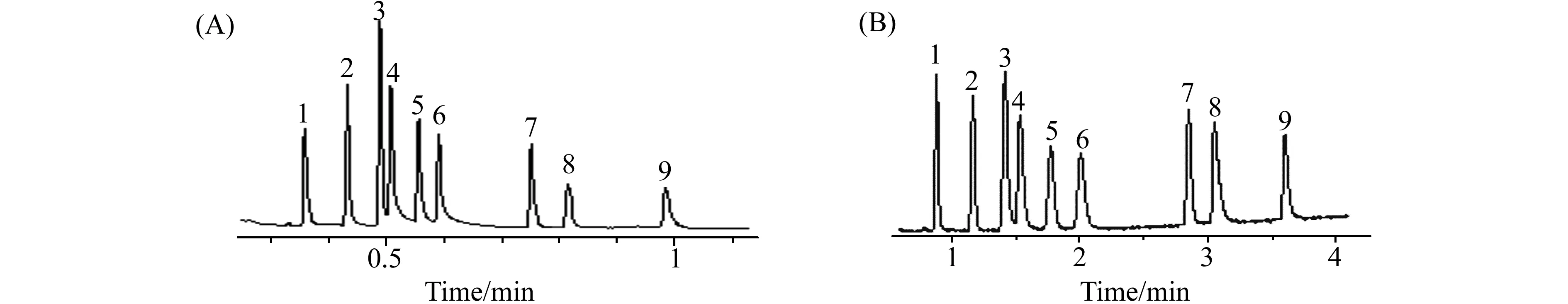
图5 酚类在快速柱A(A) 和柱B(B) 上的分离色谱图Fig.5 Chromatograms of the phenols on fast column A (A) and column B (B)1.o-chlorophenol);2,6-dimethylphenol;3.o-cresol;4.phenol;5.2,4-dimethylphenol;m-cresol;6.m-cresol;7.p-tert-butylphenol;8.m-chlorophenol;9.p-bromophenol,Conditions:(A) Temperature programmed from 130 ℃ to 200 ℃ at 60 ℃/min,linear velocity:24 cm/s;(B) Temperature programmed from 140 ℃ to 200 ℃ at 30 ℃/min,linear velocity:11 cm/s.
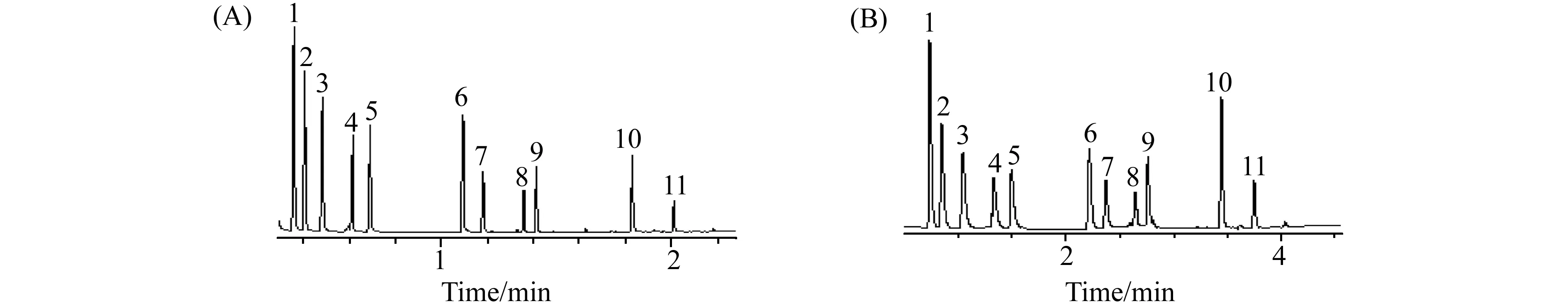
图6 醇类在快速柱A(A) 和柱B(B) 上的分离色谱图Fig.6 Chromatogram of the alcohols on fast column A (A) and column B (B)1.n-propanol;2.isobutanol;3.n-butanol;4.2-pentanol;5.n-pentanol;6.cyclohexanol;7.n-heptanol;8.linalool;9.n-octanol;10.n-decanol;11.n-undecanol,Conditions:(A) 60 ℃ for 0.5 min,50 ℃/min to 150 ℃,linear velocity:19 cm/s;(B) 60 ℃ for 1 min,30 ℃/min to 150 ℃,linear velocity:10 cm/s.
3 结论
本文将聚硅氧烷离子液体[PSOMIN][NTf2]用于制备快速气相色谱柱,通过快速柱与常规柱的对比以及不同涂层厚度的快速柱之间的对比,发现该聚硅氧烷离子液体固定相具有良好的涂渍性能和分离选择性,在大幅提高分离速度的同时仍能维持较好的分离度;在膜厚仅0.056 μm的情况下,色谱柱仍然表现出良好的分离性能。由此可见,聚硅氧烷离子液体在快速气相色谱方面具有良好的应用前景。

