过氧化氢-茜素红s体系催化动力学分光光度法测量痕量钴(II)
张皓爽, 姬泓巍, 宰敬喆, 韩婷婷
(中国海洋大学化学化工学院,海洋化学理论与工程技术教育部重点实验室,山东 青岛 266100)
研究简报
过氧化氢-茜素红s体系催化动力学分光光度法测量痕量钴(II)
张皓爽, 姬泓巍*, 宰敬喆, 韩婷婷
(中国海洋大学化学化工学院,海洋化学理论与工程技术教育部重点实验室,山东 青岛 266100)
本文利用催化动力学原理,建立了新的测定痕量钴(II)的分析方法。研究体系为:钴(II)-茜素红s-过氧化氢-碳酸钠。所得的最佳反应条件为:pH = 11.00,反应时间t= 7.50 min,反应温度θ= 35.0 ℃,ρ(C14H7O7SNa·H2O)=6.400 × 10-2g·L-1,Φ(H2O2) = 7.200 × 10-2%。在该反应条件下,此分析方法的相对标准偏差为1.85%~2.96%,检出限为4.21×10-2ng/mL。在淡水体系中相对标准偏差在1.93%~2.79%之间,而加标回收率在98.7%~101.3%之间。相较于其他测量方法,本文所建立的分析方法具有操作简单,分析温度低,准确度高,检出限低,分析时间短等优点。
钴(II)的测定;催化动力学分光光度法;茜素红s;过氧化氢
钴是人体所必需的微量元素,但如果钴的浓度低于或高于人体所需的正常值,则会对人体的健康产生不利影响[1-2]。由于在工业生产中的广泛应用,如不锈钢、电子的制造,放射性同位素治疗等,钴元素在土壤及水体中的含量逐渐增加[3-4]。因此探究痕量钴的测定方法对环境化学、水化学中重金属钴污染的检测有着重要的意义。
测定钴(II)的方法有很多,譬如溶出伏安法[5-6],高效液相色谱法[7-8],电感耦合等离子体质谱法[9-10],原子吸收法[11-12],化学发光法[13]等。以上方法具有仪器昂贵、分析成本高、分析过程复杂、样品易损耗、实验条件要求苛刻等不足,因此在应用上有一定的局限性。
在测定痕量金属的诸方法中,催化动力学分光光度法因具有选择性好,准确度高,检出限低,仪器简单等优点而得到了广泛的应用。高杰[14]研究了钴(II)与三乙醇胺协同催化H2O2氧化邻苯氨基苯甲酸的反应,建立了测定钴(II)的催化动力学方法;赵丽杰等[15]利用Co(II)对过氧化氢氧化中性红的反应有较强的负催化作用来测定钴(II)的含量;王晓菊等[16]提出了在增敏剂溴代十六烷基吡啶和活化剂氨基乙酸的存在下,钴对高碘酸钾氧化酸性铬兰K的反应具有催化作用;王洪福等[17]发现柠檬酸对双氧水氧化罗丹明B的褪色反应具有阻抑作用,加入钴(II)离子后,阻抑作用明显加强,从而提出测定痕量钴(II)的新方法;孙桃等[18]利用痕量钴(II)对过氧化氢氧化5′-硝基水杨基荧光酮褪色反应的催化作用,提出了测定钴(II)的催化动力学方法; Abouhiat等[19]采用多注射流动自动化系统研究了钴(II)对过氧化氢氧化羟基苯甲酸褪色反应的催化作用,提出了钴(II)-羟基苯甲酸-过氧化氢体系的催化动力学分光光度法; Chaparro等[20]同样应用多注射流动自动化系统对痕量钴(II)的测定方法进行了探究。迄今,虽然这些方法可以用于测定痕量钴(II)的含量,但仍存在一些缺点,如分析温度大多处于高温条件,操作时需采取一定措施使反应骤停,易产生分析误差等。因此,本文对痕量钴(II)在H2O2氧化茜素红s的褪色反应中的催化作用进行了研究,确定了反应体系及最佳反应条件,建立了在室温下能够快速准确测定钴(II)的分析方法。
1 催化动力学光度法原理
催化动力学光度法是利用化学反应的反应速率与金属催化剂浓度之间的关系来进行定量分析的方法,具有检出限低、选择性高、准确度高、仪器简单等优点。
设某一催化反应体系的反应方程式如下:
其中:A为显色剂;B为氧化剂;M为催化剂。因此,显色剂A的反应速率方程式:
(1)
若固定酸度,且反应体系中A、B浓度大大过量时,物质A、B在反应中的浓度变化可忽略,则可视为常数。
在催化动力学实验中,可选用与显色剂浓度有线性关系的物理量来进行测量。因此,可通过测定显色剂的吸光度来监测实验进程。根据Lambert-Beer定律可知,吸光度A与浓度c之间呈线性关系,即:
(2)
其中:A0为无催化剂时反应t时刻的吸光度值;At为有催化剂时反应t时刻的吸光度值。
通过固定时间法,即在反应进行到某一确定时间时读出反应体系的吸光度值,催化剂浓度与吸光度差值呈线性关系。
(3)
由公式(3)可以看出,应用固定时间法,ΔA与体系中催化剂浓度之间具有线性关系,利用非催化体系和催化体系之间的吸光度差值,绘制出待测金属的工作曲线,通过测定未知样品的吸光度值,即可得到未知样品中待测金属的浓度。
2 实验部分
2.1 实验方法
于两支25 mL比色管中分别加入一定量的茜素红s溶液(1.000 g·L-1)和碳酸钠溶液(1.000 mol·L-1),固定体系的pH,其中一支加入一定量的Co(II) 标准溶液,另一支不加Co(II),再分别向两支比色管中加入3% 的过氧化氢溶液,用蒸馏水定容至刻度,摇匀并开始计时。用1 cm比色皿,以蒸馏水为参比,用紫外-可见分光光度仪(HP8453美国惠普公司)在波长334 nm处测定在特定时间下催化和非催化反应体系的吸光度A和A0,计算吸光度的差值ΔA=A0-A。在此过程中反应体系均处于35°C的环境中。
2.2 实验设计
配制不同的反应体系,按2.1中的实验方法进行操作,绘制出吸收曲线,确定实验所需的测量波长。为初步确定分析方法的主要因素及其对应的水平,首先进行正交实验。选取茜素红s质量浓度、过氧化氢体积分数、介质的pH、反应温度和反应时间作为5个影响因素,每个因素选取4个水平,建立5因素4水平正交表L16(45),如表1所示。根据正交实验所得到的影响因素及相应的水平,进行单因素实验,得到最佳的实验反应条件。

表1 5因素4水平L16(45)正交表
3 结果与讨论
3.1 吸收光谱
不同反应体系的吸收光谱如图1所示。3种条件下的吸收曲线形状相同,各自的最大吸收波长均为λ=334 nm。这说明:反应介质对茜素红s的最大吸收波长无明显影响;过氧化氢能够氧化茜素红s,使溶液褪色;痕量Co(II)可加快过氧化氢氧化茜素红s的褪色反应,导致吸光度降低。因此本实验选定的测量波长为λ=334 nm。

(1.溶液组成:6.400×10-2g·L-1茜素红s溶液(pH=11.00);2.溶液组成:6.400×10-2g·L-1茜素红s溶液+7.20×10-2% H2O2溶液(pH=11.00);3.溶液组成:6.400×10-2g·L-1茜素红s溶液+7.20×10-2% H2O2溶液 +0.2000 μg·L-1Co2+(pH=11.00)。Solution composition:1.ρ(C14H7O7SNa·H2O)=6.400×10-2g·L-1(pH=11.00);2.ρ(C14H7O7SNa·H2O)=6.400×10-2g·L-1+Φ(H2O2)=7.20×10-2%(pH=11.00);3.ρ(C14H7O7SNa·H2O) = 6.400×10-2g·L-1+Φ(H2O2)=7.20×10-2%+ρ(Co2+)=0.2000 μg·L-1(pH=11.00).)
图1 吸收光谱
Fig.1 Absorption spectra of alizarin red s
据研究表明,过氧化氢的分解受到pH的限制,在pH=12.0时分解速率达到最高值,同时H2O2的分解受到茜素红或其他相似分子的抑制,而痕量钴可以阻止这种抑制,加速H2O2分解[21]。蒽醌自由基具有芳环离域π键,因此茜素红s易与·OOH发生亲核反应,最后被氧化成为邻苯二甲酸衍生物[22]。这为该体系测量痕量Co(II)提供了理论依据。
3.2 正交试验
正交试验分析结果如表2所示。
通过极差R可以看出,所选5个因素的影响顺序依次为:pH > 反应时间t>反应温度θ> 茜素红s质量浓度 > 过氧化氢体积分数。根据表2中的结果,可以初步确定此分析方法的影响因素及水平,如表3。
3.3 单因素实验
3.3.1 pH值的影响 在正交实验确定的反应条件下,探究pH在10.10~11.65范围内对ΔA的影响,3次实验取平均值,实验结果如图2所示。
由图2可以看出,pH在10.10~11.00范围内,随着体系pH的增大,吸光度的差值ΔA逐渐增大,在pH = 11.00时,ΔA值达到最大;当pH值大于11.00时,ΔA逐渐减小,因此,选择反应体系的最佳pH为pH = 11.00。
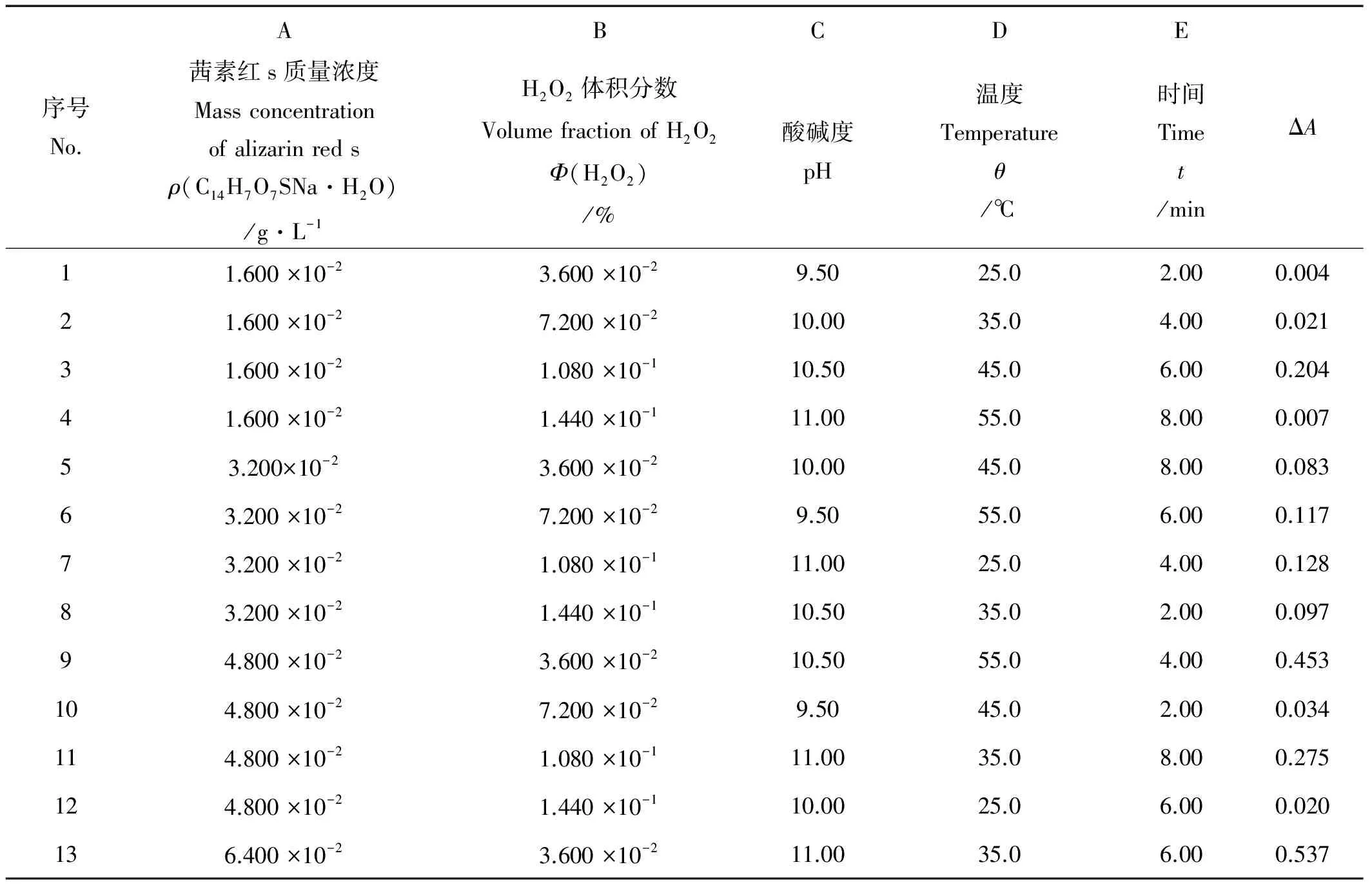
表2 正交实验结果Table 2 The results of the orthogonal experiment
续表2
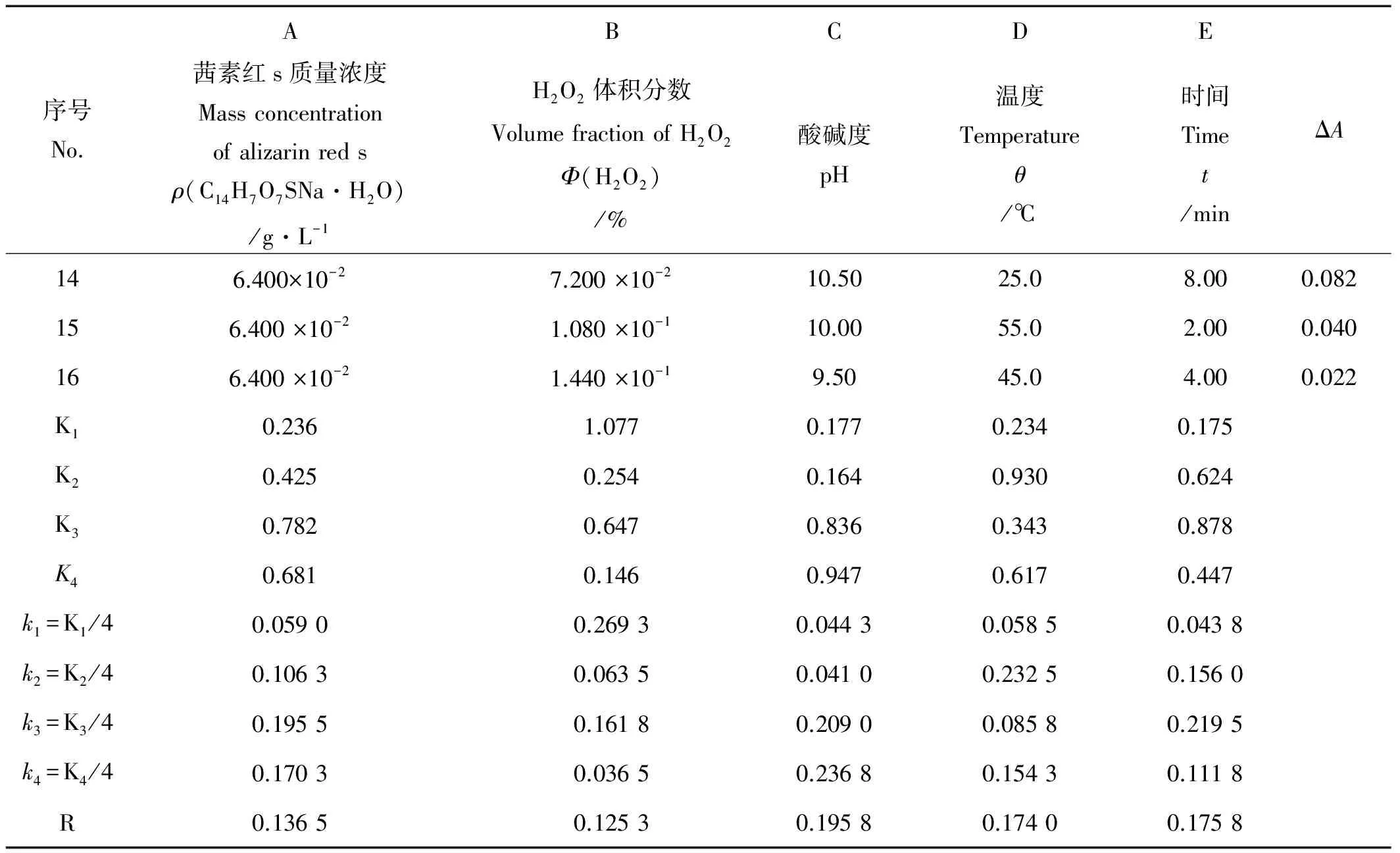
序号No.ABCDE茜素红s质量浓度Massconcentrationofalizarinredsρ(C14H7O7SNa·H2O)/g·L-1H2O2体积分数VolumefractionofH2O2Φ(H2O2)/%酸碱度pH温度Temperatureθ/℃时间Timet/minΔA146.400×10-27.200×10-210.5025.08.000.082156.400×10-21.080×10-110.0055.02.000.040166.400×10-21.440×10-19.5045.04.000.022K10.2361.0770.1770.2340.175K20.4250.2540.1640.9300.624K30.7820.6470.8360.3430.878K40.6810.1460.9470.6170.447k1=K1/40.05900.26930.04430.05850.0438k2=K2/40.10630.06350.04100.23250.1560k3=K3/40.19550.16180.20900.08580.2195k4=K4/40.17030.03650.23680.15430.1118R0.13650.12530.19580.17400.1758
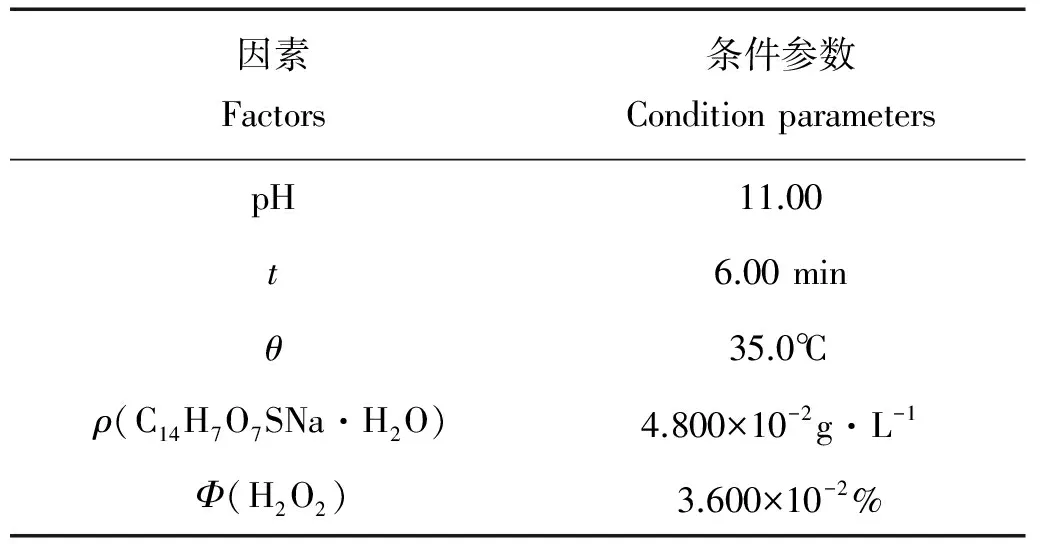
表3 初步确定的影响因素和水平Table 3 Initially identified the influencing factors and levels

图2 pH对ΔA的影响Fig.2 The effect of pH on ΔA
3.3.2 反应时间t的影响 在pH为11.00及正交实验确定的其他反应条件下,探究反应时间t在1.50~9.50 min范围内对ΔA的影响,3次实验取平均值,实验结果如图3所示。
由图3可以看出,t在1.50~7.50 min范围内,ΔA随着反应时间的增加而迅速增大。当t>7.50 min时,ΔA基本不变。因此,选择反应体系的最佳反应时间为t= 7.50 min 。
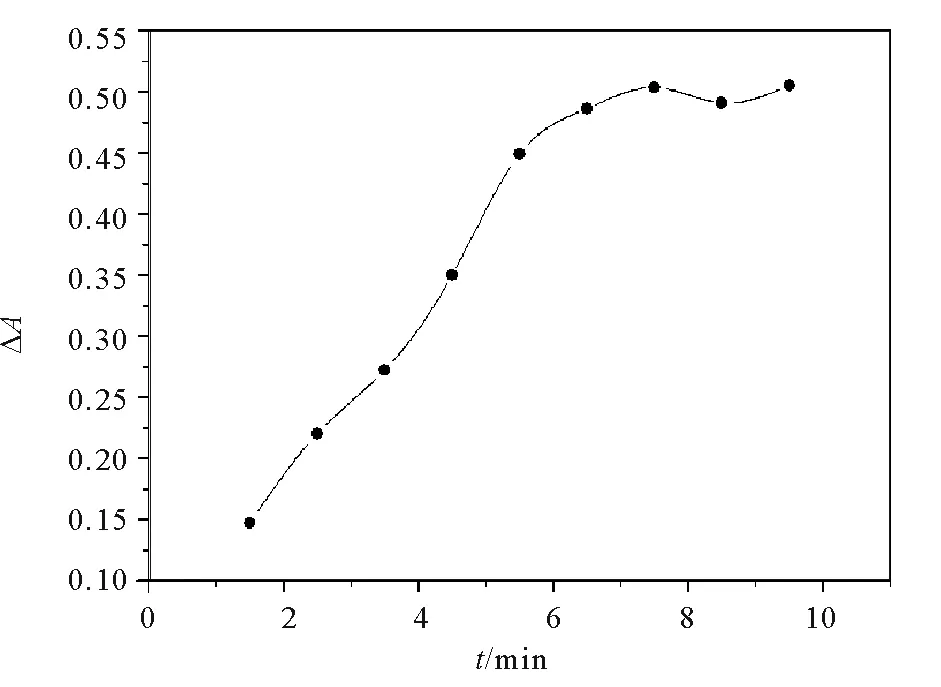
图3 反应时间t对ΔA的影响
3.3.3 反应温度θ的影响 在pH =11.00、反应时间t= 7.50 min及正交实验确定的其他反应条件下,探究反应温度θ在25.0~50.0 ℃范围内对ΔA的影响,3次实验取平均值,实验结果如图4所示。
由图4可以看出,θ在25.0~35.0 ℃范围内,ΔA随着温度的增加而增大,其在θ= 35.0 ℃时达到最大值;而当θ>35.0 ℃时,ΔA随着温度的增加而减小。因此,选择反应体系的最佳反应温度为θ= 35.0 ℃。
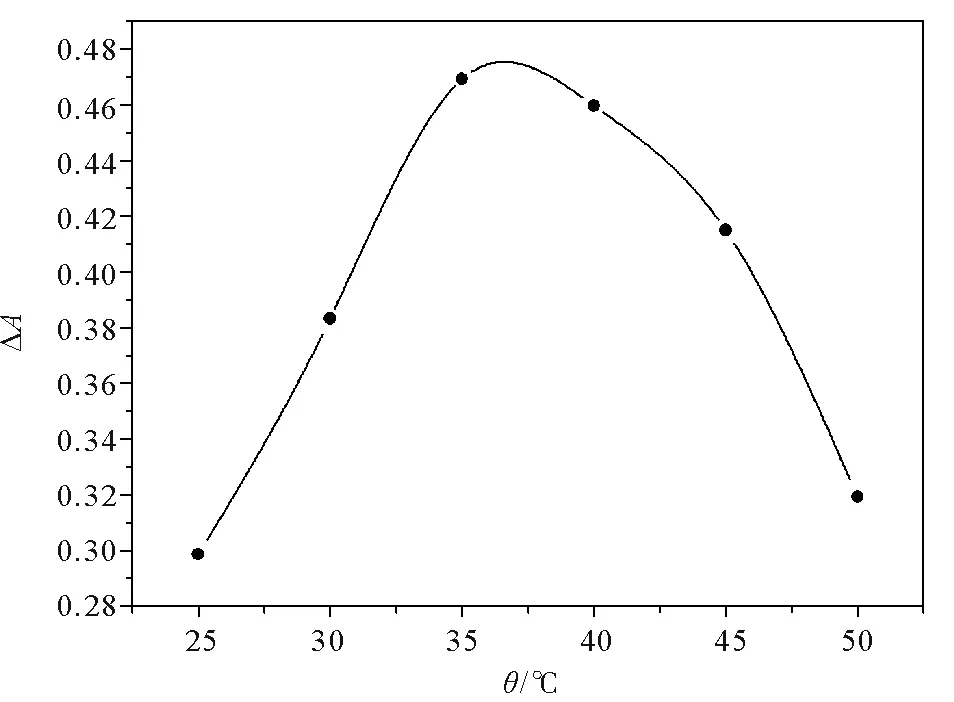
图4 反应温度θ对ΔA的影响
3.3.4 显色剂浓度的影响 在pH =11.00、反应时间t= 7.50 min、温度θ= 35.0 ℃及Φ(H2O2) = 3.600×10-2%的反应条件下,研究茜素红s质量浓度在4.800× 10-2~8.000× 10-2g·L-1范围内对ΔA的影响,3次实验取平均值,实验结果如图5所示。
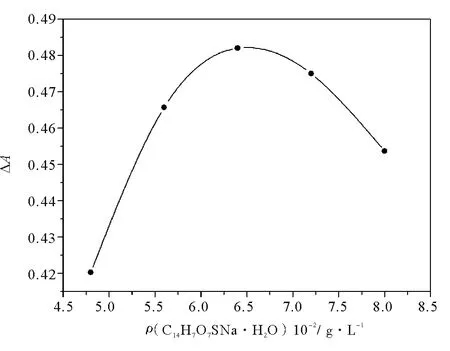
图5 茜素红s质量浓度对ΔA的影响Fig.5 The effect of mass concentration of alizarin red s on ΔA
由图5可以看出,在ρ(C14H7O7SNa·H2O)=4.800×10-2~6.400×10-2g·L-1范围内,ΔA随着茜素红s溶液的浓度的增加而增大,其在ρ(C14H7O7SNa·H2O)=6.400×10-2g·L-1时出现峰值;而当ρ(C14H7O7SNa·H2O)>6.400×10-2g·L-1时,ΔA随着茜素红s溶液浓度的增加而减小。因此,选择反应体系的最佳茜素红s溶液浓度为ρ(C14H7O7SNa·H2O)=6.400×10-2g·L-1。
3.3.5 氧化剂含量的影响 在pH =11.00、反应时间t=7.50 min、温度θ=35.0 ℃及ρ(C14H7O7SNa·H2O) = 6.400× 10-2g·L-1的反应条件下,研究过氧化氢体积分数在2.400× 10-2%~1.200× 10-1%范围内对ΔA的影响,3次实验取平均值,实验结果如图6所示。
由图6可以看出,在Φ(H2O2)=2.400×10-2%~7.200×10-2%范围内,ΔA随着过氧化氢体积分数的增加而增大,其在Φ(H2O2) = 7.200× 10-2%时出现峰值;而当Φ(H2O2)>7.200× 10-2%时,ΔA随着过氧化氢体积分数的增加而减小。因此,选择反应体系的最佳过氧化氢体积分数为Φ(H2O2) = 7.200× 10-2%。
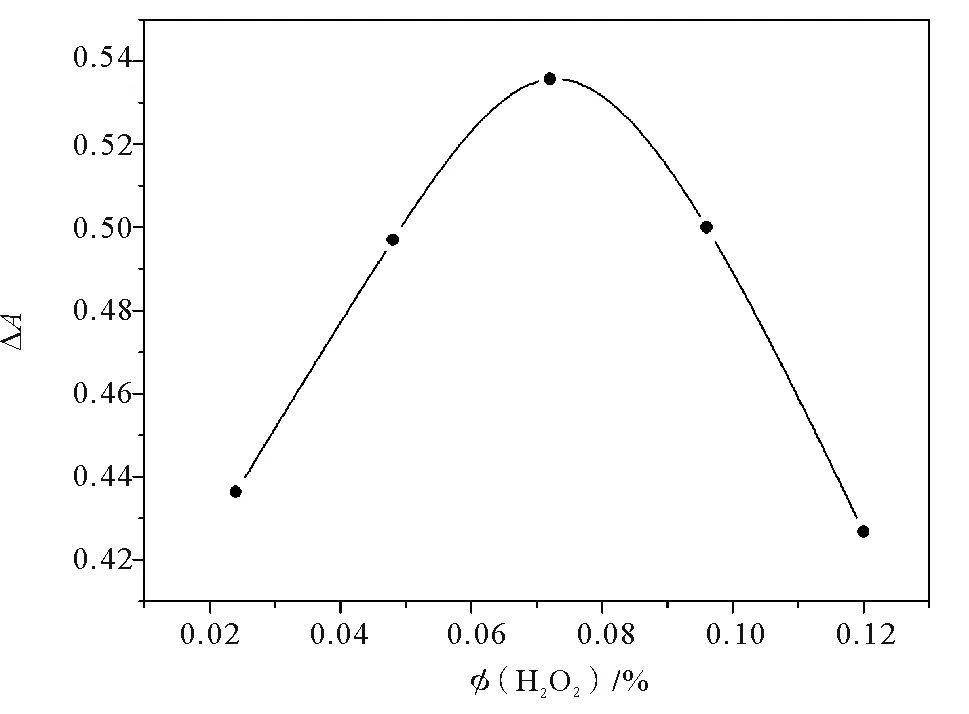
图6 过氧化氢体积分数对ΔA的影响Fig.6 The effect of volume fraction of H2O2 on ΔA
3.3.6 最佳反应条件 通过单因素实验,可得到此分析方法的最佳反应条件,如表4所示。
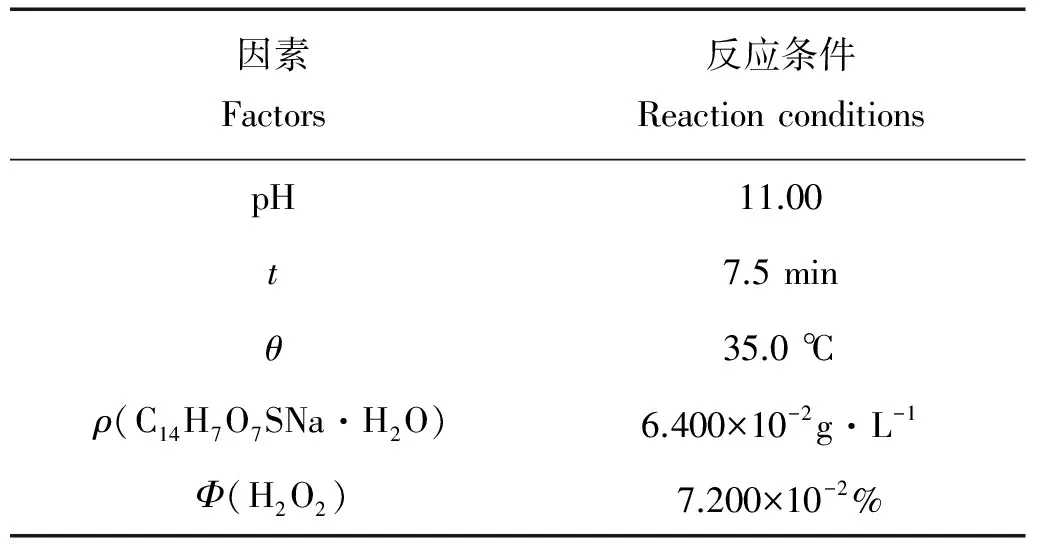
表4 最佳反应条件Table 4 The optimal reaction conditions
3.4 工作曲线的绘制
在最佳反应条件下,改变所加入Co2+的浓度,测溶液吸光度的变化,绘制工作曲线,如图7所示。

图7 ρ(Co2+)与ΔA的线性关系
结果表明,在ρ(Co2+) = 0~0.600 0 ng/mL范围内,ρ(Co2+)与ΔA之间具有良好的线性关系。其工作曲线的回归方程为:
ΔA= 0.754 3ρ(Co2+) + 0.009 3,R2= 0.997 9。
3.5 分析方法的准确度及精密度
按2.1部分的实验方法及所选定的最佳分析条件,分别测定ρ(Co2+) = 0.2000 ng/mL和ρ(Co2+) =0.4000 ng/mL的Co2+标准溶液的ΔA。根据所得到的回归方程求得ρ(Co2+)的测量平均值,检验此分析方法的准确度和精密度,6次实验结果如表5所示。由表5可看出,测量结果的相对标准偏差RSD在1.85%~2.96%之间。
3.6 分析方法的检出限
按2.1实验方法,进行11次空白实验,所得平均值和标准偏差列于表6。根据检出限= 3S/K,得到该分析方法的检出限为4.21×10-2ng/mL。
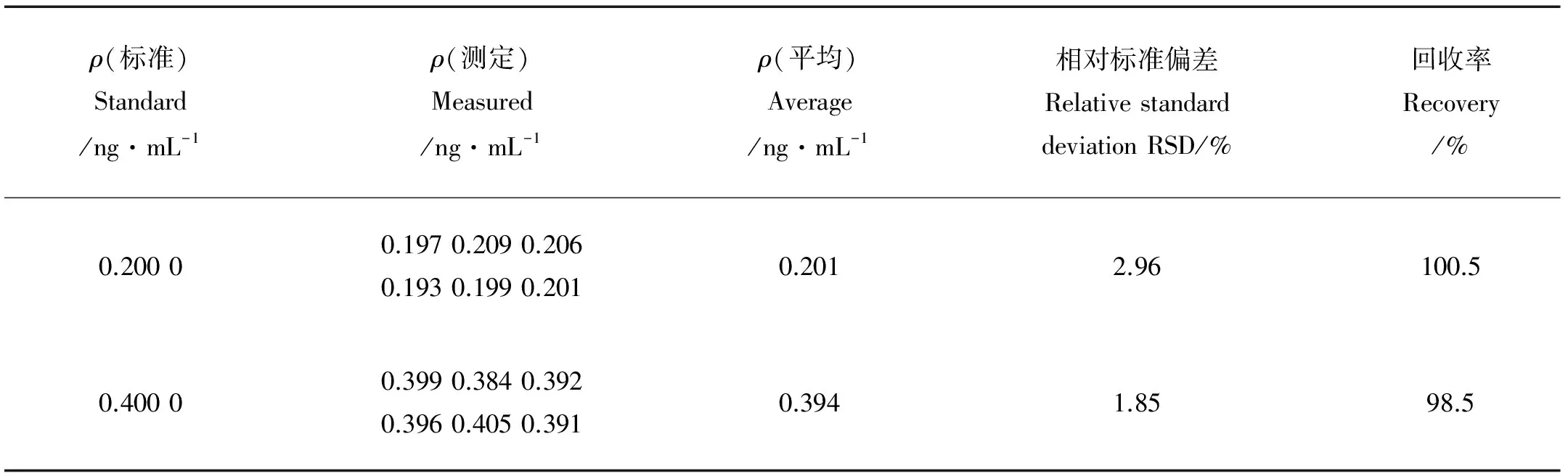
表5 分析方法的准确度及精密度Table 5 The experimental results of accuracy and precision
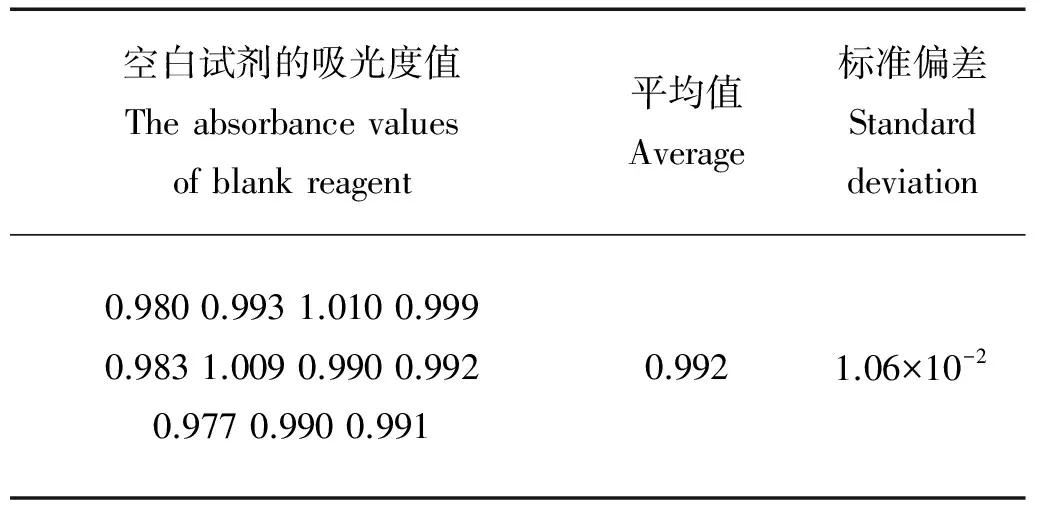
表6 空白试剂的吸光度值Table 6 The absorbance values of blank reagent
3.7 淡水体系中的准确度及精密度
通过对青岛市海泊河和山东利津段黄河水样进行加标回收实验,得到该方法在淡水体系中的准确度及精密度,每组进行3次平行实验,结果如表7所示。由表7可以看出:测定结果的相对标准偏差在1.93%~2.79%之间,而加标回收率在98.7%~101.3%之间。实验结果表明本方法在淡水体系中可以测量痕量钴(II),且具有较高的准确度和精密度。
4 本法与其他同类方法的比较
本文所建立的分析方法与其他同类分析方法相比,具有检出限低,分析温度低(常温),所需时间短等优点。

表7 准确度和精密度实验结果Table 7 The experimental results of accuracy and precision
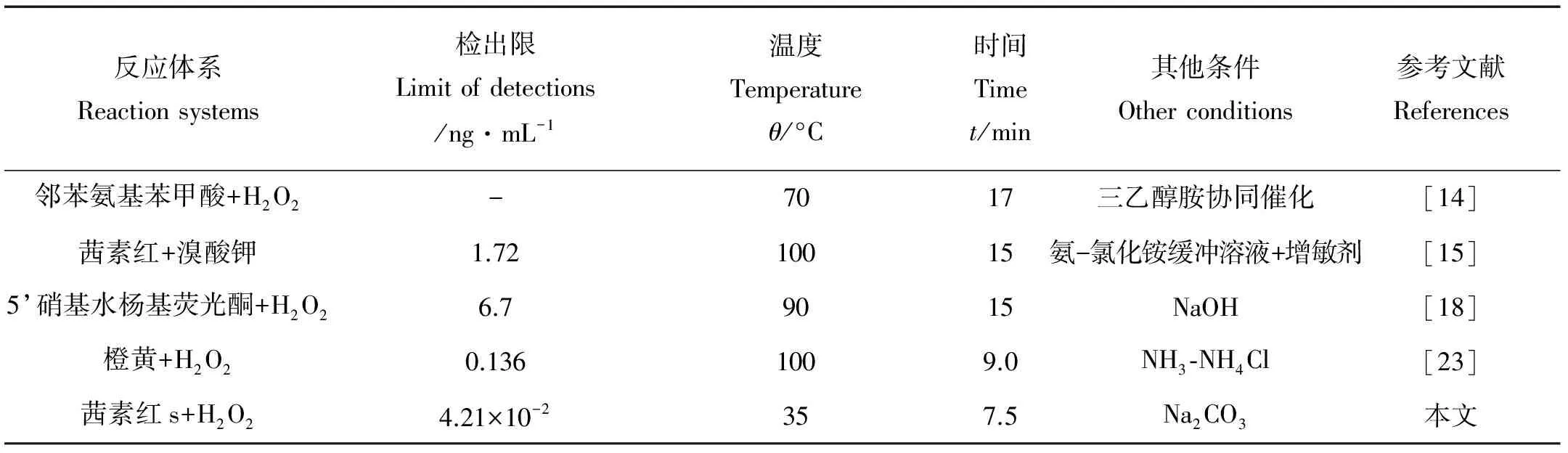
表8 本法与其他同类方法的比较
5 结语
本文研究了应用过氧化氢氧化茜素红s的褪色反应直接测定痕量钴(II)的催化动力学分析方法。该分析方法的检出限为4.21×10-2ng/mL,相对标准偏差为1.85%~2.96%,在室温条件下即可进行。应用在淡水体系加标回收率在98.7%~101.3%。与文献中同类分析方法相比,本文所建立的分析方法具有分析温度低,检出限低、准确度高、分析时间短等优点。
[1] 李青仁, 苏斌, 李胜钏. 微量元素钴, 镍与人体健康[J]. 广东微量元素科学, 2008(1): 66-70. Li Q R, Su B, Li S C. Trace element cobalt, nickel and human health [J]. Guangdong Trace Elements Science, 2008(1): 66-70.
[2] 贾如宝. 钼伴生元素钴——人体健康的强壮剂[J]. 中国钼业, 1994, 18(3): 44-46. Jia R B. The element, cobalt, concomitant with molybdenum - the strong agent of human health [J]. China Molybdenum Industry, 1994, 18(3): 44-46.
[3] Yan X, Li Q, Chai L, et al. Formation of abiological granular sludge-A facile and bioinspired proposal for improving sludge settling performance during heavy metal wastewater treatment [J]. Chemosphere, 2014, 113: 36-41.
[4] 谢洪科, 邹朝晖, 彭选明, 等. 重金属钴污染土壤的修复研究进展[J]. 现代农业科技, 2013(7): 222-223. Xie H K, Zou Z H, Peng X M, et al. Research progress on remediation of heavy metal polluted soil by cobalt [J]. Modern Agricultural Sciences and Technology, 2013(7): 222-223.
[5] Safavi A, Shams E. Highly sensitive and selective measurements of cobalt by catalytic adsorptive cathodic stripping voltammetry [J]. Talanta, 2000, 51(6): 1117-1123.
[6] Kapturski P, Bobrowski A. The silver amalgam film electrode in catalytic adsorptive stripping voltammetric determination of cobalt and nickel [J]. Journal of Electroanalytical Chemistry, 2008, 617(1): 1-6.
[7] Kaur V, Aulakh J S, Malik A K. A new approach for simultaneous determination of Co (II), Ni (II), Cu (II) and Pd (II) using 2-thiophenaldehyde-3-thiosemicarbazone as reagent by solid phase microextraction-high performance liquid chromatography [J]. Analytica Chimica Acta, 2007, 603(1): 44-50.
[8] Zhou Q, Xing A, Zhao K. Simultaneous determination of nickel, cobalt and mercury ions in water samples by solid phase extraction using multiwalled carbon nanotubes as adsorbent after chelating with sodium diethyldithiocarbamate prior to high performance liquid chromatography [J]. Journal of Chromatography A, 2014, 1360: 76-81.
[9] Harrington J M, Young D J, Essader A S, et al. Analysis of human serum and whole blood for mineral content by ICP-MS and ICP-OES: development of a mineralomics method [J]. Biological Trace Element Research, 2014, 160(1): 132-142.
[10] Choi H J, Lim S J, Park Y S, et al. Simple and robust ICP-MS method for simultaneous determination of serum Co and Cr in routine clinical practice [J]. Clinica Chimica Acta, 2015, 439: 91-96.
[11] 陈静. 火焰原子吸收分光光度法测定土壤中痕量钴[J]. 现代农业科技, 2011(11): 11-12. Chen J. Determination of trace amount of cobalt in soil by flame atomic absorption spectrometry [J]. Modern Agricultural Sciences and Technology, 2011(11): 11-12.
[12] Ghaedi M, Shokrollahi A, Ahmadi F, et al. Cloud point extraction for the determination of copper, nickel and cobalt ions in environmental samples by flame atomic absorption spectrometry [J]. Journal of Hazardous Materials, 2008, 150(3): 533-540.
[13] Pulgarín J A M, Bermejo L F G, Durán A C. Fast simultaneous determination of traces of Cu (II) and Co (II) in soils and sediments with the luminol/perborate chemiluminescent system [J]. Environmental Monitoring and Assessment, 2013, 185(1): 573-580.
[14] 高杰. 应用催化动力学分析法测定痕量钴的研究[J]. 化学研究与应用, 1998, 10(4): 413-413. Gao J. Study on determination of trace cobalt (II) by catalytic kinetic spectrophotometry [J]. Chemical Research and Application, 1998, 10(4): 413-413.
[15] 赵丽杰, 赵丽萍, 李良, 等. 负催化动力学光度法测定痕量钴[J]. 大连民族学院学报, 2004, 6(3): 16-18. Zhao L J, Zhao L P, Li L, et al. The negative catalytic kinetic photometric method for the determination of trace cobalt [J]. Journal of Dalian Nationalities University, 2004, 6(3): 16-18.
[16] 王晓菊, 郭飞君, 盖永胜. 以溴代十六烷基吡啶为增敏剂催化动力学光度法测定痕量钴 (II) [J]. 食品科学, 2008, 29(1): 228-230. Wang X J, Guo F J, Gai Y S. Catalytic spectrophotometric method for determination of trace cobalt (II) with cetyl pyridine bromide as sensitizet [J]. Food Science, 2008, 29(1): 228-230.
[17] 王洪福, 张素兰, 何黎明, 等. 柠檬酸-罗丹明 B 体系阻抑动力学光度法测定痕量钴 (II) [J]. 化学研究与应用, 2009, 21(4): 531-533. Wang H F, Zhang S L, He L M, et al. Determination of trace cobalt (II) by inhibitory kinetic spectrophotometric method of citric acid - rhodamine B system [J]. Chemical Research and Application, 2009, 21(4): 531-533.
[18] 孙桃, 季剑波. 催化动力学分光光度法测定痕量钴(II)[J]. 光谱实验室, 2013, 30(1): 349-351. Sun T, Ji J B. Determination of trace cobalt (II) by catalytic kinetic spectrophotometry [J]. Chinese Journal of Spectroscopy Laboratory, 2013, 30(1): 349-351.
[19] Abouhiat F Z, Henríquez C, El Yousfi F, et al. Sensitive kinetic-catalytic spectrophotometric method for cobalt determination using a chip coupled to a multisyringe flow injection analysis system [J]. Talanta, (2015) doi: 10.1016/j.talanta. 2015.12.005.
[20] Chaparro L, Ferrer L, Leal L, et al. A multisyringe flow-based system for kinetic-catalytic determination of cobalt (II) [J]. Talanta, 2015, 133: 94-99.
[21] Batley G E. A catalytic method for the determination of cobalt impurities in reactor cooling-water circuits [J]. Talanta, 1971, 18(12): 1225-1232.
[22] Thompson K M, Griffith W P, Spiro M. Mechanism of bleaching by peroxides. Part 2.—Kinetics of bleaching of alizarin and crocetin by hydrogen peroxide at high pH [J]. Journal of the Chemical Society, Faraday Transactions, 1993, 89(22): 4035-4043.
[23] 高芝, 高楼军, 柴红梅. 过氧化氢-橙黄催化动力学光度法测定痕量钴的研究[J]. 江西师范大学学报(自然科学版), 2009, 33(4): 437-439. Gao Z, Gao L J, Chai H M. Catalytic kinetic spectrophotometric determination of trace cobalt with peroxide hydrogen-orange G system [J]. Journal of Jiangxi Normal University (Natural Sciences Edition), 2009, 33(4): 437-439.
Abstract: Based on catalytic kinetic theory, a new spectrophotometric method to analyze cobalt (II) is established. The new reaction system is put forward for the determination of trace cobalt (II) using alizarin red s as indicator and hydrogen peroxide as oxidant. The optimal reaction conditions are as follows: pH=11.00, reaction timet= 7.50 min, reaction temperatureθ= 35.0℃,ρ(C14H7O7SNa·H2O) = 6.400 ×10-2g·L-1,Φ(H2O2) = 7.200 ×10-2%. Under the optimal reaction conditions, the relative standard deviation of the proposed method is in the range of 1.85%~2.96%, and the detection limit is 4.21 ×10-2ng·mL-1. The new method can be successfully applied to the measurement of cobalt (II) in the Yellow River from Lijin district and Haibo river. Compared with other measurement methods, the proposed method has low detection limit, simple operation, and can be used at low temperature.
Key words: determination of cobalt (II); catalytic kinetic spectrophotometry;alizarin red s; hydrogen peroxide
责任编辑 徐 环
Catalytic Kinetic Determination of Trace Cobalt (II) Based on Oxidation of Alizarin Red s by Hydrogen Peroxide
ZHANG Hao-Shuang, JI Hong-Wei, ZAI Jing-Zhe, HAN Ting-Ting
(The Key Laboratory of Marine Chemistry Theory and Technology, Ministry of Education, College of Chemical Engineering, Ocean University of China, Qingdao 266100,China)
P734.4
A
1672-5174(2017)11-061-09
10.16441/j.cnki.hdxb.20160255
张皓爽, 姬泓巍, 宰敬喆, 等. 过氧化氢-茜素红s体系催化动力学分光光度法测量痕量钴(II)[J]. 中国海洋大学学报(自然科学版), 2017, 47(11): 61-69.
ZHANG Hao-Shuang, JI Hong-Wei, ZAI Jing-Zhe, et al. Catalytic kinetic determination of trace cobalt (II) based on oxidation of alizarin red s by hydrogen peroxide[J]. Periodical of Ocean University of China, 2017, 47(11): 61-69.
2016-07-13;
2016-12-18 作者简介:张皓爽 (1992-),女,硕士生。E-mail: hshuangz@163.com
* 通讯作者:E-mail: hwji@ouc.edu.cn

