汾河流域水系和表层沉积物中多环芳烃的空间变化规律及其生态风险研究
赵颖,党晋华,王飞
1. 山西省环境科学研究院,太原 0300272. 山西大学体科所,太原 030006
汾河流域水系和表层沉积物中多环芳烃的空间变化规律及其生态风险研究
赵颖1,党晋华1,王飞2,*
1. 山西省环境科学研究院,太原 0300272. 山西大学体科所,太原 030006
本研究在汾河流域上、中、下游及其部分支流布设29个采样点,对其水体和表层沉积物多环芳烃(PAHs)的空间分布规律及生态风险进行了分析和讨论。结果表明,汾河流域水相中丰水期PAHs总量浓度范围是0.530~16.002 μg·L-1,平均浓度为(2.738±3.078) μg·L-1,枯水期PAHs总量浓度范围是0.588~12.916 μg·L-1,均值为(2.762±3.132) μg·L-1。就空间分布而言,汾河流域整体呈现上游污染较轻,中下游污染严重的特点。PAHs的组成规律显示,丰水期和枯水期PAHs含量均以低环(2~3环)为主,不同采样期低环PAHs所占比例分别为96.5%和90.4%。与其他15个研究地区水体PAHs含量比较,汾河流域水体中PAHs污染程度的国内外对比处于中等到较高程度的污染。丰水期和枯水期水体中PAHs来源于石油源和植物、木材、煤的燃烧,主要受到流域煤化工、燃煤电厂排放污染物的影响。地表水健康风险评价结果显示,汾河流域丰水期和枯水期分别有13.8%和20.7%的点位存在一定的健康风险。汾河流域沉积相中16种PAHs平均浓度为(3.774±1.987) μg·g-1,其污染主要集中在流域中下游地区。PAHs的组成规律显示,PAHs含量集中在低环(2~3环),约占总量的75%左右。与本研究提到的河流、湖泊及港口沉积物中PAHs含量比较,汾河流域沉积物中PAHs污染程度仍处于中等偏高的污染水平。丰水期沉积相中PAHs以燃烧源和石油源为主,部分来自典型石油类产品的输入。表层沉积物生态风险评价结果显示,对于提出的12种PAHs的生态风险的效应区间低值(ERL值)或效应区间中值(ERM值)以及苯并(b)荧蒽(BbF)和苯并(k)荧蒽(BkF)这2类没有最低安全值的PAHs化合物来说,汾河上、中、下游流域均有采样点的PAHs可能存在着对生物的潜在生态风险。通过本研究可全面地了解该流域多环芳烃的空间分布规律及其可能的来源,并且为汾河流域多环芳烃污染的控制和生态风险评价提供科学依据。
多环芳烃;汾河流域;分布;风险;来源
Received12 September 2016accepted14 December 2016
Abstract: The spatial variety and ecological risk of polycyclic aromatic hydrocarbons (PAHs) in water and surface sediments were analyzed based on 29 samples collected from upstream region to downstream region, as well as some of its tributaries of Fenhe River Basin. The results showed that the average concentrations of PAHs in waterbody were (2.738±3.078) μg·L-1and (2.762±3.132) μg·L-1in wet and dry season, respectively. The total PAHs concentrations ranged from 0.530 to 16.002 μg·L-1, and from 0.588 to 12.916 μg·L-1in wet and dry season, respectively. The spatial distribution of PAHs indicated the slight pollution in the upstream and the severe pollution in the middle and lower reaches. The low molecular weight PAHs (2-ring and 3-ring) were the most common components in waterbody both in wet and dry season with the ratio to the total PAHs by 96.5% and 90.4%, respectively. Comparing with other 15 areas in the world, PAHs concentration in waterbody of Fenhe River ranged from moderate pollution to higher pollution. The results from the source analysis of PAHs suggested that petroleum PAHs and the combustion of plants, wood and coal were the main source both in wet and dry season. The possible reasons were the discharges of coal chemical industry and power plants. The results of ecological risk assessment 13.8% and 20.7% of the whole sampling sites showed the potential health risk in waterbody in wet and dry period, respectively. The average concentration of total 16 PAHs in sediment was (3.774±1.987) μg·g-1, which occurred mainly in the middle and lower reaches of the Fenhe River. The low molecular weight PAHs (2-ring and 3-ring) were the most common components in sediment with the approximate ratio of 75% to the total PAHs contents. Comparing with other areas in the world, PAHs concentration in sediment of Fenhe River reached higher pollution. The PAHs in sediments were mainly from the incomplete combustion of coal and wood, and partly from petroleum in wet season. The results of ecological risk assessment in surface sediment showed potential ecological risk for creatures based on reference to ERM value or ERL value for 12 PAHs, as well as the existence of BbF and BkF.
Keywords: PAHs; Fenhe Basin; distribution; risk; source
持久性有毒污染物(Persistent Toxic Substances, PTS)是一类毒性很强,难降解,可长距离输送,并随食物链在动物和人体中累积、放大,具有内分泌干扰特性的污染物。其中,多环芳烃(polycyclic aromatic hydrocarbons, PAHs)是广泛存在于环境中的典型高毒性PTS,它们中的16种被认为具有较高毒性、致突变性及致癌性,因而被美国环保署列为优先控制污染物[1],主要通过干湿沉降、地表径流进入河流水体[2]。环境中PAHs一般来源于化石燃料和生物质等有机化合物的不完全燃烧和有机高分子化合物的化学合成,以及石油等产物开采、运输和加工过程中的泄漏及自然途径等。饮用水源地水中PAHs的含量直接关系到人体健康,而沉积物是PAHs的汇和潜在污染源[3]。因此,研究水、沉积物中多环芳烃的浓度水平、风险及来源对评价区域环境污染具有重要意义。
自然水体中PAHs的分布、组成和污染来源研究成为世界范围内的研究热点,国内外已开展了大量的研究工作[4-10],主要包括PAHs的污染特征、迁移转化、来源分析等方面。
汾河是山西境内第一大河,是黄河第二大支流,全长716 km,流域面积3 9471 km2,汾河流域是山西省工业集中、农业发达的地区,在山西省的经济发展中具有举足轻重的作用。同时沿途人口稠密,厂矿众多,也是山西省主要的粮棉产地。长期以来,在汾河流域的开发建设中,由于忽略了经济建设与环境协调发展的关系,致使汾河水体受到污染,植被遭到破坏,水土流失加剧,土地退化等,这些因素已严重影响到流域生态系统的健康和流域经济的健康发展。目前对水源地PAHs污染的研究还很少,而关于汾河流域有机污染的研究仅见少量报道且主要为局部区域的研究而未涉及全流域的考察[11-12]。因此,本研究通过分析汾河上、中、下游水、表层沉积物PAHs的浓度、组成和分布特征,并对其进行风险评价,探讨PAHs的输入途径与来源,以期对汾河流域持久性有机污染物的综合整治提供理论基础和科学依据。
1 材料与方法(Materials and methods)
1.1 样品采集
在汾河丰水期(2013年8月)进行河水和底泥以及枯水期(2013年10月)河水样品的采集。采样范围选取为汾河源头至汾河入黄口的汾河上、中、下流及其部分支流,采样点主要布设在国控点断面位置上,此外,在畜禽养殖场密集区的下游、市政污水口下游及典型污水退水渠排水口增设采样点,本研究在汾河流域布设29个采样点,包括21个干流样点,5个支流样点,3个退水渠样点(表1)。汾河流域干流、支流采样点和退水渠出口处的采样点分布如图1所示。表层沉积物样品利用抓斗式采样器在每个断面采集1个表层沉积物样品,并去除上层1 cm作为样品,置于事先用甲醇清洗过的铝盒中,每个采样点采集的沉积物样品不少于1 kg,做3个平行,在运输过程中用冰块保持低温,冷冻干燥后过100目筛,-20 ℃冷藏以备分析。每个采样点采集的水样总量不少于2 L,在24 h内用0.45 μm的玻纤滤膜进行过滤,做3个平行。
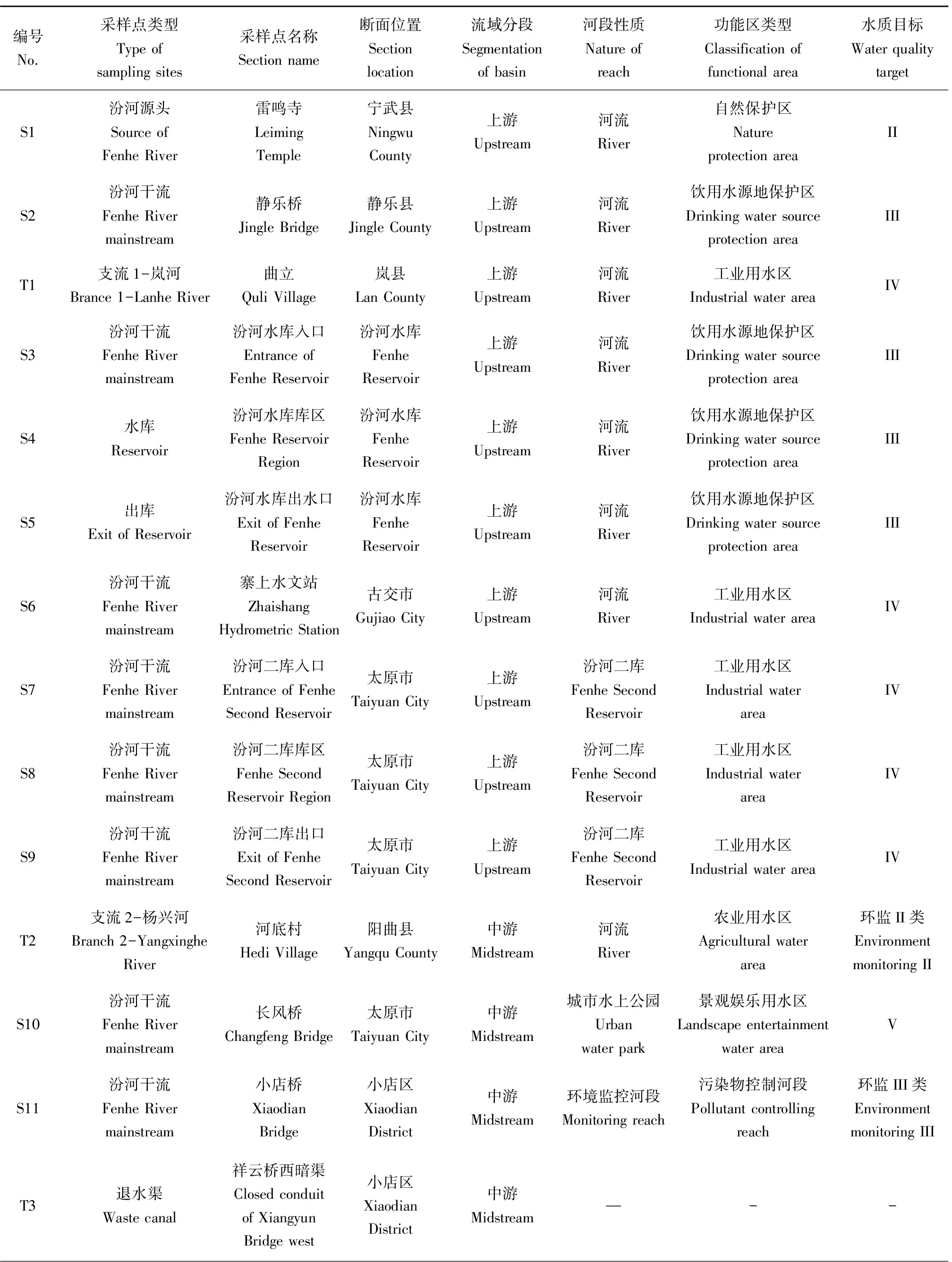
表1 汾河流域采样断面设置Table 1 Introduction of sampling sites of Fenhe Basin
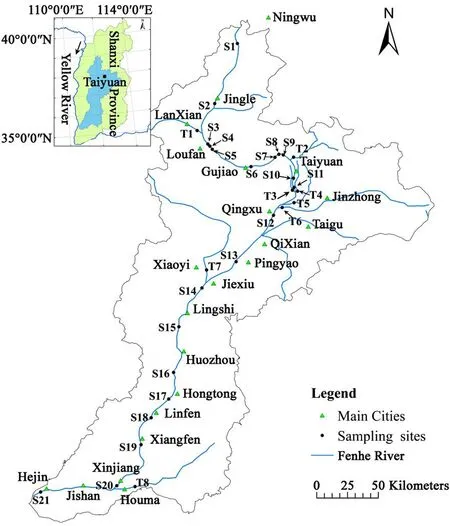
图1 汾河流域采样点位置Fig. 1 Locations of the sampling sites in Fenhe Basin
1.2 标准样品与试剂
PAHs混合标样:包含16种同系物,萘(Naphthalene, NAP)、苊烯(Acenaphthylene, ACY)、苊(Acenaphthene, ANA)、芴(Fluorene, FLU)、菲(Phenanthrene, PHE)、蒽(Anthracene, ANT)、荧蒽(Fluoranthene, FLT)、芘(Pyrene, PYR)、苯并(a)蒽(Benzo(a)anthracene, BaA)、(Chrysene, CHR)、苯并(b)荧蒽(Benzo(b)fluoranthene, BbF)、苯并(k)荧蒽(Benzo(k)fluoranthene, BkF)、苯并(a)芘(Benzo(a)pyrene, BaP)、茚并(1,2,3-cd)芘(Indeno(1,2,3-cd)pyrene, IPY)、二苯并(a,h)蒽(Dibenzo(a,h)anthracene, DBA)、苯并(ghi)苝(Benzo(g,h,i)perylene, BPE),浓度为2 000 μg·mL-1,购自Sigma-Aldrich公司,直接作为标准储备液。
回收率指示物:氘代菲(Phe-d10),浓度为200 μg·mL-1,溶于二氯甲烷,购自AccuStandard 公司。
其他有机溶剂:二氯甲烷为农残级,正己烷为HPLC级,甲醇为农残级,均购于美国Fisher Scientific公司,使用前经过重复蒸馏;硫酸、无水硫酸钠等均为分析纯。
1.3 样品预处理
环境水体样品前处理:1 L水样经0.45 μm的GF/F(Whatman, 0.7 μm)玻璃纤维滤膜过滤后进行固相萃取。HLB固相萃取柱活化:每一个固相萃取柱分别用5 mL二氯甲烷,10 mL甲醇和10 mL MilliQ超纯水活化,活化时,不要让甲醇和水流干(液面不低于吸附剂顶部)。吸附:取经过滤的1 L水样,加入50 mL甲醇,混匀,以5 mL·min-1的流量通过固相萃取柱。干燥:用10 ml MilliQ超纯水冲洗固相萃取柱后,真空抽滤,使柱干燥。洗脱:用5 mL二氯甲烷洗脱固相萃取柱2次,收集洗脱液。洗脱液在35 ℃以下,用低流量氮气吹至近干,加入内标,溶剂定容至1 mL,密封冷藏待分析[6]。
环境沉积物样品前处理:经冷冻干燥后研磨,通过60目标准筛。称取5 g沉积物,加入适量硅藻土,混匀后倒入快速溶剂萃取池,采用丙酮∶二氯甲烷(体积比1∶1)溶液萃取,萃取温度100 ℃,压力1 500 psi,预热5 min,静态萃取5 min,循环2次,氮气40 s吹扫,收集全部萃取液;移至球形瓶,25 ℃下旋转浓缩至近干,取5 mL丙酮/正己烷混合液(体积比为1∶9)加入柱管,用真空泵以低于5 mL·min-1的流量抽至液面与固相物质持平,再加入5 mL正己烷同上处理,将2 mL萃取液加到柱内,用少量正己烷清洗容器,将清洗液一并加入柱内,真空泵抽空,用顶空瓶收集流出液,再用5 mL丙酮/正己烷混合液(体积比为1∶9),淋洗,抽空,收集淋洗液于同一顶空瓶中。氮吹至近干,加入内标,溶剂定容至1 mL,密封冷藏待分析[13]。
质量保证与质量控制:分析测定过程中,GC-MS仪器的标定和指标的定量采用多环芳烃标准溶液,根据质量控制与质量保证的要求,进行方法空白、空白加标、基体加标和平行样分析,控制水样预处理的质量。每个样品在液液萃取前加入回收率指示物,回收率范围为73.1%~94.6%,空白样品中目标化合物均未检出,总的数据质量可靠。
1.4 仪器分析条件
采用气相色谱质谱仪(GCMS-QP2010,日本岛津)分析样品中的多环芳烃,色谱柱为石英毛细管柱(Rtx-5ms, 30 m×0.25 mm×0.25 μm);进样口温度270 ℃,吹扫流量3 mL·min-1,柱流量1 mL·min-1,载气为恒压65.2 kPa,不分流进样,不分流时间1.8 min,进样量1 μL。程序升温条件为:初始温度80 ℃(2 min),以30 ℃·min-1升至200 ℃,再以15 ℃·min-1升至240 ℃,再以10 ℃·min-1升至290 ℃,保持13 min,总时间为26.67 min。接口温度为300 ℃,离子源温度为200 ℃[14]。
1.5 数据处理
本研究采用SPSS18.0 统计软件(SPSS Inc.)进行单因素方差分析(One-way ANOVA),以P < 0.05, P < 0.01表示差异显著。文中图和表的绘制采用Origin 8.0和Excel 2010绘制。
2 结果与讨论(Result and discussion)
2.1 汾河流域水体中PAHs浓度分布与来源辨析2.1.1 环境水体中PAHs浓度分布
汾河流域水相中PAHs浓度见表2。由表可知,16种PAHs在不同采样时间不同断面均有不同程度的检出。丰水期PAHs总量变化范围为0.53~16 μg·L-1,平均浓度为(2.738±3.078) μg·L-1,其中苯并[a]芘(BaP)的浓度范围为N.D.~0.022 μg·L-1。枯水期PAHs总量变化范围为0.588~12.916 μg·L-1,均值为(2.762±3.132) μg·L-1,BaP的浓度为N.D.~0.017 μg·L-1。丰水期PAHs的污染浓度与枯水期相近。虽然丰水期可汇入大量的外源物质,如大气颗粒物的沉降和地表径流带来的表层土壤冲刷,而不少颗粒物中吸附有大量的PAHs;但是,另一方面PAHs很容易被悬浮颗粒物吸附而沉降至底泥中,从而降低了丰水期水相中PAHs的浓度。因此,丰水期PAHs总量与枯水期相当,在本研究中,PAHs含量没有明显的季节变化特征。
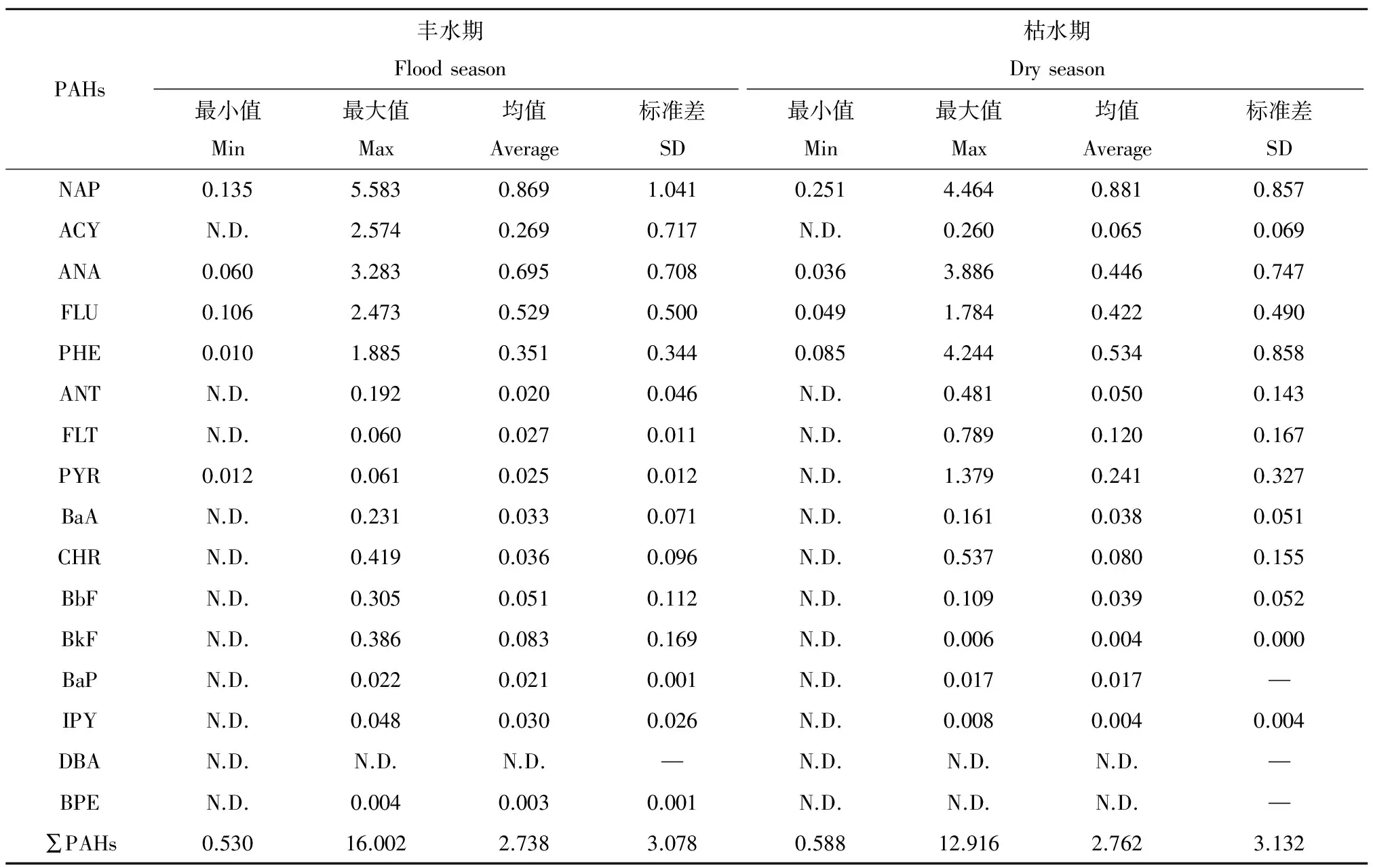
表2 汾河丰水期和枯水期水相中PAHs的含量(μg ·L-1)Table 2 PAHs contents in water of Fenhe River in flood season and dry season (μg ·L-1)
注:NAP为萘,ACY为苊烯,ANA为苊,FLU为芴,PHE为菲,ANT为蒽,FLT为荧蒽,PYR为芘,BaA为苯并(a)蒽,CHR为,BbF为苯并(b)荧蒽,BkF为苯并(k)荧蒽,BaP为苯并(a)芘,IPY为茚并(1,2,3-cd)芘,DBA为二苯并(a,h)蒽,BPE为苯并(g,h,i)。
Note: NAP stands for Naphthalene; ACY stands for Acenaphthylene; ANA stands for Acenaphthene; FLU stands for Fluorene; PHE stands for Phenanthrene; ANT stands for Anthracene; FLT stands for Fluoranthene; PYR stands for Pyrene; BaA stands for Benzo(a)anthracene; CHR stands for Chrysene; BbF stands for Benzo(b)fluoranthene; BkF stands for Benzo(k)fluoranthene; BaP stands for Benzo(a)pyrene; IPY stands for Indeno(1,2,3-cd)pyrene; DBA stands for Dibenzo(a,h)anthracene; BPE stands for Benzo(g,h,i)perylene.
由图2可知,汾河流域从上游至下游各断面的PAHs浓度差异较大,其中T5采样点的PAHs浓度为最高值,浓度为16.0 μg·L-1。T5采样点位于汾河流域中游太榆退水渠,承载了周边企业的工业废水和居民生活污水。有研究指出,PAHs主要来源于有机物的不完全燃烧,人类的生产活动如化石产品的燃烧、各种固体废弃物的焚烧,炼焦、做饭等都产生大量的PAHs,其中工业发达区由于消耗大量化石燃料,其PAHs的排放量明显高于人类生活区[15]。本研究中,太榆退水渠主要接受太原钢铁集团排水、太原市河东及河西生活污水。太钢集团有焦化、钢铁、机械制造、化工等企业,大气沉降、地表径流及工业废水排放是水体中PAHs污染较为严重的原因。
本研究中,由于枯水期汾河二库封库,S7、S8站点样品未采集。丰水期汾河流域水相中16种PAHs以NAP、ANA、FLU和PHE为主,浓度分别为0.869 μg·L-1、0.695 μg·L-1、0.529 μg·L-1和0.351 μg·L-1;枯水期流域6环PAHs(DBA和BPE)未检出,代表性PAHs为NAP、ANA、FLU和PHE,含量分别为0.881 μg·L-1、0.446 μg·L-1、0.422 μg·L-1和0.534 μg·L-1。NAP、ANA、FLU和PHE为不同采样时间典型代表性PAHs,为汾河流域水相PAHs的优势种类。按环数区分(图2),丰水期PAHs含量以3环>2环>4环>5环>6环的顺序递减,2环和3环PAHs所占比例分别为31.7%和64.8%,高环含量较低,这与PAHs的水溶性有关。枯水期PAHs与丰水期相似,其中2环和3环PAHs分别占到PAHs总量的33.5%和56.9%。因此尽管采样时间不同,汾河流域水相中的PAHs均以低环(2~3环)为主。

图2 汾河丰水期和枯水期水相中PAHs的组成及含量分布Fig. 2 Compositions and concentrations of PAHs in water of wet and dry seasons of Fenhe River
2.1.2 与国内外其他河流水体中PAHs含量的比较
将研究区水相中PAHs浓度同国内外已有研究报道的河流、湖泊水体中PAHs浓度进行了比较(表3)。与国内一些河流水体PAHs总量相比,汾河流域水相PAHs总量(丰水期530~16 002 ng·L-1,平均浓度2 378 ng·L-1;枯水期588~12 916 ng·L-1,平均浓度2 762 ng·L-1)高于巢湖(浓度范围95.63~370.13 ng·L-1)[17]、珠江三角洲河口(平均浓度367 ng·L-1)[20]、长江口(平均浓度145.9 ng·L-1)[21]、黄河中下游(179~2 182 ng·L-1)[22]、厦门海(平均浓度367 ng·L-1)[20]、钱塘江(平均浓度283 ng·L-1)[23]、天津河(平均浓度174 ng·L-1)[24]、渭河(平均浓度920 ng·L-1)[25]PAHs量的平均浓度,低于九龙河口PAHs总量的平均浓度(17 000 ng·L-1)[19],与大辽河口PAHs总量的平均浓度处于同一数量级(6 471.1 ng·L-1)[18];与国外河流相比,远高于美国Chesapeake湾(平均浓度52 ng·L-1)[16]、墨西哥Todos santos湾(平均浓度96 ng·L-1)[16]和韩国Kyenoggi湾(平均浓度120 ng·L-1)[16]PAHs总量的平均浓度,低于美国Casco Bay湾PAHs总量的平均浓度(66 700 ng·L-1)[16],与加拿大Kitimat港PAHs总量的平均浓度基本相同(2 900 ng·L-1)[16]。因此,相对于上述15个研究地区水体PAHs含量,汾河流域水体中PAHs污染程度处于中等到较高程度的污染。

表3 汾河流域水相中PAHs污染浓度与其他河流比较Table 3 Comparison of PAHs concentrations in water of Fenhe River and other rivers all over the world
注:*不包括汾河太原段退水渠中(T3、T4和T5这3个样点)的PAHs浓度。
Note: *PAHs concentrations of waste canals (T3, T4 and T5) were not included.
2.1.3 环境水体中PAHs的来源辨析
PAHs除自然成因外,主要来自化石燃料和木材等不完全燃烧产物的排放,化石燃料在使用过程中的泄露等。通常可用2~3环和4环以上环数的相对丰度来估测该区的多环芳烃的来源,4环及其以上的具有高分子量的PAHs主要来源于化石燃料高温燃烧,而低分子量(2~3环)的则来源于石油类污染。一般认为,油类污染的PAHs以烷基化多环芳烃为主,而不完全燃烧的PAHs则以母体多环芳烃为主。石油是低温下形成的,烷基化程度很高,特别是C2以上的烷基取代多环芳烃较多,因此石油化工企业排放的污水中,来源于油类和石油类烷基取代的多环芳烃含量最高,而且母体多环芳烃多是低环数的多环芳烃;对于来源于燃料不完全燃烧的多环芳烃,由于在高温下形成,烷基取代的多环芳烃的支链被打断,所以一般烷基化程度不高,且母体多环芳烃以难以开环裂解的高环数多环芳烃为主。
石油类产品中常常含有组分菲(PHE),而组分蒽(ANT)由于稳定性较差,在石油形成过程中早已分解,因而含量很低。燃烧过程产生PAHs,PHE和ANT是同分异构体,产生PHE的同时也产生了ANT,一般ANT的含量会较高。因此如果样品中ANT/(ANT+PHE)<0.1,PAHs主要来源于石油类PAHs的污染;如果样品中ANT/(ANT+PHE)>0.1则是受燃烧源PAHs的污染。FLU/(FLU+PYR)<0.4说明是典型的石油源PAHs污染;FLU/(FLU+PYR)>0.5表明PAHs主要来源于木柴、煤的不完全燃烧;介于0.4与0.5之间意味着由燃油排放的尾气造成[26]。
图3列出了汾河流域水相丰水期和枯水期中上、中、下游的FLU/(FLU+PYR)和ANT/(ANT+PHE)的特征比值。由图可知,流域丰水期水相中上、中、下游FLU/(FLU+PYR)的比值范围是0.819~0.981,大于0.5,说明丰水期该研究区PAHs主要来源于植物、煤炭等不完全燃烧,工业生产中常需要消耗大量的燃煤和木材等,这些材料燃烧时产生PAHs及其他有毒有害物质进入空气中并吸附在大气悬浮颗粒物上,随大气降水落到水体或地表土壤中,土壤中的PAHs又会随雨水冲刷进入水体。流域丰水期水相ANT/(ANT+PHE)的比值除中游S10采样点大于0.1,其余采样点的比值介于0.026~0.092,均小于0.1,石油源样点占到93%。流域枯水期水相中上、中、下游FLU/(FLU+PYR)的比值是0.513~0.848,大于0.5,与丰水期比值范围相同,以燃烧源为主。流域枯水期水相ANT/(ANT+PHE)的比值分布范围较大,其中上、中、下游各采样点的比值在ANT/(ANT+PHE)大于0.1和小于0.1的范围内均有分布,燃烧源采样点占50%,其余样点既有石油源又有燃烧源。因此PAHs的组成特征表明,汾河流域丰水期和枯水期水体中PAHs来源于石油源和植物、木材、煤的燃烧,主要受到流域煤化工、燃煤电厂排放污染物的影响。
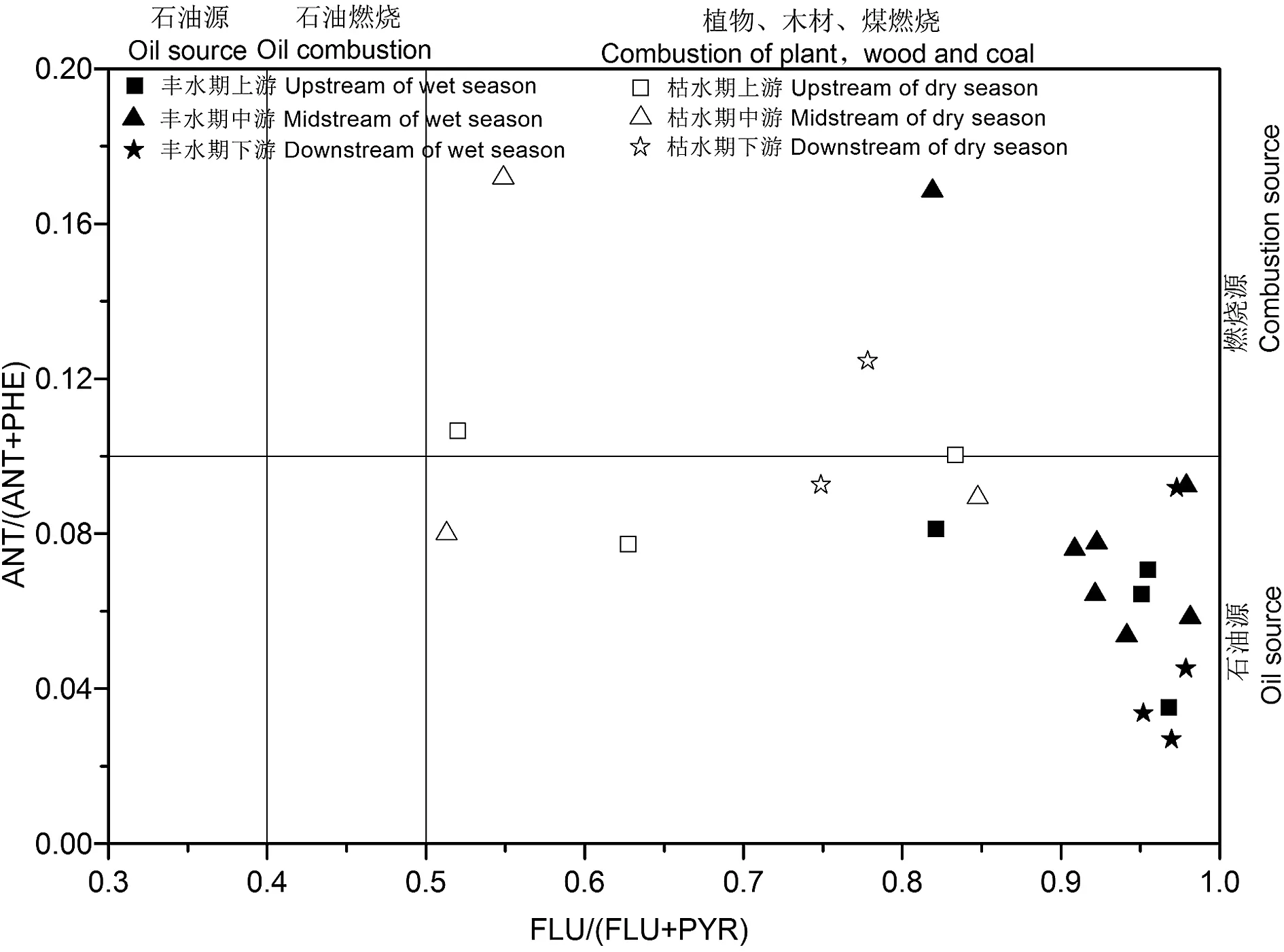
图3 汾河水相多环芳烃来源Fig. 3 Source analysis of PAHs in water of Fenhe River
2.2 汾河流域水体中PAHs的健康风险评估
我担心她怀孕情绪不稳,没敢提起胖子。直到一顿饭吃完,买了单,我们两个傻坐在餐厅的落地窗边等七哥来接她,她却没头没脑地开了口——
关于水体PAHs含量的生态风险评估,Nisbet等[27]于1992年由毒性试验得出各PAHs相对于BaP的毒性当量因子(toxicity equivalence factor, TEF),并用来分析环境中PAHs的健康风险。本研究中,汾河流域上、中、下游均存在有直接饮用水源功能的区域或是与之相关的保护饮用水的河段,其中汾河水库作为太原市最大的集中式饮用水水源地,目前日供太原市生活用水约60万m3·d-1,约占太原市总供水量的43%,因此采用此方法来进行水体PAHs的健康风险评价。
BaP的毒性当量(BaP equivalents, EBaP)计算公式为:EBaP=CBaA×0.1+CBaP+CBbF×0.1+CBkF×0.01+CIP×0.1+CDA+CCh×0.001
式中,EBaP表示7种多环芳烃相对于BaP的毒性当量之和(ng·L-1);C表示各种单体多环芳烃在水中的浓度(ng·L-1)。
本研究中丰水期EBaP值在0~127.8 ng·L-1,平均值为59.9 ng·L-1,枯水期EBaP值在0~34.5 ng·L-1,平均值为32.4 ng·L-1(图4)。其中,丰水期和枯水期分别有4个和6个采样点超出原国家环保总局(China Environmental Protection Administration, CEPA)制定的EBaP = 2.8 ng·L-1的风险值[28],其他采样点EBaP值均低于此风险值,但均值已高于此风险值。这些信息都表明,汾河流域水中的PAHs已经具有不利健康的风险,随着工业和交通的不断发展,PAHs污染日益严重,并会进一步影响生态环境,危害人类健康,因此,有必要加强对汾河饮用水源PAHs的监测与研究。
2.3 汾河流域沉积相中PAHs的浓度分布与来源辨析
2.3.1 沉积相中PAHs浓度分布
汾河沉积物中16种PAHs浓度见表4,PAHs浓度范围为1.29~8.44 μg·g-1,均值为(3.774±1.987) μg·g-1。这可能是由于在采样期间大量PAHs通过城市地表径流、土壤淋溶及雨水洗刷作用(湿沉降作用)进入水环境,进而被悬浮物颗粒吸附沉降至底泥中;同时丰水期气温高、雨量充沛,地表径流量大不仅使水体PAHs得到稀释,也使底泥扰动释放较多的PAHs到水环境中。
沉积相PAHs组成及含量分布见图5(在采样过程中,有几处采样点水深较深,沉积物未采集到,数据空缺)。由图所示,沉积物中PAHs沿河分布并不均匀,主要集中在流域中下游地区,越接近工业园区、人口稠密区及商业集中区,PAHs含量越高,这与人为源输入有关。采样点S12、S13、T3、S15、S16、S17、S18、S19、T8、S20沉积物PAHs含量高于均值(3.744 μg·g-1),多数集中在流域中下游,其中S16采样点PAHs浓度最高,为8.442 μg·g-1。近年来,汾河下游临汾段、运城段等周边地区经济总量不断增长,人口持续增长,城市化进程不断加快,在调查时发现聚集分布着纺织印染厂、污水处理厂等工业企业,这些企业附近有污水排放口,造成了水体浑浊。此外,大气干湿沉降、雨水洗刷及工业废水排放可能是PAHs高含量的主要原因,因此人为活动加大了有机污染物的输入。

图4 汾河流域各采样点丰水期和枯水期EBaP值Fig. 4 EbaP values of each sampling sites in wet and dry seasons of Fenhe River

表4 汾河丰水期沉积相中PAHs的含量(μg·g-1)Table 4 PAHs contents in sediment of Fenhe River in wet season (μg·g-1)
按PAHs的环数来区分,PAHs均集中在低环(2~3环),而高环(5~6环)含量很少,其组成为3环>2环>4环>5环>6环,其中3环含量约占总量的50.4%,2环含量约占总量的25%,4、5、6环PAHs含量较低,分别占PAHs总量的15%、8.4%和1.2%。与丰水期和枯水期水相中PAHs相比,沉积物中4、5、6环PAHs所占的百分比总和分别增加了21.1%和15%,说明在PAHs迁移分配的过程中,高环PAHs更易于富集在沉积物中。造成沉积物中较高分子量PAHs增加的原因是高分子量PAHs比低分子量的溶解度和蒸气压都低,而辛醇-水分配系数(Kow)、有机碳归一化系数(Koc)值都高,且水相迁移能力较弱[24],更易分配吸附到沉积物中,沉积物成为其蓄积库。此外,许多相关研究也报道了沉积物pH值、TOC含量、组成类型、粒径大小等均可能成为PAHs分布的重要控制因素[29-31]。16种PAHs化合物中,苯并[a]芘(Bap)的含量虽然不高,约占PAHs总量的23%,但它具有强致癌性,并且研究表明,河流沉积物中Bap具有从沉积物转入水中的性质[24],因而河流沉积物中Bap会因经常受到冲刷而使地面水处于污染状态,从而对沿岸居民健康构成一定的威胁。
汾河流域沉积物与国内外其他河流沉积物中PAHs的比较见表5。与国内河流沉积物中PAHs的含量相比,本研究区域的PAHs浓度范围(1 285~8 442 ng·g-1)与珠江三角洲(138~6 793 ng·g-1)[5]处于同一个污染水平,要高于北格河(17.7~407.7 ng·g-1)[7]、厦门湾(247~480 ng·g-1)[34]、九龙河(99~1 117ng·g-1)[19]、黄河中下游(31~133 ng·g-1)[35]、长江武汉段(72.4~3 995.2 ng·g-1)[4]、北京通惠河(127~928 ng·g-1)[36]、滦河(6.7~1 585.7 ng·g-1)[38]PAHs的浓度范围,低于海河天津段(774.8~255 371 ng·g-1)[37]和天津潮白河(787~1 943 000 ng·g-1)[24]等PAHs的浓度范围;与国外一些城市化的河口和港口相比,低于韩国Hyeongsan River(5.3~768 000 ng·g-1)[32]和美国New York Harbor(1 900~70 000 ng·g-1)[33]PAHs总量的浓度范围。综上所述,与本研究提到的河流、湖泊及港口沉积物中PAHs含量比较,汾河流域沉积物中PAHs污染程度仍处于中等偏高的污染水平。

图5 汾河沉积相中PAHs的组成及含量分布Fig. 5 Compositions and concentrations of PAHs in sediment of Fenhe River
汾河流域不同点位的方差分析见表6,该表仅统计了有显著性差异的结果。结果显示,上游水体PAHs总量分别与中游水体和沉积物PAHs总量有显著性差异(P<0.05),特别是与下游沉积物PAHs总量差异性显著(P<0.01);上游沉积物PAHs总量与下游沉积物PAHs总量有显著性差异(P<0.05)。结合图2和图4的结果可知,汾河流域上游PAHs总量显著低于下游PAHs总量,因此,汾河流域PAHs污染主要集中在中下游。

表5 汾河流域沉积相中PAHs污染浓度与其他地区的比较Table 5 Comparison of PAHs concentrations in sediment of Fenhe River and other rivers all over the world
注:*不包括汾河太原段退水渠中(T3、T4和T5这3个样点)的PAHs浓度。
Note:*PAHs concentrations of waste canals (T3, T4 and T5) were not included.

表6 汾河流域丰水期上、中、下游水体和沉积相中PAHs总量的方差分析Table 6 Variance analysis of total PAHs contents in water and sediment of Fenhe River in wet season
注:*P < 0.05,**P<0.01。
Note:*P < 0.05, **P<0.01.
汾河流域不同种类PAHs含量的方差分析见表7,该表仅统计了有显著性差异的结果。结果显示,汾河流域水体和沉积物中2环PAHs含量分别与水体中3、4、5、6环数PAHs含量有显著性差异(P<0.05),与沉积物中3环和6环PAHs含量有显著性差异(P<0.05)。水体和沉积物中3环PAHs含量分别与水体和沉积物中2、4、5、6环PAHs含量差异显著(P<0.01)。结合图2和图5的结果发现,汾河流域水体和沉积物中2、3环PAHs含量显著高于其他环数PAHs含量,是汾河流域PAHs污染的主要类型。
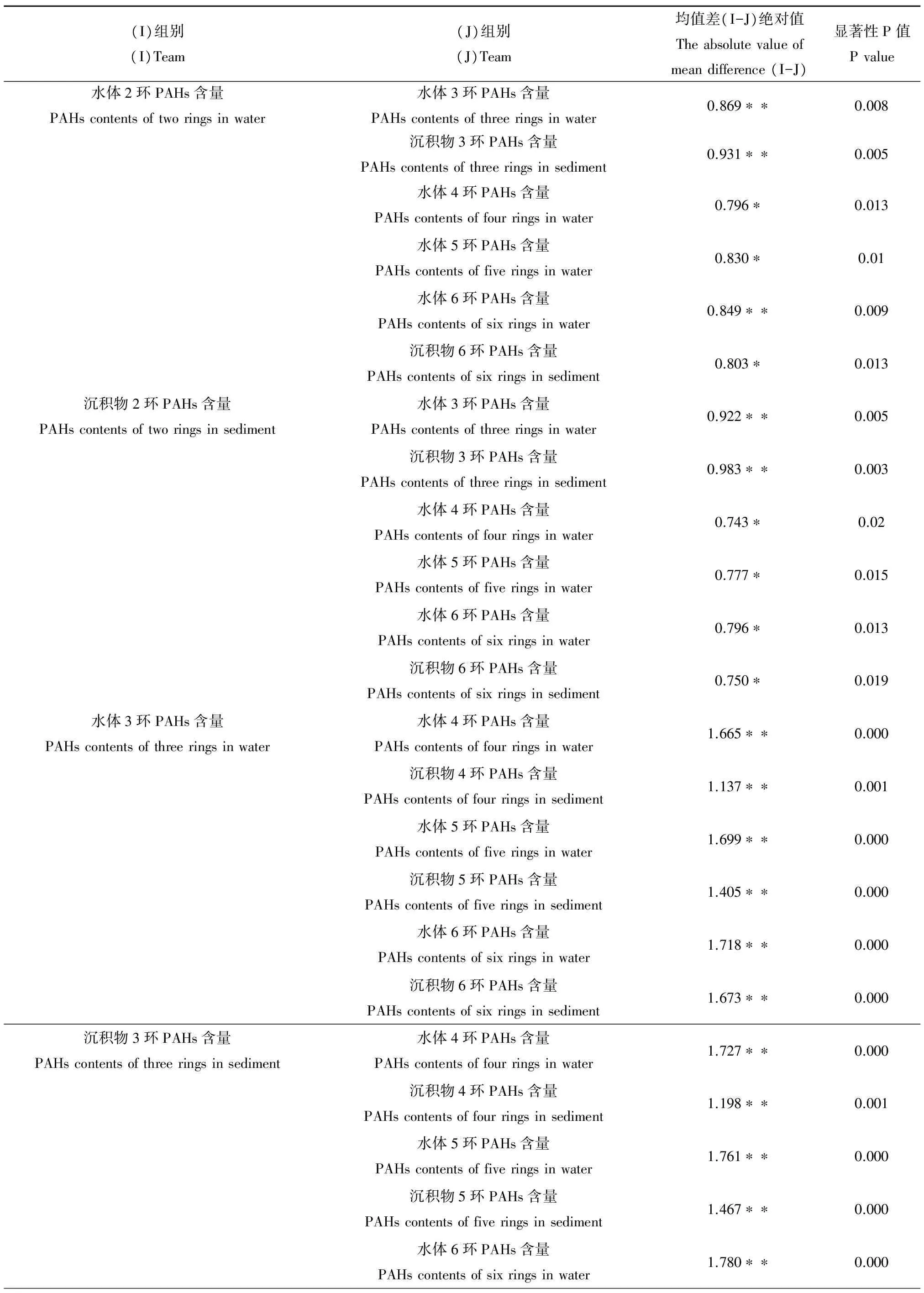
表7 汾河流域丰水期水体和沉积相不同种类PAHs含量的差异性分析Table 7 Variance analysis of contents of different kinds of PAHs in water and sediment of Fenhe River in wet season
注:*P < 0.05,**P<0.01。
Note: *P < 0.05, **P<0.01.

图6 汾河丰水期沉积相多环芳烃来源Fig. 6 Source analysis of PAHs in sediment of Fenhe River in wet season
2.3.3 沉积相中PAHs的来源辨析
对汾河流域丰水期上、中、下游沉积相PAHs来源进行分析(图6),结果表明,大部分采样点沉积相中FLU/(FLU+PYR)比值均大于0.5,与代表了木材、煤炭等的不完全燃烧比值接近,中、下游有少量采样点该比值小于0.5,表明存在典型的石油源污染。丰水期沉积相中ANT/(ANT+PHE)的比值范围为0.023~0.175,其中50%的采样点ANT/(ANT+PHE)的比值大于0.1,代表了煤炭、木材等的不完全燃烧。此外,有个别采样点的ANT/(ANT+PHE)值小于0.1、FLU/(FLU+PYR)值小于0.4,表明有来自石油类产品的输入。可能由于流域周围存在着油库、加油站等设施,并且丰水期汾河水库附近有许多观光游船,这些游船大部分使用汽油或柴油作为燃料,因而来往船只的燃油泄漏可能造成石油类产品的来源。因此,PAHs的组成特征表明汾河流域丰水期沉积相中PAHs以燃烧源为和石油源为主,部分来自典型石油类产品的输入。
对比丰水期水体和沉积物的FLU/(FLU+PYR)和ANT/(ANT+PHE)值,两者的特征比值并不完全一致。这是因为PAHs以吸附于颗粒物、溶解态或乳化态存在于水环境中,吸附态占优势并最终归于沉积物[39]。而水底沉积物中PAHs不易受到阳光照射且深水中含氧量较低,很难发生光解,性质较稳定。此外,受PAHs自身性质影响,进入水中的PAHs大部分会被分配到非水相中,而且分子量越大的PAHs水溶解度越小,因此溶解于水中的PAHs以低环、低分子量为主,高环、高分子量的PAHs趋向于分布在颗粒物及沉积物中,从而导致水中与沉积物中的PAHs种类不同,反映不同的污染源,即水体中PAHs的源解析结果显示石油源的比例较大,而沉积物中PAHs以高温燃烧源为主。
2.4 汾河流域沉积相中PAHs的生态风险评估
目前对于沉积物中污染物风险评价尚未建立统一的标准,通过相平衡分配(EqP)法建立沉积物质量基准(SQC)的方法是美国环境保护署(US EPA)推荐的方法之一[40]。此外,Long等[41](1995)研究有机污染物的环境影响时,提出了用于确定海洋和河口沉积物中有机物污染物潜在生态风险的效应区间低值(ERL: effects range low,生物负效应几率<10%),效应区间中值(ERM: effects range median,生物负效应几率>50%),鉴于该方法便于比较,当今国内外学者多采用此种方法来指示沉积物的风险程度[42-45]。ERL和ERM这2个指标用于指示相应级别的生态风险,若PAHs单组份质量分数小于ERL相应值,则其对生物体几乎不产生危害或危害极小;若PAHs单组份质量分数在ERL和ERM相应值之间,则其只对生物体产生一定程度的危害;若PAHs单组份质量分数大于ERM相应值,则其对生物体产生危害的可能性极大。
本文将汾河表层沉积物16种多环芳烃与相应的沉积物生态风险标准水平进行比较,结果见表8。从表8可以看出,对于提出的12种PAHs的ERL值或ERM值,均存在采样点表层沉积物含量高于ERL值或ERM值的现象。这表明汾河流域沉积物对生物产生危害的可能性极大。此外,对于BbF和BkF这2类没有最低安全值的PAHs化合物来说,只要在环境中存在就会对生物产生不利影响。而这2类化合物在汾河流域上、中、下游均有样点检出,表明在存在较大的生态风险。
汾河流域水相中丰水期PAHs平均浓度为2.738 μg·L-1,枯水期PAHs总量均值为2.762 μg·L-1,丰水期PAHs的污染浓度与枯水期相近。就空间分布而言,汾河流域从上游至下游各断面的PAHs浓度差异较大,整体呈现上游污染较轻,中下游污染严重的特点。PAHs的组成规律显示,丰水期和枯水期PAHs含量均以低环(2~3环)为主,丰水期和枯水期低环PAHs所占比例分别为96.5%和90.4%。地表水健康风险评价结果显示,汾河流域丰水期和枯水期分别有13.8%和20.7%的点位存在一定的健康风险。
汾河流域沉积相中16种PAHs平均浓度为3.774 μg·g-1,其污染主要集中在流域中下游地区。方差分析结果表明,上游水体PAHs总量分别与中游水体和沉积物PAHs总量有显著性差异(P<0.05),特别是与下游沉积物PAHs总量差异性显著(P<0.01);上游沉积物PAHs总量与下游沉积物PAHs总量有显著性差异(P<0.05)。PAHs的组成规律显示,PAHs含量集中在低环(2~3环),约占总量的75%左右。方差分析结果表明,汾河流域水体和沉积物中2环PAHs含量分别与水体中3、4、5、6环数PAHs含量有显著性差异(P<0.05),与沉积物中3环和6环PAHs含量有显著性差异(P<0.05)。水体和沉积物中3环PAHs含量分别与水体和沉积物中2、4、5、6环PAHs含量差异显著(P<0.01)。表层沉积物生态风险评价结果显示,对于提出的12种PAHs的ERL值或ERM值以及BbF和BkF这2类没有最低安全值的PAHs化合物来说,汾河流域上、中、下游均存在采样点表层沉积物含量高于ERL值或ERM值或BbF和BkF超标的现象。与本研究提到的国内外其他河流、湖泊及港口的水体和沉积物相比,汾河流域PAHs的污染程度处于中等到较高程度的污染。
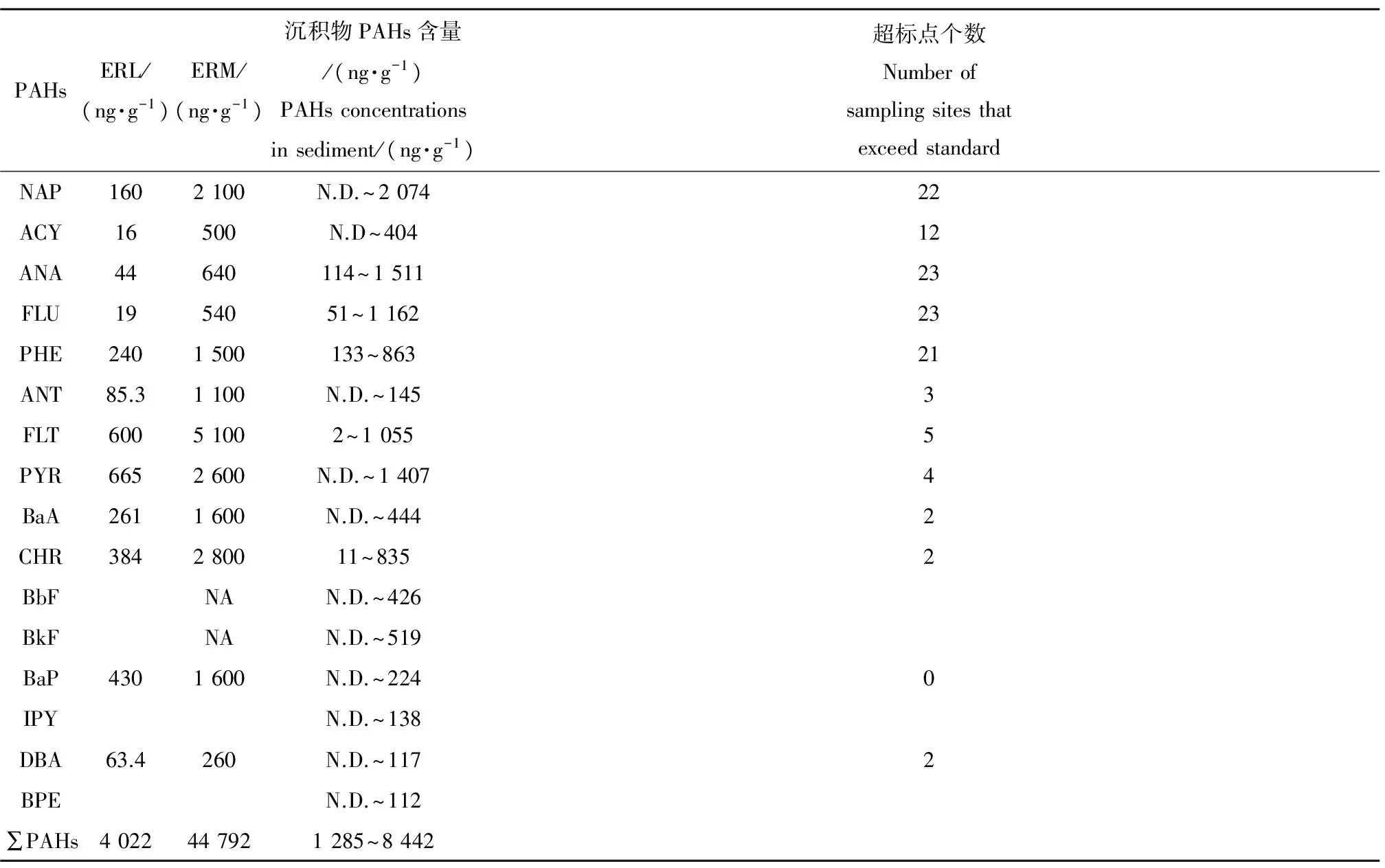
表8 汾河流域表层沉积物16种PAHs生态风险评价Table 8 Ecological risk assessment of 16 PAHs in surface sediment of Fenhe Basin
注:NA表示无最低安全值,ERL表示效应区间低值,ERM表示效应区间中值。
Note: NA indicates the safe values did not exist, ERL means effects range low, ERM means effects range median.
汾河流域丰水期和枯水期水相中FLU/(FLU+PYR)的特征比值均大于0.5,丰水期大部分采样点ANT/(ANT+PHE)比值小于0.1,枯水期有50%采样点该比值大于0.1;汾河流域丰水期沉积相中FLU/(FLU+PYR)的特征比值均大于0.5,有50%采样点沉积相ANT/(ANT+PHE)的比值大于0.1,有个别采样点的ANT/(ANT+PHE)值小于0.1、FLU/(FLU+PYR)值小于0.4,因此,汾河流域丰水期和枯水期水体中PAHs来源于石油源和植物、木材、煤的燃烧,主要受到流域煤化工、燃煤电厂排放污染物的影响;丰水期沉积相中PAHs以燃烧源和石油源为主,部分来自典型石油类产品的输入。
综上所述,汾河流域PAHs含量整体呈现上游污染较轻,中下游污染严重,存在潜在的生态风险。据此,我们提出汾河流域保护措施及管理政策建议:(1) 对汾河流域上游卡站采取更为严格的生态保护措施,并提供生态补偿保障机制;加强对流域中下游周边工业、企业污染物排放的控制,应结合实际情况,建议污水先通过城市污水厂处理,再通过湿地系统处理后排放入河,对于水环境容量较低、自净能力较弱的汾河来讲是十分必要的,同时控制农村生活污染及农业面源污染。(2) 加强汾河流域枯水期的水资源管理,严格监控石油源和植物、木材、煤的燃烧来源,控制流域煤化工、燃煤电厂污染物的排放,对生活污水及工业废水要进行源头治理,坚决杜绝未经处理直接向汾河排污。在沿岸几个重点排污城市应增扩建污水厂,扩大处理规模,中小城市也应因地制宜地建设合适规模的污水处理厂或污水处理设施。(3) 加强汾河流域沉积物的污染控制,以减小其作为河流内源重新进入水中向下游转移的风险。(4) 加强汾河支流流域治理,在汾河支流干线和汾河支流入汾河河口处实施生态修复,营建人工湿地,利用潜流湿地、功能表流湿地和景观表流湿地相结合的方式进一步改善汾河的支流水质。
[1] Krupadam R J, Khan M S, Wate S R. Removal of probable human carcinogenic polycyclic aromatic hydrocarbons from contaminated water using molecularly imprinted polymer [J]. Water Research, 2010, 44(3): 681-688
[2] Dickhut R M, Gustafson K E. Atmospheric inputs of selected polycyclic aromatic hydrocarbons and polychlorinated biphenyls to Southern Chesapeake Bay [J]. Marine Pollution Bulletin, 1995, 30(6): 385-396
[3] 周怀东, 赵健, 陆瑾, 等. 白洋淀湿地表层沉积物多环芳烃的分布、来源及生态风险评价[J]. 生态毒理学报, 2008, 3(3): 291-299
Zhou H D, Zhao J, Lu J, et al. Distribution, sources and ecological risk assessment of polycyclic aromatic hydrocarbons in sediments from Baiyangdian wetland [J]. Asian Journal of Ecotoxicology, 2008, 3(3): 291-299 (in Chinese)
[4] 徐雄, 李春梅, 孙静, 等. 我国重点流域地表水中29种农药污染及其生态风险评价[J]. 生态毒理学报, 2016, 11(2): 347-354
Xu X, Li C M, Sun J, et al. Residue characteristics and ecological risk assessment of twenty-nine pesticides in surface water of major river-basin in China [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 347-354 (in Chinese)
[5] Luo X J, She J C, Mai B X, et al. Distribution source apportionment and transport of PAHs in sediment from the Pearl River Delta and the Northern South China Sea [J]. Archives of Environmental Contamination and Toxicology, 2008, 55(1): 11-20
[6] 黄亮, 张经, 吴莹. 长江流域表层沉积物中多环芳烃分布特征及来源解析[J]. 生态毒理学报, 2016, 11(2): 566-572
Huang L, Zhang J, Wu Y. Distribution and source of polycyclic aromatic hydrocarbons in surface sediment from the Yangtze River [J]. Asian Journal of Ecotoxicology, 2016, 11(2): 556-572 (in Chinese)
[7] Zhang S Y, Zhang Q, Shameka D, et al. Simultaneous quantification of polycyclic aromatic hydrocarbons (PAHs), polychlorinated biphenyls (PCBs), and pharmaceuticals and personal care products (PPCPs) in Mississippi River water, in New Orleans, Louisiana, USA [J]. Chemosphere, 2007, 66(6): 1057-1069
[8] Malik A, Verma P, Singh A K, et al. Distribution of polycyclic aromatic hydrocarbons in water and bed sediments of the Gomti River, India [J]. Environmental Monitoring and Assessment, 2011, 172(1-4): 529-545
[9] 卜庆伟, 王东红, 王子健. 基于风险分析的流域优先有机污染物筛查: 方法构建[J]. 生态毒理学报, 2016, 11(1): 61-69
Bu Q W, Wang D H, Wang Z J. A risk-based screening approach for priority organic contaminants at the watershed scale: Method development [J]. Asian Journal of Ecotoxicology, 2016, 11(1): 61-69 (in Chinese)
[10] 张明, 唐访良, 吴志旭, 等. 千岛湖表层沉积物中多环芳烃污染特征及生态风险评价[J]. 中国环境科学, 2014, 34(1): 253-258
Zhang M, Tang F L, Wu Z X. Pollution characteristics and ecological risk assessment of polycyclic aromatic hydrocarbons (PAHs) in surface sediments from Xin’anjiang Reservoir [J]. China Environmental Science, 2014, 34(1): 253-258 (in Chinese)
[11] 东口朋宽, 史江红, 张晖, 等. 汾河流域太原段河水及沉积物中PFOS和PFOA的浓度分布特征[J]. 环境科学, 2013, 34(11): 4211-4217
Higashiguchi T, Shi J H, Zhang H, et al. Distribution of perfluorooctanesulfonate and perfluorooctanoate in water and the sediment in Fenhe River, Shaixi Province [J]. Environmental Science, 2013, 34(11): 4211-4217 (in Chinese)
[12] 郭掌珍, 孟会生, 张渊, 等. 汾河表层沉积物PCBs和OCPs含量、来源及生态风险[J]. 中国环境科学, 2013, 33(4): 714-721
Guo Z Z, Meng H S, Zhang Y, et al. Polychlorinated biphenyl and organochlorine pesticides in surface sediments of Fenhe River: The concentration, sources and ecological risk [J]. China Environmental Science, 2013, 33(4): 714-721 (in Chinese)
[13] Jiang Y F, Wang X T, Wang F, et al. Levels, composition profiles and sources of polycyclic aromatic hydrocarbons in urban soil of Shanghai, China [J]. Chemosphere, 2009, 75(8): 1112-1118
[14] Tao S, Cui Y H. Determination of PAHs in wastewater irrigated agricultural soil using accelerated solvent extraction [J]. Journal of Environmental Science and Health, 2002, 37(2): 141-150
[15] 宋雪英, 李玉双, 伦小文, 等. 太子河水体中多环芳烃分布与污染源解析[J]. 生态学杂志, 2010, 29(12): 2486-2490
Song X Y, Li Y S, Lun X W, et al. Distribution and related source identification of polycyclic aromatic hydrocarbons in surface water of Taizi River [J]. Chinese Journal of Ecology, 2010, 29(12): 2486-2490 (in Chinese)
[16] Mc Cready S, Slee D, Birch G, et al. The distribution of polycyclic aromatic hydrocarbons in surficial sediments of Sydney Harbour, Australia [J]. Marine Pollution Bulletin, 2000, 40(11): 999-1006
[17] 秦宁, 何伟, 王雁, 等. 巢湖水体和水产品中多环芳烃的含量与健康风险[J]. 环境科学学报, 2013, 33(7): 1116-1117
Qin N, He W, Wang Y, et al. Residues and health risk of polycyclic aromatic hydrocarbons in the water and aquatic products from Lake Chaohu [J]. Acta Scientiae Circumstantiae, 2013, 33(7): 1116-1117 (in Chinese)
[18] Guo W, He M, Yang Z, et al. Distribution of polycyclic aromatic hydrocarbons in water, suspended particulate matter and sediment from Daliao River watershed, China [J]. Chemosphere, 2007, 68(1): 93-104
[19] Maskaoui K, Zhou J, Hong H, et al. Contamination by polycyclic aromatic hydrocarbons in the Jiulong River Estuary and western Xiamen Sea, China [J]. Environmental Pollution, 2002, 118(1): 109-122
[20] 麦碧娴, 林峥, 张干, 等. 珠江三角洲河流和珠江口表层沉积物中有机污染物研究-多环芳烃和有机氯农药的分布及特征[J]. 环境科学学报, 2000, 20(2): 192-197
Mai B X, Lin Z, Zhang G, et al. Organic contaminants in surface sediments from rivers of the Pearl River Delta and Estuary: The distributions and characteristics of PAHs and organochlorine pesticides [J]. Acta Scientiae Circumstantiae, 2000, 20(2): 192-197 (in Chinese)
[21] 许士奋, 蒋新, 王连生, 等. 长江和辽河沉积物中的多环芳烃类污染物[J]. 中国环境科学, 2000(2): 128-131
Xu S F, Jiang X, Wang L S, et al. Polycyclic aromatic hydrocarbons (PAHs) pollutants in sediments of the Yangtze River and Liaohe River [J]. China Environmental Science, 2000(2): 128-131 (in Chinese)
[22] 李恭臣, 夏星辉, 王然, 等. 黄河中下游水体中多环芳烃的分布及来源[J]. 环境科学, 2006, 27(9): 1738-1743
Li G C, Xia X H, Wang R, et al. Pollution of polycyclic aromatic hydrocarbons (PAHs) in middle and lower reaches of the Yellow River [J]. Environmental Science, 2006, 27(9): 1738-1743 (in Chinese)
[23] Chen Y, Zhu L, Zhou R. Characterization and distribution of polycyclic aromatic hydrocarbon in surface water and sediment from Qiantang River, China [J]. Journal of Hazardous Materials, 2007, 141(1): 148-155
[24] Shi Z, Tao S, Pan B, et al. Contamination of rivers in Tianjin, China by polycyclic aromatic hydrocarbons [J]. Environmental Pollution, 2005, 134(1): 97-111
[25] 焦琳. 渭河流域水体中外源性环境激素的污染调查及分析[D]. 西安: 西安科技大学, 2010: 28-43
Jiao L. Study on determination of exogenous environment endocrine disruptors in Weihe River Basin [D]. Xi’an: Xi’an University of Science and Technology, 2010: 28-43 (in Chinese)
[26] 刘书臻. 环渤海西部地区大气中的PAHs污染[D]. 北京: 北京大学, 2008: 95-114
Liu S Z. Atmospheric PAH contamination in the Western Watershed of Bohai Sea, China [D]. Beiing: Peking University, 2008: 95-114 (in Chinese)
[27] Nisbet I C T, Lagoy P K. Toxic equivalency factors (TEFs) for polycyclic aromatic hydrocarbons (PAHs) [J]. Regulatory Toxicology and Pharnacology, 1992, 16: 290-300
[28] 国家环境保护总局. GB3838—2002 地表水环境质量标准[S]. 北京: 中国标准出版社, 2002
[29] Hoch M. Assessment of salinity variations in TBT adsorption onto kaolinite and montmorillonite at different pH levels [J]. Water, Air, & Soil Pollution, 2004, 152(1): 349-362
[30] Wang X C, Zhang Y X, Chen R F. Distribution and partitioning of polycyclic aromatic hydrocarbons (PAHs) in different size fractions in sediments from Boston Harbor, United States [J]. Marine Pollution Bulletin, 2001, 42(11): 1139-1149
[31] 曹启民, 王华, 伍卡兰, 等. 汕头红树林湿地表层沉积物环境因子对PAHs分布的影响[J]. 生态环境学报, 2009, 18(3): 844-850
Cao Q M, Wang H, Wu K L, et al. Effects of physical-chemical properties on distribution of polycyclic aromatic hydrocarbons in surface sediment of Shantou mangrove wetlands [J]. Ecology and Environmental Sciences, 2009, 18(3): 844-850 (in Chinese)
[32] Koh C H,Khim J S, Kannan K, et al. Polychlorinated dibenzo-p-dioxins (PCDDs), dibenzofurans (PCDFs), biphenyls (PCBs), and polycyclic aromatic hydrocarbons (PAHs) and 2,3,7,8-TCDD equivalents in sediment from the Hyeongsan River, Korea [J]. Environmetal Pollution, 2004, 132: 489-501
[33] Yan B, Abrajano T A, Bopp R F, et al. Combined application of δ13C and molecular ratios in sediment cores for PAH source apportionment in the New York/New Jersey harbor complex [J]. Organic Geochemistry, 2006, 37(6): 674-687
[34] Zhou J L, Hong H S, Zhang Z L, et al. Multi-phase distribution of organic micropollutants in Xiamen Harbour, China [J]. Water Research, 2000, 34: 2132-2150
[35] Li G C, Xia X H, Yang Z F. Distribution and sources of PAHs in the middle and lower reaches of the Yellow River [J]. Environmental Pollution, 2006, 144: 985-993
[36] Zhang Z L, Huang J, Yu G, et al. Occurrence of PAHs, PCBs and organochlorine pesticides in the Tonghui River of Beijing China [J]. Environmental Pollution, 2004, 130: 249-261
[37] Jiang B, Zheng H I, Huang G Q, et al. Characterization and distribution of polycyclic aromatic hydrocarbon in sediments of Haihe River, Tianjin, China [J]. Journal of Environmental Science, 2007, 19: 306-311
[38] Bai Y J, Li X Q, Liu W X, et al. Polycyclic aromatic hydrocarbon (PAH) concentrations in the dissolved, particulate and sediment phases in the Luan River watershed China [J]. Journal of Environmental Science and Health (Part A), 2008, 43: 365-374
[39] 许云竹, 花修艺, 董德明, 等. 地表水环境中PAHs源解析的方法比较及应用[J]. 吉林大学学报: 理学版, 2011, 49(3): 565-574
Xu Y Z, Hua X Y, Dong D M, et al Comparison among methods of source apportionment of PAHs and their application in surface water analysis [J]. Journal of Jilin University: Science Edition, 2011, 49(3): 565-574 (in Chinese)
[40] EPA. Procedures for the Derivation of Equilibrium Partitioning Sediment Benchmarks (ESBs) for the Protection of Benthic Organisms: PAH Mixtures. EPA/600/R-02/013 [R]. Washington DC: US EPA, 2003
[41] Long E R, MacDonald D D, Smith S L, et al. Incidence of adverse biological effects within ranges of chemical concentrations in marine and estuarine sediments [J]. Environmental Management, 1995, 19(1): 81-97
[42] Chen Q Y, Liu J L, Liu F, et al. Biologic risk and source diagnose of 16 PAHs from Haihe River Basin, China [J]. Frontiers of Environmental Science and Engineering, 2016, 10(1): 46-52
[43] Kanzari F, Asia L, Syakti A D, et al. Distribution and risk assessment of hydrocarbons (aliphatic and PAHs), polychlorinated biphenyls (PCBs), and pesticides in surface sediments from an agricultural river (Durance) and an industrialized urban lagoon (Berre Lagoon), France [J]. Environmental Monitoring and Assessment, 2015, 187: 591-602
[44] Kanzari F, Syakti A D, Asia L, et al. Distributions and sources of persistent organic pollutants (aliphatic hydrocarbons, PAHs, PCBs and pesticides) in surface sediments of an industrialized urban river (Huveaune), France [J]. Science of the Total Environment, 2014, 478: 141-151
[45] 陈卫锋, 倪进治, 杨红玉, 等. 福州内河沉积物中多环芳烃的分布、来源及其风险评价[J]. 中国环境科学, 2010, 30(12): 1670-1677
Chen W F, Ni J Z, Yang H Y, et al. Distribution, sources and ecological risks of PAHs in inland river sediments of Fuzhou City [J]. China Environmental Sciences, 2010, 30(12): 1670-1677 (in Chinese)
◆
SpatialVarietyandEcologicalRiskofPolycyclicAromaticHydrocarbons(PAHs)inWaterandSurfaceSedimentsofFenheRiverBasin,China
Zhao Ying1, Dang Jinhua1, Wang Fei2,*
1. Shanxi Academy of Environmental Sciences, Taiyuan 030027, China2. Physical Science Institute of Shanxi University, Taiyuan 030006, China
10.7524/AJE.1673-5897.20160912002
2016-09-12录用日期2016-12-14
1673-5897(2017)3-579-18
X171.5
A
王飞(1980—),男,环境科学博士,副教授,主要研究方向为流域水环境过程,发表学术论文30余篇。
国家自然科学基金项目(41401020,41601202);山西省青年科技研究基金项目(2015021173);山西省自然科学基金项目(2013011040-7)
赵颖(1982-),女,高级工程师,研究方向为湿地水环境化学,E-mail: shadowying210@163.com
*通讯作者(Corresponding author), E-mail: nemo@sxu.edu.cn
赵颖, 党晋华, 王飞. 汾河流域水系和表层沉积物中多环芳烃的空间变化规律及其生态风险研究[J]. 生态毒理学报,2017, 12(3): 579-596
Zhao Y, Dang J H, Wang F. Spatial variety and ecological risk of polycyclic aromatic hydrocarbons (PAHs) in water and surface sediments of Fenhe River Basin, China [J]. Asian Journal of Ecotoxicology, 2017, 12(3): 579-596 (in Chinese)

