异甘草素合成工艺优化及其清除自由基活性研究
张光辉,张拴,龙旭,郭惠,孟庆华,左振宇
(陕西中医药大学 药学院, 陕西 咸阳 712046)
异甘草素合成工艺优化及其清除自由基活性研究
张光辉,张拴*,龙旭,郭惠,孟庆华,左振宇
(陕西中医药大学 药学院, 陕西 咸阳 712046)
对异甘草素的合成工艺进行优化和体外清除自由基活性进行研究。通过间苯二酚、冰醋酸、对羟基苯甲酸合成异甘草素,考察物料比、温度、反应时间对产率的影响,通过紫外分光度法对其清除自由基活性进行研究。酚与酸物料比1∶2.5,240 W微波辐射3 min,2,4-二羟基苯乙酮产率最高为65.75%;当醛酮物质的量比为3∶1,温度控制在120~130 ℃,回流6 h,异甘草素产率最高为28.10%;反应时间控制20 min,异甘草素加入量为1.00 mL清除DPPH自由基能力最强,为66.4%。异甘草素具有一定的抗自由基活性。
异甘草素;合成;抗自由基
Abstract:The synthesis process of isoliquiritigenin was optimized and its activity of scavenging free radicals in vitro was studied. Firstly, isoliquiritigenin was prepared from resorcinol, acetic acid and p-hydroxybenzoic acid. The influence of molar ratio of reactants, reaction temperature and reaction time on the yield of isoliquiritigenin product was investigated. The results showed that, when the molar ratio of resorcinol and acetic acid was 1:2.5, microwave radiation was 240 W for 3 min, the product yield of 2, 4-dihydroxyacetophenone reached the maximum value, 65.75%;When the molar ratio of aldehyde and ketone was 3:1, the temperature was about 120~ 130 ºC with reflux time of 6 h,the yield of isoliquiritigenin product was as high as 28.10%. Then, the activity of scavenging DPPH free radicals was the highest, about 66.4 when 1.00 mL isoliquiritigenin was added to the solution with the reaction time of about 20 min.The results indicated that isoliquiritigenin has good anti-free radicals ability.
Key words:Isoliquiritigenin; Synthesis; Anti-free radicals
甘草为豆科植物甘草,胀果甘草和光果甘草的根及根茎[1],又名拉乌尔草,早在《神农本草经》上就列为上品中药,其性味甘平,传统中医药认为它具有补脾益气、清热解毒、通淋利尿、祛痰止咳、缓急止痛、调和诸药的功效等作用,在我国主要分布于新疆、甘肃、西藏等地区。异甘草素是甘草中黄酮中的主要成份之一,结构如图1示,属于二氢黄酮类化合物,分子式为C15H12O4,熔点198~200℃,黄色针状结晶[2]。异甘草素有抗溃疡、抗炎[3]、解痉、抗菌、抗肿瘤[4]、美白、抗氧化[5]、预防动脉粥样硬化、保护肝脏[6]等广泛的药理作用,但是甘草中的异甘草素的含量低,价格昂贵,提取过程繁琐,限制了它的应用。
为此,本实验拟对化学方法合成异甘草素条件进行优化,并对其体外清除自由基活性进行研究,旨在为进一步开发利用异甘草素提供实验基础。

图1 异甘草素的结构Fig.1 The structure of isoliquiritigenin
1 实验部分
1.1 实验试剂与仪器
间苯二酚(AR,天津市科密欧化学试剂有限公司),氯化锌(AR,天津市天力化学试剂有限公司),冰醋酸(AR,天津市科密欧化学试剂有限公司),对羟基苯甲醛(AR,国药集团化学试剂有限公司),石油醚(AR,成都市科龙化工试剂厂),乙酸乙酯(AR,成都市科龙化工试剂厂),二苯代苦味肼基自由基(日本东京化成工业株式会社) 。
1.1.2 实验仪器
显微熔点测定仪(XT4A,精确度1 ℃),恒温磁力搅拌器(HJ-3A),微波化学反应器(WBFY-205),循环水多用真空泵(SHB-III),紫外/可见分光光度计UV1102(日本岛津)。
1.2 实验试剂与仪器
1.2.1 异甘草素的合成工艺优化
以间苯二酚、冰醋酸和对羟基苯甲酸为原料[7],通过两步反应,第一步通过微波反应合成 2,4-二羟基苯乙酮,第二步再与对羟基苯甲醛反应得到异甘草素[7,8],考查反应过程中物料比、反应温度、反应时间条件对产率的影响。
(1) 2,4-二羟基苯乙酮的合成
称取间苯二酚1.10 g,冰醋酸1.5 mL,无水氯化锌1.45 g于100 mL圆底烧瓶中,于240 W微波辐射3 min,然后将反应物倒入30 mL水中,有桔黄色沉淀析出,减压抽滤,用去离子水洗涤 2~3次,得到淡桔黄色固体 2,4-二羟基苯乙酮[9],熔点144 ℃。
(2) 异甘草素的合成
取上步合成的产物 2,4-二羟基苯乙酮与对羟基苯甲醛物质的量比为1:3,再加硼酸2.0 g和助溶剂甘油3.0 g于100 mL圆底烧瓶,液体石蜡浴加热升温到120~130 ℃,反应6 h,将反应物倒入盛有10 mL水的烧杯中,趁热抽滤,滤渣经硅胶柱(石油醚-乙酸乙酯比例为 2:1)洗脱,挥干,即得黄色针状晶体异甘草素。
建立多元供应体系,大力推进煤炭清洁高效利用,着力发展非煤能源,形成煤、气、油、可再生能源多轮驱动的能源供应体系。
1.3 异甘草素抗自由基活性
称取异甘草素样品和DPPH自由基溶于乙醇,分别配制成浓度为0.50 mg/L和0.10 mmol/L的溶液。取样品0.20、0.40、0.60、0.80、1.00 mL分别加入2.00 mL DPPH自由基溶液,加无水乙醇至4 mL摇匀,10 min后以无水乙醇为参比,在517 nm波长处测吸光度A 样;将样品用等体积水代替[10],按上述方法配制测定吸光度A空;利用公式:
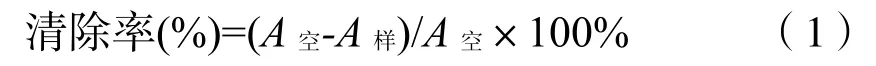
计算清除率。A样为加样品反应后DPPH溶液的吸光度;A空为不加样品, 只加 DPPH溶液的吸光度。
2 结果与讨论
2.1 2,4-二羟基苯乙酮产率的影响因素
2.1.1 酚酸物料比对2,4-二羟基苯乙酮产率的影响
在无水ZnCl2用量不变的情况下,改变间苯二酚与冰醋酸的用量,冰醋酸用量为1.5 mL时240 W微波辐射3 min,物料比为1∶2.5时,2,4-二羟基苯乙酮的产率最高。结果见表1。

表1 酚酸比对二羟基苯乙酮产率的影响Table 1 Effect of phenolic acid ratio on yield of dihydroxyacetophenone

表2 反应时间对-二羟基苯乙酮产率的影响Table 2 Effect of reaction time on yield of dihydroxyacetophenone
2.2 异甘草素产率的影响因素
2.2.1 2,4-二羟基苯乙酮与对羟基苯甲醛的物质的量比对异甘草素产率的影响
其他条件一定时,酮醛的物质的量比3∶1时,异甘草素的产率最高,结果见表3。

表3 醛酮比对异甘草素产率的影响Table 3 Effect of aldehyde and ketone ratio on yield of isoliquiritigenin
2.2.2 反应温度对异甘草素产率的影响
改变反应温度,发现在 120~130 ℃异甘草素产率最高,结果见表4。

表4 反应温度对异甘草素产率的影响Table 4 Effect of reaction temperature on yield of isoliquiritigenin
2.2.3 反应时间对异甘草素产率的影响
固定其它条件不变,在 120~130 ℃温度段,改变反应时间,发现反应6 h时异甘草素产率最高,结果见表5。

表5 反应时间对异甘草素产率的影响Table 5 Effect of reaction time on yield of isoliquiritigenin
2.3 异甘草素结构表征
样品熔点测定结果为 183~185 ℃,与异甘草素熔点基本一致。核磁共振与文献报道一致[11]。1H NMR (DMSO-d6,400MHz) δ∶13. 60 (1H,s,OH-2'),10.66 (1H,s,OH-4'),10. 14 (1H,s,OH-4),8. 15 (1H,d,J =8.4 Hz,H-6'),7. 74 (4H,m,H-α,H-β, H-2,6),6. 84(2H,d,J = 8. 4 Hz,H-3,5),6. 39 (1H,dd,J = 8. 4,2. 4 Hz,H-5'),6. 27 (1H,d,J = 2. 4 Hz,H-3')。从化学位移数据可以看出,在7. 74处有4个H,2,4-二羟基苯乙酮的甲基氢和对羟基苯甲醛的醛基氢的化学位移消失,说明醛酮发生了反应,证明产物为异甘草素。
2.4 异甘草素的抗自由基活性
DPPH (2, 2-diphenyl-1-picry-hydrazylradical)自由基较为稳定,其乙醇溶液呈蓝紫色,最大吸收波长为517 nm。当其孤对电子配对后,吸光度值会降低,吸光度与其所接受的电子数呈反比关系。结果见图2。
吸光度测定表明,当反应20 min以后,吸光度趋于水平,所以最佳显色时间控制在20 min;随着异甘草素用量增加,吸光度逐渐减小,表明清除自由基能力逐渐增强;当加入异甘草素量为1.00 mL时,利用公式(1)计算清除率最大为66.4%,表明异甘草素具有一定的抗氧化性。

图2 异甘草素不同加入量时吸光度Fig.2 The absorbance of different dosage isoliquiritigenin.
3 结 论
当间苯二酚与冰醋酸物料比1∶2.5,240 W微波辐射 3 min,2,4-二羟基苯乙酮产率最高为65.75%;当醛酮物质的量比为 3∶1,温度控制在120~130 ℃,回流 6 h,异甘草素产率最高为28.10%。活性测试结果表明,反应时间控制20 min,异甘草素加入量为1.00 mL清除DPPH自由基能力最强,为66.4%。异甘草素有一定的抗自由基活性,可以作为药品或者保健美容产品。
[1] 国家药典编委会.中国药典[S].北京:中国医药科技出版社,2010:230-231.
[2] 陈日来,李玉珍,李成.异甘草素的研究进展[J].临床医药实践杂志,2008(6):413-415.
[3] 曲晓梅,金钟太,尚艳华,等.甘草水煎液抗炎作用的实验研究[J].实用药物与临床, 2005, 8(5): 14-16.
[4]王志强,张秀英,李文广,等. 异甘草素抗肿瘤活性及初步机制研究[J].中国药理学通报,2015,31( 8):1159-1164.
[5] 潘英明,粱英.槐花米中清除自由基活性成分的提取及其性能研究[J].现代化工,2005, 11 (5):16 -20.
[6] 尹龙武,吕晓君,杨静,等.异甘草素对小鼠兔疫性肝损伤的保护作用及其机制[J].中国药理通讯,2007, 24(3):27.
[7]杨昆,杨泽华,刘显华,等.甘草素的合成及其抗癌活性[J].合成化学,2010,18(4):513-516.
[8] 杨立,沈凤嘉.甘草素与异甘草素的合成[J].药学学报,1994,29(11):877-880.
[9] 徐锁平,徐郭,裴元,等.2,4-二羟基苯乙酮的微波合成及晶体结构[J].徐州师范大学学报:自然科学版,2010,28(1):68-70.
[10]张晓璐,徐凯宏.山楂叶总黄酮清除 DPPH和超氧阴离子自由基的活性研究[J].林业科技,2008, 3(5):51-54.
[11]李宏智,艾尼瓦尔·买买提,木合布力·阿布力孜,等.异甘草素的合成及结构表征[J].中国新药杂志,2009,10(19):1882-1885.
Optimization of Synthesis Process of Isoliquiritigenin and Its Activity of Scavenging Free Radicals in Vitro
ZHANG Guang-hui,ZHANG Shuan*,LONG Xv,GUO Hui,MENG Qing-hua,ZUO Zhen-yu
(College of Pharmacy, Shaanxi University of Chinese Medicine, Shaanxi Xianyang 712046, China)
R 284
A
1671-0460(2017)09-1749-03
陕西中医药大学青年基金,项目号:2015QN22。中国博士后基金面上项目,编号:2016M602994。陕西省教育厅项目:16JK1220。
2017-03-01
张光辉(1987-),男,陕西咸阳人,讲师,硕士,2013年毕业于陕西师范大学无机化学专业,研究方向:天然药物结构修饰。E-mail:1038109280@qq.com。
张拴(1976-),男,副教授,研究方向:中药物质基础研究。E-mail:4216827116@163.com。

