高效液相色谱法同时测定兽用复方氨基比林注射液中二组分含量的研究
陈锡龙,孙真峥,王庆红
(贵州省兽药饲料监察所,贵阳550003)
高效液相色谱法同时测定兽用复方氨基比林注射液中二组分含量的研究
陈锡龙,孙真峥,王庆红
(贵州省兽药饲料监察所,贵阳550003)
建立了兽用复方氨基比林注射液二组分含量测定的高效液相色谱法。以C18柱为固定相,0.05 mol/L的磷酸二氢钾(用三乙胺调节pH值到8.2)︰乙腈=75︰25为流动相,流速为1.0 mL/min,柱温30 ℃,检测波长240 nm。采用外标法定量计算含量。巴比妥的线性范围为5.6~280 μg/mL,回归方程为y=21.856x+42.143(n=5),相关系数R2=1.0000;氨基比林的线性范围为14.3~715.0 μg/mL,回归方程为y=22.267x-13.009 (n=5),相关系数R2=1.0000。巴比妥80%、100%、120%三个添加水平的回收率在97.86%~101.06%之间,相应的氨基比林的回收率在99.48%~100.84%之间。方法专属性强,灵敏度佳,准确度高,能够有效控制兽用复方氨基比林注射液的质量。
复方氨基比林注射液;含量测定;高效液相色谱法
Abstract: A method was developed to determine two components of veterinary Compound Aminophenazone Injection by HPLC, with C18 column as stationary phase, a solution of 0.05 mol/L potassium dihydrogen phosphate (pH adjusted to 8.2 by triethylamine)-acetonitrile=75︰25 as mobile phase,flow rate of 1.0 mL/min, column temperature of 30 degree Celsius, and wavelength of 240 nm. It was quantified by external standard method and the linear range of barbital was between 5.6 and 280.0 μg/mL, and the regression equation wasy=21.856x+42.143,R2=1.0000; the linear range of aminophenazone was between 14.3 and 715.0 μg/mL, and the regression equation wasy=22.267x-13.009,R2=1.0000. Results showed that recoveries of 80%, 100%, 120% adding level of barbital were between 97.86% and 101.06%, and relative recoveries of amino ̄phenazone were between 99.48% and 100.84%. The method was precise, specific and accurate, and could be used for the content determination of veterinary Compound Aminophenazone Injection.
Keywords: compound aminophenazone injection; content determination; HPLC
兽用复方氨基比林注射液为临床常用的解热镇痛药,主要用于马、牛、羊、猪等动物的解热和抗风湿,也可用于马和骡的疝痛。复方氨基比林注射液收载于2015版《中华人民共和国兽药典》[1],其两个组分的含量测定均采用滴定法。该方法操作繁琐,专属性不强[2]。有文献[2-4]报道了人用药品中复方氨基比林注射液或复方氨林巴比妥注射液中三组分的HPLC测定法,但关于兽药的测定法未见报道。文献[5-6]只报道了兽药安痛定注射液中氨基比林和安替比林含量的HPLC法,但不包括巴比妥。本试验采用普通C18柱作为固定相,通过高效液相色谱法同时测定了复方氨基比林注射液中两个组分的含量,并进行了方法学验证。
1 材料与方法
1.1 仪器和试药 Agilent 1260 infinity高效液相色谱仪(配紫外检测器);BP211D型电子分析天平(德国塞多利斯公司);巴比妥对照品(中国食品药品检定研究院,批号:171202-201206,含量:99.6%);氨基比林对照品(中国食品药品检定研究院,批号:100503-201302,含量:99.9%);试验样品复方氨基比林注射液四批,规格均为10 mL:氨基比林0.715 g+巴比妥0.285 g,编号分别为:A、B、C、D (标称生产企业名称及批号分别为:上海申亚动物保健品有限公司,150531;山西易多利动物药业有限公司,150801;上海申亚动物保健品有限公司,160319;遵义县兽药厂,160401);甲醇为色谱纯;水为纯净水;其他试剂均为分析纯。
1.2 方法
1.2.1 色谱条件 色谱柱:Zorbax SB C18(5 μm, 4.6 mm×250 mm);流动相:0.05 mol/L磷酸二氢钾溶液(用三乙胺调节pH值到8.2)︰乙腈=75︰25;流速为1.0 mL/min;柱温为30 ℃;检测波长为240 nm[2-3];进样体积为10 μL。在此色谱条件下,复方氨基比林混合标准溶液及供试品溶液色谱图见图1。

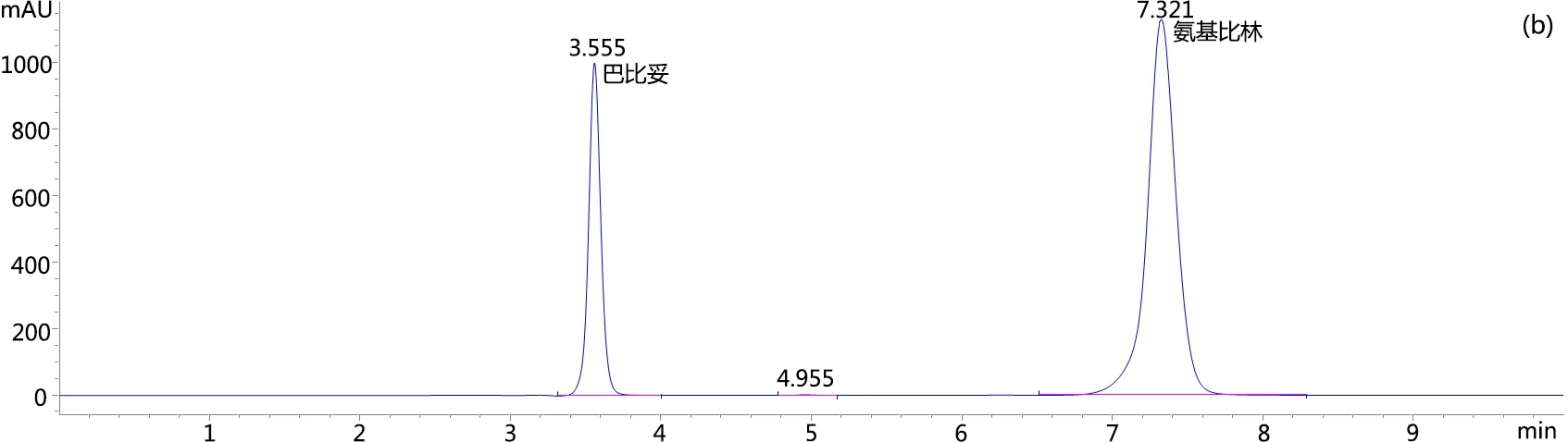
图1 复方氨基比林混合标准溶液(a)及供试品溶液(b)色谱图Fig 1 Chromatograms of standards (a) and sample (b) of compound aminophenazone
1.2.2 标准溶液的制备 分别精密称取巴比妥对照品28.0 mg和氨基比林对照品71.5 mg,置100 mL量瓶中,加流动相溶解并定容至刻度,混匀,即得巴比妥浓度为280.0 μg/mL,氨基比林浓度为715.0 μg/mL的氨基比林混合标准溶液。
1.2.3 供试品溶液的制备 精密量取复方氨基比林注射液1.00 mL,置100 mL量瓶中,加流动相溶解并定容至刻度,混匀,制成巴比妥浓度为285.0 μg/mL,氨基比林浓度为715.0 μg/mL的复方氨基比林溶液作为供试品溶液。
2 结 果
2.1 线性范围 精密量取巴比妥浓度为280.0 μg/mL、氨基比林浓度为715.0 μg/mL的氨基比林混合标准溶液适量,分别置于10 mL容量瓶中,加流动相稀释至刻度,得含巴比妥浓度分别为5.6、28.0、56.0、140.0、280.0 μg/mL和氨基比林浓度分别为14.3、71.5、143.0、357.5、715.0 μg/mL的混合标准溶液系列。精密吸取各标准溶液10 μL,注入液相色谱仪,记录色谱图。巴比妥及氨基比林标准曲线数据分别见表1和表2。
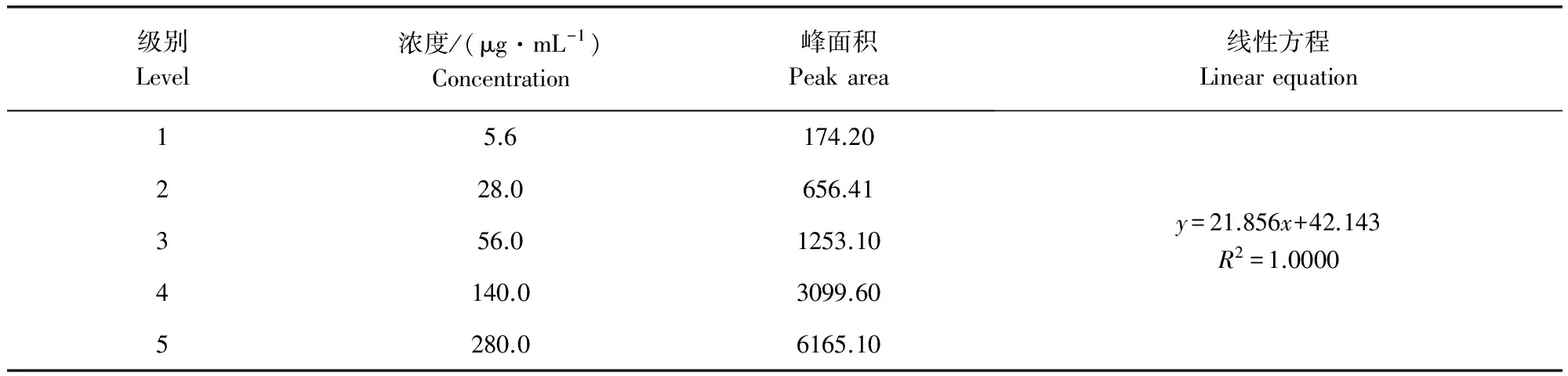
表1 巴比妥溶液的标准曲线数据Tab 1 Data of barbital standard curve

表2 氨基比林溶液的标准曲线数据Tab 2 Data of aminophenazone standard curve
2.2 仪器精密度试验 精密量取巴比妥浓度为280.0 μg/mL和氨基比林浓度为715.0 μg/mL的混合标准溶液10 μL,上机测定。重复测定6次,巴比妥和氨基比林测量结果峰面积的RSD值分别为0.04%和0.08%,说明方法具有良好的精密度。
2.3 重复性试验 取批号为160401的D样品,精密量取适量,分别按标示量用流动相稀释制成1 mL含巴比妥285.0 μg和氨基比林715.0 μg的供试品溶液,作6个平行,按上述方法中的色谱条件测定,每个平行进样2针,结果巴比妥和氨基比林的平均含量分别为标示含量的96.0%和95.1%,RSD值分别为0.05%和0.06%。
2.4 回收率试验 精密称取巴比妥和氨基比林标准物质适量,按处方分别制成含巴比妥和氨基比林分别为80%(L)、100%(M)、120%(H)的三种不同浓度的添加样品各3份,然后分别量取100 μL添加样品置10 mL量瓶中,用流动相溶解并定容至刻度。精密吸取10 μL上机测定,计算各添加样品的回收率,结果见表3和表4。
2.5 溶液稳定性试验 取复方氨基比林注射液,精密量取适量,用流动相稀释制成1 mL含巴比妥285.0 μg和氨基比林715.0 μg的供试品溶液,分别于0、12、24 h,测定峰面积,结果表明溶液在24 h内稳定。
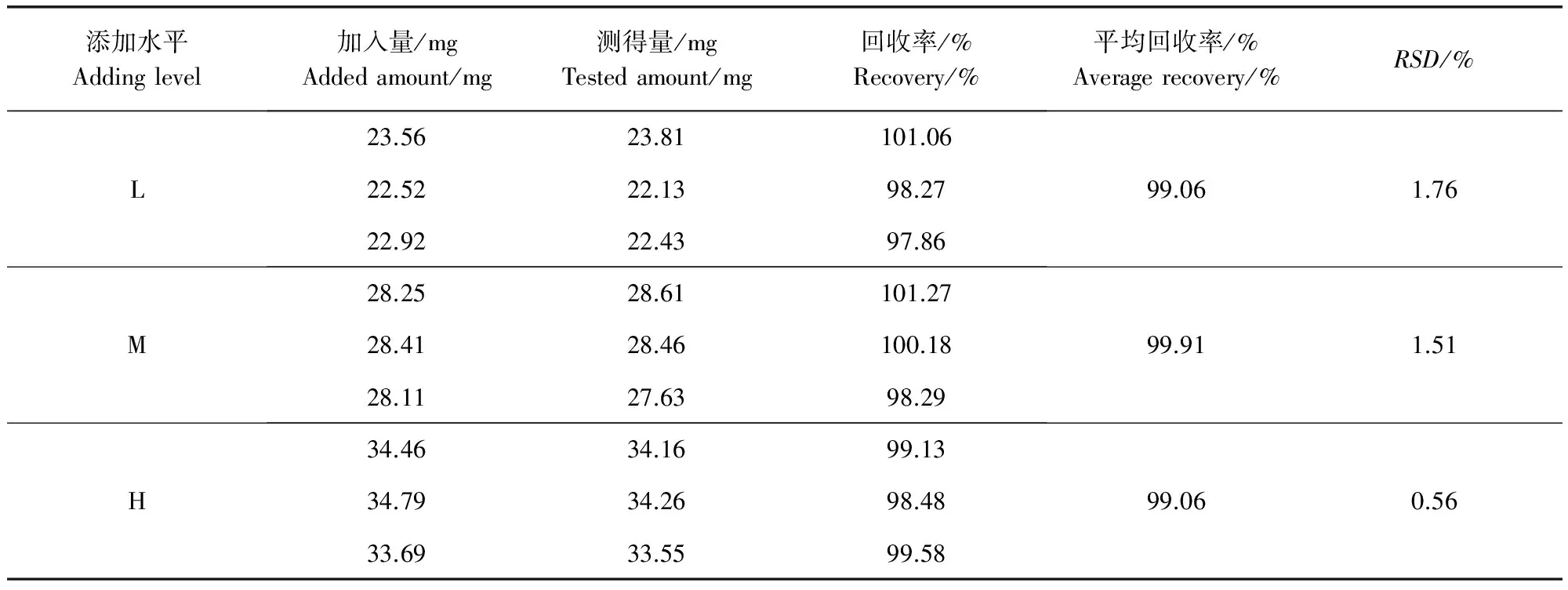
表3 巴比妥回收率试验结果Tab 3 Recovery results of barbital in different adding level
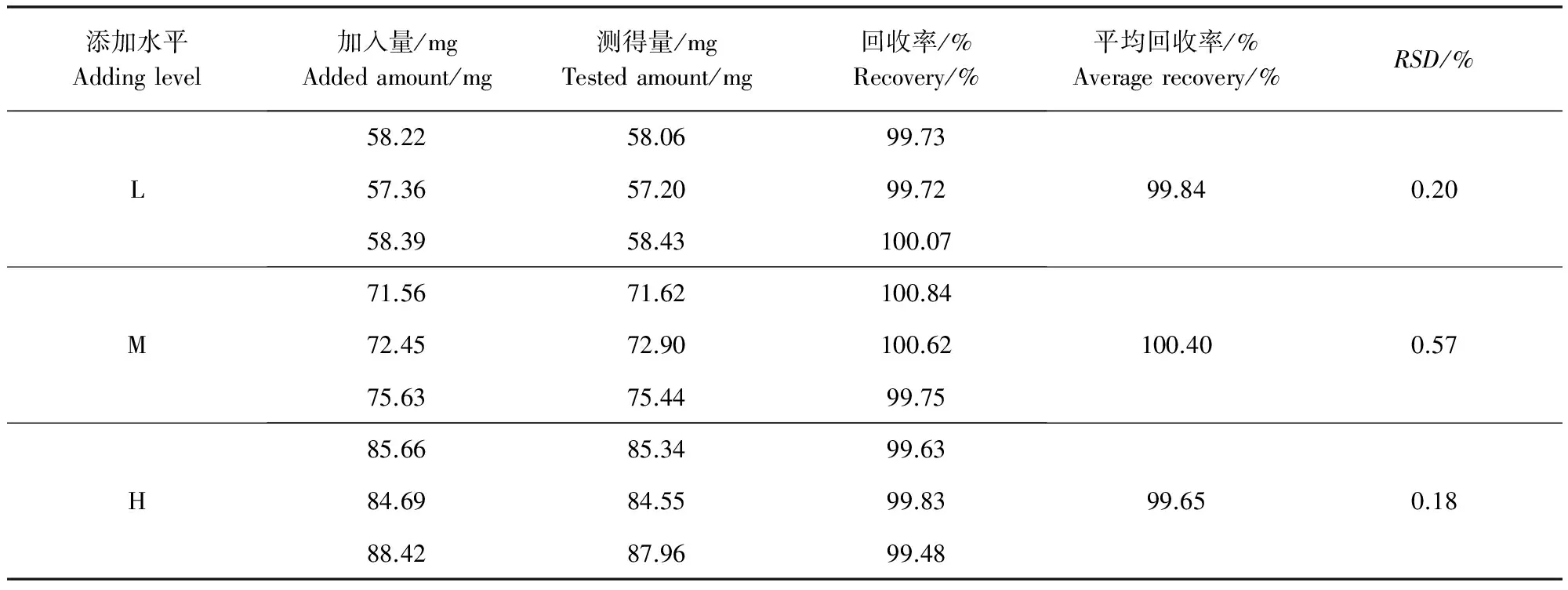
表4 氨基比林回收率试验结果Tab 4 Recovery results of aminophenazone in different adding level
2.6 样品含量的测定 取A、B、C、D四公司生产的复方氨基比林注射液样品,精密量取1.00 mL置100 mL量瓶中,用流动相稀释至刻度,作为供试品溶液,精密吸取10 μL上机测定。另取1 mL含巴比妥280.0 μg和氨基比林715.0 μg的混合标准溶液,作为对照品溶液,同法测定。按外标法以峰面积计算含量,巴比妥结果分别为96.6%、95.0%、94.9%和95.9%;氨基比林结果分别为101.9%、99.8%、96.1%和95.1%。而传统的滴定法对应的巴比妥测量结果分别为102.6%、103.2%、99.1%和95.7%;氨基比林结果分别为99.4%、103.2%、100.0%和98.2%。
3 讨论与小结
3.1 流动相pH值的选择 使用0.05 mol/L磷酸二氢钾溶液和乙腈作为流动相时,巴比妥和氨基比林的色谱峰重合在一起无法分离。当用三乙胺调节pH值到8.0以上时,即可把巴比妥和氨基比林的色谱峰分离开。pH越高,得到的峰形越好,不过,普通的C18柱对pH值的耐受有限,一般应低于8.0,最高不能超过8.5。为避免操作不当损坏柱子,故选择用三乙胺调节pH值为8.2的0.05 mol/L磷酸二氢钾溶液和乙腈作为流动相。
3.2 流动相比例的选择 使用0.05 mol/L磷酸二氢钾溶液(用三乙胺调节pH值到8.2)︰乙腈=73︰27、75︰25及 80︰20的比例运行样品,其中,73︰27的流动相在运行低浓度样品时,巴比妥的色谱峰会受到试剂峰或杂质峰的干扰; 80︰20的流动相运行样品时,氨基比林的色谱峰拖尾较严重,峰形较差;而 75︰25的流动相峰形良好,保留时间适当,故选择使用0.05 mol/L磷酸二氢钾溶液(用三乙胺调节pH值到8.2)︰乙腈=75︰25 作为流动相。
3.3 色谱柱的选择 分别采用粒径5 μm,4.6 mm×250 mm Waters公司的Symmetry C18,Agilent公司的ZORBAX SB-C18、5TC-C18(2),Shimadzu 公司的VP-ODS C18以及粒径3.5 μm,4.6 mm×100 mm的Agilent公司的Eclipse plus C18色谱柱进行试验。结果表明,普通的C18柱在弱碱性条件下均可分离复方氨基比林注射液中的两个组分。同时,由于流动相的pH值较高,为避免碱性物质对色谱柱造成损害,宜使用专用的色谱柱。
3.4 滴定法与液相法对检测结果的影响及原因 复方氨基比林注射液的含量采用传统的滴定方法进行测定时,所得到的巴比妥的结果略有偏高,这与检测员判断滴定是否到达终点有比较密切的关系。当滴定已经到达终点时,滴定经验不够丰富的检测员一般不敢断定为终点,而是要等到混浊比较明显时才会终止滴定,而此时终点已过,故滴定结果一般均会略有偏高。同时,样品中的某些杂质如氯离子等可能也会影响对终点的判定。采用高效液相色谱法进行测量,结果更为准确,因为减少了人为因素带来的终点误差。
3.5 试验方法与文献报道方法的差异 曾有文献报道了人用药品复方氨基比林注射液或复方氨林巴比妥注射液三组份含量测定的高效液相色谱法。但李世彩等[3]所采用的磷酸缓冲液为磷酸二氢钾及磷酸氢二钾混合配制而成,未使用三乙胺调节pH值;而杨锡祥等报道的方法[2]中未给出磷酸盐缓冲液的配制方法,但使用三乙胺调节pH值至8.0,使用的色谱柱长度分别为150 mm和200 mm。许润娟等[4]使用的流动相为乙腈-0.0025 mol/L庚烷磺酸钠-三乙胺(35︰65︰0.05,用50%醋酸调节pH到8.0),色谱柱长度为250 mm,流速为0.6 mL/min,检测波长为220 nm,柱温为30 ℃。试验中使用的是常用的250 mm长的色谱柱,并大胆地把pH值提高到8.2,得到的色谱峰峰形也极为理想。其次,流动相比例与文献报道的也略有差异。虽然240 nm的检测波长并非氨基比林及巴比妥的最佳检测波长,但在该波长下巴比妥的色谱峰峰形尖锐,峰宽较窄,不易受到试剂峰的干扰,故也选择240 nm作为检测波长。
3.6 小结 采用C18柱作为固定相,0.05 mol/L磷酸二氢钾溶液(用三乙胺调节pH值到8.2)∶乙腈=75∶25作为流动相,使用高效液相色谱法测定兽用复方氨基比林注射液的含量,方法专属性强,灵敏度佳,准确度高,能够有效控制兽用复方氨基比林注射液的质量。
[1] 中华人民共和国兽药典委员会. 中华人民共和国兽药典,2015年版一部 [S].北京: 中国农业出版社, 2016: 281-282.
Pharmacopoeia Commission of People's Republic of China. People's Republic of China Veterinary Pharmacopoeia, first edition in 2015[S]. Beijing: Chinese Agricultural Press, 2016: 281-282.
[2] 杨锡祥, 张 影. 高效液相色谱法同时测定复方氨林巴比妥注射液三组份的含量[J]. 安徽医药, 2009, 13(3): 271-273.
Yang X X, Zhang Y. Determination of compound aminopyrine, quinizine, barbitone injection by HPLC[J]. Anhui Medical and Pharmaceutical Journal, 2009, 13(3): 271-273.
[3] 李世彩, 牛景云, 孙 山. 复方氨基比林注射液三组分的HPLC测定[J]. 中国药业, 2000, 9(6): 24-32.
Li S C, Liu J Y, Sun S. Determination of compound aminopyrine, quinizine, barbitone injection by HPLC[J]. China Pharmaceuticals, 2000, 9(6): 24-32.
[4] 许润娟, 魏雪芳. RP-HPLC法测定复方氨林巴比妥注射液三组分的含量[J]. 药物分析杂志, 2005, 25(8):967-969.
Xu R J, Wei X F. Determination of three component in compound anlin barbituo injection[J]. Chinese Journal of Pharmaceutical Analysis, 2005, 25(8):967-969.
[5] 刘红云, 郑 举,张 莉, 等. HPLC法同时测定安痛定注射液中氨基比林和安替比林的含量[J]. 中国兽药杂志, 2009, 43(9): 5-7.
Liu H Y, Zheng J, Zhang L. Simultaneous determination of aminophenazone and phenazone in antondine injection by HPLC[J]. Chinese Journal of Veterinary Drug, 2009, 43(9): 5-7.
[6] 闰小峰, 孙志文. 高效液相色谱法测定安痛定注射液中氨基比林和安替比林的含量[J]. 中国兽药杂志, 2011, 47(2):77-79.
Yuan X F, Sun Z W. Determination of aminophenazone and phenazone in antondine injection by HPLC[J]. Chinese Journal of Veterinary Drug, 2011, 47(2): 77-79.
(编辑:李文平)
SimultaneousDeterminationofTwoComponentsinVeterinaryCompoundAminophenazoneInjectionbyHPLC
CHEN Xi-long, SUN Zhen-zheng, WANG Qing-hong
(GuizhouProvincialSupervisoryInstituteofVeterinaryDrugandFeeds,Guiyang550003,China)
10.11751/ISSN.1002-1280.2017.9.10
2017-03-02
A
1002-1280 (2017) 09-0056-06
S859.79
陈锡龙, 高级兽医师,从事兽药质量检验检测及相关研究工作。E-mail: cxlofyjs@163.com

