纳米钛酸钾生物薄膜在模拟体液中的电化学腐蚀
张超超,陈恒利,赵立臣,戚玉敏,崔春翔
(河北工业大学材料科学与工程学院,天津300130)
纳米钛酸钾生物薄膜在模拟体液中的电化学腐蚀
张超超,陈恒利,赵立臣,戚玉敏,崔春翔
(河北工业大学材料科学与工程学院,天津300130)
以自行设计制备的低模量Ti-25Nb-6Zr-3Mo医用β钛合金为基体材料,采用阳极氧化与水热处理相结合的方法在该合金表面制备出纳米钛酸钾生物薄膜,并通过扫描电子显微镜、表面能谱仪和X射线衍射仪对该生物薄膜进行微结构表征.采用三电极体系,测试了纳米钛酸钾生物薄膜在模拟生理体液中的耐蚀性能.结果表明,纳米钛酸钾生物薄膜在模拟体液中表现出更好的稳定性和耐蚀性,是一种具有很好应用前景的种植体材料.
生物材料;医用β钛合金;纳米钛酸钾生物薄膜;表面改性;电化学腐蚀
与Co-Cr合金和医用不锈钢相比,医用钛及其合金以其良好的耐蚀性和优异的生物相容性、生物力学适应性、综合机械性能成为用于硬组织替换材料的首选金属生物材料[1-2].其临床应用中造成种植体植入失败的原因主要有:钛及钛合金与骨组织的弹性模量间的差距造成的“应力屏蔽”引起的植入失败[1-2];其表面呈生物惰性而无法实现种植体与骨组织间形成骨性结合造成的植入失败[3].因此开发更低弹性模量的医用β钛合金并对其进行表面改性以赋予其生物活性成为材料工作者的研究热点.
HA已经成为公认的生物活性涂层材料[3-6],但其与钛合金基体间的界面结合力弱易造成涂层脱落.因此,人们在改进表面改性技术的同时,也在致力于开发能与钛合金形成强界面结合的生物活性涂层.本课题组多年来在医用钛合金的设计、制备及其表面改性方面做了大量的研究工作[7-9],开发了系列新型低模量医用β钛合金,并采用原位制备技术在钛合金的表面制备了能与其形成良好界面结合的微米级钛酸钾生物活性薄膜,通过生物学试验证明钛酸钾生物薄膜具有非常高的成骨活性.随着纳米技术的发展,对钛合金表面进行纳米化改性来提高其生物活性的研究越来越多.本研究拟采用阳极氧化与水热处理相结合的方法在自行设计的Ti-25Nb-6Zr-3Mo β钛合金表面制备纳米钛酸钾生物薄膜.大量的研究表明,钛及钛合金虽然具有较高的耐蚀性[10-12],但在复杂的人体生理环境中,若将其长期直接植入体内,因腐蚀引起的金属离子溶出不可避免地会造成周围细胞和组织的变性,因此对钛合金进行表面改性的另一个目的是为了进一步提高钛合金种植体的耐蚀性.本文侧重于研究纳米钛酸钾生物薄膜在模拟体液中的电化学腐蚀行为.
1 材料和方法
1.1 纳米钛酸钾生物薄膜的制备
本研究采用自行设计的低弹性模量Ti-25Nb-6Zr-3Mo医用β钛合金作为基体材料,该合金采用5 kg水冷铜坩埚真空感应磁悬浮熔炼炉熔炼而成,铸态的合金棒经轧制退火处理后测得其压缩弹性模量为20 GPa,与人体致密骨的压缩弹性模量(17~18.9 GPa)相当接近,作为种植体材料,其生物力学适应性很好.采用DK77系列电火花数控线切割机床将该合金切割成10 mm×10 mm×1.5 mm的片状试样,样品经系列砂纸打磨,丙酮、无水乙醇、去离子水超声清洗后,于抛光液(n(HF)∶n(HNO3)∶n(H2O)=1∶4∶5)中抛光浸蚀30 s后清洗干燥备用.
采用阳极氧化法与水热处理相结合的方法在抛光后的钛合金表面制备纳米钛酸钾生物薄膜,即将抛光后的钛合金样品为阳极,铂电极为阴极,0.3%(质量分数)HF水溶液为电解液,阳极氧化反应所用电源为WWL-LDX型直流稳压稳流电源,钛合金样品在10~20 V电压下阳极氧化一定时间后,样品取出用去离子水清洗烘干.然后将阳极氧化后的样品放入定量低浓度的KOH溶液中,置于反应釜中在150℃下水热反应12 h,样品经再次去离子水清洗干燥.
1.2 材料的微结构表征
用Hitachi s-4800场发射扫描电镜对样品的表面形貌进行表征,用EDAX能谱仪对样品的表面元素组成进行表征,用Bruker D8 FOCUS多晶X射线衍射仪对样品的相组成进行表征.
1.3 电化学腐蚀试验
采用三电极体系进行电化学测试,试样作为工作电极,饱和甘汞电极为参比电极,碳棒电极为辅助电极,腐蚀介质为人工模拟体液(简称SBF),其配方见表1[13],用1M的HCl溶液和三羟甲基氨基甲烷(简称Tris)来调节该溶液的pH值为7.4,试验温度为37℃.用美国GAMRY电化学工作站测试纳米钛酸钾生物薄膜在模拟体液中电化学腐蚀行为,并计算相应的电化学参数.

表1 配制1 000 mL模拟体液(SBF)所用试剂及其质量[13]Tab.1 Reagents and their mass for preparing 1 000 mL SBF
2 结果与讨论
2.1 纳米钛酸钾生物薄膜的表面微结构表征与分析
图1为抛光后的钛合金及纳米钛酸钾生物薄膜的SEM照片及EDS图谱.可见,钛合金经化学抛光后表面变得光滑,在砂纸上研磨留下的划痕基本消失,如图1a)所示.图1b)是对应于钛合金的表面能谱,可见该合金的元素组成为Ti、Nb、Zr、Mo,其质量分数如表2中数据所示,达到了所设计合金Ti-25Nb-6Zr-3Mo的各元素的质量浓度要求.图1c)是经阳极氧化与水热法联合处理后的钛合金表面形貌,与处理前钛合金表面形貌相比,其表面形成了由相互交错的纳米片构成的薄膜,对应的能谱分析表明,该薄膜除了Ti、Nb、Zr、Mo外,还出现了明显的K元素和O元素的峰,可见,由纳米片状形成的薄膜可能为Ti、K、O组合的化合物,其K/Ti/O的原子比为1∶3.1∶6.8(见表2中数据),与六钛酸钾(其分子式为K2Ti6O13)中的K/Ti/O的原子比接近,由此推知,所获得纳米片状结构的薄膜可能为六钛酸钾生物薄膜,六钛酸钾的化学稳定性强,该生物涂层良好的化学稳定性有望对钛合金起到好的保护作用.
图2为钛合金及纳米钛酸钾生物薄膜的XRD的全谱图和局部放大图.从图2a)中可以看到3个明显的衍射峰,这3个衍射峰为Ti-25Nb-6Zr-3Mo合金基体的衍射峰,通过图谱标定可知,该合金为β型钛合金.由于钛合金基体表面的纳米生物薄膜很薄,其衍射峰强度较弱,对其XRD衍射图谱进行放大后可见除了钛合金基体的三个强衍射峰外,还出现了很多小衍射峰,如图2b所示,通过图谱标定可知,该纳米生物薄膜为K2Ti6O13生物薄膜.K2Ti6O13的化学稳定性强,具有良好的耐酸碱腐蚀的能力.
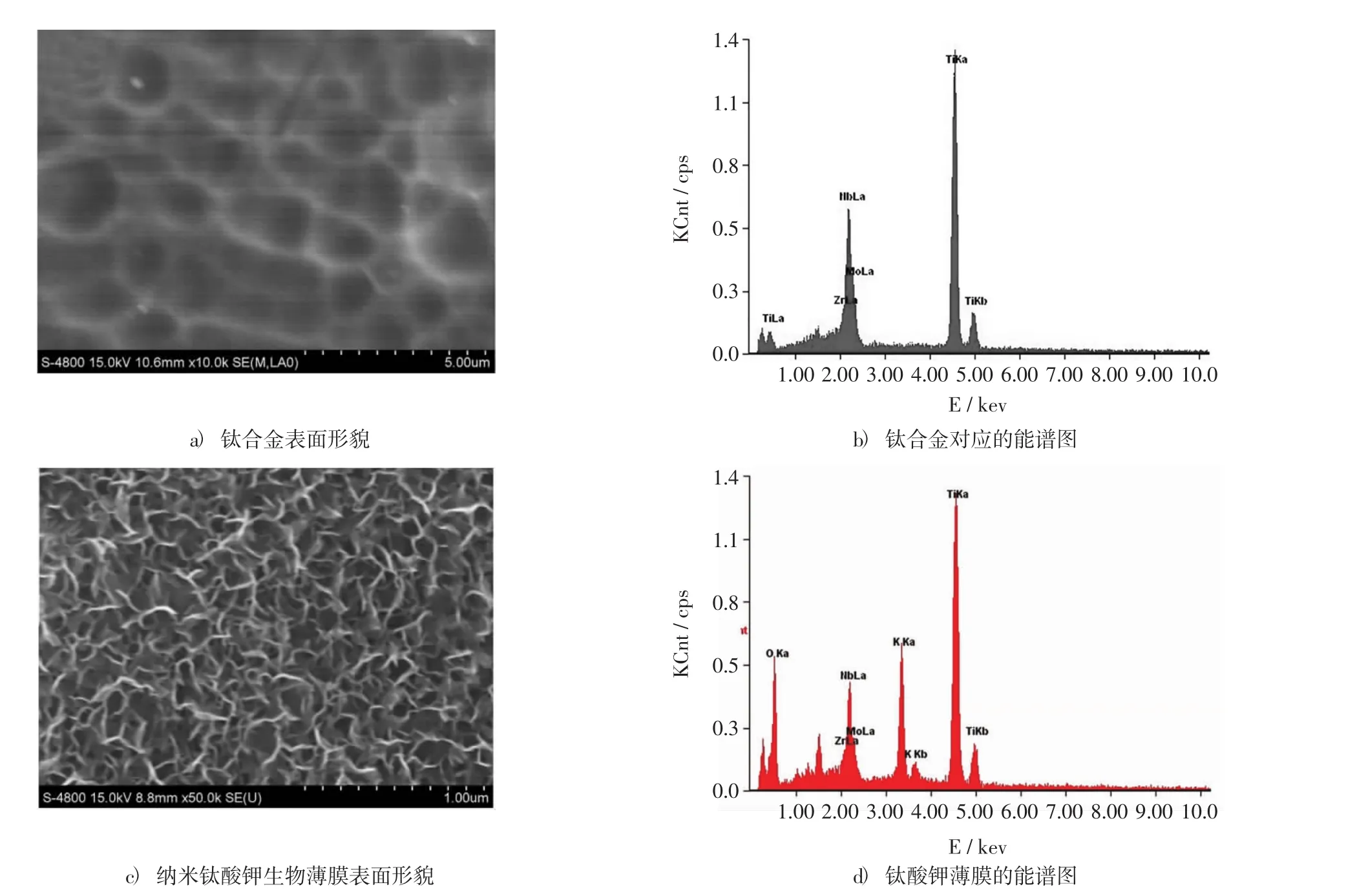
图1 抛光后的钛合金及纳米钛酸钾生物薄膜的SEM照片及其EDS图谱Fig.1 SEM images and EDS spectrums of polished titanium alloy and nano potassium titanate biological film
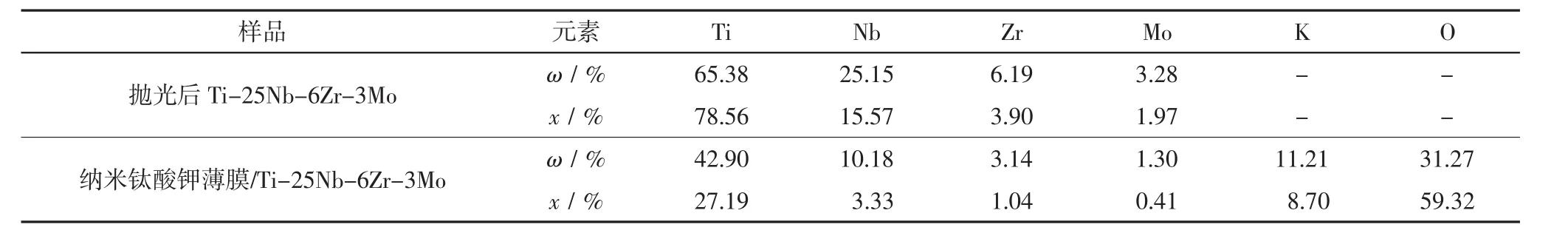
表2 抛光钛合金及纳米钛酸钾生物薄膜表面元素及其质量分数和原子数分数Tab.2 The weight percentage and atomic percentage of the surface elements of polished titanium alloy and nano potassium titanate biological film
2.2 电化学腐蚀
人体的生理环境为37℃、pH值为7.4左右的水溶液,体液中含有溶解的气体、电解液、细胞和蛋白质,种植体长期处于这样的环境中,将会发生电化学腐蚀.腐蚀一方面导致腐蚀产物进入人体,从而引起严重的生理危害,如组织毒化、细胞畸变等.另一方面,会造成植入假体的松脱、早期断裂等失效行为.因此,研究材料的电化学腐蚀行为是评价种植体材料耐蚀性的一项重要试验.
图3为抛光后钛合金及纳米钛酸钾生物薄膜/钛合金在模拟体液中的阳极极化曲线,相应的电化学参数列于表3中.观察极化曲线可见,二者均出现了稳定钝化区,且纳米钛酸钾生物薄膜的维钝电流密度明显小于钛合金的,维钝电流密度用于表征合金表面形成的钝化膜的稳定性,其值越小,钝化膜越稳定,因此该生物薄膜较钛合金表面形成的氧化膜的稳定性好.从表3中数据可见,有纳米钛酸钾生物薄膜的钛合金的自腐蚀电位Ecorr明显高于钛合金的,Ecorr用来表征金属的腐蚀倾向,该值越低,越易发生腐蚀.由此可见,纳米钛酸钾生物薄膜降低了钛合金的腐蚀倾向.从自腐蚀电流密度(Icorr)来看,有纳米钛酸钾生物薄膜的钛合金的Icorr比钛合金的小了两个数量级,Icorr是反映电极腐蚀速度快慢的电化学参数,与腐蚀速度成正比关系,故纳米钛酸钾生物薄膜能大大降低钛合金的腐蚀速度.综合上述分析,与Ti-25Nb-6Zr-3Mo合金相比,纳米钛酸钾生物薄膜在模拟体液中表现出更好的耐蚀性.

图2 钛合金及纳米钛酸钾生物薄膜的XRD的全谱图和局部放大图Fig.2 XRD spectrums and their local magnification of titanium alloy and nano potassium titanate biological film

表3 钛合金和纳米钛酸钾生物薄膜在模拟体液中的自腐蚀电位和自腐蚀电流密度Tab.3 The Ecorr and Icorr of polished titanium alloy and nano potassium titanate biological film in SBF
3 结论
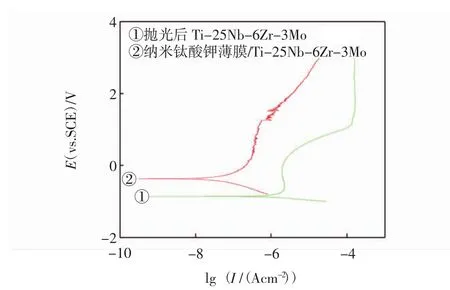
图3 抛光后的钛合金及纳米钛酸钾生物薄膜在模拟体液中的阳极极化曲线Fig.3 Anodic polarization curves for polished titanium alloy and nano potassium titanate biological film in SBF solute
综合上述结果,得出如下结论:
1)以Ti-25Nb-6Zr-3Moβ钛合金为基体,采用阳极氧化与水热处理相结合的方法能在合金表面制备出纳米钛酸钾生物薄膜,该生物薄膜均匀致密,稳定性好.
2)电化学腐蚀试验表明,与Ti-25Nb-6Zr-3Mo相比,纳米钛酸钾生物薄膜/Ti-25Nb-6Zr-3Mo生物材料作为种植体材料在模拟体液中表现出更好的耐蚀性能.
[1]李兆峰,黄伟九,刘明.人体用金属植入材料的研究进展[J].重庆工学院学报,2006,20(5):42-46.
[2]戚玉敏,崔春翔,申玉田,等.生物医用β-钛合金[J].河北工业大学学报,2003,33(6):7~12
[3]Ma J,Wang C,Peng K M.Electrophoretic deposition of porous hydroxyapatite scaffold[J].Biomaterials,2003,24:3505-3510.
[4]Layrolle P,Van der Valk,Dalmeijer R,et al.Biomimetic calcium phosphate coatings and their biological performances[J].Key Engineering Material,2001,192-195(22-26):391-394.
[5]Milella E,Cosentino F,Licciulli A,et al.Preparation and characterization of titania/hydroxyapatite composite coatings obtained by sol-gel process[J]. Biomaterials,2001,22:1425-1431.
[6]Xiang Lia,Tao Chena,Jing Hua,et al.Modified surface morphology of a novel Ti-24Nb-4Zr-7.9Sn titanium alloy via anodic oxidation for enhancedinterfacial biocompatibility and osseointegration[J].Colloids and Surfaces B:Biointerfaces,2016,144(1):265-275.
[7]QI Yumin,HE Yun,CUI Chunxiang,et al.Fabrication and biocompatibility in vitro of potassium titanate biological thin film/titanium alloy biological composite[J].Front Mater Sci China,2007,1(3):252-257.
[8]Cui C X,Qi Y M,Zhang M F,et al.Histological and Mechanical Evaluation of the in vivo Bone-bonding Ability on the K2TinO2n+1/β-Ti Alloy as a Novel Bioactive Material[J].Materials Research Society Symposium Proceedings,2009,1187:175-184.
[9]戚玉敏.原位生成钛酸钾/钛合金梯度生物材料的制备及生物学评价[D].天津:河北工业大学,2008.
[10]Vlaudia Fleck,Dietmar Eifler.Corrosion,fatigue and corrosion fatigue behavior of metal implant materials,especially titanium alloys[J].Inernational Journal of Fatigue,2010,32:929-935.
[11]Atapour M,Pilchak A L,Frankel G S,et al.Corrosion behavior of β titanium alloys for biomedical applications[J].Materials Science and Engineering C,2011,31:885-891.
[12]Kim Ji-Woo,Hwang Moon-Jin,Han Mi-Kyung,et al.Effect of manganese on the microstructure,mechanical properties and corrosion behavior of titanium alloys[J].Materials Chemistry and Physics,2016,180:341-348.
[13]Tadashi Kokubo,Hiroaki Takadama.How useful is SBF in predicting in vivo bone bioactivity[J].Biomaterials,2006,27:2907-2915.
[责任编辑 田丰]
Electrochemical corrosion of nano potassium titanate biological film in simulated body fluid
ZHANG Chaochao,CHEN Hengli,ZHAO Lichen,QI Yumin,CUI Chunxiang
(School of Materials Science and Engineering,Hebei University of Technology,Tianjin 300130,China)
The new low elastic modulus Ti-25Nb-6Zr-3Mo β Titanium alloy was designed and prepared by ourselves for biomedical application.Nano potassium titanate biological film was formed in situ on the surface of the alloy by the combination method of anodic oxidation and hydro-thermal treatment.Microstructure characteristics of titanium alloy specimens with nano potassium titanate were studied by a field emission scanning electron microscopy(FE-SEM)equipped with an energy dispersive X-ray spectrometer(EDS)and X ray diffractometer(XRD),in order to confirm the composition of the film.The three-electrode system was adopted to test the corrosion resistance of nano potassium titanate biological film in simulated body fluid(SBF)(by contrast with the Titanium alloy).The results haveindicated that nano potassium titanate biological film/Ti-25Nb-6Zr-3Mo showed excellent stability and corrosion-resistant.The material is a better prospect for application asimplant material.
biomaterial;biomedical β Titanium alloy;nano potassium titanate biological film;surface modification; electrochemical corrosion
TB321
A
1007-2373(2017)04-0053-05
10.14081/j.cnki.hgdxb.2017.04.009
2017-03-14
河北省应用基础研究重点项目(11965151D)
张超超(1991-),男,硕士研究生.通讯作者:戚玉敏(1973-),女,副研究员,ymqi@hebut.edu.cn.

