制备高纯超细氧化铝粉体新方法
聂玉娟,王二东,王许云
制备高纯超细氧化铝粉体新方法
聂玉娟1,王二东2,王许云1
(1青岛科技大学化工学院,山东青岛 266042;2中国科学院大连化学物理研究所,辽宁大连116023)
以99.99% 高纯铝板为阳极原料,采用电化学方法制备氧化铝前体氢氧化铝,讨论分析了氢氧化铝的焙烧温度、保温时间对制备高纯超细氧化铝的影响,考察了不同电流密度放电对氧化铝形貌和粒度的影响。结果表明:在70 mA·cm-2的较高电流密度下铝/空气电池放电过程可得到平均粒度为268 nm的氢氧化铝;制备的氢氧化铝经洗涤,在1400℃焙烧,保温3 h,可得到平均粒度为200 nm,形貌为近似球状的99.99% 的超细氧化铝粉体;而低电流密度所得氧化铝颗粒团聚严重。主要原因是高电流密度使放电过程中产生的氢氧化铝晶体的介稳区宽度变窄所致。
电化学;氢氧化铝;高纯超细氧化铝;铝/空气电池;粉体
引 言
高纯超细氧化铝在硬度、强度、亮度、隔电性、耐磨损性、耐高温和耐腐蚀性等方面展现出的卓越性能,被广泛应用于化工、电子、冶金、航天以及医学等领域[1-3]。目前,高纯超细氧化铝的应用大致可分为3个层次:低端市场、中端市场和高端市场。低端市场氧化铝主要应用在集成电路、荧光粉、消费电子等领域,而中高端市场主要包括蓝宝石衬底、电池隔膜等高新技术领域,其对氧化铝的纯度、粒径、形貌、产品稳定性等要求较高。根据国内外相关文献资料和已公开的专利报道,目前国内生产高纯氧化铝与国际水平还有一定差距,一些高端产品需要进口[4-7]。
氧化铝的制备方法众多,主要包括化学法、水解法、溶胶-凝胶法、沉淀法、分解法等十余种方法[8-18],由此衍生出来的改良拜耳法、醇盐水解法、水热法能较好地生产出高纯度的氧化铝[19-24]。其中,醇盐水解法和水热法被认为是目前生产高纯氧化铝的最佳方法。但因其工艺复杂,成本高或者生产过程存在安全隐患而难以实现商业化。因而,如何简化高纯超细氧化铝的生产工艺,降低生产成本,并实现成熟工业化一直是研究人员广泛关注的问题。
近年来,不少研究人员将注意力转向使用电化学方法来生成不同金属氧化物纳米颗粒,主要采用金属阳极溶解的方式。目前,通过该方法已成功制备出纳米级氧化锌、氧化镁以及金属钴复合物[25-27]。后来,Starowicz等[28]通过电解液中金属铝阳极溶解的方式制备出了铝基氧化物纳米颗粒。但该团队仅对整个电化学过程产生的铝基氧化物纳米颗粒进行了研究,并未进一步探索生成的纳米颗粒是否具备转化为纳米级高纯氧化铝的可能性。
本文提出利用不同电流密度下铝/空气电池放电来生产高纯超细氧化铝的方法。使用高纯铝做阳极,在制备出氢氧化铝前体后,通过焙烧获得了高纯超细氧化铝,并对产物进行了一系列的表征分析。本方法将有望制备出适合市场应用的高纯超细氧化铝,降低电池使用成本。
1 实验材料和方法
1.1 材料
氢氧化钠,由上海阿拉丁生化科技股份有限公司提供,电子级,纯度为99.99%,实验所用电解液均为氢氧化钠溶于超纯水制成,浓度为4 mol·L-1。99.99%高纯铝板,由北京环球金鼎科技有限公司提供,切割成30 mm×30 mm×3 mm的尺寸用作电池阳极。表1为所用高纯铝的化学组成。焙烧所用料舟为纯度99.9%氧化铝料舟。实验室用水为超纯水(UP)。

表1 高纯铝化学组成
1.2 分析测试仪器
X射线粉末衍射仪,X'pert Pro型,荷兰PANalytical B.V.; SEM, JSM-7800F型,日本电子株式会社;Zetasizer 激光粒度分析仪,Zetasizer Nano型,英国Malvern公司;电感耦合等离子体发射光谱仪ICP-OES,PerkinElmer ICP-OES 7300DV型,PerkinElmer。
1.3 氢氧化铝前体的制备与后处理
氢氧化铝前体由铝/空气电池放电过程产生。铝/ 空气电池由1片铝阳极和两侧各1片阴极平行放置构成。使用蓝电电池测试系统(武汉市蓝电电子有限公司提供)将铝/空气电池分别在20、50和70 mA·cm-2的放电电流密度下进行放电,截止电压均为0.6 V。将放电结束后电解液中的沉淀产物依次进行如下处理:使用循环水式多用真空泵对含沉淀电解液进行多次洗涤,抽滤得饼状产物;在真空干燥箱中80℃条件下干燥24 h;将干燥后粉饼进行研磨,备用。
2 实验结果与讨论
2.1 前体氢氧化铝分析
图1给出的是前体氢氧化铝的XRD谱图和多次测量的粒度分析图。从XRD结果可知:前体氢氧化铝晶型主要为Gibbsite型,对应的PDF卡片号为33-0018,另外还存在极少部分的Bayerite型。粒度分析结果则显示,氢氧化铝颗粒尺寸在200~600nm之间,且颗粒尺寸分布均匀性较差,平均粒度为268 nm。
2.2 焙烧条件选择
2.2.1 焙烧温度对氧化铝的影响 70 mA·cm-2放电,不同焙烧温度下(保温时间均为2 h)所得晶体的XRD谱图结果见图2。由图可知,不同焙烧温度下均得到了氧化铝,但氧化铝的晶型不尽相同。1000℃条件下得到的是δ-Al2O3,θ-Al2O3和χ-Al2O3,其对应的PDF卡片号分别为46-1131,23-1009和13-0373,但以δ-Al2O3晶型为主,占晶格比例的92.8%。此温度下XRD谱线宽化明显,推测生成的产物颗粒细小;1200℃下得到的是θ-Al2O3,κ-Al2O3和a-Al2O3,对应PDF卡片号分别为23-1009, 04-0878和10-0173,以θ-Al2O3晶型为主(三强峰对应的2分别为31.597°,32.848°和67.481°)。而1400℃下只存在a-Al2O3(PDF卡片号为10-0173),该种晶型的氧化铝为高端市场所需的氧化铝,且近几年其在二次电池领域的应用已经引起了广泛关注与研究[29-30]。结果表明,随焙烧温度升高,氧化铝晶型趋向于单一化。峰强度和尖锐程度随温度升高增加明显,推知高温下晶体结晶度明显改善,晶体由颗粒细小的多晶向形貌规则的单晶转化。即随焙烧温度升高,晶型主要发生了从δ-Al2O3到θ-Al2O3再到a-Al2O3的相转化。
由数据分析知1400℃时产物已完全转化为a-Al2O3,因此确定1400℃为本实验条件下适宜的焙烧温度。
2.2.2 保温时间对氧化铝的影响 已知1400℃时产物已完全转化为a-Al2O3,此时结晶度良好。为更好地探讨保温时间对氧化铝表观形貌的影响,根据XRD结果选择产物焙烧温度为1200℃,电流密度仍选择70 mA·cm-2。该条件下在不同保温时间所得到的氧化铝SEM图和平均粒度分布图如图3所示。从图中可以看出,相比氢氧化铝,氧化铝的颗粒尺寸增加明显,这主要是高温和长保温时间导致的颗粒团聚所引起的。由图3(a)~(c) 可知,随着保温时间延长,氧化铝结晶度逐渐升高,结晶形貌由细小颗粒逐渐向板状、块状转变,最终有转变为蠕虫状的趋势。在由板状或块状向蠕虫状形貌转变过程中,晶体尺寸逐渐减小。该形貌与XRD结果表现出良好的一致性。由图3(d) 可知,随保温时间延长,颗粒平均粒度分布逐渐增加,尺寸分布均匀性明显变差,该结果看似与SEM结果不符,但实际上由于保温3 h时颗粒蠕虫状尺寸虽然减小,由于团聚作用并未实现相互分离,所以表观尺寸仍然是增大的。
2.3 电流密度对氧化铝的影响
为进一步确定电流密度对最终产物氧化铝表观形貌的影响,在控制焙烧温度为1400℃、保温时间为3 h的条件下,考察了放电电流密度分别为20,50和70 mA·cm-2下,铝/空气电池放电产物通过焙烧所得最终产物氧化铝的表观形貌和平均粒度分布,如图4所示。从图4(a)~(c) 可以看出,低电流密度条件下焙烧产生的氧化铝颗粒间团聚现象显著,颗粒尺寸较大,均匀性差,为明显的蠕虫状;随电流密度升高,所得焙烧产物逐渐向近球状颗粒转变,近球状颗粒尺寸逐渐减小且相对均匀。尤其是在70 mA·cm-2条件下,平均粒度可减小到200 nm,但颗粒内部的蠕虫状趋势仍存在。该结果和图4(e)平均粒度结果表现出很好的一致性。由此可知:相同焙烧条件下,较高电流密度一定程度上有利于细化氧化铝颗粒。
将放电电流密度为70 mA·cm-2焙烧所得氧化铝[图4(c)]和商品氧化铝[图4(d)]比较,本实验所得氧化铝形貌和商品氧化铝具有很好的可比性。但氧化铝颗粒均匀性和商品氧化铝(99.9%,30 nm)相比还存在一定差距,需进一步改善和提升。
2.4 电流密度对产物影响的机理分析
金属铝溶于强碱(以NaOH为例)生成氧化铝的化学反应方程式如下
2Al + 6H2O + 2NaOH2NaAl(OH)4+ 3H2(1)
NaAl(OH)4MIAl(OH)3+ NaOH (2)
式(1)的驱动力为化学驱动,即主要为化学势差以及浓度差。然而,通过铝/空气电池放电生成氢氧化铝,在电池放电过程中虽然总反应也为式(1),但主要的驱动力为电化学驱动。在恒电流放电条件下,可以恒定的速率源源不断地产生Al(Ⅲ),从而避免了传统方法中陈化时间对氢氧化铝沉淀产生的影响,大大减少了生成氢氧化铝的时间,简化了生产工艺和成本。结晶过程如式(2)所示,其中MI为介稳态中间体。电池放电过程金属阳极的电化学反应方程式如式(3)
AlAl3++3e-(3)
Al3+产生的速率可依据式(4)计算(排除析氢腐蚀的影响)
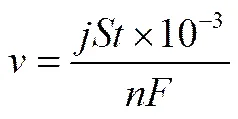
铝/空气电池放电过程中不同电流密度下生成的氢氧化铝形貌如图5所示。从图中可以看出:小电流密度下生成的氢氧化铝颗粒粒度相对较大,且均匀性较差;大电流密度下生成的颗粒则较小,尺寸较均匀,但团聚现象显著。从图1已知,氢氧化铝主要为Gibbsite型。Gibbsite型的生长基元的形成能低,在Al-H2O反应中成核速率快,而其溶解度在较低温度下相对Bayerite型更低,所以可认为其在溶液中更容易生成[31]。无论是在高电流密度还是低电流密度条件下,推测化学反应均会导致溶液系统迅速达到局部过饱和状态,促使介稳区宽度(MSZW)[32-33]减小,使Bayerite晶体成核受到抑制,促进Gibbsite晶体在介稳态环境中迅速生长,从而使最终沉淀主要为Gibbsite型。由式(4)可知,电化学条件下Al(Ⅲ)的产生不受其在溶液中溶解度的限制,根据MSZW理论可知,晶体成核和生长机理在MSZW中是决定性因素。较高电流密度条件下Al(Ⅲ)产生迅速,晶体生成过程为成核控制,随着晶核不断形成,晶体生长会受到抑制,使最终晶体尺寸较小。而低电流密度下晶体生成过程主要为扩散控制,晶体有足够的空间稳定生长,所以其颗粒尺寸较大,且分散性更好。可认为高电流密度下介稳区宽度相比低电流密度下更窄,是Gibbsite型氢氧化铝迅速产生,且颗粒细小的重要原因。
图5 不同电流密度下产生的氢氧化铝的SEM图
Fig.5 SEM images of aluminum hydroxide under different current densities
2.5 氧化铝粉末纯度分析
对70 mA·cm-2的放电电流密度下通过焙烧得到的氧化铝进行了纯度分析,结果如表2所示。其中S3对应的为样品经过比S1、S2更多次洗涤和使用非玻璃仪器后所测的纯度。由表可知,最终氧化铝的纯度超过了99.9%,主要杂质元素是Na和Si。Na+主要来源于电解液中的NaOH,是氧化铝洗涤不充分所致;而含Si杂质可能来源于周围环境中的灰尘以及实验过程所使用的玻璃仪器。通过进一步改善实验环境,Si和Na的来源可得到有效控制,氧化铝的纯度可达到99.99%以上。

表2 氧化铝纯度分析
3 结 论
(1)采用电化学途径生产高纯超细氧化铝粉末。通过铝/空气电池放电过程制备氧化铝前体氢氧化铝,并通过改变放电过程中电流密度大小来调控Al(Ⅲ)产生的速率,从而影响电解液中氢氧化铝晶核的形成和晶体的生长。通过调控焙烧温度和保温时间来控制产生的氧化铝颗粒的粒度和表观形貌。结果表明:当放电电流密度为70 mA·cm-2,1400℃焙烧,保温3 h可制备出平均粒度为200 nm,纯度高达99.99% 的类球状超细氧化铝粉末。
(2)所制备的氢氧化铝的颗粒尺寸与放电电流密度具有较大的相关性。低电流密度下颗粒尺寸较大,形貌良好。高电流密度下颗粒细小且无固定形貌。通过引入晶体介稳区宽度理论,分析认为随电流密度增加,晶体生长介稳区宽度逐渐变窄,使颗粒尺寸细化,最终得到粒径较小的氧化铝。
符 号 说 明

F——Faraday常数,C·mol-1 j——放电电流密度,mA·cm-2 n——铝阳极失电子数 S——铝阳极有效放电面积,cm2 t——放电时间,s v——Al3+生成速率,mol·s-1
References
[1] 韩东战, 尹中林, 王建立. 高纯氧化铝制备技术及应用研究进展[J]. 无机盐工业, 2012, 44(9): 8-11.HAN D Z, YIN Z L, WANG J L.Research progress in preparation and application of high purity alumina[J]. Inorganic Chemicals Industry, 2012, 44(9): 8-11.
[2] GOLESTANI-FARD F, MAZAHERI M, AMINZARE M,. Microstructural evolution of a commercial ultrafine alumina powder densified by different methods[J]. Journal of the European Ceramic Society, 2011, 31(14): 2593-2599.
[3] DU M X, CHEN K L, XIONG Y G. Advances in high-purity alumina and resource distribution[J]. Advanced Materials Research, 2014, 926/930: 36-39.
[4] FU X F, XU B J, HUANG C J. Preparation of high purity alumina technology overview[J]. Advanced Materials Research, 2013, 734/737: 2496-2500.
[5] MAHRABI K, KHODABAKHSHI F, ZAREH E,. Effect of alumina nanoparticles on the microstructure and mechanical durability of meltspun lead-free solders based on tin alloys[J]. Journal of Alloys and Compounds, 2016, 688: 143-155.
[6] QIAN M, SUN Y, XU X,. 2D-alumina platelets enhance mechanical and abrasion properties of PA612interfacial hydrogen-bond interactions[J]. Chemical Engineering Journal, 2017, 308: 760-771.
[7] HOSSAIN A M S, BALBIN A, ERAMI R S,. Synthesis and study of the catalytic applications in C—C coupling reactions of hybrid nanosystems based on alumina and palladium nanoparticles[J]. Inorganica Chimica Acta, 2017, 455(2): 645-652.
[8] 李继光, 孙旭东, 王亚蓉, 等. α-Al2O3纳米粉的烧结初期机理研究[J]. 硅酸盐学报, 1998, 26(4): 471-475. LI J G, SUN X D, WANG Y R,.Sintering mechanism of α-Al2O3nano-crystalline powder in initial stage[J].Journal of the Chinese Ceramic Society, 1998, 26(4): 471-475.
[9] 吴义权, 张玉峰, 黄校先, 等. 低温制备α-Al2O3粉体[J]. 无机材料学报, 2001, 16(2): 349-352. WU Y Q, ZHANG Y F, HUANG X X,. Preparation of nano-sized alumina powders at low temperatures[J]. Journal of Inorganic Materials, 2001, 16(2): 349-352.
[10] 邹力. 无机盐前驱体复合陶瓷膜制备及表征[D]. 西安: 西安工程大学, 2013. ZOU L. Preparation and characterization of composite ceramic membranes with inorganic precursors abstract[D]. Xi’an: Xi’an Polytechnic University, 2013.
[11] 龚茂初, 林之恩, 袁书华, 等. 成胶条件对耐高温高表面积氧化铝热稳定性的影响[J]. 催化学报, 2001, 22(6): 520-522. GONG M C, LIN Z E, YUAN S H,. Effects of colloid forming conditions on thermal stability of high-temperature-resistant alumina with high surface area[J]. Chinese Journal of Catalysis, 2001, 22(6): 520-522.
[12] 王雅娟, 李春喜, 王子镐, 等. 超声波-化学沉淀法制备纳米氧化铝粒子[J]. 北京化工大学学报(自然科学版), 2002, 29(4): 8-13. WANG Y J, LI C X, WANG Z H,.Preparation of alumina nanometer particles by an ultrasonic precipitation method[J]. Journal of Beijing University of Chemical Technology (Natural Science Edition), 2002, 29(4): 8-13.
[13] 张豪, 林闯, 张爱生, 等. 有机铝水解制备亚微米高纯氧化铝[J]. 科学中国人, 2013, (6): 75-77. ZHANG H, LIN C, ZHANG A S,.Infenor micron high-purity alumina prepared by hydrolysis of organic aluminium[J].Scientific Chinese, 2013, (6): 75-77.
[14] KASHCHEEV I D, ZEMLYANOI K G, DORONIN A V,. New possibilities for an acid method of preparing aluminum oxide 1[J]. Refractories and Industrial Ceramics, 2014, 55(2): 87-92.
[15] ZHANG X. Preparation of alumina powders through pyrocatechol, resorcinol mediated sol-gel method[J]. Materials Science Forum, 2016, 850: 742-747.
[16] KONG J, CHAO B, WANG T,. Preparation of ultrafine spherical AlOOH and Al2O3powders by aqueous precipitation method with mixed surfactants[J]. Powder Technology, 2012, 229(6): 7-16.
[17] WANG L Y, ZHANG N. Synthesizing process of prepared ultrafine alumina powder by ammonia precipitation method[J]. Advanced Materials Research, 2014, 1079/1080: 62-65.
[18] ZHAO Y T, TAO R, ZHOU D F,. Regulatory process for preparing an all-micron ultra-high purity alumina powder method: 103787395A[P].2015-09-02.
[19] FANELLI A J, BURLEW J V. Preparation of fine alumina powder in alcohol[J]. Journal of the American Ceramic Society, 2010, 69(8): C-174-C-175.
[20] OGIHARA T, OGATA N, FUJITA K,. Continuous synthesis of monodispersed alumina particles by the hydrolysis of metal alkoxide using taylor vortex[J]. Powder & Particle, 2010, 20: 231-237.
[21] 于严淏. 异丙醇铝水解制备高纯氧化铝及水合氧化铝[D].大连: 大连理工大学, 2014. YU Y H. Synthesis of high-purity alumina and aluminium hydroxide from aluminium isopropoxide[D]. Dalian: Dalian University of Technology, 2014.
[22] ROUSSEAUX J M, PIGNOL G, MAGNAN Y. Bayer process for production of alumina trihydrate, the said improvement relating to separation of aluminate liquor and insoluble residues: US7807119[P]. 2010-05-10.
[23] TAKATORI K, KADOURA H, MATSUO H,. Microstructural evolution of high purity alumina ceramics prepared by a templated grain growth method[J]. Journal of the Ceramic Society of Japan, 2016, 124(4): 432-441.
[24] VLASKIN M S, GRIGORENKO A V, ZHUK A Z,. Synthesis of high-purity α-Al2O3from boehmite obtained by hydrothermal oxidation of aluminum[J]. High Temperature, 2016, 54(3): 322- 329.
[25] STYPULA B, BANAS J, STAROWICZ M,. Production of nanoparticles of copper compounds by anodic dissolution of copper in organic solvents[J]. Journal of Applied Electrochemistry, 2006, 36(12): 1407-1414.
[26] STAROWICZ M, STAROWICZ P, ZUKROWSKI J,. Electrochemical synthesis of magnetic iron oxide nanoparticles with controlled size[J]. Journal of Nanoparticle Research, 2011, 13(12): 7167-7176.
[27] STYPULA B, STAROWICZ M, HAJOS M,. Electrochemical synthesis of ZnO nanoparticles during anodic dissolution of zinc in alcohols solvents[J]. Archives of Metallurgy and Materials, 2011, 56(2): 286-292.
[28] STAROWICZ M, STAROWICZ P, STYPULA B. Alumina-based nanoparticles obtained by anodic dissolution of Al in electrolytes with alcohol solvents[J]. Journal of Solid State Electrochemistry, 2014, 18(11): 3065-3071.
[29] FAN X, LIU G, LIU J. Preparation of high-purity ultra-fine alumina used for lithium battery ceramic diaphragm coating, involves preparing slurry using alpha-alumina powder spray drying, and jet milling: 105347778-A[P]. 2016-02-24.
[30] CHUNG H S, JUN T Y. Manufacture of high-purity alumina used for.. secondary battery, involves dissolving aluminum hydroxide in supersaturated sodium hydroxide, preparing mother liquor, filtering, precipitating, separating, heating, and calcining: KR2016076832-A[P]. 2016-07-01.
[31] DEMICHELIS R, CIVALLERI B, NOEL Y,. Structure and stability of aluminium trihydroxides bayerite and gibbsite: a quantum mechanical, study with the Crystal 06 code[J]. Chemical Physics Letters, 2008, 465(4/5/6): 220-225.
[32] WANG H, WANG Z, LIU L,. Alumina hydrate polymorphism control in Al-water reaction crystallization by seeding to change MSZW[J].Crystal Growth & Design, 2016, 16(2): 1056-1062.
[33] WANG H, WANG Z, GUO J,. Boehmite preparationalditols-interacting transformation of metastable intermediates in Al-H2O reaction crystallization[J]. Crystal Growth & Design, 2017, 17(1): 183-190.
New approach to prepare high purity and superfine alumina powder
NIE Yujuan1, WANG Erdong2, WANG Xuyun1
(1College of Chemical Engineering, Qingdao University of Science and Technology, Qingdao 266042, Shandong, China;2Division of Fuel Cell & Battery, Dalian National Laboratory for Clean Energy, Dalian Institute of Chemical Physics, Chinese Academy of Sciences, Dalian 116023, Liaoning, China)
99.99% high-purity aluminum is introduced as anode material to obtain aluminum hydroxide, the precursor of alumina, by an electrochemical method. The influence of calcination temperature and holding time on preparing high purity and superfine alumina is discussed. And effects on morphology and size of alumina at different current densities are studied. Experimental results show that the average size of 268 nm aluminum hydroxide can be obtained at 70 mA·cm-2, a relative high current density in aluminum/air batteries. After washing aluminum hydroxide and roasting at 1400℃, holding3 h, the average size of 200 nm and near-spherical alumina powder is received. However, alumina particles agglomerate seriously at low current densities, which is mainly caused by narrowing of metastable zone width at high current densities.
electrochemical method; aluminum hydroxide; high purity and superfine alumina; aluminum/air batteries; powder
10.11949/j.issn.0438-1157.20170176
TQ 133.1
A
0438—1157(2017)09—3616—07
2017-02-22收到初稿,2017-05-15收到修改稿。
王许云,王二东。
聂玉娟(1990—),女,硕士研究生。
中国科学院科技服务网络计划项目;中国科学院青年创新促进会优秀会员项目。
2017-02-22.
Prof. WANG Xuyun, wangxy@qust.edu.cn; Prof. WANG Erdong, edwang@dicp.ac.cn
supported by the Science and Technology Service Network Initiative of Chinese Academy of Sciences and the Outstanding Member Project of Youth Innovation Promotion Association, Chinese Academy of Sciences.

