基于离子液体的“可设计性”和“软酸”性质萃取分离电镀污泥中Cr6+/Fe3+
魏君怡,李勇,薛向欣
基于离子液体的“可设计性”和“软酸”性质萃取分离电镀污泥中Cr6+/Fe3+
魏君怡,李勇,薛向欣
(东北大学冶金学院,辽宁沈阳 110819)
基于离子液体的“可设计性”和“软酸”性质对于其在电镀污泥酸浸液中铬铁萃取分离方面的应用及其机理进行研究。结果表明:咪唑环上烷基链的长度对于铬铁萃取分离效果有较大的影响,阴离子为[BF4]-的离子液体对于铬铁萃取分离能力大于阴离子为[PF6]-的离子液体。在所研究的离子液体中,[Omim][BF4]对于铬铁具有较好的萃取分离效果,实现了电镀污泥中铬铁分离。结合斜率法、红外光谱分析、Raman光谱分析,[Omim][BF4]萃取铬符合离子缔合机理,可推测[Omim][BF4]咪唑阳离子与Cr2O72-阴离子形成离子缔合物而进入有机相,达到萃取分离,从而实现电镀污泥资源化目的,具有一定的应用性。
离子液体;萃取分离;可设计性;软硬酸碱理论
引 言
电镀污泥是电镀企业处理废水产生的固体废物[1],我国每年产量达到1000万吨。由于其中含有铬、铜、铁、锌等多种重金属元素,其中尤以Cr6+含量较高,会对土壤、大气、水体等产生严重的污染从而威胁人体健康。但同时电镀污泥中的铬又是重要的战略资源,我国每年缺口很大,需要大量进口铬资源来弥补。因此,对电镀污泥进行资源化利用研究,具有解决环境污染和资源循环的双重意义[2-5]。
由于电镀污泥中铬铁元素通常共伴生存在,二者性质相差很小,难于分离,因此铬/铁共存就成为了制约电镀污泥中铬元素资源化利用的“瓶颈”[6]。目前,国内外对电镀污泥进行了广泛的无害化和资源化研究,多数是将电镀污泥进行酸浸[7],然后再进行不同处理过程。胡国荣等[8]、Wu等[9]分别采用针铁矿法以及莫尔盐结晶法分离铬与铁,虽然实验结果较为理想,但工艺复杂,且无法避免二次污染问题,致使该方法基本上无实用价值。虽然“酸浸法”[10]和“氨浸-催化水解”工艺[11]具有金属浸出效率高、生产成本低的优点,但存在浸出选择性差和铁渣难处理的不足。Silva等[12]将Cr3+氧化成Cr6+,利用碱性体系中Cr6+与Fe3+溶解度差异达到分离目的,但是该方法无法回避Cr6+毒性的问题。Bewtra等[13]利用细菌吸附金属离子作用进行了电镀污泥的处理,但该方法也存在着生物对金属离子选择性差的难题。上述研究表明,采用一定方法可以使电镀污泥达到无害化的目标,且易于实现。但由于电镀污泥中多种成分共存,实现铬的资源化目标,首要任务就是铬元素的分离提取。但是目前还缺乏铬/铁分离的有效方法,因此研究一种新型铬/铁分离方法具有重要的环境意义。
电镀污泥中的铬铁分别以Cr6+和Fe3+形式存在,由于二者原子半径相近且有重叠,又同为阳离子,化学性质差异极小,致使Cr6+/Fe3+分离极其困难。在酸性溶液中铁能以Fe2+或Fe3+两种阳离子形式存在,而铬能以其阳离子Cr3+或者阴离子Cr2O72–两种形式存在,在pH<3.0时,电镀污泥可以形成Cr2O72--Fe3+共存体系,铬与铁分别为不同的离子电性,物理化学性质差异极大,为Cr6+/Fe3+分离创立了较大的前提基础。根据软硬酸碱理论[14-15],由于Cr2O72-的可极化性更大而属于“软碱”,Fe3+属于“硬酸”,所以电镀污泥酸浸液中的Cr2O72--Fe3+体系属于“软碱-硬酸”体系。根据“软硬酸碱理论”中“硬酸优先与硬碱结合,软酸优先与软碱结合”的经验规律,并借鉴有机溶剂萃取原理,外加新的“硬碱-软酸”体系,发生平衡移动,Cr2O72-与Fe3+可以分别进入不同相,从而达到分离的目的。因此探寻新的“硬碱-软酸”就是本文的主要内容。
根据离子液体的可设计性,本文分别选择了碳原子分别为2、4和8个的烷基咪唑,阴离子分别为[BF4]-和[PF6]-,二者不同组合的几种离子液体,设计出不同结构的“咪唑软酸”探索其与Cr2O72-的结合能力。以电镀污泥酸浸液为水相,以正戊醇为有机相溶剂,将咪唑离子液体作为萃取剂应用,为电镀污泥的资源化进行有益的探索研究。
1 实验材料和方法
1.1 材料
所用的电镀污泥原料源自某电镀污泥处理厂,其成分波动较大,经多批混料均勾取样分析,料液的主要化学成分如表1所示。1-辛基-3-甲基咪唑四氟硼酸盐([Omim][BF4])、1-辛基-3-甲基咪唑六氟磷酸盐([Omim][PF6])、1-丁基-3-甲基咪唑四氟硼酸盐([Bmim][BF4])、1-乙基-3-甲基咪唑四氟硼酸盐([Emim][BF4]),化学纯,购于林州市科能材料科技有限公司。

表1 料液的化学组成
1.2 分析测试仪器
PXSJ-216型离子计(上海精密仪器科学公司)、Nicolet 380型傅里叶变换红外光谱仪(美国热电集团)、氟硼酸根离子选择性电极(上海圣科仪器有限公司)、232参比电极(上海圣科仪器有限公司)、SHA-C型恒温水浴振荡器(巩义市予华仪器有限公司)、TG-60型高速离心机(巩义市予华仪器有限公司)、Optima 8300D型电感耦合等离子体发射光谱仪(美国PE公司)。
1.3 实验步骤
以戊醇作稀释剂,按照一定萃取剂浓度配制有机相。按既定实验方案准确量取20.0 ml有机相与20.0 ml水相置于250 ml具塞磨口锥形瓶中,将其放入恒温水浴振荡器中,在一定温度下、匀速振荡至设定时间后,经离心机在4000 r·min-1下离心5.0 min实现有机相和水相的快速分离,下层水相中金属离子浓度采用电感耦合等离子体发射光谱仪测定,有机相中金属离子浓度由物料衡算求得。萃取体系的萃取率()、分配比()、分离系数()根据式(1)~式(3)进行计算
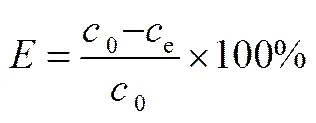
(2)
(3)
其中,分配比为有机相中被萃取物的总浓度与水相中被萃取物的总浓度之比。分配比大的物质,易从水相中转移到有机相,分配比小的物质,易留在水相,借此将它们分离。分离系数表示某一单元分离操作或某一分离流程将两种物质分离的程度。通常有两种定义:单级分离系数,表示物料中两种物质在某一单元分离操作(单级分离操作)前后相对含量的比值;流程分离系数,表示物料中两种物质在经过某一分离流程前后相对含量的比值。本文即是铬铁的分离系数,因铬铁分离系数较大,所以本文作图采用lg。
2 结果与讨论
由于离子液体的种类很多,结构各不同。随着近年来离子液体研究、应用的不断深入,通过对阴、阳离子的修饰或改变,可精确调控离子液体的熔点、热稳定性、酸碱性、极性等物理化学性质,例如,调节阴、阳离子的体积大小、对称性和电荷分散程度,可调控离子液体的熔点;阴阳离子体积的大小可以影响离子液体的密度;离子液体的黏度与阴、阳离子之间的相互作用也有关;通过改变阴、阳离子的种类还可得到不同电导率的离子液体;通过调节阴阳离子,可以调节其酸性,有时其酸度甚至可调至超酸性。因此离子液体的“可设计性”已成为离子液体继“绿色性”之外的又一突出优点与价值。离子液体最主要的特点之一是具有碳链长度可变的自由烷基咪唑阳离子(),它具有极化性大,离子结合能力强等优点,属于“软酸”。本文应用软硬酸碱理论作为探究铬铁分离的理论基础,为难于分离的多元素体系分离提供一种新的角度。
2.1 离子液体“可设计性”和“软酸”性质探究
2.1.1 离子液体烷基碳链长度对萃取分离效果的影响 阴离子为[BF4]-的离子液体对Cr2O72--Fe3+的萃取分离能力随离子液体咪唑环上烷基链的增长而增强,实验结果表明,离子液体对于Fe3+结合能力很弱,而[Omim][BF4]对于Cr2O72-结合能力较强,[Bmim][BF4]、[Emim][BF4]与水互溶难以达到分层目的,不能实现铬铁深度分离。
首先亲水性离子液体具有更高的离子强度,能够夺取反应体系中更多的水,从而更大程度地改变了包围在金属离子周围的微水环境,导致化学反应受到抑制。此外,[Bmim][BF4]、[Emim][BF4]亲水性离子液体在水溶液中会解离为具有极性区域和非极性区域的微小结构,影响萃合物的生成,进而影响离子液体对于金属离子的静电吸引能力,最终导致亲水性离子液体抑制萃取反应。此外通过比较3种离子液体与水的润湿角,可以得出[Omin][BF4]>[Bmin][BF4]>[Emin][BF4],实验结果表明,[Omim][BF4]具有较好的疏水性能,而[Bmim][BF4]、[Emim][BF4]疏水性能较差,这与离子液体的黏度有很大关系,影响黏度的因素主要有氢键、范德华力和静电相互作用,其中范德华力影响十分明显,在具有相同阴离子的咪唑类离子液体中,随着烷基碳链长度的增加,导致范德华力的明显增强,进而离子液体的黏度增大,有效提高离子液体的疏水性[28-30]。
通过萃取率(表2)可以看出,[Omim][BF4]与Cr2O72-结合能力最强,由软硬酸碱理论可知,离子所带电荷越高,离子半径越小,其硬度越高,+3价铁离子由于具有高的电荷数,属于硬酸。咪唑阳离子体积大,具有极强的可极化性,属于软酸[31-32]。根据HSAB原则可知离子液体不具备与Fe3+结合的能力。其中,关键的是Cr2O72-的半径比Fe3+的大,可极化性高,属于软碱,与咪唑阳离子软酸具有较强的结合能力。通过萃取率可以看出,[Omim][BF4]与Cr2O72-结合能力最强,说明其酸性最强。Cr2O72-依靠共价键为主的相互作用力首先与咪唑阳离子发生极化作用结合生成稳定的萃合物,而Fe3+与其亲和能力较弱。
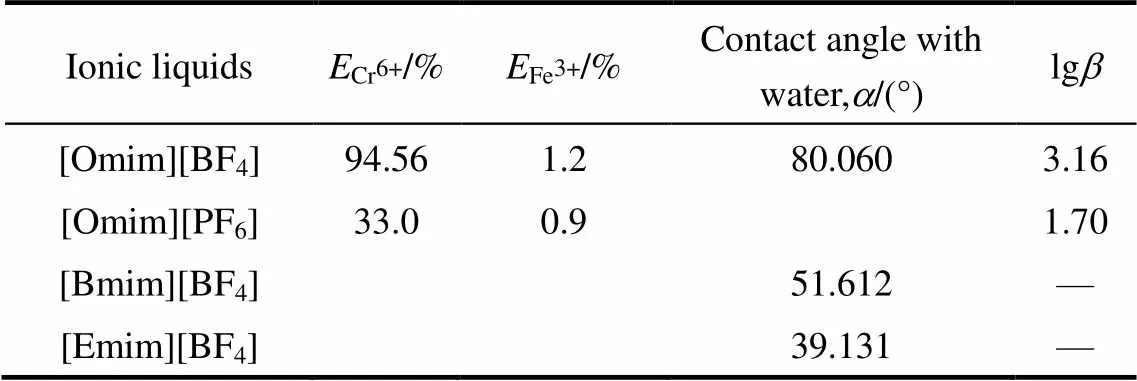
表2 不同离子液体润湿角以及对铬铁萃取分离效果
2.1.2 离子液体阴离子种类对萃取分离效果的影响 通过萃取率可以看出,当烷基碳链长度相同,阴离子种类不同时,不同离子液体对于Fe3+结合能力都很低,而离子液体对于Cr2O72-结合能力大小为[Omim][BF4]>[Omim][PF6],与阴离子疏水性能保持一致。对于含有[PF6]-的离子液体为疏水性的,而含有[BF4]-的离子液体其亲疏水性与阳离子上的取代基有关。即离子液体阴、阳离子的组成是影响其溶解性的关键,因而调整其组成使其达到某种溶解性以满足研究的需要,这也是离子液体“可设计性”的优势所在[33]。
首先,[PF6]-阴离子是对称的八面体结构并且电荷体积相对较大,[PF6]-被平行地固定在咪唑环的两侧,而不是填充于其中,阴阳离子之间具有较强的配合作用以及极性分子之间的亲和力。当Cr2O72-与离子液体阳离子咪唑环相互作用时,会产生一定的位阻,阻碍了Cr2O72-与离子液体的相互作用,为亲水性的Cr2O72-进入到离子液体相中增加了阻碍。而且[Omim][PF6]具有疏水疏油性质,难以与戊醇组成有机相,在该萃取体系中难以应用。重要的一点,近几年有报道含[PF6]-阴离子的离子液体在酸性条件下遇水会水解,产生有毒气体HF[34]。
最后,离子液体完全由阴阳离子组成,具有非常好的导电性以及比较宽的电化学窗口,可达3~5 V。对于同样阳离子的离子液体,阴离子体积越小(范德华力小),电荷越分散(静电力小),与阳离子成氢键的作用越弱,其缔合作用越弱,离子自由度越强,电导率越大。因此,与下列阴离子[PF6]-、[BF4]-构成的离子液体导电性依次增大,进而离子迁移率越大,其对于金属离子的静电吸引能力越强。因此,根据阴阳离子的不同组合,形成具有不同导电性能的离子液体,探究其对于不同金属离子的吸引能力在萃取分离金属离子方面具有广阔的研究前景。
综上所述,[Omim][BF4]对于铬铁的萃取分离效果较好,因此在后续的研究工作中采用[Omim][BF4]作为金属离子的萃取分离体系。
2.2 [Omim][BF4]离子液体萃取Cr(Ⅵ)、Fe(Ⅲ)的机理研究
萃取机理对于萃取剂的选择、萃取工艺参数等工艺条件的确定具有至关重要的作用,因此对于本文所研究体系进行萃取机理研究也显得非常重要。本文采用斜率法确定萃取机理。由于Cr2O72-的面电荷密度低于[BF4]-面电荷密度,Cr2O72-与[BF4]-的交换可降低体系的自由能,故可假定[Omim][BF4]萃取Cr2O72-反应为式(4)。
Cr2O72-(aq)+[Omim][BF4](org)= [([Omim])Cr2O 7](n-2)+(org)+[BF4]-(4)
式中,为萃合物中[Omim][BF4]的配位数(下角标aq代表水相,org代表有机相,下同)。
萃取平衡常数
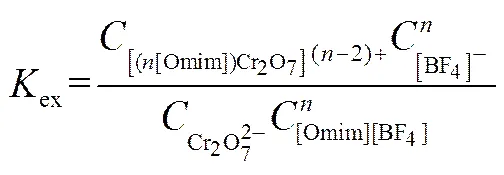
分配比
(6)
整理得
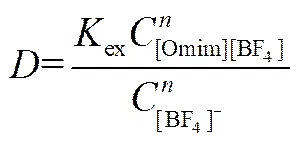
取对数
(8)
利用实验数据作lg-lg[Omim][BF4]图,得到直线
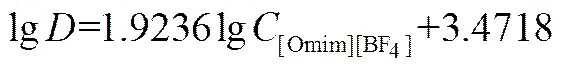
2=0.9987,直线斜率为1.9236,取整数得2,表明Cr2O72-的萃合物中[Omim][BF4]的配位数为2。
图1 lg-lg曲线
Fig.1 lg-lg curves
由图2可知,萃合物曲线中1058 cm-1处[BF4]-的振动吸收峰消失,说明铬的萃合物中不存在[BF4]-,同时萃合物中在940 cm-1出现了强的振动吸收峰,表明Cr2O72-的存在,与文献[35]报道一致。萃合物红外光谱图中并未出现铁盐的吸收峰。由图3可知,离子液体萃取之后出现了907 cm-1的Cr2O72-Raman吸收峰,与文献[36]所述保持一致。
由图2、图3可以推断出[Omim][BF4]萃取铬的萃取机理为离子液体中咪唑阳离子与Cr2O72-通过静电吸引作用形成电子对,结合比为2:1,符合离子缔合机理。
2.3 实际电镀污泥酸浸液铬铁萃取分离条件优化
选取了4个不同因素萃取剂浓度、时间、pH、金属离子初始浓度研究萃取分离过程的内在机制的影响。实验结果如图4所示。
(a) electroplating sludge acid dipping 20.0 ml, organic phase 20.0 ml, shaking at 200 r·min-1for 6.0 min, pH=1.33; (b) electroplating sludge acid dipping 20.0 ml, organic phase 20.0 ml, shaking at 200 r·min-1, concentration of ionic liquid is 50.0 g·L-1, pH=1.33; (c) electroplating sludge acid dipping 20.0 ml, organic phase 20.0 ml, shaking at 200 r·min-1for 6.0 min, concentration of ionic liquid is 50.0 g·L-1; (d) electroplating sludge acid dipping 20.0 ml, organic phase 20.0 ml, shaking at 200 r·min-1for 6.0 min, concentration of ionic liquid is 50.0 g·L-1, pH=1.33
由图4可以看出,改变不同反应因素,[Omim][BF4]萃取体系对于铬铁萃取分离效果较好,二者分离系数最高可达1431,因此[Omim][BF4]萃取分离电镀污泥中铬铁具有一定的应用性,而其他几种离子液体则远远不如该体系,不能实现铬铁深度分离。[Omim][BF4]具有亲油疏水性质,能够更好地与戊醇组成萃取体系,有利于金属离子的高效富集。图4(a)表明,[Omim][BF4]-戊醇萃取体系中,铬铁分离系数随着离子液体浓度的升高而显著提高,这主要是因为离子液体浓度的升高,在两相中分散程度增加,有利于铬铁萃取分离效率的提高。当离子液体浓度为50.0 g·L-1的时候可以保证实验效果,之后再增加离子液体浓度,萃取分离效果保持不变,同时整个萃取过程在短时间内达到平衡。由图4(b)可知,经过6.0 min萃取后达到最高值。图4(c)表明,pH对于铬铁分离系数的影响很大。首先,对于离子液体而言,由于其自身构成的特殊性,由于离子液体本身对于酸碱具有一定的适应性,在强酸强碱条件下也不会发生水解,因此不是离子液体本身结构的变化造成的。在pH=1~2时,铬的萃取率较高,而铁的萃取率较低。这是因为在强酸性条件下,铬是以Cr2O72-形式存在,而铁是以Fe3+形式存在。强酸性条件下,Cr2O72-的软度以及碱度要比Fe3+大的多,而属于软酸。根据HSAB原理,优先和Cr2O72-结合生成稳定的萃合物,故铬的萃取率大于铁。随着pH的增大,铬的萃取率有所下降,整个萃取过程是复杂的。并不仅是硬度这一个因素来影响萃取。不同pH条件下,金属离子存在状态不一致,随着pH的升高,铬在溶液中以CrO42-形式存在,萃取率下降。离子液体对于不同金属离子选择性也存在差异。此外氢离子对其性质产生一定影响,阳离子的咪唑环上的H原子与[BF4]-或者[PF6]-中的F原子之间有较强的氢键作用。相比之下,[BF4]-离子中的F原子具有较强的负电性和较强的形成氢键的能力,可与H+进行配合作用形成更强的氢键,促进萃取反应的进行。而[PF6]-则与H+结合能力较弱,难以影响化学平衡。这也是影响实验结果的因素之一。图4(d)表明,随着Cr(Ⅵ)浓度的增加,体系的铬铁分离系数降低明显,分离系数降低主要是因为Cr(Ⅵ)浓度高到一定程度后会出现活度降低的趋势,导致有机相中游离萃取剂浓度降低,从而降低分配比,而铁的分配比变化不大所导致。
综上所述,最适宜工艺条件:萃取剂浓度为50.0 g·L-1、时间为6.0 min、萃取液pH=1.33~2.06。研究成果为酸性溶液体系中铬、铁分离开辟了一条可行、经济的新途径,对于混合电镀污泥中铬铁的无害化和资源化具有重要意义。
3 结 论
(1)本研究基于[Omim][BF4]、[Omim][PF6]、[Bmim][BF4]、[Emim][BF4]离子液体结构极好的可调节性及软酸性质,建立了电镀污泥酸浸液中Cr6+/Fe3+的分离方法。
(2)[Omim][BF4]对于Cr6+具有较好的结合能力,而对于Fe3+结合能力较弱。结合斜率法、红外光谱分析,Raman光谱分析,[Omim][BF4]萃取铬符合离子缔合机理,可推测[Omim][BF4]咪唑阳离子与Cr2O72-阴离子形成离子缔合物而进入有机相,从而达到萃取分离的目的。
(3)使用该方法可以实现[Omim][BF4]萃取分离电镀污泥酸浸液中铬铁,具有一定的应用性。
符 号 说 明

C0,Ce——分别为萃取前和萃取后水相中金属离子的浓度,g·L-1 DCr,DFe——分别为Cr(Ⅵ)、Fe(Ⅲ)分配比 E——萃取率,% Δn——金属离子物质量的变化量 Vaq,Vorg——分别为水相和有机相溶液的体积,L b——分离系数 下角标 aq——水相 e——萃取后 0——萃取前
References
[1] WU J Y, CHOU W S, CHEN W S,Recovery of eupric oxide from copper—containing wastewater sludge by acid leaching and ammonia purification process[J]. Desalin Water Treat, 2012, 47(1): 120-129.
[2] 李磊, 唐伟, 朱渊博, 等. 电镀污泥的铁氧体研究[J]. 现代化工, 2013, 33(10): 62-65. LI L, TANG W, ZHU Y B,Ferrite research on electroplatingsludge[J]. Modern Chemical, 2013, 10(33): 62-65.
[3] 康义. 我国有色金属工业全面协调可持续发展值得重视的若干问题[J]. 中国钨业, 2004, 19(5): 15-17. KANG Y. Important problems of Chinese nonferrous metals industry in comprehensive balanced and sustainable development[J]. China Tungsten Industry, 2004, 19(5): 15-17.
[4] 陈从喜, 曹苏扬, 王静波. 矿产资源综合利用与发展循环经济[J]. 中国工程科学, 2005, 7(suppl.): 143-146. CHEN C X, CAO S Y, WANG J B. Comprehensive utilization of mineral resources and the development of circular economy[J]. Chinese Engineering Science, 2005, 7(suppl.): 143-146.
[5] ZHANG Y, LI Z H, QI T,Green manufacturing process of chromium compounds[J]. Environ. Prog., 2005, 24(1): 44-50.
[6] LONG H M, MENG Q M , WANG P. Preparation of chromium-iron metal powder from chromium slag by reduction roasting and magnetic separation[J]. Journal of Iron and Steel Research International, 2015, 9(22): 771-776.
[7] 张波, 杨达朋, 赵青, 等.铬铁矿硫酸浸出液中Cr3+与Fe3+的分离[J]. 有色金属, 2014, 7: 1-10. ZHANG B, YANG D P, ZHAO Q,Separation of Cr3+and Fe3+from sulphuric acid leaching solution of chromite[J]. Nonferrous Metals, 2014, 7: 1-10.
[8] 胡国荣, 李国, 邓新荣, 等. 针铁矿法从铬铁合金硫酸浸出液中除铁[J]. 湿法冶金, 2006, 25(4): 195-200. HUO G R, LI G, DENG X R,Goethite method from ferrochrome alloys in sulfuric acid leaching liquid iron[J].Hydrometallurgy, 2006, 25(4): 195-200.
[9] WU J H, YANG L Z, ZHAN J,. Research on separation of chromium and iron in waste ferrochromium alloy[J]. Hydrometallurgy, 2011, 30(1): 51-56.
[10] 郭学益, 石文堂, 李栋, 等. 从电镀污泥中回收镍、铜和铬的工艺研究[J]. 北京科技大学学报, 2011, 33(3): 328-33. GUO X Y, SHI W T, LI D,Study on recycling nickel copper and chromium from the electroplating sludge[J]. Journal of University of Science and Technology Beijing, 2011, 33(3): 328-333.
[11] ZHANG Y, WANG Z K, XU X,Recovery of heavy metals from electroplating sludge and stainless steel pickle waste liquid by ammonia leaching method[J]. Journal of Environmental Sciences, 1999, 11(3): 381-384.
[12] SILVA J E, PAIVA A P, SOARES D,Extraction and recovery of chromium from electroplating sludge[J]. Journal of Hazardous Materials, 2006, 128(1): 39-43.
[13] BEWTRA J K, BISWAS N, HENDERSON W D,Recent advances in treatment of selected hazardous wastes[J]. Water Pollution Research of Canada, 1995, 30(1): 115-125.
[14] NAGARAJ P, RANESH N G. HSAB-driven regioselectivity difference in the Lewis-acid catalyzed reactions of 2-C-subtituted glycals with sulfur and oxygen nucleophiles: direct versus allylic substitution[J]. Tetrahedron, 2011, 67(48): 9322-9328.
[15] GAUDEN P A, WISNIEWSKI M. Studies of the reactivity of carbon nanotubes towards selected alkali cations and chlorides based on the HSAB theory[J]. Catalysis Today, 2010, 150(1): 147-150.
[16] 吴京珂, 沈兴海, 陈庆德. CMPO-离子液体萃取分离铀(VI)体系的电化学性质[J]. 物理化学学报, 2013, 29(8): 1705-1711. WU J K, SHEN X H, CHEN Q D. Electrochemical behavior of the system of uranium(Ⅵ) extraction with CMPO-ionic liquid[J]. Acta Phys.-Chim., 2013, 29(8): 1705-1711.
[17] 石成龙, 景燕, 肖江, 等. 离子液体体系用于盐湖卤水提取锂[J]. 化工学报, 2015, 66(S1): 266-271. SHI C L, JING Y, XIAO J,. Application of ionic liquids for extraction of lithium from salt lake brine[J]. CIESC Journal, 2015, 66(S1): 265-271.
[18] WELTON T. Room-temperature ionic liquids. Solvents for synthesis and catalysis[J]. Chem. Rev., 1999, 99(8): 2071-2083.
[19] JIN B Y, DONG R C, TING Z,Application of Brönsted acid ionic liquids as green catalyst in the synthesis of 2-propanol with reactive distillation[J]. Chinese Journal of Chemical Engineering, 2016: 24(11): 1561-1569.
[20] 黄浩军, 杨莉萍, 徐子君, 等. 咪唑型离子液体热物理性质测量[J]. 化工学报, 2015, 66(S1): 49-53. HUANG H J, YANG L P, XU Z J,Thermo-physical properties measurement of imidazolium ionic liquids[J]. CIESC Journal, 2015, 66(S1): 49-53.
[21] CHEN S M, ZHANG S J, LIU X M,Ionic liquids clusters: structure, formation mechanism and effect on the behavior of ionic liquids[J]. Physical Chemistry Chemical Physics, 2014, 16(3): 5893-5906.
[22] VISSER A E, JENSEN M P, LASZAK I,Uranyl coordination environment in hydrophobic ionic liquids: aninvestigation[J]. Inorg. Chem., 2003, 42(7): 2197-2199.
[23] VISSER A E, ROGERS R D. Room-temperature ionic liquids: new solvents for-element separations and associated solution chemistry[J]. Solid State Chem., 2003, 171: 109-113.
[24] VISSER A E, SWATLOSKI R P, REICHERT W M,Task-specific ionic liquids incorporating novel cations for the coordination and extraction of Hg2+and Cd2+: synthesis, characterization, and extraction studies[J]. Environmental Science & Technology, 2002, 36(11): 2523-2529.
[25] VISSER A E, SWATLOSKI R P, REICHERT W M,Task-specific ionic liquids for the extraction of metal ions from aqueous solutions[J]. Chem. Comun., 2001: 135-136.
[26] NAKASHIMA K, KUBOTA F, MARUYAMA T,Ionic liquids as a novel solvent for lanthanide extraction.[J]. Anal. SCI, 2003, 8(19): 1097-1098.
[27] WHITEHEAD J A, LAWRANCE G A, MCCLUSKEY A. Green leaching: recyclable and selective leaching of gold-bearing ore in an ionic liquid[J]. Green Chem., 2004, 6(7): 313-315.
[28] BONHOTE P, DIAS A P, PAPAGEORGIOU N,Hydrophobic, highly conductive ambient-temperature molten salts[J]. 1996, 35(5): 1168-1178.
[29] BRANCO L C, ROSA J N, RAMOS J J M,Preparation and characterization of new room temperature ionic liquids[J]. Chem. Eur., 2002, 8(16): 3671-3677.
[30] GU Z, BRENNECKE J F. Volume expansivities and isothermal compressibilities of imidazoliun and pyrinium-based ionic liquids[J]. Chem. Eng. Data, 2002, 47(2): 339-345.
[31] LIU Y, XING Z, ZHANG X,Inorganic anion-dependent assembly of zero-, one-, two- and three-dimensional Cu(Ⅱ)/Ag(Ⅰ) complexes under the guidance of the HSAB theory: synthesis, structure, and magnetic property[J]. Journal of Solid State Chemistry, 2017, 246: 48-56.
[32] CHERMAHINI A N, HOSSEINZADEH B, BENI A S,Theoretical studies on the reactivity of mono-substituted imidazole ligands[J]. Stru. Chem., 2014, 25: 583-592.
[33] 路瑞岭, 刘建华, 李臻, 等. 亲水性离子液体及其在催化反应中的应用[J]. 分子催化, 2008, 22(2): 185-192. LU R L, LIU J H, LI Z,Applications in catalytic reaction of hydrophilic ionic liquids[J]. Journal of Molecular Catalysis (China), 2008, 22(2): 185-192.
[34] VISSER A E, SWATLOSKI R P, REICHERY W M,Traditional extractants in nontraditional solvents: groups 1 and 2 extraction by crown ethers in room-temperature ionic liquids[J]. Ind. Eng. Chem. Res., 2000, 39(10): 3596-3604.
[35] 葛战勤, 杨永会, 孙思修, 等. 伯胺N1923萃取铬Cr(Ⅵ)的研究[J]. 应用化学, 1995, 12(3): 59-63. GE Z Q,YANG Y H,SUN S X,The study on extraction of chromium(Ⅵ) with primary amine N1923[J]. Practical Chemistry, 1995, 12(3): 59-63.
[36] 王献伟, 王芳芳. 重铬酸钾在银胶中的表面增强Raman散射研究[J]. 中国科技信息, 2005, 13: 14. WANG X W, WANG F F. Study on Raman scattering surface enhanced of potassium dichromate on the elargol[J]. China Science and Technology Information, 2005, 13: 14.
Cr6+/Fe3+extractionseparationfrom electroplating sludge based ondesignability and soft acidity of ionic liquids
WEI Junyi, LI Yong, XUE Xiangxin
(School of Metallurgy, Northeastern University, Liaoning 110819, Shenyang,China)
The application and mechanism of ionic liquids in extraction separation of hexavalentchromium and ferriciron from acid dipping electroplating sludge was studied on the basis of designability and soft acidity of the ionic liquids. The experimental results showed that alkyl chain length on iminazole ring had remarkable effect onefficacy of extraction separation and ionic liquid with [BF4]-anion had higher extraction separation efficiency than that with [PF6]-anion. Among the ionic liquids in the study, [Omim][BF4] exhibited best extraction separation efficiency of Cr6+/Fe3+in electroplating sludge. Slope analysis, FTIR and Roman spectra suggested ionic associationmechanismin this extraction separation, which imidazolium cation formedassociation complex with dichromate anion and entered into organic phase by extraction. Consequently the technique could be applicable for transformingelectroplating sludge waste into resources.
ionic liquids; extraction and separation; designability; HSAB
10.11949/j.issn.0438-1157.20170288
O 652.62
A
0438—1157(2017)09—3451—08
2017-03-23收到初稿,2017-06-15收到修改稿。
李勇。
魏君怡(1991—),女,硕士研究生。
国家自然科学基金项目(U1502273)。
2017-03-23.
Prof.LI Yong, liyong@smm.neu.edu.cn
supported by the National Natural Science Foundation of China (U1502273).

