肥厚型梗阻性心肌病的外科治疗
马红艳 张勤斌 周宏
临床研究
肥厚型梗阻性心肌病的外科治疗
马红艳 张勤斌 周宏
目的 评价外科手术治疗肥厚梗阻性心肌病的临床疗效。方法 2010年1月至2013年10月,72例患者因肥厚梗阻性心肌病在我院行外科手术治疗,男性36例,女性36例,年龄13~70(46.51±13.45)岁。手术在全麻低温体外循环下完成,按常规经主动脉切口行室间隔心肌切除术,同期行冠状动脉旁路移植术4例、二尖瓣置换术8例、二尖瓣成形术2例、主动脉瓣置换术2例、主动脉瓣成形术1例、动脉导管结扎术1例、右室流出道疏通术1例、左房血栓清除1例、左心耳结扎2例、冲洗式射频消融改良迷宫术4例、安装永久起搏器2例。围术期心脏超声心动图(UCG)或食管超声心动图(TEE)评价左心室舒张末径、左室流出道流速及压差(LVOT)、室间隔厚度、左室射血分数(EF)、二尖瓣结构和功能。结果 与术前比较,左室流出道压差[(9.42±7.48)mm Hg 比(79.76±51.9)mm Hg,P<0.01]及室间隔厚度[(1.87±0.57)cm 比(2.36±0.48)cm,P<0.01]明显下降,长期随访发现左室流出道压差进一步下降[(7.57±5.21)mm Hg],室间隔厚度进一步变薄[(1.69±0.45)cm]。左室舒张末径在出院时有所扩大,长期随访有进一步扩大趋势。EF值较术前有所下降(P<0.01),但仍在正常范围内。手术死亡0例。主要并发症:完全性左束支传导阻滞52例,右束支传导阻滞2例,室内传导阻滞3例,心房颤动7例(其中3例为阵发性房颤),短暂Ⅱ~Ⅲ度房室传导阻滞5例,持续Ⅲ度房室传导阻滞2例,室间隔穿孔1例,术后脑出血2例,急性胆囊炎1例。远期随访:5例失访,余67例术后随访3~53个月(平均18个月),所有患者症状消失,生活质量明显改善,心功能I~Ⅱ级,无远期死亡或并发症。结论 肥厚梗阻性心肌病外科手术治疗可有效地减轻左室流出道梗阻,提高患者的生活质量。
心肌病; 肥厚性; 二尖瓣关闭不全; 外科手术; SAM征
肥厚型梗阻性心肌病(HOCM)目前尚无特异有效的治疗措施,未经外科手术治疗的患者年病死率1.7%~4.0%,多数为猝死,自然预后差。近年来,随着心血管外科诊疗技术的成熟和发展,HOCM的外科治疗取得显著的进步。本研究总结了武汉亚洲心脏病医院2010-2013年外科治疗HOCM的疗效和经验。
1 对象与方法
1.1 研究对象 自2010年1月至2013年10月,经外科治疗HOCM 72例,其中男性36例、女性36例,年龄 13~70(46±13)岁。术前 34 例患者有胸痛,20例有黑蒙,18例有明确的晕厥症状。术前心电图显示存在病态窦房结1例,心房颤动7例,心室预激2例,Ⅱ度房室传导阻滞1例,频发室性早搏3例。术前心脏彩超示:左室壁及室间隔非对称性增厚,二尖瓣SAM征,致左室流出道狭窄,左室流出道峰值压差均>50 mm Hg(1 mm Hg=0.133 kPa),激发压差均>100(151±47)mm Hg。大部分患者术前服用钙通道阻滞剂或β受体阻滞剂,但因症状不能控制而行手术治疗。合并病变:冠状动脉粥样硬化性心脏病4例,主动脉瓣二瓣化畸形并狭窄或关闭不全3例,二尖瓣重度关闭不全12例,二尖瓣中度关闭不全20例,感染性心内膜炎1例,动脉导管未闭1例,室间隔心肌化学消融术后1例,左房血栓1例。
1.2 手术方法 手术均在全麻低温体外循环下进行。术中常规行经食管心脏超声(transesophageal echocardiographv,TEE)监测,常规升主动脉及上、下腔静脉插管建立心肺转流。主动脉阻断后,经主动脉根部冷灌心脏停跳满意后,在右冠状动脉开口上方斜形切开主动脉,暴露肥厚的室间隔,探查二尖瓣乳头肌有无畸形和二尖瓣前叶大小。全部患者采用扩大的室间隔肌肉切除术,即改良的Morrow心肌切除方法。切除范围从右冠瓣中点下方至左右冠瓣交界下方近二尖瓣前叶0.5~1.0 cm处,但膜部间隔不宜切除。切除时纵向不仅切除主动脉瓣下,而且切除范围扩大至心尖;横向不仅局限在右冠瓣下,还包括左冠瓣达左无冠交界,必要时还切除部分左室游离壁的肥厚肌肉,切除后使室间隔厚度达到正常标准。切除时需避免切穿室间隔深达二尖瓣前乳头肌根部水平。异常肌肉切除后能清晰辨认二尖瓣结构,若存在二尖瓣瓣下结构异常需同时处理。心脏复跳后常规TEE检测左心室流出道、室间隔厚度及二尖瓣情况。同期行冠状动脉旁路移植术4例,二尖瓣置换术8例(其中1例患者术中3次转机行MVR),二尖瓣成形术2例,主动脉瓣置换术2例,主动脉瓣成形术1例,动脉导管结扎术1例,因术中发现右室流出道狭窄行右室流出道疏通术1例,左房血栓清除1例,左心耳结扎2例,因房颤行冲洗式射频消融改良迷宫术4例,因术前存在病态窦房结综合征及慢速房颤伴房室传导阻滞于术中安装永久起搏器2例。
1.3 统计学方法 采用SPSS19.0统计软件分析。数据以±s表示,组内两样本均数比较采用配对t检验。P<0.05为差异有统计学意义。
2 结果
全组无一例死亡。术后主要并发症:完全性左束支传导阻滞52例,右束支传导阻滞2例,室内传导阻滞3例,心房颤动7例(其中3例为阵发性房颤),短暂Ⅱ~Ⅲ度房室传导阻滞5例,持续Ⅲ度房室传导阻滞2例(其中1例术后第7天安装永久性起搏器),室间隔穿孔1例,术后脑出血2例(无严重后遗症),急性胆囊炎1例(转综合医院治疗)。所有患者均痊愈出院,除5例失访外,余67例患者术后随访(来院复查超声心动图、心电图及胸部X线片)3~53个月(平均18个月)。1例患者术后1个月因胸痛再入院,心电图示加速性室性自主心律,药物治疗后好转出院。1例患者术后2个月因快速房颤行射频导管消融术转为窦性心律。1例患者术后7个月因主动脉瓣中度关闭不全、二尖瓣重度关闭不全、三尖瓣重度关闭不全再次入院行主动脉瓣成形+二尖瓣成形+三尖瓣成形术,术后恢复良好。所有患者症状明显减轻,心功能Ⅰ~Ⅱ级,生活质量提高。
与术前比较,出院时及随访超声均提示左室流出道压差较术前显著下降,室间隔厚度变薄,左室顺应性改善(见表1)。出院时超声心动图(UCG):与术前相比,左室流出道压差显著下降[(9.42±7.48)mm Hg 比(79.76±51.9)mm Hg,P<0.01],室间隔厚度变薄[(1.87±0.57)cm 比(2.36±0.48)cm,P<0.01];长期随访发现左室流出道压差进一步下降[(7.57±5.21)mm Hg],室间隔厚度进一步变薄[(1.69±0.45)cm]。左室舒张末径在出院时有所扩大,长期随访有进一步扩大趋势。EF值较术前有所下降(P<0.01),但仍在正常范围内。1 例患者二尖瓣仍残留轻度SAM征,余患者SAM征消失,二尖瓣返流基本消失或显著减轻(1例患者中度返流,11例轻度返流),长期随访二尖瓣返流有加重趋势,仅1例需要再次手术矫治。见表2。
表1 患者不同时间段超声检查结果比较(±s)
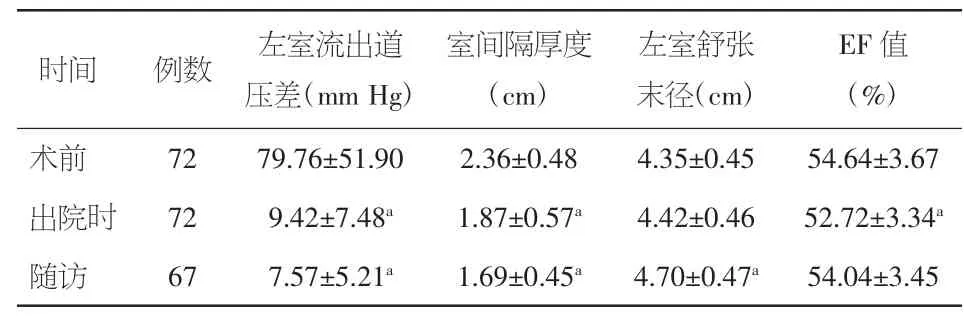
表1 患者不同时间段超声检查结果比较(±s)
注:与术前比较,aP<0.01
EF值(%)术前 72 79.76±51.90 2.36±0.48 4.35±0.45 54.64±3.67出院时 72 9.42±7.48a 1.87±0.57a 4.42±0.46 52.72±3.34a随访 67 7.57±5.21a 1.69±0.45a 4.70±0.47a 54.04±3.45时间 例数 左室流出道压差(mm Hg)室间隔厚度(cm)左室舒张末径(cm)

表2 患者手术前后二尖瓣返流(MR)程度及SAM征比较(例)
3 讨论
肥厚型心肌病(hypertrophic cardiomyopathy)是以心室肌非对称性肥厚、肥厚的肌肉突向左心室腔为特征,导致左心室腔变小,左室收缩功能正常,但舒张功能受损的心肌病。根据有无左心室流出道梗阻分为肥厚型梗阻性心肌病和肥厚型非梗阻性心肌病。肥厚型心肌病的发病率为0.2%,病因与遗传基因相关,故具有一定的家族遗传性。未经外科治疗的肥厚型心肌病,年死亡率为1.7%~4%,5年死亡率为15%。自1960年开始进行心肌切开术解除流出道梗阻至今,外科手术一直是治疗肥厚型梗阻性心肌病的疗效可靠、不可替代的治疗方式。外科治疗主要通过解除左室流出道梗阻、纠正二尖瓣收缩期前向运动(SAM),从而缓解临床症状,改善心力衰竭。Altarabshed等[1]对成人及青少年肥厚型梗阻性心肌病的外科治疗做了长期随访,并与药物治疗和经皮室间隔化学消融结果进行了比较,结果显示,对青少年,外科治疗长期疗效达92%,再次手术率仅5%;成人围术期死亡率低于1%,症状缓解率99%,起搏器植入率<2%,10年生存率90%,再次手术率仅33%。对于无症状肥厚型梗阻性心肌病患者,尽早手术疗效更佳[2]。经皮室间隔化学消融的围术期死亡率为1.5%,但并发症的发生率远高于外科手术,25%的患者因为房室传导阻滞或室性心律失常而放置永久起搏器或体内自动除颤仪,症状缓解率为89%,再次手术率达6%[3-7]。许多心脏中心的回顾分析表明,外科手术的死亡率、症状复发率、合并症发生率均低于介入治疗[3,4,8,9]。最近的Meta分析表明,外科手术能够稳定、彻底、快速地缓解症状,尤其年龄<65岁的患者,与介入治疗比较,外科手术大大降低了左室流出道的压差、手术并发症如完全性房室传导阻滞起搏器植入率、恶性心律失常发生率[7]。
二尖瓣收缩期前向运动是肥厚型心肌病左室流出道梗阻时最常见的现象。许多研究表明,该现象不仅是室间隔异常肥厚引起的,且与二尖瓣结构的异常有密切关系。10%~20%的HOCM患者二尖瓣本身有先天性发育异常或继发性病变。尽管室间隔肥厚肌束已充分切除,左室流出道疏通满意,TEE仍显示在二尖瓣瓣尖水平存在梗阻,SAM现象不能完全解除,同时存在不同程度MR。UCG常常提示二尖瓣瓣叶或瓣下结构病变,如二尖瓣叶脱垂、腱索断裂、瓣缘纤维化、瓣环显著钙化、乳头肌形态结构异常、风湿性病变、感染性病变等。少数室间隔肥厚肌束切除过程中可能伤及邻近的二尖瓣腱索,尽管左室流出道疏通满意,TEE检查左室流出道压差下降,SAM征消失,但MR持续存在,且大多是偏前交界或中心性返流,与左室流出道压差和SAM征无显著相关性。此时需要同期行MVP或MVR。MVP的目的是降低二尖瓣瓣叶的面积和矫治瓣下异常错位的二尖瓣结构,包括交界环缩术、人工腱索、乳头肌松解术、后瓣叶矩形切除成形术、双孔MVP等,对需要植入成形环者,建议植入较大的人工成形环,以避免或减少人工成形环MVP术后二尖瓣SAM征的发生。Nasseri等[10]对25例有明显SAM征的肥厚型梗阻性心肌病患者实施了经主动脉下室间隔部分心肌切除联合保留二尖瓣前瓣修补术,随访0.8~14年,Kaplan-Meier生存评估1年生存率100%,5年生存率82.6%,5年免再手术率83.8%,术后左室流出道平均压从(84±32)mm Hg降到(19±11)mm Hg(P<0.01),仅有 2 例患者术后有轻度残留或再发SAM征,二尖瓣返流程度及New York心功能分级在随访中明显改善,结论是保留前瓣的二尖瓣成形术可以阻止残留或再发左室流出道梗阻,改善二尖瓣返流。尽管室间隔部分切除术是一种安全且有效的手术方法,二尖瓣返流和左室流出道梗阻经常会再发,尤其是那些有严重SAM征的患者。为解决这些问题,Cooley和他的同事们[11-13]推荐采用二尖瓣置换术,特别是成年患者。然而,如今大多数外科医生尽力避免为HOCM患者首先进行二尖瓣置换。
本组患者术后心律失常主要为心房颤动,发生率约为9.7%,需要及时的药物治疗。一般用胺碘酮、β受体阻滞剂,将心室率控制在70次/min左右。本组1例患者术后2个月因快速房颤行射频导管消融术转为窦性心律。快速的心律失常,引起心脏舒张期缩短,心脏不能完全充盈,导致血压下降,冠状动脉灌注不足,容易引发心力衰竭。术后常规需要应用β受体阻滞剂,发生房颤时,静脉应用胺碘酮多能控制。术后处理的关键是保证心脏前负荷,控制心室率,必要时加用钙通道阻滞剂。本组患者术后需要安装永久起搏器的约为2.7%。Ⅲ度房室传导阻滞与手术切除范围较大有关,特别是在右冠瓣中点下方做切口时,向无冠瓣侧偏离过多,容易损伤传导束。室间隔心肌切除术后,大多数患者出现左束支传导阻滞。如果患者术前合并右束支阻滞,术后安装起搏器的可能性较大。
Dominic等[14]在行室间隔部分肌切除术同时行前降支肌桥分离术及主动脉横切缩短术。该研究将所有患者均行冠脉造影检查,发现有接近50%存在前降支肌桥。年轻的有症状的患者发病率最高,可能反映了该疾病更具侵袭的表现形式,前降支肌桥是儿童猝死的一个危险因子。成人前降支肌桥导致心肌缺血的程度还存在争议,可能的机制是冠脉痉挛或肌桥在舒张期没有足够的放松,从而减少了冠脉血流[15]。另外,近端前降支肌桥的存在与冠状动脉粥样硬化性心脏病的发展有关[16]。常规分离所有的前降支肌桥可以去除将来因肌桥引起的症状。该研究还第一次提到了对有S型弯曲室间隔形态和升主动脉延长的患者在做室间隔部分肌切除术的同时做了主动脉横切及缩短术。升主动脉随着年龄增长而延长[17,18],解剖学上,由于心包的依附及大血管的起源,升主动脉和主动脉弓的连接位置是相对固定的。当主动脉延长时就会出现以下2种情况:①弓和主动脉瓣的距离保持不变,导致主动脉向右弯曲与左室流出道形成一个相对的水平。②心脏随着主动脉扩张发生移位,使主动脉瓣下移,左室流出道和升主动脉之间的角度变小。后者使增厚的室间隔看起来呈S型。通过缩短主动脉重建正常的解剖关系,可能改善左室流出道血流动力学,减轻SAM征。这两种附加手术目前较少有报道,值得我们关注。
本组随访结果表明,室间隔心肌切除术后室间隔厚度下降,左心室后壁厚度变薄,二尖瓣返流减轻,左心室舒张功能改善,这些均有利于左心室的重塑。患者症状及心功能改善,治疗结果满意。
[1]Altarabsheh SE,Dearani JA,Burkhart HM,et al.Outcome of septal myectomy for obstructive hypertrophic cardiomyopathy in children and young adults.Ann Thorac Surg,2013,95:663-669.
[2]Schaff HV,Dearani JA,Ommen SR,et al.Expanding the indications for septal myectomy in patients with hypertrophic cardiomyopathy:results of operation in patients with latent obstruction.Thorac Cardiovasc Surg,2012,143:303-309.
[3]Bown ML,Schaff HV.Surgical management of obstructive hyper-trophic cardiomyopathy:the gold standard.ExpertRev Cardiovasc Ther,2008,6:715-722.
[4]Maron BJ,Yacoub M, Dearani JA.Controversies in cardiovascular medicine,Benefits of surgery in obstructive hypertrophic cardiomyopathy:bring septal myectomy back for European patients.Eur Heart J,2011,32:1055-1058.
[5]Braunwald E.Obstruction in hypertrophic cardiomyopathy:hou often does it occur?Should it be treated?If so,how?Circulation,2012,126:2369-2370.
[6]Maron BJ.Commentary and re-appraisal:surgical septal myectomy vs alcohol ablation::after a decade of controversy and mismatch between clinical practice and guidelines.Prog Cardiovasc Dis,2012,54:523-528.
[7]Agarwal S,Tuzcu EM,Desai MY,et al.Updated meta-analysis of septal alcohol ablation versus myectomy for hypertrophic cardiomyopathy.J Am Coll Cardiol,2010,55:823-834.
[8]高长青,任崇雷,肖苍松,等.改良Morrow手术治疗梗阻性肥厚型心肌病.中华外科杂志,2012,50:434-437.
[9]Dearani JA,Ommen SR,Gersh BJ,et al.Surgery insight:Septal myectomy for obstructive hypertrophic cardiomyopathy-the Mayo Clinic experience.Nat Clin Pract Cardiovasc Med,2007,4:503-512.
[10]Nasseri BA,Stamm C,Siniawski H,et al.Combined anterior mitral valve leaflet retention plasty and septal myectomy in patients with hypertrophic obstructive cardiomyopathy.Eur J Cardiothorac Surg,2011,40:1515-1520.
[11]Cooley DA,Leachman RD,Hallman GL,et al.Idiopathic hypertrophic subaortic stenosis.Surgical treatmentincluding mitral valve replacement.Arch Surg,1971,103:606-609.
[12]Krajcer Z,Leachman RD,Cooley DA,et al.Septal myotomymyomectomy versus mitral valve replacement in hypertrophic cardiomyopathy:Ten-year follow-up in 185 patients.Circulation,1989,80:157-164.
[13]Walker WS,Reid KG,Cameron EW,et al.Comparison of ventricular septal surgery and mitral valve replacement for hypertrophic obstructive cardiomyopathy.Ann Thorac Surg,1989,48:528-535.
[14]Dominic JP,Robert ER,Jeffery A.Short and Medium Term Outcomes of Surgery for Patients With Hypertrophic Obstructive Cardiomyopathy.Ann Thorac Surg,2015,99:1213-1219.
[15]ErbelR, GeJ, Mohlenkamp S.Myocardialbridginga congenital variant as an anatomic risk factor for myocardial infarction.Circulation,2009,120:357-359.
[16]Ishikawa Y,Akasaka Y,Suzuki K,et al.Anatomic properties ofmyocardialbridge predisposing to myocardialinfarction.Circulation,2009,120:376-383.
[17]Dotter CT,Roberts DJ,Steinberg I.Aortic length:angiocardiographic measurements.Circulation,1950,2:915-920.
[18]Sugawara J,Hayashi K, Yokoi T, et al Age-associated elongation of the ascending aorta in adults.JACC Cardiovasc Imaging,2008,1:739-748.
Clinical experience of surgical treatment on hypertrophic obstructive cardiomyopathy
MA Hong-yan,ZHANG Qin-bin,ZHOU Hong.Cardiovascular Surgery,Wuhan Asia Heart Hospital,Wuhan 430000,China
MA Hong-yan,E-mail:ludy17@126.com
ObjectiveTo evaluate the surgical outcome of hypertrophic obstructive cardiomyopathy(HOCM).MethodsFrom January 2010 to October 2013,72 HOCM patients underwent surgical treatment in our hospital.There were 36 males and 36 females ranging from 13-70 (46.51±13.45)years old.Operation was performed under general anesthesia and cardiopulmonary bypass(CPB) with the moderate systemic temperature and low volume blood flow.The concomitant operations included coronary artery bypass grafting in 4 cases,mitral valve re-placement in 8 cases,mitral valve plasty in 2 cases,aortic valve replacement in 2 cases,aortic valve plasty in 1 case,closure of patent ductus arteriosus in 1 case,right ventricular outflow dredging operation in 1 case,left atrial thrombus removal in 1 case,left atrial appendage ligation in 2 cases,maze procedure in 4 cases,intraoperative pacemaker implantation in 2 cases.Preoperative and postoperative left ventricular end diastolic diameter,left ventricular outflow tract(LVOT),interventricular septal thickness,LVEF,mitral valve function and value were evaluated by Ultrasonic echocardiography and transesophageal echocardiograph examination(TEE).ResultsComparing with the pre-operative echocardiographic parameters,the pressure of left ventricular outflow tract[(9.42±7.48)mm Hg vs (79.76±51.9)mm Hg,P<0.01],and the thickness of septum[(1.87±0.57)cm vs (2.36±0.48)cm,P<0.01]significantly decreased.Long-term follow-up of left ventricular outflow tract pressure decreased further(7.57±5.21)mm Hg,the thickness of septum thinner further(1.69±0.45)cm.Left ventricular end diastolic diameter at the time of discharge has been expanded,and has further expanded at long-term follow-up.EF decreased (P<0.01),but still in the normal range.There was no one dead.The main complications:complete left bundle branch block in 52 cases,right bundle branch block in 2 cases,intraventricular block in 3 cases,atrial fibrillation in 7 cases(including 3 cases of paroxysmal atrial fibrillation),transientⅡ-Ⅲ degree A-V block in 5 cases,continuous A-V block in 2 cases,ventricular septal perforation in 1 case,cerebral hemorrhage in 2 cases,acute cholecystitis in 1 case.Long term follow-up:5 cases were lost to follow-up,the remaining 67 cases were followed up for 3-53 months(average 18 months),the symptoms disappeared in all patients,improved quality of life,heart function I-Ⅱ,no long-term death or complications.ConclusionSurgical outcome for HOCM patients is satisfactory.Most HOCM patients achieve such a satisfactory relief of LV outflow tract obstruction as to lead a better life.
Cardiomyopathy; Hypertrophic; Mitral regurgitation; Surgical procedures; SAM sign
430000 湖北省武汉市,武汉亚洲心脏病医院心脏中心
马红艳,E-mail:ludy17@126.com
10.3969/j.issn.1672-5301.2017.04.016
R654.2
B
1672-5301(2017)04-0354-05
2016-09-21)

