术中变温毯的应用对心脏手术术后苏醒时间的影响分析
吴秀婷, 袁晓燕, 李 娜
(陕西省汉中市中心医院, 1. 手术麻醉科; 2. 手术整形美容科; 3. 手术心胸外科, 陕西 汉中, 300072)
术中变温毯的应用对心脏手术术后苏醒时间的影响分析
吴秀婷1, 袁晓燕2, 李 娜3
(陕西省汉中市中心医院, 1. 手术麻醉科; 2. 手术整形美容科; 3. 手术心胸外科, 陕西 汉中, 300072)
变温毯; 心脏手术; 苏醒时间; 并发症
体温是人体重要生命体征指标之一,在正常生理条件下,人体核心体温为(37.0±0.4) ℃, 恒定的体温是机体各个器官维持正常运作的生理基础,而人体在麻醉状态下,体温很难维持在正常水平[1]。研究[2]显示,围术期患者轻度低体温的发生率为50%~70%, 引起患者围术期体温下降的因素很多,如麻醉药物的影响,手术类型、输血、输液及术中大量冲洗液等。围术期低温能够引起术后多种并发症,如麻醉恢复时间延长、术中出血量增多,术后寒颤、感染发生,甚至增加循环、呼吸、神经系统并发症,严重者会危及患者生命[3-4]。心脏手术操作复杂,手术时间长,同时需要采用静脉-吸入复合和全身麻醉,患者在手术过程中极易出现体温降低[5]。近年来,如何加强术中体温监测、预防低体温的发生,成为临床医生研究的热点[6]。本研究通过对心脏手术患者术中应用变温毯进行保温处理,观察对患者术后苏醒时间及术后并发症的影响,并取得满意疗效,现报道如下。
1 资料与方法
1.1 一般资料
选取2014年7月—2016年6月于本院心外科行心脏手术(冠脉搭桥手术、心脏瓣膜置换术)患者60例为研究对象,纳入标准: 符合美国新版冠脉搭桥手术指南[7]和美国心脏瓣膜疾病治疗指南[8]且有手术指征患者; 年龄18~70岁; SAS等级为Ⅱ~Ⅲ级; 所有患者均无严重的脑、肺、肝、肾等重要脏器疾病; 患者知情且签署知情同意书。排除标准: 既往有心脏手术史患者; 合并严重心脏瓣膜或同时患有肝肾疾病; 恶性肿瘤患者或多功能脏器缓解患者。按随机数字表法将患者分为观察组和对照组,每组30例,其中观察组男21例,女9例; 年龄35~68岁,平均年龄(48.52±12.31)岁; 手术类型: 冠脉搭桥手术19例、心脏瓣膜置换术11例; 手术时间(3.65±1.12) h; BMI指数(23.51±2.51) kg/m2; 术中输液量(2 531.68±856.24) mL。对照组男19例,女11例; 年龄33~70岁,平均年龄(49.21±11.36)岁; 手术类型: 冠脉搭桥手术21例、心脏瓣膜置换术9例; 手术时间(3.84±1.26) h; BMI指数(24.37±2.28) kg/m2; 术中输液量(2 566.74±861.74) mL。2组患者在性别、年龄、手术类型、手术时间、BMI指数、术中输液量等一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
术前准备: 所有患者术前均常规禁食禁饮8 h。术前30 min肌肉注射哌替啶1 mg/kg、东莨菪碱0.3 mg, 入室后采用Philips M8005A型监护仪监测患者心电图、心率(HR)和SpO2, 建立外周静脉通道,然后于局麻下行桡动脉穿刺及右颈内静脉穿刺置管,监测患者有创动脉血压及中心静脉压。经外周静脉麻醉诱导注射咪唑安定0.04 mg/kg、依托咪酯0.2 mg/kg、罗库溴铵6 mg/kg、舒芬太尼5 μg/kg, 给予面罩纯氧辅助呼吸, 5 min后行气管内插管,连接麻醉机行间歇正压通气。潮气量6~8 mL/kg, 呼吸频率10~15次/min, 吸气呼气比值(I: E)=1: 2, 吸入氧浓度40%~50%, 根据呼气末ETCO2调整通气参数。
对照组患者常规消毒铺巾覆盖处理后进行手术,术中使用Biss脑电监测仪监测麻醉深度,术中输注液体为常温。观察组患者采用变温毯保温处理,在患者麻醉诱导前预先在手术台上平铺循环水变温毯,连接STOCKERT热交换水箱,变温毯设置温度37~40 ℃, 术中输注液体均经保温箱预热处理,温度设置为37 ℃, 术中使用Biss脑电监测仪监测麻醉深度,实时监测患者体温并调节变温毯的温度维持患者核心体温在36.5 ℃, 待手术结束时关闭变温毯。手术期间2组患者均采用中度低温(26~28 ℃)体外循环,采用滚压泵和膜肺氧合,灌流量设置为2.0 L/(m2·min), 灌注压维持在50~90 mmHg,采用α稳态来平衡酸碱管理。维持动脉血酸碱度PH在7.35~7.40之间,p(CO2) mmHg, 术后所有患者送入ICU观察。
1.3 观察指标
比较2组患者入室前、手术30 min、手术60 min、手术120 min及手术结束时鼻咽温度、HR、平均动脉压(MAP)。同时,比较2组患者围术期拔管时间、术后苏醒时间、失血量等指标及术后恢复期并发症。
2 结 果
2.1 2组患者术中各时间点的鼻咽温度、HR及MAP比较
2组患者在入室前和手术30 min时,鼻咽温度差异无统计学意义(P>0.05),观察组患者在手术60 min、手术120 min和手术结束时鼻咽温度显著高于对照组,差异具有统计学意义(P<0.05)。而2组患者在术中各时间点HR、MAP均出现降低,且观察组患者各时间点HR及MAP均低于对照组,但2组比较差异无统计学意义(P>0.05)。见表1。
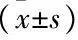
表1 2组患者术中各时间点的鼻咽温度、HR及MAP变化
与本组入室前比较, *P<0.05; 与同时间点对照组比较, #P<0.05。
2.2 2组患者围术期指标比较
观察组患者拔管时间、术后苏醒时间、失血量均显著低于对照组,差异具有统计学意义(P<0.05)。见表2。

表2 2组患者围术期指标比较±s)
与对照组比较, *P<0.05。
2.3 2组患者术后恢复期并发症比较
观察组寒战5例,心动过速3例,低氧血症2例; 对照组分别为12例、8例、6例。观察组患者术后寒颤发生率显著低于对照组,差异具有统计学意义(P<0.05)。而观察组在心动过速、低氧血症发生率低于对照组,但2组比较差异无统计学意义(P>0.05)。
3 讨 论
临床上通常将核心体温低于36℃称为低体温,其中34~35.9 ℃为轻度低体温, 32~33.9 ℃为中度低体温,小于32℃为重度低体温[9-10]。研究[11]显示,低体温可导致患者肌松药物代谢缓慢,增加患者术后呼吸抑制风险,同时低温使得患者凝血功能降低,血小板功能降低,延迟伤口愈合,增加术中出血量,增加心血管意外发生率,影响患者术后功能恢复。体温过低会影响机体血液流动速度,导致肝肾血液量减少,延缓麻醉药物在体内的代谢,导致术后苏醒时间延迟,同时会引起麻醉苏醒期寒颤,肌体氧耗量及代谢率增加[12-13]。
临床上体外循环手术期间直肠温度与血液温度具有高度正相关性,开胸手术往往时间较长,术中长时间经过体外循环,血液在低温循环条件下进入机体内,容易使机体核心温度降低,低温的皮肤血液循环差,容易引起患者损伤[14]。张曙东[15]在开胸手术患者采用体外循环干预,表明其能够加强术中重要器官的保护和减少术后并发症。目前,临床采用术中变温毯对体外循环血液装置进行预热,根据患者核心温度来调节,达到血液复温的目的[16]。研究[17]显示,开胸手术患者术中低体温在临床中比较常见,而心脏手术过程复杂,手术时间长同时需要对患者进行静脉-吸入复合和全身麻醉均会影响患者体温调节。目前,关于心脏手术过程中引起患者出现低温的原因主要有: ① 环境因素: 由于手术室室温过低、空调风及体外循环手术等为配合心脏降温有意降低环境温度,均可能引起患者体温降低[18-19]; ② 心脏手术尤其是冠状动脉塔桥手术,术前需要对患者大部分皮肤进行消毒,而碘酊、酒精等消毒液挥发使会带走患者皮肤表面大量热量,同时心脏手术需要打开胸腔,且手术复杂,使脏器等长时间暴露于室温条件下,均可能引起患者体温降低[20]; ③ 心脏手术中需要对患者进行麻醉处理,麻醉药物会导致肌肉舒张,血管扩张,抑制调节温度的血管收缩,也可以引起患者体温降低[21]; ④ 心脏手术过程中需要对患者输注大量血液及体液,术中采用生理盐水进行胸腔冲洗均可能引起患者体温降低[22]。本研究通过在心脏手术过程中应用变温毯对患者进行保温处理,且在术中输注体液使对血液制品及体液进行预热处理,结果显示,在患者术中60、120 min及手术结束时,使用变温毯患者鼻咽温度显著高于对照组患者(P<0.05), 而2组HR及MAP均出现降低,且观察组各时间点HR及MAP均低于对照组,提示在心脏手术过程中手术时间长、术中麻醉药物使用、血液及体液输注均对患者体温有明显影响,体温降低会对血液循环造成影响,最终影响患者心脏功能,而观察组患者术中采用变温毯,不仅能够维持患者机体外表温度,还能对体外循环中血液进行复温,有利于维持患者机体内温度,降低体外循环对血液循环的影响,减少对心脏功能的影响。同时观察组患者在拔管时机、术后苏醒时间、术中失血量等均显著低于对照组,说明变温毯通过保持患者体温恒定,有利于促进机体麻醉药物的代谢,使患者快速苏醒,同时降低低体温对机体凝血功能影响,从而减少术中输血量。观察组患者寒颤、心动过速、低氧血症并发症发生率均低于对照组,提示在心脏手术术中对患者进行保温处理,有利于减少患者术后不良并发症的发生。
综上所述,心脏手术术中应用变温毯有利于维持患者体温稳定,缩短患者术后苏醒时间,减少术中失血量和术后不良反应的发生,值得临床推广使用。
[1] 黄一乐, 胡文娟. 手术患者术中低体温危险因素评价指标体系的构建[J]. 中国实用护理杂志, 2016, 32(35): 2727-2730.
[2] 张倩, 易杰, 黄宇光. 胸科手术患者术中低体温的危险因素[J]. 中华麻醉学杂志, 2015, 35(4): 397-400.
[3] 谢言虎, 陈旭, 吴运香, 等. 术中低体温危险因素分析[J]. 临床麻醉学杂志, 2016, 32(9): 925-927.
[4] 姜雪, 陈丽媛, 陈素兰, 等. 冲洗液温度对开胸手术患者生命体征及麻醉恢复期的影响[J]. 解放军护理杂志, 2011, 28(7): 16-18.
[5] 邱璇, 杨森, 宋波. 复合式保温护理对冠心病搭桥手术患者术后的影响[J]. 中国心血管病研究, 2016, 14(6): 572-574.
[6] 夏玲, 姜云, 肖美云, 等. 复合保温对高危患者胸科手术中低体温影响的研究[J]. 护士进修杂志, 2012, 27(16): 1448-1450.
[7] 罗勇, 张力, 王伟, 等. 全动脉化非体外循环冠状动脉搭桥术的临床应用[J]. 西部医学, 2013, 25(3): 357-359.
[8] 彭素云. 循证护理在心脏瓣膜置换术治疗中的效果探讨[J]. 国际医药卫生导报, 2012, 18(18): 2773-2775.
[9] 朱诗利, 张溪英, 屈双权. 新生儿胸腔镜手术的麻醉管理[J]. 医学临床研究, 2016, 33(6): 1232-1233.
[10] 姜升立. 围术期意外低体温的监测及预防[J]. 中华医院感染学杂志, 2013, 23(21): 5378-5380.
[11] 马素柯, 刘俊宝, 曹璐. 术中保温对妇科腹腔镜手术患者体温及凝血功能的影响[J]. 中国妇产科临床杂志, 2016, 17(2): 158-160.
[12] 朱儒红. 全身麻醉苏醒期患者寒战的护理干预[J]. 检验医学与临床, 2015, 12(3): 424-425.
[13] 郑彩娟. 肠道手术围术期低体温与手术部位感染关系研究[J]. 中华医院感染学杂志, 2013, 23(12): 2891-2892.
[14] 忻元峰, 张涛, 李钦传, 等. 体外循环心肌保护中心肌热成像数据与心肌能量代谢指标的相关性研究[J]. 中国心血管病研究, 2013, 11(9): 722-724.
[15] 张曙东, 王天策, 孙卫红, 等. 104例胸主动脉瘤手术的体外循环转流经验[J]. 中国体外循环杂志, 2012, 10(1): 36-40.
[16] 许旸晖, 陈小潍, 姜云. 体外循环术后患者体温监测方法的对比研究[J]. 护士进修杂志, 2013, 28(1): 64-66.
[17] 周岩, 王东信, 张锋. 全麻与硬膜外复合全麻对开胸手术患者术后并发症影响的比较[J]. 中华麻醉学杂志, 2015, 35(12): 1417-1421.
[18] 王果艳. 预防术中低体温对开胸手术患者麻醉恢复期的作用评价[J]. 内蒙古医科大学学报, 2015, 37(S1): 336-338.
[19] 陈京缦, 韩小红. 心脏直视手术围术期低体温和体温监测进展[J]. 护理研究, 2012, 26(31): 2887-2889.
[20] 朱勤春, 王春灵, 方玲. 循证护理预防开胸手术患者低体温的效果观察[J]. 中国临床医学, 2015, 22(6): 808-811.
[21] 吴桂芬, 周学颖, 李静. 开胸手术围术期低体温与手术部位感染的关系研究[J]. 中华医院感染学杂志, 2013, 23(9): 2084-2085.
[22] 吴荷玉, 王平, 高兴莲, 等. 深低温停循环手术围术期体温的监测研究[J]. 护理研究, 2013, 27(31): 3522-3523.
2017-02-01
R 472.3
A
1672-2353(2017)16-161-03
10.7619/jcmp.201716055

