水热法合成球花状二硫化钼及其电化学性能
李美娟沈舒宜罗国强张联盟
水热法合成球花状二硫化钼及其电化学性能
李美娟*,1沈舒宜1罗国强2张联盟2
(1武汉理工大学化学化工与生命科学学院化学系,武汉430070)
(2武汉理工大学材料复合新技术国家重点实验室,武汉430070)
采用二水钼酸钠(Na2MoO4·2H2O)和硫脲(CS(NH2)2)分别作为钼源和硫源,通过水热合成法获得球花状二硫化钼,其较佳的水热条件为:180℃下反应48 h,钼硫原子比为1∶4,反应物浓度为0.001 mol·L-1,在100 mL反应釜中的填充体积为90 mL。采用X射线衍射(XRD)、扫描电镜(SEM)和透射电镜(TEM)、对样品的物相和形貌进行了表征,并利用低温氮吸附BET模型测试了样品的比表面积。结果表明,合成的二硫化钼结晶性良好,平均粒径约为1 μm,比表面积约为87 m2·g-1,分布均匀且无明显团聚。通过循环伏安(CV)曲线、恒电流充放电曲线(GCD)、阻抗谱图(EIS)表征其电化学性能,测试表明:在3 mol·L-1KOH水相电解液中,单电极比电容可达130.6 F·g-1(扫速为5 mV·s-1)和110.9 F·g-1(电流密度为0.1 A·g-1),界面转移电阻Rct为0.33 Ω;循环1 000圈后比电容损失为14.7%。说明采用该水热法合成的二硫化钼可以成为超级电容器电极的理想材料。
二硫化钼;水热法;电化学性能
0 引言
近年来,层状过渡金属硫化物二硫化钼(MoS2)由于其优异的性能引起了众多研究者的关注[1]。MoS2具有类似石墨烯的层状结构,晶型分别是四方晶系(1T)、斜方对称晶系(3R)以及六方对称晶系(2H)。1TMoS2的结构特点是Mo原子与6个S原子形成八面体配位,每个Mo原子构成一个晶胞,表现出类金属性质。3R-MoS2结构为Mo原子是三棱柱配位,3个层单元构成1个晶胞;3R与1T均为亚稳相。2H晶系是MoS2最稳定的晶型,2H-MoS2中四价的Mo原子为三棱柱配位,2个S原子层中间夹1个Mo原子层,Mo、S原子之间以较强共价键结合形成单元层;而单元层之间则以微弱的范德华力结合,容易插进离子或分子且形成滑移面;该构型表现出半导体行为[2-5]。MoS2独特的结构和性能使其在工业润滑[6]、催化行业[7-8]、光电传感[9]和电化学储能等方面都有良好的应用前景[10-11]。电性能的运用主要体现在锂电池和电容器方面。MoS2在电化学储能器件上作为活性电极材料的应用得益于其独特的夹层结构,十分有利于电解质中离子的扩散与转移,达到存储及释放电子的目的,因此MoS2有望成为高能量密度电池和高功率密度超级电容器的电极材料[12],但在储能设备中的应用因其半导体特性而受到影响。针对如何制备出性能优良、成本低、环境友好的MoS2已做了大量研究,目前较为常见的方法有气相沉积法[13]、锂离子插层剥离法[14]、超声剥离法[15]和水热法等[16];一些新型的方法也被用来制备具有特定结构的MoS2材料,如:Choudhary等通过磁控溅射法在铜箔上沉积纳米MoS2薄膜[17],Yang等则先用电化学法将钼箔氧化后再硫化,制备出具有核壳结构的MoS2纳米列阵[18]。研究表明,不同形貌的MoS2作为超级电容器电极材料时均表现出较佳的电化学性能。其中水热法作为一种操作简便、反应温度低且污染性小的化学合成方法,成为制备MoS2的常用方法。如Krishnamoorthy等采用水热法、以钼酸铵和硫脲作为前驱体制备出球花状MoS2,并在Na2SO4电解液中测得其比电容为106 F·g-1(扫速5 mV·s-1)[19]。但水热合成条件也需要精细控制,否则合成的产物结晶性较差,且容易团聚。为解决此类问题,田野等通过在(NH4)6Mo7O24·4H2O和Na2S·9H2O的水热反应体系中加入微量的十二烷基苯磺酸钠表面活性剂,有效阻止了MoS2纳米棒的团聚[20];Ma等则通过退火处理来提高水热反应产物的结晶性[21]。但是表面活性剂的添加会降低产物的纯度,而热处理过程又增加了工艺的复杂程度。为此,本论文采用一种更为简便的水热合成方法,以二水钼酸钠和硫脲作为钼源和硫源,通过调控水热反应多方面影响因素,兼顾其结晶性与分散性,制备出规整球花状的MoS2晶体。论文着重研究了在较佳合成工艺下得到的MoS2的电化学性能,包括循环伏安(CV)曲线、恒电流充放电(GCD)和阻抗(EIS)等。
1 实验方法
1.1 实验
本论文采用正交试验法探究反应温度T、反应时间t、反应浓度C以及钼硫原子比等4因素对合成球花状MoS2的影响,以寻求最优水平组合。实验过程中所用化学试剂均为分析纯试剂,未经过二次纯化处理。
按照制备MoS2的四因素三水平试验表(见表1)将Na2MoO4·2H2O和CS(NH2)2以一定比例和浓度溶解在去离子水中,混合搅拌10 min后,转移至100 mL聚四氟乙烯内胆的不锈钢水热反应釜中密封,经水热反应后自然冷却至室温。小心刮下反应釜内壁的黑色沉积物,用去离子水和乙醇交叉洗涤3次,通过离心分离收集产物,最后将产物置于真空干燥箱内,80℃干燥12 h。

表1 制备MoS2的四因素三水平试验表Table1 Four factors and Three horizontal test of the preparation of MoS2
1.2 测试
采用X射线衍射分析仪(XRD,型号D/MAX-Ⅲ,日本Rigaku)来分析样品物相,测试条件为:以Cu靶Kα线为辐射源,波长为0.154 18 nm,工作电压和电流分别为40 kV和40 mA,步长0.02°,扫速4°·min-1,扫描范围5°~90°;利用扫描电镜(SEM,型号S-3400N,日本Hitachi)和场发射扫描电镜(FESEM,型号Quanta-250,美国FEI)观察样品形貌和分散状态,测试加速电压为15 kV;通过透射电子显微镜(TEM,型号JEM-2010,日本Jeol)观察合成晶粒的内部结构,测试加速电压为200 keV;采用多通道比表面积及孔径分析仪(型号TriStarⅡ3020,美国Micromeritics)测试样品的N2吸附-脱附。
采用电化学工作站(型号660D,上海辰华)测试所制备MoS2的电化学性能。将制备得到的MoS2试样、乙炔黑和60%的聚四氟乙烯水溶液按18∶1∶1的质量比称量,在研钵内混合均匀;然后取10 mg左右碾压成片,夹在两泡沫镍之间直接压合,并在80℃真空干燥12 h后制备成电极片备用。测试参比电极为Hg/HgO电极,对电极为铂片电极。在浓度为3 mol·L-1的KOH水溶液中,对电极片分别进行循环伏安扫描(CV)、恒电流充放电(GCD)、电化学阻抗谱(EIS)测试。
2 结果与讨论
2.1 合成产物的物相表征
通过正交试验,综合产物形貌与结晶性,确定水热法合成MoS2的较佳工艺参数为(见支持文件):180℃下反应48 h,反应物浓度0.001 mol·L-1,钼硫原子比为1∶4。图1是水热法合成的MoS2的XRD图,其衍射峰位与峰强均与六方MoS2的标准PDF卡片(PDF No.37-1492)相吻合且无其他杂峰,证明制备的产物是较为纯净的2H-MoS2;衍射峰峰位显著、峰形尖锐,说明合成产物的结晶性较好;而其中(002)和(100)晶面对应的峰强最为显著,说明MoS2层与层之间的堆垛良好。分析认为,水热合成的反应分成两个步骤:首先是硫脲在高温高压下和水反应,分解生成硫化氢(H2S),反应式为:
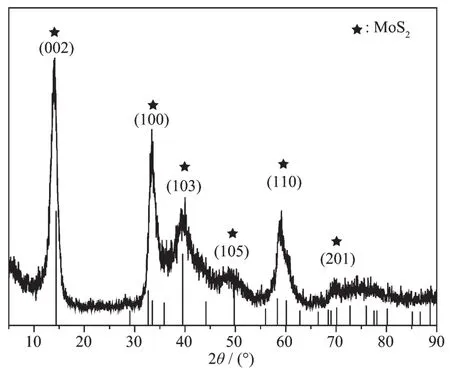
图1 水热法合成MoS2的XRD图Fig.1 XRD pattern of as-prepared MoS2

然后H2S作为硫源和还原剂,将MoO42+中的Mo还原成Mo并生成MoS2,反应式为:
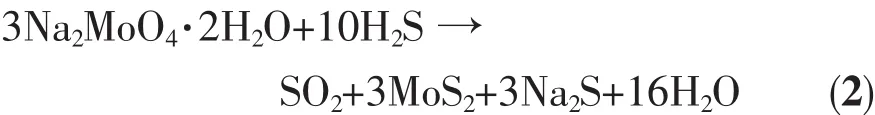
总的反应式为:
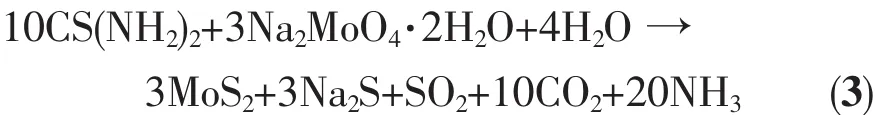
反应过程中产生的CO2和NH3气体提高了密闭的反应釜内的压力,并有助于提高合成产物的结晶性[22]。
2.2 MoS2的形貌表征

图2 水热合成球花状MoS2的SEM照片Fig.2 SEM image of flower sphere-like MoS2

图3水热合成MoS2的TEM照片Fig.3 TEM images of as-prepared MoS2
图2 是本实验中合成的MoS2的SEM图。SEM观察表明,所合成的MoS2呈球形,为表面粗糙的球花状产物,平均直径约为1 μm,大小比较均匀,无团聚现象;分析认为,这是由于硫脲还原性并不是特别强,有利于反应初期形成多个晶核,而后晶粒均匀生长。TEM图片显示球花状的MoS2是由许多薄层纳米片蜷曲而成(如图3a所示),这是由于MoS2纳米片边缘悬挂了很多不饱和键,能量较高,为降低表面能,纳米片会自动弯曲蜷缩成球花状[23];高分辨TEM图片中可以观察到构成球花的纳米片厚度约为几个纳米(如图3b所示),堆垛良好,晶格间距约为0.614 nm,对应的是(002)晶面,与XRD测试结果中最强峰位14.4°相符。在球花边缘的纳米片尤其是层弯曲处晶格出现了一定程度的收缩,这是表面张力作用导致的边缘的晶格常数小于体材料晶格常数。
测试表明所合成的MoS2比表面积为87 m2· g-1,相较于其他文献[24]中所报道的比表面积有显著增加,这是由于本实验中所制备的MoS2二维纳米片层蜷曲且形成了规整的球花形,而且单个球花之间基本无团聚现象,这极大地提高了其比表面积。
2.3 水热合成MoS2的电化学性能
图4a为工作电极在-1.0~-0.15 V电位窗口条件下,扫速分别为5、10、20、30、50、100 mV·s-1时MoS2电极片的循环伏安曲线。从循环伏安曲线上可以观察到:当扫速较快时,CV闭合曲线类似矩形,这是因为在电压变化过程中电极未发生电子得失反应,表现出双电层电容行为;当扫速逐渐减慢时,CV曲线出现了微小的氧化还原峰。分析认为,这是因为扫速慢时电压变化较为缓慢,有利于电解质中的离子向电极表面接近和转移,有效接触比较充分;由于MoS2活性材料尺寸较小,边缘悬挂有较多的不饱和化学键,容易结合和释放电子,发生氧化还原反应,因此低扫速下的CV曲线表现出赝电容和双电层电容两种电容特性。图4b显示的是从不同扫速下CV曲线中获得的MoS2电极片材料的比电容,当扫速为5、10、20、30、50、100 mV·s-1时,比电容分别为130.6、104.9、84.4、62.4、45.5、27.1 F· g-1。可以发现,随着扫速加快,材料的比电容降低。这是因为扫速降低,KOH电解液有充分的时间与薄层边缘MoS2发生氧化还原反应,增大了电子储存量,使得材料同时具备双电层电容和法拉第电容,导致比电容的增加。

图4MoS2在不同扫速下的CV曲线图(a)和相应的比电容(b)Fig.4 (a)CV curves and(b)corresponding specific capacitance at different scan rate of the as-prepared MoS2
图5 是测试的MoS2电极片交流阻抗的Nyquist曲线图,测试频率范围为10-3~105Hz,放大后高频区出现的半圆形能体现活性材料与电解液的界面电荷转移阻力,反映材料在充放电时电荷转移的难易程度,半圆直径越小,则界面转移电阻Rct越小,表明材料的导电性能越好。通过放大图反映的半圆直径可以看出,在所选择的水热工艺条件下合成的MoS2,其Rct约为0.33 Ω,具有较好的导电性。分析认为,所合成的球花状MoS2具有较大的比表面积,这有利于减小离子和电子在充放电过程中转移和扩散的时间;同时其较高的结晶性也有利于电子在材料内部有序移动,降低电子的损失。

图5MoS2在频率范围10-3~105Hz时的Nyquist曲线图Fig.5 Nyquist plot in the frequency range of 10-3~105Hz
图6 是在电流密度分别为0.1、0.2、0.3、0.5、1 A·g-1时的恒电流充放电曲线,比电容分别为110.9、102.6、88.5、65.6、46.7 F·g-1。从图中可以看出三角形充放电曲线展现出良好的线性。当电流密度为0.1和0.2 A·g-1时,放电曲线存在2个电压阶段,快速电压降(-0.2~-0.35 V)和缓慢电压衰减(-0.35~-1 V),分别代表了双电层和赝电容2种放电过程,这说明在低电流密度下,电解液中的离子能更加充分地进入电极内部并在其中移动,提高了电极的利用率。电流密度为0.3、0.5、1 A·g-1时,充放电曲线对称性良好,充电与放电时间基本一致,无明显电压降,更多的展现出双电层电容的特性。
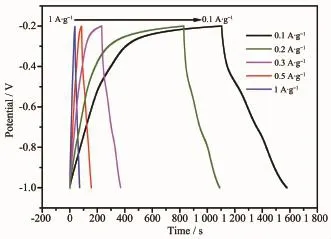
图6MoS2在不同电流密度下的恒电流充放电图Fig.6 GCD curves at different current density
图7 显示的是球花状MoS2在1 A·g-1电流密度下充放电循环1 000圈时的比电容变化,结果表明,充放电500次后其电容损失仅为4.3%,1 000次循环后的比电容损失为14.7%,表现出较好的电化学稳定性。图8是循环充放电完成后活性材料的SEM图片。观察显示,在1 000次充、放电循环后的电极片样品中,残留有一定量的导电剂乙炔黑和粘结剂聚四氟乙烯(图中的碎片状物质);原球花状的MoS2具有一定程度的团聚和变形,团聚主要是在制电极片过程中粘结剂和电极材料经反复研磨后的紧密结合造成的,而反复充放电导致MoS2表面部分片状结构出现膨胀突起。但从整体上来看,仍基本保持了MoS2的球形形貌,其球花片状依然清晰可现,表明材料的三维球花形貌对于二维纳米片起到了支撑作用,使其具有较好的机械强度。
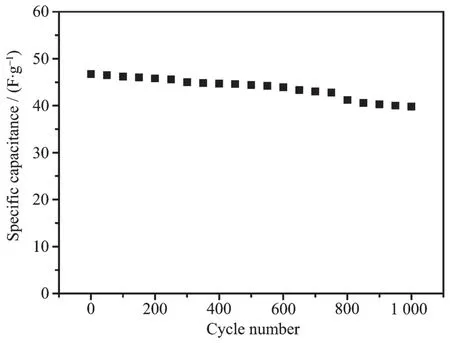
图7 MoS2在1 A·g-1电流密度下循环1 000圈比电容变化图Fig.7 Capacitance retention behavior of as-prepared MoS2

图8 循环测试后球花状MoS2的SEM图Fig.8 SEM image of flower sphere-like MoS2after charge-discharge cycling
3 结论
本研究中以Na2MoO4·2H2O和CS(NH2)2为钼源和硫源,通过水热合成方法制备出结晶性较好的MoS2晶体。XRD检测表明,合成产物是2H-MoS2;SEM和TEM观察发现,合成的MoS2呈球花状,直径约为1 μm,粒径比较均匀且分散性良好,无团聚现象。比表面积约为87 m2·g-1。经电化学性能测试发现,当CV扫速为5 mV·s-1时,比电容量可达130.6 F·g-1;电流密度为0.1 A·g-1时比电容为110.9 F·g-1;循环1 000圈后电容损失为14.7%;EIS测试得到材料界面转移电阻Rct约为0.33 Ω,具有较高的电导率;GCD曲线三角形的对称性良好,充电与放电时间基本一致,无明显电压降。因此所制备MoS2的综合电化学性能较好,可以成为超级电容器的电极材料。
Supporting information is available at http://www.wjhxxb.cn
[1]Hu K H,Hu X G.Mater.Sci.Technol.,2009,25(3):407-414
[2]ZHANG Wen-Zheng(张文钲).China Molybdenum Ind.(中国钼业),1997(z1):130-132
[3]Frindt R F.J.Appl.Phys.,1966,37(4):1928-1929
[4]Wypych F.J.Chem.Soc.,Chem.Commun.,1992,19(19): 1386-1388
[5]Yue Q,Chang S,Qin S,et al.Phys.Lett.A,2013,377(19/ 20):1362-1367
[6]Chermette H,Rogemond F,Beqqali O E,et al.Surf.Sci., 2001,472(1/2):97-110
[7]Rao B G,Matte H S S R,Chaturbedy P,et al.ChemPlusChem, 2013,78(5):419-422
[8]Yang Y,Fei H,Ruan G,et al.Adv.Mater.,2014,26(48): 8163-8168
[9]Eda G,Yamaguchi H,Voiry D,et al.Nano Lett.,2011,11 (12):5111-5116
[10]Wang J Z,Lu L,Lotya M,et al.Adv.Energy Mater.,2013,3 (6):798-805
[11]Acerce M,Voiry D,Chhowalla M.Nat.Nanotechnol.,2015, 10(4):313-318
[12]XU Dou-Dou(徐豆豆),WANG Xian-Bao(王贤宝),QIU Jia-Le(邱家乐),et al.Chin.J.Colloid Polym.(胶体与聚合物), 2015(1):37-40
[13]Jia M S,Loh K P.Electrochem.Solid-State Lett.,2007,10 (11):A250-A254
[14]Joensen P,Frindt R F,Morrison S R.Mater.Res.Bull., 1986,21(4):457-461
[15]Coleman J N,Lotya M,O Neill A,et al.Science,2011,331 (6017):568-571
[16]Zhou X,Xu B,Lin Z,et al.J.Nanosci.Nanotechnol.,2014, 14(9):7250-7254
[17]Choudhary N,Patel M,Ho Y H,et al.J.Mater.Chem.A, 2015,3(47):24049-24054
[18]Yang Y,Fei H,Ruan G,et al.Adv.Mater.,2014,26(48): 8163-8168
[19]Krishnamoorthy K,Veerasubramani G K,Radhakrishnan S, et al.Mater.Res.Bull.,2014,50(50):499-502
[20]Tian Y,Zhao J,Fu W,et al.Mater.Lett.,2005,59(27):3452-3455
[21]Ma L,Xu L M,Zhou X P,et al.Mater.Lett.,2014,132:291-294
[22]SHI Er-Wei(施尔畏),XIA Chang-Tai(夏长泰),WANG Bu-Guo(王步国),et al.Chinese J.Inorg.Chem.(无机化学学报),1996,11(2):193-206
[23]Wang X,Ding J,Yao S,et al.J.Mater.Chem.A,2014,2 (38):15958-15963
[24]Huang K J,Zhang J Z,Shi G W,et al.Electrochim.Acta, 2014,132(3):397-403
Hydrothermal Synthesis of MoS2Flower-like Spheres with Electrochemical Performances
LI Mei-Juan*,1SHEN Shu-Yi1LUO Guo-Qiang2ZHANG Lian-Meng2
(1School of Chemistry,Chemical Engineering and Life Science,Wuhan University of Technology,Wuhan 430070,China)
(2State key Lab of Advanced Technology for Materials Synthesis and Processing, Wuhan University of Technology,Wuhan 430070,China)
A simple but useful hydrothermal method is developed to prepare molybdenum disulfide(MoS2)flowerlike spheres by sodium molybdate dehydrate(Na2MoO4·2H2O)and thiocarbamide(CS(NH2)2).In this work,the appropriate hydrothermal condition is at 180℃reaction temperature for 48 h and the atomic ratio of S and Mo is 1:4 in 0.001 mol·L-1aqueous solution.The morphologies and microstructures of as-prepared MoS2are characterized by X-ray diffraction(XRD),scanning electron microscopy(SEM),transmission electron microscopy(TEM)and specific surface area test method(BET).Results indicate that the average diameter of as-prepared products is about 1 μm with good crystallinity and dispersibility,and their specific surface area is about 87 m2·g-1.In order to character the electrical properties of MoS2,the electrochemical performance was studied by cyclic voltammetry (CV),galvanostatic charge-discharge cycling(GCD)and electrochemical impedance spectroscopy(EIS).Analysis results show that in 3 mol·L-1KOH electrolyte,the specific capacitance of single electrode is 130.6 F·g-1at 5 mV·s-1scan rate and 110.9 F·g-1at 0.1 A·g-1current density.The charge-transfer resistance(Rct)is of 0.33 Ω. The loss of specific capacitance is 14.7%after 1 000 cycles.These electric properties illustrate the MoS2prepared by hydrothermal processing can act as an ideal material for supercapacitor electrode.
molybdenum disulfide;hydrothermal method;electrochemical performances
O614.61+2
A
1001-4861(2017)09-1521-06
10.11862/CJIC.2017.201
2017-05-07。收修改稿日期:2017-07-28。湖北省自然科学基金项目(No.2014CF258)资助项目。*
。E-mail:meijuanli@whut.edu.cn

