应用血管紧张素转换酶抑制剂不良反应的特征分析
徐朝飞
应用血管紧张素转换酶抑制剂不良反应的特征分析
徐朝飞1
目的 分析应用血管紧张素转换酶抑制剂(ACEI)的不良反应特征。方法 选取高邮中医医院心内科于2011年5月~2016年5月收治的应用ACEI治疗后发生不良反应的患者412例,其中男性243例,女性169例,年龄18~75岁,平均(52.5±4.9)岁。回顾性分析入组患者的年龄、用药情况、不良反应表现、发生时间、治疗情况等。结果 本组患者中,年龄<30岁和30~39岁比例较小,主要分布在40~49岁、50~59岁、60~69岁、≥70岁。卡托普利致不良反应的比例最高,为77.91%;其次为贝那普利与依那普利分别为8.74%、7.04%;雷米普利、福辛普利、培哚普利、赖诺普利致不良反应比例较低,分别为2.91%、1.46%、1.46%和0.49%。ACEI不良反应的临床表现以喘憋、咳嗽、咽部不适为主,主要累及呼吸系统,占65.05%;7.77%的患者不良反应累及皮肤,临床表现为皮疹、水肿、炎症、溃疡等;7.77%累及泌尿生殖系统,有尿频、蛋白尿、血尿等表现。另外还有7.04%累及心血管系统,4.85%累及血液系统,4.85%累及消化系统,2.18%累及关节肌肉。412例患者中,26例在用药当天即出现不良反应,占6.31%,386例在用药第2 d后出现不良反应,占93.69%,不良反应的平均出现时间为(16.9± 10.4)d。患者经对症治疗或停药处理后,绝大多数症状明显缓解并逐渐消失,其中30例患者复用药物后再次发生相同不良反应。结论 应用ACEI发生的不良反应表现多样、原因复杂,多数需对症治疗或停药才可消失,临床用药过程中要密切监测不良反应,提高用药安全性。
血管紧张素转换酶抑制剂;心内科;不良反应;合理用药
血管紧张素转换酶抑制剂(ACEI)是高血压治疗指南中的一线药物,其通过抑制循环系统及组织局部的血管紧张素转换酶活性,减少血管紧张素生成达到降压效果[1]。临床实践证实[2],ACEI对各类高血压都有显著疗效,并且长期用药并未增加机体耐药性。目前,ACEI已逐步成为心内科的常用药物,且ACEI引起的不良反应也逐步引起人们重视。越来越多的研究报道,ACEI治疗心内科疾病可引起不良反应,并且个体差异明显,有的患者甚至死亡。本研究旨在分析ACEI的不良反应特征,为临床合理用药提供指导。
1 资料与方法
1.1 研究对象 选取高邮中医医院心内科于2011年5月~2016年5月收治的应用ACEI治疗后发生不良反应的患者412例,其中男性243例,女性169例,年龄18~75岁,平均(52.5±4.9)岁。所有患者不良反应均在用药后出现,在停药后消失,复用药后又出现,停药后又消失,除外其他原因引起的不良反应。原发性高血压211例,心肌梗死27例,心力衰竭18例,慢性肺源性心脏病34例,风湿性心脏病51例,冠心病71例。
1.2 方法 收集入选者的临床资料,包括年龄、疾病类型、用药名称、用药方法、不良反应发生时间、不良反应临床表现、不良反应治疗及转归等情况。
1.3 统计学方法 计数资料以例数/百分比表示。
2 结果
2.1 发生不良反应患者年龄分布 本组患者中,年龄<30岁和30~39岁比例较小,主要分布在40~49岁、50~59岁、60~69岁、≥70岁(表1)。
2.2 用药情况 卡托普利致不良反应的比例最高,为77.91%;其次为贝那普利与依那普利分别为8.74%、7.04%;雷米普利、福辛普利、培哚普利、赖诺普利致不良反应比例较低,分别为2.91%、1.46%、1.46%和0.49%(表2)。
2.3 不良反应表现及受累系统/器官 ACEI不良反应的临床表现以喘憋、咳嗽、咽部不适为主,主要累及呼吸系统,占65.05%;7.77%的患者不良反应累及皮肤,临床表现为皮疹、水肿、炎症、溃疡等;7.77%累及泌尿生殖系统,有尿频、蛋白尿、血尿、外因瘙痒等表现。另有7.04%累及心血管系统,4.85%累及血液系统,4.85%累及消化系统,2.18%累及关节肌肉(表3)。

表1 不良反应患者的年龄分布
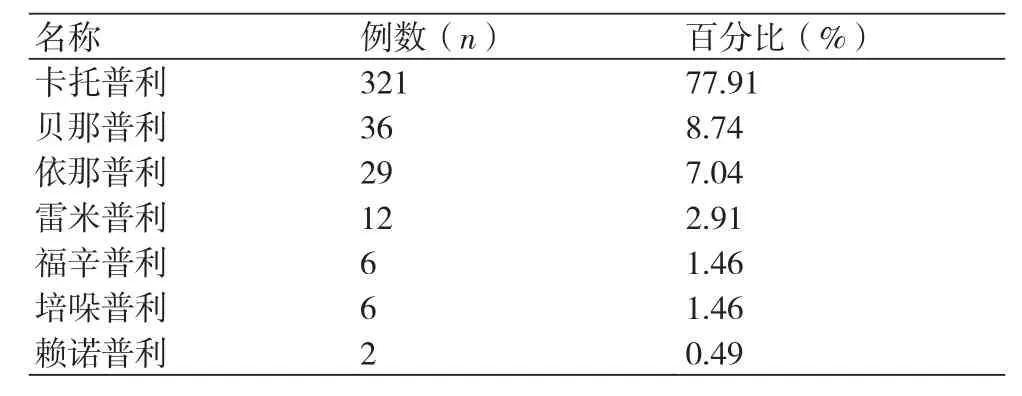
表2 患者的ACEI用药情况
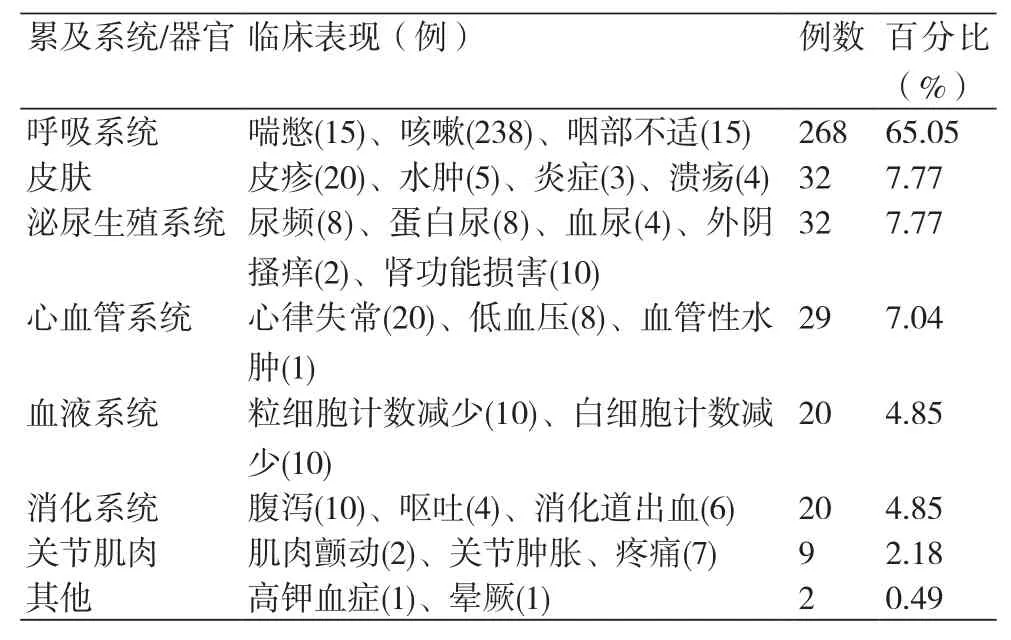
表3 ACEI不良反应表现及受累系统/器官
2.4 不良反应发生时间 412例患者中,26例在用药当天即出现不良反应,占6.31%,386例在用药第2 d后出现不良反应,占93.69%,不良反应的平均出现时间为(16.9±10.4)d。其中呼吸系统受累不良反应最早在用药3 d后出现,最晚在用药2个月后出现,大部分在用药后1个月内出现;心血管系统受累不良反应最早在用药2 d后出现,最晚在用药10 d后出现;皮肤受累不良反应最早在用药30 min后出现,最晚在用药25 d后出现。
2.5 不良反应的治疗与转归情况 本组患者经对症治疗或停药处理后,绝大多数患者症状明显缓解并逐渐消失,其中30例患者复用药物后再次发生相同不良反应症状,1例因心律失常控制不理想而最终引发死亡。
3 讨论
ACEI自问世以来在临床上得到了广泛应用,已从第1代发展至第2代,该药物也从早期的单纯治疗高血压病逐渐延伸到了肺心病、心力衰竭、肾衰竭等多种疾病的治疗中。
ACEI虽然在多种疾病的临床治疗中都具有显著优势,但其存在着一定缺陷,有较为明显的不良反应。有文献报道[3],应用ACEI治疗的不良反应发生率较高,特别是一些年龄偏大的患者。本研究中,发生不良反应的患者年龄<30岁和30~39岁比例较小,大部分为40岁以上。可能与心内科患者中老年居多有关;另一方面,也可能是随着年龄增长,机体对药物的排出、利用减弱,更容易发生药物不良反应[4]。ACEI的不良反应可累及多个系统,如呼吸系统、心血管系统、血液系统、消化系统、皮肤等。本研究结果显示,ACEI不良反应累及呼吸系统、皮肤、泌尿系统、心血管系统、血液系统、消化系统、关节肌肉的占比分别为65.05%、7.77%、7.77%、7.04%、4.85%、4.85%、2.18%。这一结果与国内多篇文献报道[5,6]相符,说明ACEI不良反应几乎可累及人体所有的器官。ACEI的一般不良反应包括皮肤瘙痒、皮疹、恶心、头痛、眩晕、腹泻、嗜酸细胞计数升高、肝功能异常等等。本研究中,共有7.77%的患者出现了皮疹、水肿、炎症、溃疡等;65.05%出现喘憋、咳嗽、咽部不适。咳嗽是ACEI最为常见的一种不良反应,有文献报道[7]ACEI用药后的咳嗽发生率可达到15%~35%,且以卡托普利的咳嗽发生率最高。另外,首剂量低血压也是ACEI患者的常见不良反应,好发于心力衰竭、血容量不足及老年患者,临床可通过减少起始剂量来避免首剂量低血压的发生[8]。本研究中,有8例因首剂量偏大而低血压,调整用药剂量后,症状缓解。由于ACEI可降低肾小球动脉张力,降低肾小球滤过率而引发肾功能损害。本组患者中共有10例发生肾功能损害,占2.43%。另外,由于ACEI具有保钾、抑制醛固酮分泌的作用,所以对于一些伴有糖尿病、肾功能恶化的患者,使用ACEI较易发生高钾血症。本组患者中发生高钾血症1例,伴明显的糖尿病肾病。研究结果还显示,ACEI不良反应的平均出现时间为(16.9±10.4)d。说明ACEI不良反应并非即时发生,多数都是在用药数天后发生,临床应当持续监测。
用药过程中要注意观察患者情况,还应根据患者的个体差异合理调整用药剂量,以减少药物不良反应的发生[9]。对于伴有肾功能不全、血钾水平偏高、接受透析治疗的患者,应当考虑使用ACEI的替代药物,以免增加不良反应风险。总之,心内科应用ACEI的不良反应表现多样、原因复杂,多数症状需对症治疗或停药才可消失,临床在用药过程中要密切监测不良反应情况,积极防治,合理用药,提高ACEI的用药安全性。
[1] 赵祺,赵林凤. 血管紧张素转换酶抑制剂在老年心力衰竭患者中的应用[J]. 中国老年学杂志,2012,32(1):210-2.
[2] 刘志,华琦. 血管紧张素转换酶抑制剂和β受体阻滞剂在慢性心力衰竭中的应用[J]. 中华老年心脑血管病杂志,2012,14(4):447-8.
[3] 杨丙华. 简述血管紧张素转换酶抑制剂的合理应用[J]. 中外医学研究,2014,12(15):153-4.
[4] 王晓华,刘玉敏. 心内科五类抗高血压药物的临床应用分析[J]. 医学综述,2014,20(5):948-50.
[5] Tung YT,Lee BH,Liu CF,et al. Optimization of culture condition for ACEI and GABA production by lactic acid bacteria[J]. Journal of Food Science,2011,76(9):M585-M591.
[6] 王金玉. 血管紧张素转换酶抑制剂不良反应及处理方法[J]. 临床医学,2012,32(7):102-3.
[7] 郑海燕. 血管紧张素转换酶抑制剂和血管紧张素Ⅱ受体拮抗剂联用治疗糖尿病肾病的不良反应的临床研究[J]. 大家健康,2014,8(24):159.
[8] 陈美光. 血管紧张素转换酶抑制剂致不良反应分析及临床合理用药[J]. 临床合理用药杂志,2016,9(6):125-6.
[9] 刘瑞婵,刘瑞丽. 血管紧张素转换酶抑制剂的不良反应及防治对策[J]. 中国药物与临床,2012,12(10):1311-3.
本文编辑:姚雪莉
Features of adverse reactions after treatment with angiotensin converting enzyme inhibitor
Xu Chaofei. Gaoyou Hospital of Chinese Medicine, Gaoyou 225600, China.
Objective To analyze the features of adverse reactions after treatment with angiotensin converting enzyme inhibitor (ACEI). Methods The patients (n=412, male 243, female 169, aged from 18 to 75 and average age=52.5±4.9) with adverse reactions after treatment with ACEI were chosen from the Department of Cardiology in Gaoyou Hospital of Chinese Medicine from May 2011 to May 2016. The age, drug administration, manifestations and occurrence time of adverse reactions and treatment conditions were retrospectively analyzed in all patients. Results The percentages of patients aged<30 and from 30 to 39 were lower, and patients’ ages mainly distributed from 40 to 49, 50 to 59, 60 to 69 and over 70. The proportion of adverse reactions induced by captopril was the highest (77.91%), and that by benazepril was 8.74% and by enalapril was 7.04%. The proportions of adverse reactions induced by ramipril (2.91%), fosinopril (1.46%), perindopril (1.46%) and lisinopril (0.49%) were lower. The clinical manifestations of adverse reactions induced by ACEI were mainly wheezing, coughing and throat discomfort, and mainly involved the respiratory system, accounting for 65.05%. The adverse reactions involved skin in 7.77% of patients, and clinical manifestations included rash, edema, inflammation and ulcer. The adverse reactions involved the urogenital system in 7.77% of patients, and clinical manifestations included frequent urination, proteinuria and hematuresis, and involved the cardiovascular system in 7.04% of patients, blood system in 4.85%, digestive system in 4.85%, and joints and muscle in 2.18%. Among 412 patients, there were 26 (6.31%) with adverse reactions at medication day and 386 (93.69%) with adverse reactions after 2 d, and the average time was (16.9±10.4) d. The symptoms of adverse reactions were relieved and disappeared in the most of patients after treatment or stopping medication, while there were 30 patients had the same adverse reactions after re-medication. Conclusion The manifestations of adverse reactions induced by ACEI are multiple and causes are complex, which will disappear after symptomatic treatment or stopping medication. The adverse reactions should be closely monitored in clinic for improving safety of medication.
Angiotensin converting enzyme inhibitor; Department of cardiology; Adverse reactions; Rational drug administration
R541
A
1674-4055(2017)08-0969-03
1225600 高邮,高邮中医医院
10.3969/j.issn.1674-4055.2017.08.21

