2024-T3铝合金在不同酸性水溶液中的电化学行为
陈跃良,王安东,卞贵学,张 勇
(海军航空工程学院,山东 青岛 266041)
2024-T3铝合金在不同酸性水溶液中的电化学行为
陈跃良,王安东,卞贵学,张 勇
(海军航空工程学院,山东 青岛 266041)
采用动电位极化和交流阻抗两种电化学测量技术,结合表面微观形貌观察,研究了2024-T3铝合金在不同种酸(包括乙酸、硫酸和盐酸)以及不同pH值水溶液中的电化学行为。结果表明:随pH值降低,合金自腐蚀电位负移,自腐蚀电流密度和腐蚀速率增大,合金表面钝化膜越易遭到破坏,溶液的腐蚀作用越强,且在不同pH值下,阴极极化过程的控制反应有所不同;在相同pH值下,以盐酸水溶液的腐蚀作用最强,硫酸水溶液相近但次之,乙酸水溶液最弱,这是酸的不同水解能力和氯离子的存在共同导致的;铝合金表面钝化膜的存在使得其在不同环境中的电化学行为表现不同,酸性条件下钝化膜失稳溶解,合金基体裸露并与溶液直接接触发生反应,而弱酸性条件下,钝化膜则能够保持相对完整性,对合金基体起到一定保护作用。
铝合金;酸;pH值;电化学;腐蚀
0 引言
实验室加速腐蚀试验是对工程材料及结构进行耐蚀性能评估和腐蚀行为研究的重要方法,其优点在于可大大缩短试验周期,降低研究成本并提高工作效率。需要注意的是,该方法中非常重要的一环是对加速腐蚀环境的酸性(包括酸的类型和pH值两方面)进行调整,这直接关乎到试验成败[1-2]。加速腐蚀环境的酸性通常会根据试验目的、相关试验标准或者编制的加速腐蚀环境谱等来确定,现多选用CH3COOH、HH2SOH4、HCl等调节。那么,不同酸性的加速腐蚀溶液对于结构材料的腐蚀行为有何影响,是否会造成其腐蚀机理的改变,哪种加速腐蚀方法能够获得最接近于其在真实服役环境中的腐蚀效果,诸如此类,都是开展加速腐蚀试验前需要考虑的重要问题[3-5]。这有助于合理选择并改进现有加速腐蚀试验方法,以达到更为接近实际腐蚀情况、获得更为可靠耐蚀性数据的目的。然而,目前关于结构材料在不同pH值腐蚀环境中腐蚀行为变化规律的研究较多,但其在不同种酸调节环境中腐蚀行为的变化规律却鲜见于报道。
海军飞机尤其是舰载机通常暴露在湿热、盐雾及工业废气等极易诱发腐蚀的恶劣环境中,腐蚀问题是其结构强度及寿命评估中的重要内容[6-8]。2024铝合金因具有较高强度和良好的切削加工性能而常用于海军某型飞机的蒙皮、隔框、翼肋和翼梁等处[9]。作为重要结构材料,其腐蚀损伤问题历来受到密切关注。通常,该铝合金表面在空气中会自发形成厚度为几纳米的氧化膜,称之为钝化膜[10],主要成分为Al2O3·H2O或Al2O3,对合金基体起保护作用,使其具有一定耐蚀性[11-12]。但在该飞机实际服役过程中,2024铝合金结构往往会出现不同程度的局部腐蚀,且在不同环境中的腐蚀行为和腐蚀机理也存在较大差异。这与其表面钝化膜在不同介质中的稳定性密切相关[13]。以2024-T3铝合金为研究对象,使用CH3COOH、H2SO4和HCl等3种酸配置不同pH值的水溶液,测量合金在其中的极化曲线、交流阻抗谱及表面微观形貌,并对所得结果进行对比、分析,研究不同酸性条件对2024-T3铝合金表面钝化膜稳定性及电化学行为的影响。
1 试验
1.1 电极制备
制备电极所选用的材料为2024-T3铝合金薄板,厚度约为3 mm,主要化学成分见表1[11]。对铝板进行线切割得到均匀的10 mm×10 mm×3 mm大小试样,将其中一个10 mm×10 mm面预留为工作面,从另一个10 mm×10 mm面引出铜导线,并用环氧树脂将非工作面绝缘封装在直径为3 cm的PVC管内;待环氧树脂完全固化后,使用万用表测量工作面与铜导线间电阻,若电阻值较小,则表明电极导通正常;使用水砂纸将电极工作面逐级打磨至1200#,一般来说,工作面越平整,测得的数据也就越平滑[14];打磨完成后,使用无水乙醇和丙酮对试样进行清洗、除油,烘干后静置于干燥皿中。
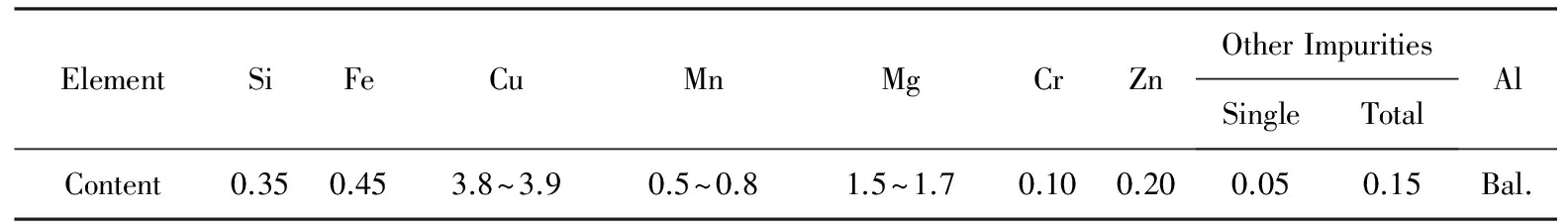
表1 2024-T3铝合金主要化学成分 (质量分数 /%)
1.2 试验方法
使用CH3COOH、H2SO4、HCl等3种不同酸以及去离子水,在烧杯中分别配制pH值为3、4、5、6的水溶液1 L,充分搅拌;将盛有上述溶液的烧杯置于25 ℃恒温水浴箱中;待温度恒定后,将电极试样(工作电极WE)、饱和甘汞电极(参比电极RE)以及铂电极(对电极CE)置于烧杯中,没于溶液下,并正确接入PARSTAT4000电化学综合测试仪,组成经典三电极体系[14];测量过程中,使用安装有VersaStudio软件的计算机进行数据采集。
采用动电位极化方法测量极化曲线,扫描范围为相对开路电位-0.35~0.4 V,扫描速率为1 mV/s,得到Tafel极化曲线;对电极表面阻抗开展测量,激励信号是幅值为10 mV的正弦波,频率范围为100 000~0.01 Hz,得到Nyquist图;在电化学测量前、后,使用KH-7700体视显微镜对电极表面形貌进行观测并拍照记录。
2 结果及分析
2.1 极化曲线
图1为2024-T3铝合金在同一pH值、不同种酸的水溶液中的极化曲线。当pH值为3时,无论是在CH3COOH、H2SO4还是HCl溶液中,合金的阳极化过程均有较为明显的钝化膜溶解区,即过低的pH值使电极表面钝化膜溶解而不能稳定存在。在膜溶解段,电流密度随着阳极过电位的增加而迅速增大。此时,因钝化膜遭受破坏,合金基体裸露,铝合金的阳极极化行为受活性溶解过程控制[14],故极化曲线基本上反映了铝合金本体的电化学行为。当pH值为4时,在H2SO4和HCl溶液中,铝合金的阳极极化过程中仍有钝化膜溶解区,而在CH3COOH溶液中虽已无明显溶解区,但其阳极区Tafel斜率较大,自腐蚀电流密度增速较快,表明尽管CH3COOH酸性较弱,但因溶液pH值较低,H+浓度较高,使得钝化膜依旧遭到一定程度破坏,造成基体合金可与溶液直接接触发生溶解,这点结合交流阻抗谱进行分析将更为直观。综上,在酸性条件(pH为3、4)下,溶液中大量的H+会严重破坏电极表面钝化膜,使得合金基体裸露并发生快速溶解,氢置换反应成为主要的阴极反应,而氧的还原反应相对来说可以忽略不计,电极过程的主要反应为[15]
(1)
(2)
当pH值分别为5、6时,合金在不同酸溶液中的Tafel曲线形状相似,即:在阴极极化段具有明显的扩散特征,说明阴极反应受到传质过程控制;在阳极极化段,随着阳极过电位的增加,电流密度缓慢增加,可见由于溶液中H+浓度较低,电极表面钝化膜未遭受到破坏或破坏程度较轻,得以保持了一定完整性,阻碍了极化反应的进行,对基体合金起到了一定保护作用。该过程中,析氢反应减弱,氧的扩散控制作用增强。氧还原反应逐步占据了主导地位[12],该反应过程如下:
(3)
(4)
(5)
(6)
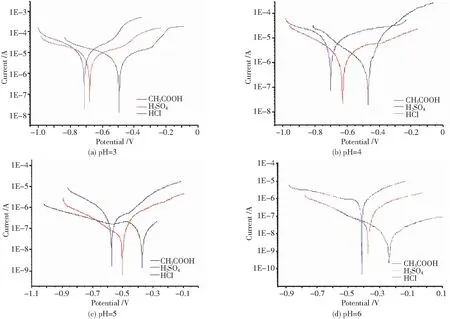
图1 2024-T3铝合金在同一pH值不同酸的水溶液中的极化曲线Fig.1 Polarization curves of 2024-T3 in different aqueous solution with the same pH value
使用CorrView软件对极化曲线进行经典Tafel拟合,得到极化相关电化学参数见表2。φcorr表示自腐蚀电位;Jcorr表示自腐蚀电流密度;Vcorr表示腐蚀速率;ba和bc分别表示阳极和阴极的Tafel斜率;Rp为极化电阻,可用来表征材料在不同环境条件下的耐蚀性强弱[15],即Rp值越大,材料的耐蚀性越强。据表中数据可知,相同pH值条件下,电极在3种溶液中的自腐蚀电位φcorr呈递减态势,表明该合金在其中的活泼性逐渐增加,发生腐蚀的倾向逐渐增大;自腐蚀电流密度Jcorr和腐蚀速率Vcorr则逐渐增大,表明合金在HCl溶液中的腐蚀最快也最剧烈,H2SO4溶液中次之,在CH3COOH溶液中最慢。
图2是2024-T3铝合金在同一种酸、不同pH值条件下的极化曲线和极化电阻。结合表2中数据可见,随着pH值的增大,合金的极化曲线发生正向移动,说明其腐蚀倾向逐渐变低,稳定性增强。当pH值为3或4时,无论在何种酸调节的水溶液中,该合金的极化行为相近;当pH值为5或6时,极化行为差别则相对较大。从极化电阻的变化趋势可知,其值随着溶液pH值的增加而增大,且同一pH值下在3种酸溶液中满足CH3COOH>H2SO4>HCl的关系。这表明,溶液pH值对合金表面钝化膜的稳定性影响很大,pH值越低,对钝化膜的破坏也就越强;合金在HCl水溶液中的耐蚀性最差,H2SO4中稍好但相近,CH3COOH中最好。另外,当pH值为4时,合金在CH3COOH溶液中的值远大于在H2SO4和HCl溶液中的值,这是因为CH3COOH酸性较弱,电极表面钝化膜在此溶液中虽有破坏但程度相对轻,在极化周期内尚能保持一定完整性,故此时合金极化曲线未出现明显钝化膜溶解区。
2.2 交流阻抗
在对2024-T3铝合金交流阻抗谱的分析中发现,该型合金对于不同酸性水溶液的电化学反馈有所不同。因此,可通过电学信号反馈的异同来分析该型合金在不同酸性环境中表面状态的变化过程[16]。分析时使用ZsimpWin软件进行交流阻抗的等效电路拟合,得到相应等效电路元件值。图3中“_msd”表示的是实测数据,“_cal”表示拟合数据。
图3中,pH值为3和4时,2024-T3铝合金在不同酸溶液中的Nyquist图趋势相近,即除了在第一象限有由等效电容引起的容抗弧外,在第四象限还存在由等效电感引起的感抗弧。其中,高-中频区的容抗弧是电极表面的双电层在受到极化电位和极化电流扰动时的非法拉第过程导致的;至于低频区的感抗弧,Keddma等[17]认为是合金表面原始氧化膜保护性减弱所致,曹楚南等[18]认为有钝化膜覆盖的金属表面可能在钝化膜孔蚀诱导期产生感抗,一旦氧化膜穿孔,孔蚀进入发展期,感抗的成分便会逐渐消失。这两种观点都指向于原始氧化膜的破坏导致了低频区感抗的出现。这说明,pH值为3或4时,在阻抗测量期间,无论是哪一种酸的水溶液,都会使2024-T3铝合金表面钝化膜遭到不同程度的破坏。这与由图极化曲线分析所得结论一致。注意,在pH值为4的CH3COOH溶液中,极化曲线未能较好地表现出合金表面钝化膜的破坏过程,但在交流阻抗谱中却得到直观表现。在酸性水溶液中,尽管合金表面的钝化膜会破坏溶解,但其难易程度并不相同。因为3种酸的水解电离能力不同,造成溶解反应在进行时遭遇到的阻力有所不同。合金在图中第一象限容抗弧半径的大小均满足CH3COOH>H2SO4>HCl的关系。通常容抗弧半径越大,电荷转移的阻力也就越大,电极反应也就越难进行[19];表3中电荷转移电阻的值在3种溶液中依次减小。这两点均证明,在CH3COOH、H2SO4、HCl溶液中,合金表面反应越来越容易进行。

表2 不同酸及不同pH值条件下2024-T3铝合金的电化学参数

图2 2024-T3铝合金在同种酸不同pH值水溶液中的极化曲线及极化电阻Fig.2 Polarization curvesand polarizationresistance of 2024-T3 in the same aqueous solution with different pH values
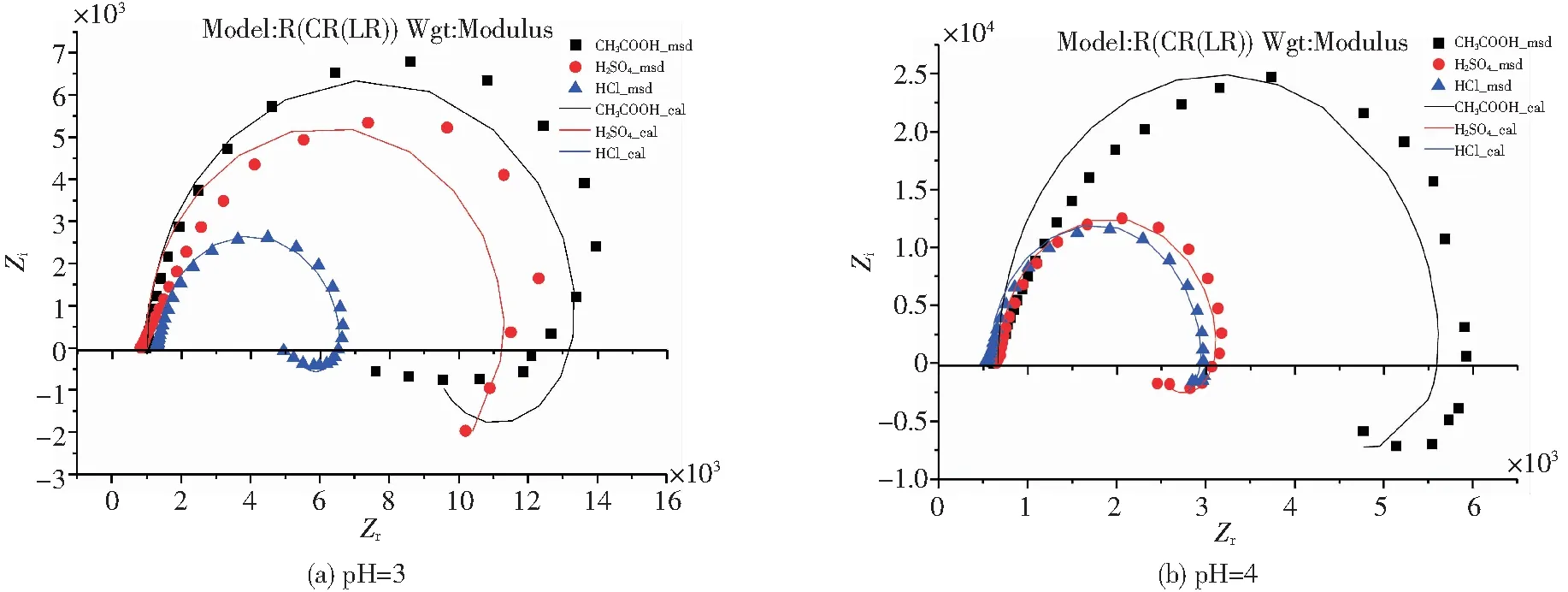
图3 pH=3或4时2024-T3铝合金在不同酸的水溶液中的阻抗谱Fig.3 Impedance spectra of 2024-T3 in different aqueous solutions with pH=3 or 4
图4中,pH值为5时,2024-T3铝合金在3种不同酸的水溶液中的交流阻抗谱变化趋势基本保持一致,即每条Nyquist曲线均包含两个时间常数,表明在实际测量时电极表面存在两处非法拉第过程。其中,高频部分为一半径较小的容抗弧,该容抗弧的产生与电极表面氧化膜有关;而中-低频部分为一半径较大的容抗弧,该容抗弧则是由电荷转移过程引起的。pH值为6时,2024-T3铝合金在三种酸的水溶液中的Nyquist图均呈现明显的Warburg阻抗特征。Warburg阻抗是由溶液内物质扩散过程引起的阻抗[20]。根据2.1节论述可知,在弱酸性环境下,电极表面钝化膜能够保持相对完整性,此时阴极同时存在析氢反应和氧还原反应,但在pH值为5和6时,合金阻抗行为差别较大,这是不同条件下不同的阴极还原反应导致的。当pH=5时,阴极极化过程为析氢反应和氧还原反应混合控制;当pH=6时,H+浓度进一步降低,氧还原反应占据主导地位,电极表面附近溶解氧在反应之初便被迅速消耗,此时法拉第电流密度比电极反应的交换电流密度大得多,随反应继续进行,电极附近溶解氧进一步消耗并形成氧浓差,推动溶液本体中的氧向反应界面移动,但氧的量始终无法满足电极反应的快速进行,该过程体现在Nyquist图中就是一条倾斜向上的直线,即电极反应受扩散过程控制,反应进行的阻力很大。

表3 pH=3或4时等效电路元件拟合值
注:Rs表示溶液电阻,Cdl表示双电层电容,Rt表示电荷转移电阻,L0和R0分别为表面氧化膜的电感和电阻,Chi-Squared表示拟合均方差
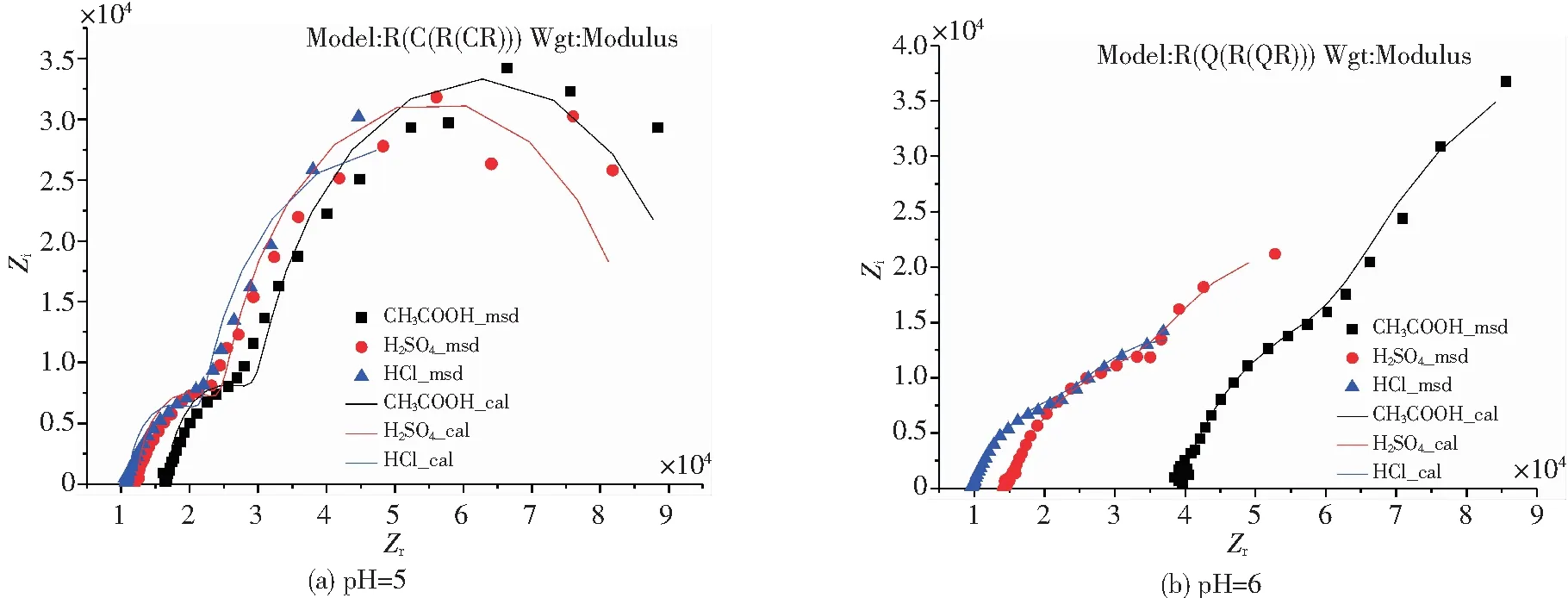
图4 pH=5或6时2024-T3铝合金在不同酸的水溶液中的阻抗谱Fig.4 Impedance spectra of 2024-T3 in different aqueous solutions with pH=5 or 6
表4中,Rs、Cdl、Rt含义与表3相同,C0和R0分别表示表面氧化膜的电容和电阻;表5中,Qdl和Q0为恒相位角元件,在扩散过程控制中分别用以代替双电层电容和氧化膜电容2个纯电容元件,其阻抗值的计算公式为:
(7)
式中,Y0和n为恒相位角元件常数;n称为弥散效应系数,0

表4 pH=5时等效电路元件拟合值
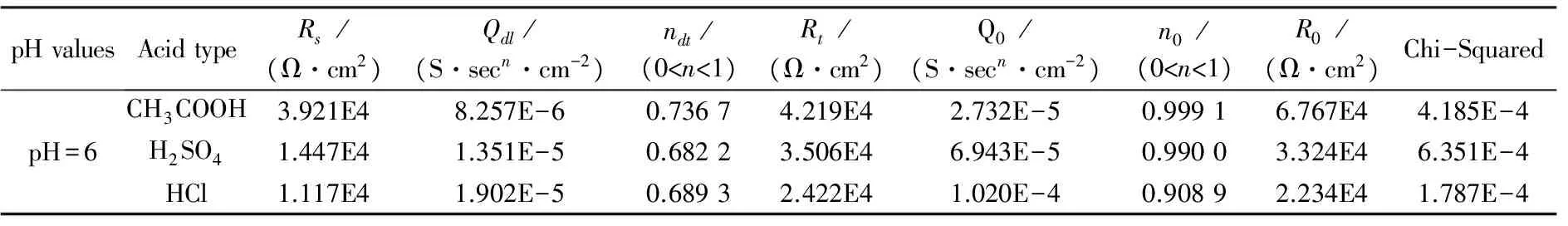
表5 pH=6时等效电路元件拟合值
2.3 微观形貌
图5为2024-T3铝合金在不同酸性溶液中开展电化学测量前、后的表面形貌图,放大倍数相同。图中,每行从左至右依次为合金在测量之前、CH3COOH溶液中、H2SO4溶液中、HCl溶液中的形貌图;除第一列外,每列从上至下分别为pH值为3、4、5、6时的形貌图。不难看出,在同一种酸的水溶液中,pH值越低合金表面氧化膜的破坏也就越严重。当pH=3时,点蚀迅速扩展连接形成较大蚀坑,此时合金基体裸露,会遭受剧烈侵蚀;在同一pH值下,合金往往在HCl溶液中遭受的腐蚀最为严重,尤其是在pH值为3或4的酸性环境中这种现象更加明显,这是因为HCl水溶液中含有丰富的Cl-,而在Cl-作用下,合金表面的氧化膜更容易发生局部破坏,进而诱发点蚀和应力腐蚀开裂[22]。
3 结论
1)在相同pH值的水溶液中,CH3COOH、H2SO4和HCl对于2024-T3铝合金的腐蚀加速作用并不相同,以HCl最强,H2SO4相近但次之,CH3COOH最弱。一是因为3种酸在去离子水中的水解电离能力有所不同,导致溶液电阻不同,其中CH3COOH为弱酸,水解能力最差,其水溶液的电阻值也就最大,故发生电极反应的阻力相应最大;二是因为HCl的水溶液中含有Cl-,Cl-会使该合金表面氧化膜更易被破坏,促进合金基体腐蚀。
2)在3种酸的水溶液中,溶液pH值越低,对于2024-T3铝合金的腐蚀加速作用也就越强。因为H+浓度决定pH值,pH值表征H+浓度,pH越低,H+浓度也就越大,电极反应速率也就越快。在pH值为3或4的酸性环境中,阴极过程受到氢的还原反应控制;在pH值为5的弱酸性环境中,阴极过程受到析氢反应和氧还原反应混合控制;在pH值为6时,氧的还原反应则占据主导地位,此时的电极反应主要受到扩散过程控制。
3)2024-T3铝合金为易钝化金属,但在不同酸性水溶液中钝化膜破坏的难易程度不同。在对合金进行电化学测量后发现其电化学行为前后表现不一致,这是因为不同条件下所测数据反映的是该合金不同部位的电化学行为。当pH值为3或4时,钝化膜失稳溶解,失去了对合金基体的保护作用,所得电化学数据基本上反映了合金基体的电化学行为;当pH值为5或6时,电极表面钝化膜则能够保持相对完整性,对基体合金保护作用较强。

图5 不同酸性条件下2024-T3铝合金的表面形貌图Fig.5 Surface morphology of 2024-T3 under different acidic conditions
[1] 刘文珽,李玉海,陈群志,等. 飞机结构腐蚀部位涂层加速试验环境谱研究[J]. 北京航空航天大学学报,2002,28(1):109-112.
[2] 骆晨,蔡健平,许广兴,等. 航空有机涂层在户内加速试验与户外暴露中的损伤等效关系[J]. 航空学报,2014,35(6):1750-1758.
[3] 樊玉光,林红先. 不同酸性介质中2种不锈钢耐均匀腐蚀性能的研究[J]. 长江大学学报:自科版,2008,5(3):244-245.
[4] 李丹,徐飞高,赵末名,等. 不同类型酸对石灰岩的模拟腐蚀实验[J]. 环境化学,2011,30(12):2069-2074.
[5] 艾芳芳,徐小连,陈义庆,等. 原油储罐钢在不同酸性盐介质中的耐蚀性能[J]. 腐蚀与防护,2012,33(12):1102-1103.
[6] 骆晨,李明,孙志华,等. 海洋大气环境中飞机的环境损伤和环境适应性[J]. 航空材料学报,2016,36(3):101-107.
[7] 陈跃良. 海军飞机结构腐蚀控制及强度评估[M]. 北京:国防工业出版社,2009:1-3.
[8] 穆志韬. 海军飞机结构腐蚀损伤规律及使用寿命研究[D]. 北京:北京航空航天大学,2001:22-24.
[9] 陈亚军,王艾伦,王付胜,等. 在航空载荷谱作用下2024铝合金的疲劳行为[J]. 航空材料学报,2016,36(5):64-69.
[10] 曹楚南. 腐蚀电化学原理[M]. 北京:化学工业出版社,2008:216-224.
[11] 贺俊光,文九巴,孙乐民,等. 用循环极化曲线研究Al和铝合金的点蚀行为[J]. 腐蚀科学与防护技术,2015,27(5):449-453.
[12] 生海,董超芳,肖葵,等. pH值对2024-T351铝合金在NaCl溶液中电化学行为的影响[J]. 腐蚀与防护,2013,34(2):107-110.
[13] 李涛,董超芳,李晓刚,等. 环境因素对铝合金大气腐蚀的影响及其动态变化规律研究[J]. 腐蚀与防护,2009,30(4):215-219.
[14] 陈跃良,王哲夫,卞贵学,等. 不同浓度NaCl溶液下典型铝/钛合金电偶腐蚀当量折算研究[J/OL]. 航空学报,2016,http://www.cnki.net/kcms/detail/11.1929.V.20160810.0847.002.html.
[15] 孙斌,宋仁国,李海,等. 7003铝合金应力腐蚀裂纹扩展的电化学阻抗谱分析[J]. 中国有色金属学报,2016,26(9):1832-1842.
[16] 王新东,武世民,刘艳芳,等. 用电化学交流阻抗法研究铝合金表面稀土转化膜[J]. 工程科学学报,2001,23(4):320-323.
[17] Keddam M, Kuntz C, Takenouti H, et al. Exfoliation corrosion of aluminium alloys examined by electrode impedance[J]. Electrochimica Acta,1997,42(1):87-97.
[18] 曹楚南,王佳,林海潮. 氯离子对钝态金属电极阻抗频谱的影响[J]. 中国腐蚀与防护学报,1989(4):261-270.
[19] Wang Y F,Cheng G X,Wu W,et al. Effect of pH and chloride on the micro-mechanism of pitting corrosion for high strength pipeline steel in aerated NaCl solutions[J]. Applied Surface Science,2015,349(15):746-756.
[20] 曹楚南,张鉴清. 电化学阻抗谱导论[M]. 北京:科学出版社,2002:109-118.
[21] Larignon C, Alexis J, Andrieu E, et al. The contribution of hydrogen to the corrosion of 2024 aluminium alloy exposed to thermal and environmental cycling in chloride media[J]. Corrosion Science,2013,69(2):211-220.
[22] Matter E A, Kozhukharov S, Machkova M, et al. Reproducibility of the corrosion parameters for AA2024-T3 aluminium alloy in chloride solution after different preliminary treatment procedures[J]. Journal of Chemical Technology and Metallurgy,2015,50:52-64.
Study on Electrochemical Behavior of 2024-T3 Aluminum Alloy inDifferent Acidic Aqueous Solutions
CHEN Yue-liang,WANG An-dong,BIAN Gui-xue,ZHANG Yong
(NavalAeronauticalEngineeringInstitute,ShandongQingdao266041,China)
The electrochemical measurement techniques of potentiodynamic polarization and AC impedance, combined with the observation on electrode surface micro-morphology, were applied to investigate the electrochemical behavior of 2024-T3 aluminum alloy in aqueous solutions with different acids (including acetic acid, sulfuric acid and hydrochloric acid) and different pH values. Results show that with the decrease of pH value, the self-corrosion potential shifts negatively, the self-corrosion current density and the corrosion rate increase, the passivation film covering on the electrode surface is more easily damaged, and the corrosive characteristic of the solution becomes stronger. Under different pH values, the reaction course of cathodic polarization is different. When pH value is the same, the corrosive characteristic of hydrochloric acid solution is the strongest, sulfuric acid aqueous solution is close but inferior, and acetic acid aqueous solution is the weakest. This is due to the different hydrolysis ability of the acid and the presence of the chloride in hydrochloric acid solution. Because of the existence of the passivation film, the electrochemical behavior of the electrode in different corrosive environment is various. The passivation film loses the stability and dissolves under the acidic condition, so the alloy matrix is exposed and contacts with the reaction solution directly. In the weak acidic solution, the passivation film can maintain relative integrity, and have a certain protective effect on the alloy substrate.
aluminum alloy; acid; pH value; electrochemistry; corrosion
2017年1月17日
2017年3月20日
国家自然科学基金(51377503)
陈跃良(1962年-),男,博士,教授,主要从事结构强度、腐蚀与防护专业等方面的研究。
TH142.3
A
10.3969/j.issn.1673-6214.2017.02.003
1673-6214(2017)02-0078-09

