AuNPs-MoS2-rGO纳米复合材料的合成及其对水合肼的电化学检测
郭玉晶,王秀芳,刘志广,张国娟
(山西大学 环境科学研究所,化学化工学院,山西 太原 030006)
AuNPs-MoS2-rGO纳米复合材料的合成及其对水合肼的电化学检测
郭玉晶,王秀芳,刘志广,张国娟
(山西大学 环境科学研究所,化学化工学院,山西 太原 030006)
以氧化石墨烯(GO)为基体,利用钼酸钠为钼源,L-半胱氨酸为硫源,通过水热法成功合成了二硫化钼-石墨烯纳米复合材料(MoS2-rGO),通过NaBH4还原氯金酸(HAuCl4),得到金纳米-二硫化钼-石墨烯纳米复合材料(AuNPs-MoS2-rGO)。通过紫外-可见吸收光谱法、透射电子显微镜和X射线光电子能谱对材料进行了表征。并且利用该新材料构建了电化学传感器,结果表明,在该复合纳米材料修饰的玻碳电极上,水合肼的氧化过电位明显减小,说明金纳米、二硫化钼和石墨烯对水合肼的催化氧化具有协同作用。用计时电流法实现了对水合肼的灵敏、快速检测,线性范围是0.05~2 000 μmol/L,检出限为0.016 7 μmol/L(信噪比S/N=3)。回收率在98.0%~105.0%之间。该传感器在水合肼的检测上显示出良好的重现性和稳定性,并且可用于水样的检测,结果令人满意。关键词:石墨烯;二硫化钼;金纳米;电化学检测;水合肼
0 引言
水合肼(N2H4·H2O)又称水合联氨,是一种重要的化工原料,除了作为火箭推进剂,还是强的还原剂,也可以应用到药品、农药、起泡剂和燃料电池。与此同时,水合肼是常见的环境污染物,有毒易挥发,不仅损害人体动物的肝脏、肾脏而且会损坏中枢神经系统[1-2]。因此,高效灵敏检测水合肼具有重要意义。目前已建立了很多检测水合肼的方法,比如分光光度测定[3]、电化学发光[4]、气相色谱(GC)和气质联用色谱法(GC-MS)[5]、高效液相色谱法(HPLC)[6]等,尽管这些方法有较好的灵敏度和重现性,但运行成本高,耗时,分离复杂。因此,迫切需要开发一种简单、可靠、灵敏的方法检测废水中微量的水合肼。电化学传感器具有检测操作方便,响应快速,样品前处理简单、成本低廉,易于现场测定等优点,引起了科研工作者的关注[7]。由于水合肼具有很强的还原性,容易在电极表面发生氧化反应,而且电化学测定水合肼已被证明是一种可行且有效的方法,为了提高水合肼在电极上反应的灵敏度和重现性,一些功能化纳米材料被用来构建水合肼电化学传感器。Zhao等人[8]成功的构建了AuNPs-CNTs-ErGO/GCE电化学传感器,可高效、快速、灵敏的检测水合肼,其线性范围低至0.065 μmol/L。Mani等人[9]电聚合四氨基酞菁钴染料(pTACoPc)于还原氧化石墨烯(RGO-pTACoPc)上,用于半胱氨酸和水合肼的电催化氧化,采用计时电流法检测水合肼,线性范围为50 nmol/L~2.6 μmol/L,其检测限为10 nmol/L。虽然以上的方法增强了水合肼的电化学反应,但是,仍然需要进一步设计新的功能纳米材料,以加快水合肼的高灵敏检测平台的发展。
石墨烯(graphene)是由单层的sp2杂化碳原子紧密堆积而成的、二维蜂窝状晶格结构的碳质新材料,具有导电性好、比表面积大等优点,使得石墨烯在电化学检测等方面有大的优势。然而,石墨烯层与层之间存在强的范德华力和π-π共轭作用,使得其在水溶液中易发生聚集,且层内容易发生卷曲,这些缺陷限制了石墨烯在电化学生物传感器中的应用[10]。但将石墨烯与其它材料进行复合,可以充分发挥不同材料之间的协同作用,从而改善石墨烯的电化学性能,拓展石墨烯在电化学领域的应用。
类石墨烯过渡金属二元化合物(MX2)因具有良好的光电催化性能,一直备受人们的关注,其中二硫化钼(MoS2)是典型代表之一。单层MoS2比表面积大,具有良好的载流子迁移率,是具有直接带隙的半导体,由中间钼原子层夹在上下两层硫原子中间,由共价键结合,层与层之间通过的范德华力相结合,易剥离,且S具有对金属很强的粘附力,形成的“三明治夹心”结构二维晶体材料[11-12],使得MoS2纳米片在传感器、超级电容器、电催化等领域都有良好的发展前景。Su等人[13]制备了AuNPs/MoS2复合材料,用于同时检测凝血酶和三磷酸腺苷(ATP),将两种不同电活性物质的适配体探针,通过Au-S键固定在电极表面的金纳米上,用加入靶分子前后引起电活性物质的信号变化,实现对凝血酶和ATP的高灵敏检测。MoS2的禁带宽度随其层厚度的改变而改变,而石墨烯是零带隙材料,如果将石墨烯和MoS2复合,可得到一种兼具二者理化特点、性能互补的复合材料。Song等人[14]通过电化学自组装,制备了MoS2/GNs纳米复合材料,用于固定HRP催化H2O2,实现对H2O2的灵敏检测。Zhao等人[15]从基底剥离出2D MoS2,不仅提高MoS2的电子迁移速率,得到高质量、高品质的MoS2,而且该过程没有引入任何污染物。
金纳米粒子(AuNPs)具有较好的生物相容性、强导电性和高的催化活性[16-17],能够加快电子转移速率,对电化学信号起到放大作用。本文利用钼酸钠、L-半胱氨酸(L-Cys)及氯金酸为前驱体,通过水热法成功合成了AuNPs-MoS2-rGO纳米复合材料,该复合材料修饰的玻碳电极用于水合肼的电催化氧化,具有很好的催化活性。图1是AuNPs-MoS2-rGO的合成及电化学传感器的构建过程。
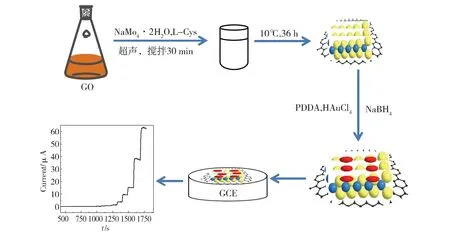
Fig.1 Schematic illustration of synthetic procedure for AuNPs-MoS2-rGO and electrochemical detection of hydrazine on AuNPs-MoS2-rGO/GCE图1 AuNPs-MoS2-rGO的合成及电化学传感器构建示意图
1 实验部分
1.1 主要试剂和仪器
试剂:氧化石墨粉(Alfa Aesar);水合肼(80.0%)(天津第三化学试剂厂);聚二甲基二烯丙基氯化铵(PDDA,Mw=400 000~500 000,质量浓度为20.0%的水溶液)、Na2MoO4·2H2O、L-Cys、氢氧化钠(1.0 mol·L-1)、HAuCl4·4H2O(北京化学试剂厂)、电解液为0.10 mol·L-1的磷酸缓冲液(PBS),实验用水为超纯水。
仪器:U-3010紫外-可见(UV-vis)分光光度计(Hitachi,ltd. 日本,东京);JEOL-2100透射电子显微镜(TEM)(VG Co.);ESCLAB-MKII 250 X-射线光电子能谱(XPS)(VG Co.);CHI660E电化学工作站(上海辰华仪器公司);三电极体系:玻碳电极为工作电极(GCE,Φ=3.0 mm),铂柱电极为对电极以及饱和甘汞(SCE)作为参比电极。
1.2 实验方法
1.2.1 AuNPs-MoS2-rGO纳米复合材料的合成
首先通过Hummers[18]方法合成氧化石墨烯(GO),将制备好的GO超声分散于水中,得到1.0 mg/mL的褐色悬浮液。MoS2-rGO的合成方法,通过L-半胱氨酸辅助溶液相方法制备而得[19]。将0.069 g Na2MoO4·2H2O加入到12.5 mL GO(1.0 mg/mL)溶液中,分别超声和搅拌30 min之后,用0.1 moL/L NaOH溶液,将溶液的pH调节至6.5,之后加入L-Cys(0.125 g),并将溶液稀释到25.0 mL,剧烈搅拌1 h之后,转入到40.0 mL的高压反应釜中,密封加热到180℃,反应36 h。待反应釜冷却之后,将反应产物分别用乙醇,超纯水各离心洗涤3次,重新超声分散并稀释成1.0 mg/mL的悬浮液备用,即MoS2-rGO。反应方式如下[20]:
HSCH2CHNH2COOH+H2O→ CH3COCOOH+NH3+H2S
(1)
4MoO42-+9H2S+6CH3COCOOH→ 4MoS2+SO42-+6CH3COCOO-+12H2O
(2)
在室温下用NaBH4还原HAuCl4进一步得到AuNPs-MoS2-rGO。合成步骤如下:将50 μL PDDA(20.0%)加入到2.0 mL 1.0 mg/mL的MoS2-rGO 中,再加入1.0 mL水,搅拌20 min。之后,向上述混合液中加入200 μL 10 mg/mL HAuCl4,搅拌20 min。在快速搅拌下,将5.0 mL新鲜配制的NaBH4(20.0 mmol/L)逐滴缓慢加入到反应瓶中。反应30 min后,得到稳定略带暗红色的悬浮液,经离心、洗涤,得到AuNPs-MoS2-rGO纳米复合材料,定容至0.25 mg/mL备用。
1.2.2 修饰电极的制备
依次用粒径为1.0,0.3,0.05 μm的Al2O3粉末对电极表面进行抛光打磨,之后用乙醇和二次水依次对其超声洗涤。清洗干净后,用N2将电极表面吹干,将6.0 μL 0.25 mg/mL的AuNPs-MoS2-rGO修饰到处理好的GCE表面,在室温下晾干,得到AuNPs-MoS2-rGO/GCE传感界面。
1.2.3 电化学检测水合肼
将制备好的AuNPs-MoS2-rGO/GCE传感界面,加入一系列不同浓度的水合肼于0.1 mol/L的PBS (pH=8.0)中,用计时电流法(i-t)检测水合肼的电化学行为。系统参数为:初始电位0.30 V,样品间隔0.1 s。
2 结果与讨论
2.1 AuNPs-MoS2-rGO纳米复合材料的表征
2.1.1 AuNPs-MoS2-rGO的紫外-可见吸收光谱
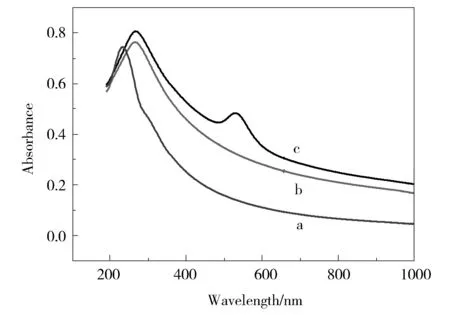
Fig.2 UV-vis absorption spectra of GO suspension (a),MoS2-rGO (b) and AuNPs-MoS2-rGO suspension(c)图2 氧化石墨烯GO(a),MoS2-rGO(b)和AuNPs-MoS2-rGO(c)的紫外-可见吸收光谱

2.1.2 AuNPs-MoS2-rGO纳米复合材料的形貌
利用TEM对MoS2-rGO和AuNPs-MoS2-rGO纳米复合材料进行了形貌表征。从图3A(a)可以看到MoS2-rGO纳米复合材料中rGO的褶皱结构,图3A(b)可看到MoS2纹理状结构,形貌和文献[22]报道相一致,表明合成了MoS2-rGO纳米复合材料。图3A(c)可以看到,AuNPs均匀分散在MoS2-rGO上,表明AuNPs-MoS2-rGO纳米复合材料被成功合成。
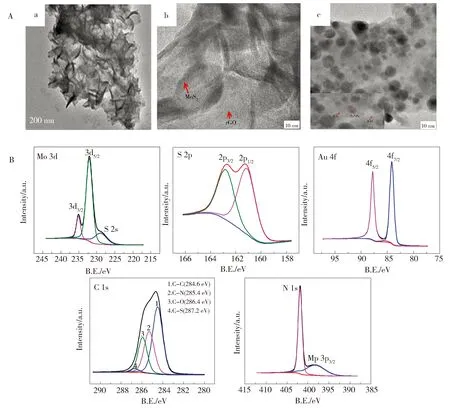
Fig.3 (A)The TEM images of MoS2-rGO (a) (b)and AuNPs-MoS2-rGO (c)(B) The XPS spectra of AuNPs-MoS2-rGO图3 (A)MoS2-rGO(a)(b)和AuNPs-MoS2-rGO(c)的TEM,(B)AuNPs-MoS2-rGO的XPS图
用X射线光电子能谱(XPS)研究了AuNPs-MoS2-rGO纳米复合材料的化学组成,图3B为MoS2和rGO的Mo 3d,S 2p,Au 4f,C 1s,N 1s的XPS谱图。Mo 3d5/2和Mo 3d3/2的特征峰,分别出现在230.7 eV和235.2 eV处,以及S 2p3/2和S 2p1/2特征峰出现在161.7 eV和162.7 eV处,证实MoS2的存在。GO中存在四种类型的碳键[23],包括:C-C(284.6 eV)、C-O(286.7 eV)、C=O(287.8 eV)和O-C=O(288.7 eV)。而从图中的C 1s光谱可以发现与氧相关的峰如O-C=O(288.7 eV)明显减弱,同时,出现了一个C-N的峰(285.4 eV)和N 1s峰,以及出现的C-S(287.2 eV)峰,分别来自于PDDA和L-Cys,这说明GO被还原成rGO,84.0 eV和87.7 eV分别是Au 4f7/2,Au 4f5/2的特征峰,以上进一步证明AuNPs-MoS2-rGO被成功合成。
2.1.3 水合肼在AuNPs-MoS2-rGO/GCE的电化学性能
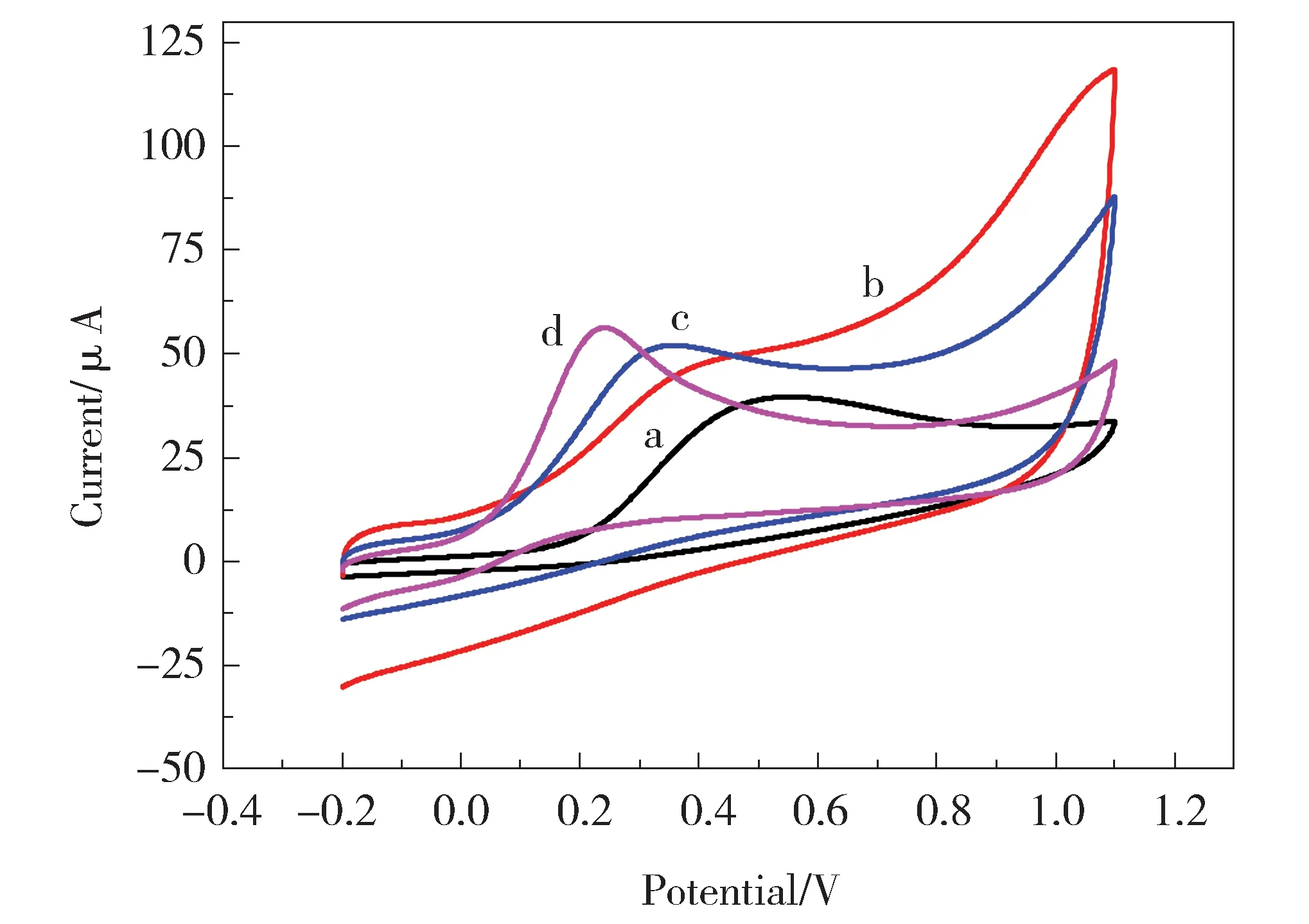
Fig.4 CVsof 1.0 mmol/L hydrazine at the bare GCE (a),rGO/GCE (b), MoS2-rGO/GCE (c)and AuNPs-MoS2-rGO/GCE (d) in 0.1 mol/L PBS (pH=8.0) at a scan rate of 0.1 V·s-1图4 (a)GCE、(b)rGO/GCE、(c)MoS2-rGO/GCE和(d)AuNPs-MoS2-rGO/GCE在含1.0 mmol/L水合肼的0.1 mol/L PBS(pH=8.0)中的循环伏安图,扫速:0.1V·s-1
利用循环伏安法(CV)研究了1.0 mmol/L水合肼在0.1 mol/L PBS(pH=8.0)中的电化学行为。图4为水合肼在GCE(曲线a)、rGO/GCE (曲线b)、MoS2-rGO/GCE(曲线c)和AuNPs-MoS2-rGO/GCE(曲线d)上的CV图,在GCE上,水合肼在0.5 V左右出现氧化峰,将rGO修饰到GCE上后,水合肼氧化峰电位约为0.35 V,过电位约降低0.15 V,峰电流相比裸玻碳电极升高,说明rGO对水合肼的氧化有较好的催化作用。曲线c为水合肼在MoS2-rGO/GCE上的发生氧化反应,峰电位进一步负移,峰电流升高,说明MoS2起到很好的作用。而在AuNPs-MoS2-rGO/GCE上,水合肼的氧化峰电流进一步升高,峰电位进一步负移,且峰形较好,这表明AuNPs-MoS2-rGO纳米复合材料具有rGO、MoS2、AuNPs三种材料的协同作用,使得水合肼在AuNPs-MoS2-rGO/GCE上的电化学行为远远好于其他电极。
2.2 扫速的影响
为了更好地探究水合肼在电极表面的反应机理,考察了水合肼的峰电流和峰电位与扫描速度的关系。由图5A可知,在50~350 mV·s-1范围内变化时,随着扫速的增加,氧化峰逐渐增高,峰位置右移。从图5B可以看出,峰电流和扫速的平方根呈线性关系,表明水合肼在AuNPs-MoS2-rGO/GCE表面的电化学氧化过程是扩散控制。此外,如图5C,水合肼的氧化峰电位与扫速的对数也呈线性关系,线性方程为:
Epa=0.0950+0.0895log ν(R2=0.9988)
(3)
对于不可逆反应,根据Laviron[24]公式:
(4)
其中,E0是标准的氧化还原电位,v是扫速,α电荷转移常数,n为电子转移数,k0是反应的标准速率常数,R是气体常数,F是法拉第常数,T是室温(298 K)。公式(4)的斜率是2.303RT/αnF,与(3)的斜率相同,即等于0.089 5,由此求得αn的值为0.661。对于不可逆反应,其α值为0.5,因此,计算得到电子转移数为1,与文献报道的电催化氧化水合肼的决速步骤是电子转移相一致[8,25]。
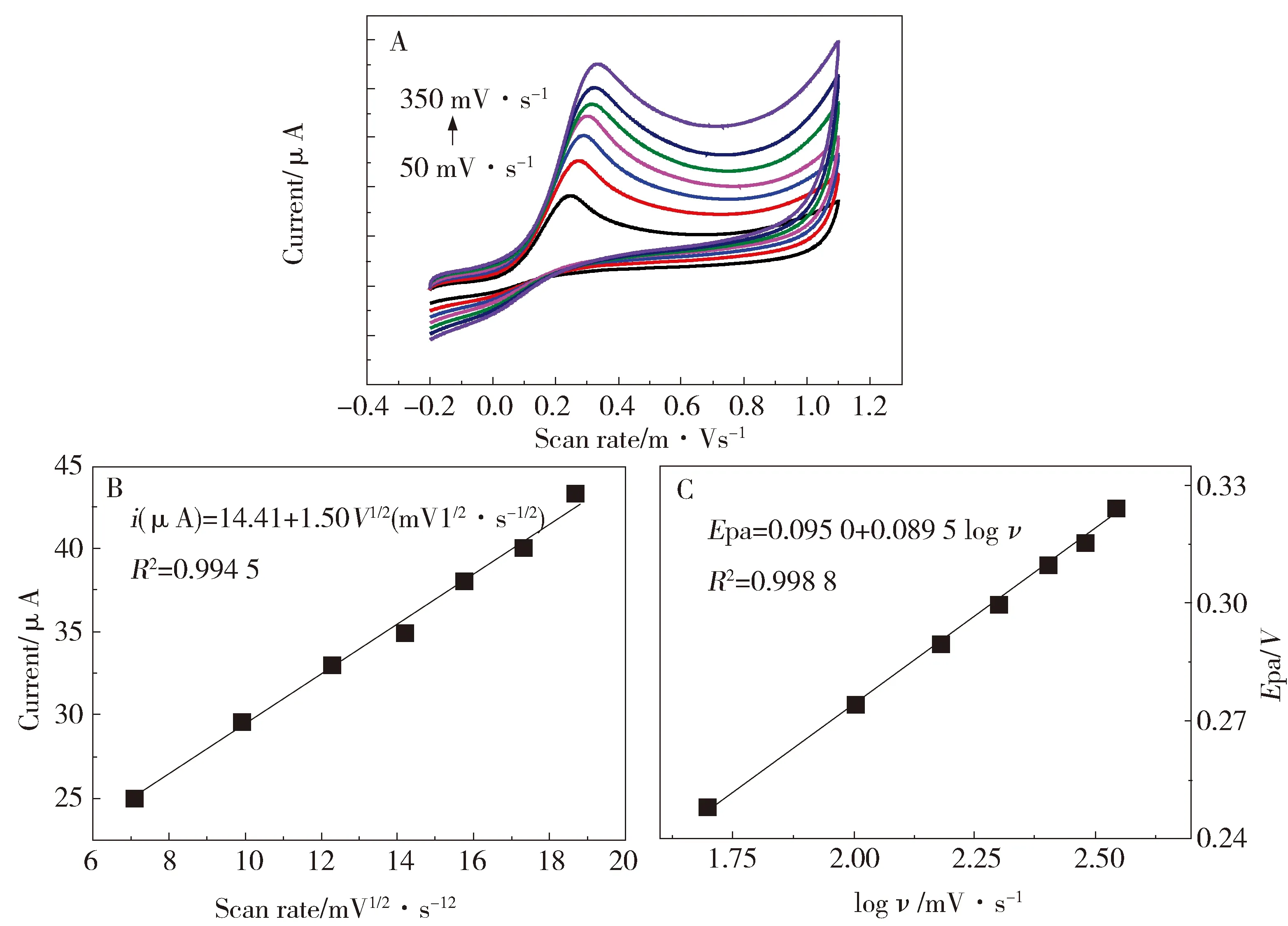
Fig.5 (A) CVs of 1.0 mmol/L hydrazine at AuNPs-MoS2-rGO/GCE in 0.1 mol/L PBS (pH=8.0) at scan rate of 50,100,150,200,250,300 and 350 mV·s-1;(B) Plot of peak current νs. ν1/2 for hydrazine;(C) Plot of Epa νs. log ν for hydrazine图5 (A)AuNPs-MoS2-rGO/GCE在含1.0 mmol/L水合肼的0.1 mol/L PBS(pH=8.0)中的CV图,扫速分别为50,100,150,200,250,300,350 mV·s-1;(B)水合肼的氧化峰电流对扫速平方根的线性关系;(C)峰电位与扫速的对数的线性关系
2.3 pH值对实验的影响
考察了pH值对水合肼在AuNPs-MoS2-rGO/GCE上的电化学行为的影响,在含1.0 mmol/L水合肼的不同pH溶液(4.0,5.0,6.0,7.0,8.0,9.0,10.0)中,利用CV检测其电化学信号。结果如图6所示,当pH从4.0增加到10.0,峰电位负移,在pH=8.0时,峰电流最大,所以,选pH=8.0的磷酸缓冲溶液作为支持电解质。
2.4 AuNPs-MoS2-rGO用量的影响
为了提高实验的灵敏度,考察了AuNPs-MoS2-rGO的用量与峰电流的关系。如图7所示,在含1.0 mmol/L水合肼的PBS(0.1 mol/L pH=8.0)中,将不同体积0.25 mg·mL-1的AuNPs-MoS2-rGO修饰在玻碳电极上,当修饰量从3.0 μL增加到6.0 μL时,水合肼的氧化峰电流明显增加,当修饰体积大于6.0 μL时,峰电流明显下降。这可能是由于电极表面AuNPs-MoS2-rGO膜厚度增大,降低电子传递速度。因此,以下实验均选用6.0 μL的AuNPs-MoS2-rGO悬浮液来修饰电极。
2.5 水合肼在AuNPs-MoS2-rGO/GCE上的电流响应
计时电流法是电化学传感器中最为常用的一种方法,也用来评定修饰电极对水合肼的电催化性能,向匀速搅拌的0.1 mol/L PBS溶液中连续加入不同浓度水合肼,记录电流变化,得到i-t曲线(图8A),检测电位为0.30 V。由图8B可以看出,水合肼的氧化峰电流与其浓度在0.05~2 000 μmol/L范围内呈良好的线性关系,线性方程为:ipa(μA)=0.0023+0.0311 C (μmol/L)(R2=0.991 5)(ipa代表氧化峰电流,C代表水合肼的浓度),检出限为0.016 7 μmol/L(S/N=3)。与文献上报道的方法相比,该方法线性范围宽,灵敏度高,具体情况见表1。说明可以利用该方法灵敏检测水合肼。
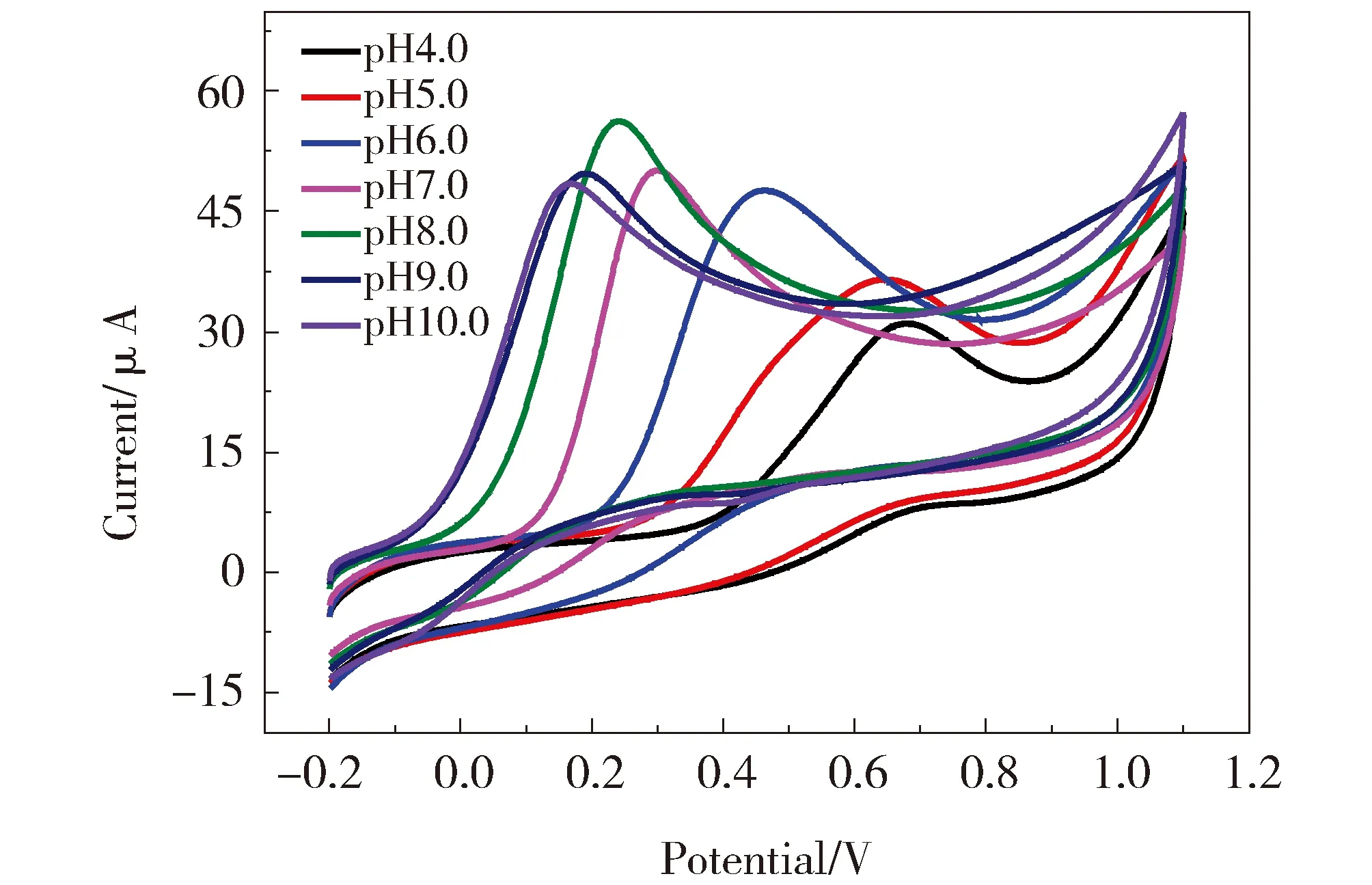
Fig.6 Influence of pH on the electrochemical response of 1.0 mmol/L hydrazine in 0.1 mol/L PBS on the AuNPs-MoS2-rGO/GCE. Scan rate: 0.1V·s-1图6 不同pH条件下,AuNPs-MoS2-rGO/GCE在含1.0 mmol/L水合肼的PBS溶液中的CV图,扫速为0.1 V·s-1

Fig.7 Effects of the modified volume of AuNPs-MoS2-rGO on the electrochemical response of 1.0 mmol/L hydrazine in 0.1 mol/L phosphate buffer at AuNPs-MoS2-rGO/GCE图7 修饰量对水合肼(1.0 mmol/L)在AuNPs-MoS2-rGO/GCE上的电化学行为的影响
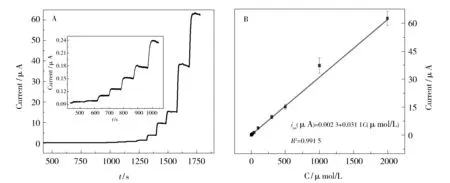
Fig.8 (A)Typical amperometric current response of the AuNPs-MoS2-rGO/GCE on successive addition of different amounts of hydrazine into stirring 0.1 mol/L PBS (pH=8.0) solution Applied potential: 0.30 V. (B) Plot of electrocatalytic current of hydrazine vs. its concentrations图8 (A)向0.1 mol/L PBS(pH=8.0)中连续加入不同浓度的水合肼时的i-t曲线(工作电位:0.30 V);(B)电流对水合肼浓度的线性拟合图

ModifiedelectrodeLinearrange(μmol/L)LOD(μmol/L)ReferenceCM/MWCNT/GCE2.0~44.01.40[33]HMWCNT/GCE2.0~122.80.68[52]Mn(Ⅱ)-complex/MWNTs/GCE1.0~1050.00.50[57]PalladiumhexacyanoferrateCatechinGCE390~100004.60[55]AuNPs/MoS2/rGO/GCE0.05~20000.0167Thiswork
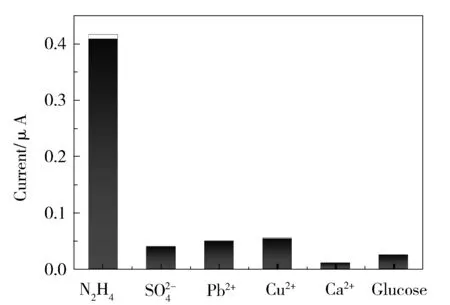
Fig.9 Selectivity investigations of the sensor for detection of 0.01 mmol/L hydrazine against 0.1 mmol/L S,Pb2+,Cu2+,Ca2+ and glucose, respectively图9 传感器的选择性考察。水合肼浓度为0.01 mmol/L,干扰物质浓度分别为以及葡萄糖
2.6 AuNPs-MoS2-rGO/GCE的选择性、重现性和稳定性

为了考察AuNPs-MoS2-rGO/GCE传感器的重现性,使用相同的电极在2.0 μmol/L的水合肼溶液中平行测定8次,相对标准偏差(RSD)为1.9%,说明该传感器对水合肼的检测具有良好的重现性。将AuNPs-MoS2-rGO/GCE在4℃条件下放置两周,之后测其在1.0 mmol/L水合肼中的峰电流,发现峰电流下降了6%,证明该传感器的稳定性较好。
2.7 实际样品中水合肼检测
我们选择自来水作为样品溶液,采用标准加入法检测其中水合肼的含量。在自来水中,加入浓度分别为10.0 μmol/L,40.0 μmol/L,50.0 μmol/L的水合肼,调节pH=8.0,利用i-t检测,结果如表2所示,回收率在98.0%~105.0%之间,这些说明该传感器可有效地检测实际样品中的水合肼。
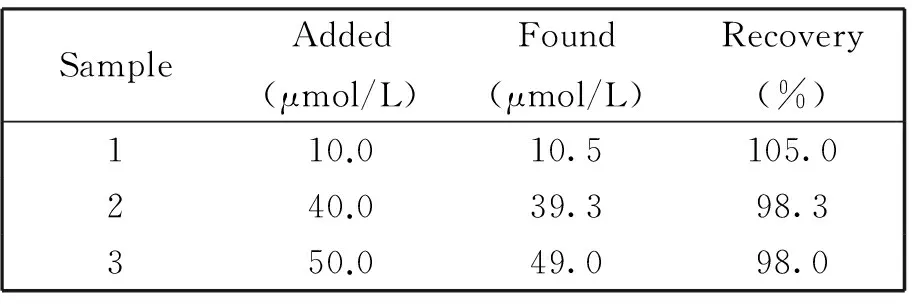
表2 水样中水合肼的检测
3 结论
通过水热法合成AuNPs-MoS2-rGO纳米复合材料,并利用该材料构建了电化学传感平台,实现了对水合肼的灵敏检测。该新的纳米材料结合石墨烯、MoS2和金纳米粒子三者的优良性能,大大提高了水合肼检测的灵敏度,并且实现了在实际水样中的准确检测。另外,该传感器具有良好的稳定性、重现性,并且成本低、速度快,有望在环境污染物的分析检测中发挥重要作用。
[1] Ragnarsson U.Synthetic Methodology for Alkyl Substituted Hydrazines[J].ChemicalSocietyReviews,2001,30(4):205-213.DOI:10.1039/B010091A.
[2] An Z,Li Z,He Y,etal.Ratiometric Luminescence Detection of Hydrazine with a Carbon Dots-hemicyaninenanohybrid System[J].RSCAdvances,2017,7(18):10875-10880.DOI:10.1039/C6RA27844B.
[3] Afsharasl A,Tsyrulneva I,Zaporozhets O.Spectroscopic,Visual Test Techniques and Optical Sensors for Determination of Hydrazine and Its Derivatives[J].Methods,2015,10(3):97-107.
[4] Liu F,Li W,Li F,etal.Determination of Hydrazine Hydrate Based on Electrochemiluminescence of Ru(bpy)32+[J].EnvironmentalMonitoringandAssessment,2013,185(5):4153-4158.DOI:10.1007/s10661-012-2857-9.
[5] Subramanian S,Narayanasastri S,Reddy A R K.Single Step Derivatization with CF3eNone of Thiophene at Ambient Temperature to Determine Propellant Grade Hydrazines:A Study by GC and GC-MS[J].Analyst,2015,140(1):330-339.DOI:10.1039/C4AN01648C.
[6] Oh J A,Shin H S.Simple and Sensitive Determination of Hydrazine in Drinking Water by Ultra-high-performance Liquid Chromatography-tandem Mass Spectrometry after Derivatization with Naphthalene-2,3-dialdehyde[J].JournalofChromatographyA,2015,1395:73-78.DOI:org/10.1016/j.chroma.2015.03.051.
[7] Gu X,Li X,Wu S,etal.A Sensitive Hydrazine Hydrate Sensor based on a Mercaptomethyl-terminated Trinuclear Ni(Ⅱ) Complex Modified Gold Electrode[J].RSCAdvances,2016,6(10):8070-8078.DOI:10.1039/C5RA23809A.
[8] Zhao Z,Sun Y,Li P,etal.Preparation and Characterization of AuNPs/CNTs-ErGO Electrochemical Sensors for Highly Sensitive Detection of Hydrazine[J].Talanta,2016,158:283-291.DOI:10.1016/j.talanta.2016.05.065.
[9] Mani V,Huang S T,Devasenathipathy R,etal.Electropolymerization of Cobalt Tetraamino-phthalocyanine at Reduced Graphene Oxide for Electrochemical Determination of Cysteine and Hydrazine[J].RSCAdvances,2016,6(44):38463-38469.DOI:10.1039/C6RA01851C.
[10] Han L,Liu C M,Dong S L,etal.Enhanced Conductivity of rGO/Ag NPs Composites for Electrochemical Immunoassay of Prostate-specific Antigen[J].BiosensorsandBioelectronics,2017,87:466-472.DOI: org/10.1016/j.bios.2016.08.004.
[11] Huang X,Zeng Z,Zhang H.Metal Dichalcogenidenanosheets:Preparation,Properties and Applications[J].ChemicalSocietyReviews,2013,42:1934-1946.DOI:10.1039/C2CS35387C.
[12] Ding Q,Czech K J,Zhao Y,etal.Basal-Plane Ligand Functionalization on Semiconducting 2H-MoS2 Monolayers[J].ACSAppliedMaterials&Interfaces,2017,9(14):12734-12742.DOI:10.1021/acsami.7b01262.
[13] Su S,Sun H,Cao W,etal.Dual-target Electrochemical Biosensing based on DNA Structural Switching on Gold Nanoparticle-decorated MoS2 Nanosheets[J].ACSAppliedMaterials&Interfaces,2016,8(11):6826-6833.DOI:10.1021/acsami.5b12833.
[14] Song H,Ni Y,Kokot S.Investigations of an Electrochemical Platform based on the Layered MoS2-Graphene and Horseradish Peroxidase Nanocomposite for Direct electrochemistry and Electrocatalysis[J].BiosensorsandBioelectronics,2014,56:137-143.DOI:org/10.1016/j.bios.214.01.014.
[15] Zhao J,Yu H,Chen W,etal.Patterned Peeling 2D MoS2 off the Substrate[J].ACSAppliedMaterials&Interfaces,2016,8(26):16546-16550.DOI:10.1021/acsami.6b04896.
[16] Huang K J,Liu Y J,Zhang J Z,etal.Aptamer/Au Nanoparticles/Cobalt Sulfide Nanosheets Biosensor for 17 Beta-estradiol Detection using a Guanine-rich Complementary DNA Sequence for Signal Amplification[J].BiosensBioelectron,2015,67:184-191.DOI:org/10.1016/j.bios.2014.08.010.
[17] Zhang Y,Han T,Wang Z,etal.In Situ Formation of N-doped Carbon Film-immobilized Au Nanoparticles-coated ZnO Jungle on Indium Tin Oxide Electrode for Excellent High-performance Detection of Hydrazine[J].SensorsandActuatorsB:Chemical,2017,243:1231-1239.DOI:org/10.1016/j.snb.2016.12.085.
[18] Humers W S,Offeman R E.Preparation of Graphitic Oxide[J].JAmChemSoc,1958,80(6):1339.
[19] Huang K J,Wang L,Liu Y J,etal.Synthesis of Polyaniline/2-dimensional Graphene Analog MoS2Composites for High-performance Supercapacitor[J].ElectrochimicaActa,2013,109:587-594.DOI:org/10.1016/j.electacta.2013.07.168.
[20] Huang K J,Liu Y J,Liu Y M,etal.Molybdenum Disulfide Nanoflower-chitosan-Au Nanoparticles Composites based Electrochemical Sensing Platform for Bisphenol A Determination[J].JournalofHazardousMaterials,2014,276:207-215.DOI:org/10.1016/j.jhazmat.2014.05.037.
[21] Ang P K,Wang S,Bao Q,etal.High-throughput Synthesis of Graphene by Intercalation-exfoliation of Graphite Oxide and Study of Ionic Screening in Graphene Transistor[J].AcsNano,2009,3(11):3587-3594.DOI:10.1021/nn901111s.
[22] Zheng X,Xu J,Yan K,etal.Space-confined Growth of MoS2Nanosheets Within Graphite:The Layered Hybrid of MoS2and Graphene as an Active Catalyst for Hydrogen Evolution Reaction[J].ChemistryofMaterials,2014,26(7):2344-2353.DOI:10.1021/cm500347r.
[23] Liu Z,Guo Y,Dong C.A High Performance Nonenzymatic Electrochemical Glucose Sensor based on Polyvinylpyrrolidone-graphene Nanosheets-nickel Nanoparticles-chitosan Nanocomposite[J].Talanta,2015,137:87-93.DOI.org/10.1016/j.talanta.2015.01.037.
[24] Laviron E.General Expression of the Linear Potential Sweep Voltammogram in the Case of Diffusionless Electrochemical Systems[J].JournalofElectroanalyticalChemistryandInterfacialElectrochemistry,1979,101:19-28.DOI:org/10.1016/S0022-0728(79)80075-3.
[25] Li J,Lin X.Electrocatalytic Oxidation of Hydrazine and Hydroxylamine at Gold Nanoparticle-Polypyrrole Nanowire Modified Glassy Carbon Electrode[J].SensorsandActuatorsB:Chemical,2007,126(2):527-535.DOI:org/10.1016/j.snb.2007.03.044.
Synthesis of Gold Nanoparticles-Molybdenum Disulfide-Graphene Nanocomposites and Electrochemical Detection of Hydrazine
GUO Yujing,WANG Xiufang,LIU Zhiguang,ZHANG Guojuan
(Institute of Environmental Science,School of Chemistry and Chemical Engineering,Shanxi University,Taiyuan 030006,China)
Gold nanoparticles supported on molybdenum disulfide functionalized graphene (AuNPs-MoS2-rGO)were synthesized through hydrothermal method and NaBH4reduction method, using graphene oxide (GO) as the matrix, sodium molybdenum as molybdenum source and L-cysteine as sulfur source. The nanocomposites were characterized by ultraviolet-visible absorption spectra, transmission electron microscope and X-ray photoelectron spectroscopy. The electrochemical sensor was constructed by using the new nanocomposite. The results show that on the nanocomposite modified glassy carbon electrode, the oxidation overpotential of hydrazine is obviously reduced, indicating that the gold nanoparticle,molybdenum disulfide and graphene have synergistic effect on the catalytic oxidation of hydrazine. Chronoamperometry was used for sensitivedetection of hydrazine. The linear range is from 0.05 μmol/L to 2 000 μmol/L. The detection limit is 0.016 7 μmol/L on the basis of the signal-to-noise characteristics (S/N=3) and the recoveries are between 98.0% and 105.0%. The developed electrochemical sensor exhibited good stability and reproducibility for the detection of hydrazine. And the AuNPs-MoS2-rGO based electrochemical sensor was also successfully demonstrated for the detection of hydrazine in water sample with satisfactory results.
graphene;molybdenum disulfide;gold nanoparticles;electrochemical detection;hydrazine
10.13451/j.cnki.shanxi.univ(nat.sci.).2017.03.021
2017-06-05;
2017-06-26
国家自然科学基金(21275093);山西省2016年青年“三晋”学者计划
郭玉晶(1969-),博士,教授,研究方向:环境分析化学和电分析化学。E-mail:guoyj@sxu.edu.cn
O657.1
A
0253-2395(2017)03-0554-09

