血必净注射液联合亚胺培南西司他丁治疗腹腔重症感染的临床观察
刘沫然,肖 铟,黄佳玲,田海容,才奇博(.齐齐哈尔医学院附属第三医院检验科,黑龙江齐齐哈尔6000;2.齐齐哈尔医学院附属第三医院肿瘤一科,黑龙江齐齐哈尔 6000)
血必净注射液联合亚胺培南西司他丁治疗腹腔重症感染的临床观察
刘沫然1*,肖 铟2#,黄佳玲1,田海容1,才奇博1(1.齐齐哈尔医学院附属第三医院检验科,黑龙江齐齐哈尔161000;2.齐齐哈尔医学院附属第三医院肿瘤一科,黑龙江齐齐哈尔 161000)
目的:观察血必净注射液联合亚胺培南西司他丁治疗腹腔重症感染的临床疗效、安全性及对患者血浆内毒素、炎症因子的影响。方法:选取2013年4月-2016年4月在我院接受治疗的腹腔重症感染患者100例,按随机数字表法分为观察组和对照组,各50例。对照组患者给予注射用亚胺培南西司他丁钠0.5 g加入0.9%氯化钠注射液500 mL中,ivgtt(时间≥40 min),q12 h;观察组患者在对照组基础上间隔8 h给予血必净注射液100 mL加入0.9%氯化钠注射液500 mL中,ivgtt,bid。两组患者均治疗5~7 d。比较两组患者治疗前后血浆内毒素和炎症因子[肿瘤坏死因子α(TNF-α)、白细胞介素6(IL-6)、IL-6/IL-10]水平及临床疗效,并记录不良反应发生情况。结果:治疗前,两组患者血浆内毒素和炎症因子水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者血浆内毒素和炎症因子水平均显著下降,且观察组水平显著低于对照组,差异均有统计学意义(P<0.05)。观察组患者优良率为98.00%,显著高于对照组的78.00%,差异有统计学意义(P<0.05)。两组患者均未见明显不良反应发生。结论:血必净注射液联合亚胺培南西司他丁治疗腹腔重症感染疗效显著,能有效控制患者内毒素以及炎症因子的释放,且安全性较高。
血必净注射液;亚胺培南西司他丁;腹腔重症感染;内毒素;炎症因子
腹腔感染可导致肠黏膜屏障的破坏,使大量内毒素进入血液循环,进而形成内毒素血症[1]。内毒素血症可能会致患者发生全身炎症反应综合征(SIRS),重症腹腔感染还可能致患者发生多脏器功能障碍综合征,临床病死率较高[2-3]。抗菌药物可以清除革兰氏阴性杆菌,同时可能会促使细菌胞壁上的内毒素释放,还可能导致患者发生SIRS,从而加重病情[4]。随着中医药学的发展,越来越多的中药被用于抗菌治疗,其中血必净注射液适用于因感染诱发的SIRS,对内毒素血症的治疗也有一定效果。因此,本研究观察了血必净注射液联合亚胺培南西司他丁治疗腹腔重症感染的临床疗效、安全性及对患者血浆内毒素、炎症因子的影响,以期为临床用药提供参考。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)符合《腹腔真菌感染》中腹腔重症感染诊断标准[1];(2)年龄≥18岁;(3)患者在用药前48 h内未接受其他抗菌药物治疗或接受过其他抗菌药物治疗但已证明无效。
排除标准:(1)严重心、肝、肾功能不全者;(2)妊娠或哺乳期妇女;(3)对本研究药物有已知或怀疑禁忌证及过敏史者;(4)癫痫、潜在神经疾病患者。
1.2 研究对象
选取2013年4月-2016年4月在我院接受治疗的腹腔重症感染患者100例作为研究对象,按照随机数字表法分为观察组和对照组,各50例。其中,观察组患者男性30例,女性20例;年龄26~64岁,平均年龄(43.7± 5.1)岁。对照组患者男性28例,女性22例;年龄28~65岁,平均年龄(43.7±5.7)岁。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究方案经医院医学伦理委员会审核批准,患者知情同意并签署知情同意书。
1.3 治疗方法
对照组患者给予注射用亚胺培南西司他丁钠[山东新时代药业有限公司,批准文号:国药准字H20133239,规格:0.5 g(C12H17N304S 0.25 g、C16H26N205S 0.25 g)]0.5 g加入0.9%氯化钠注射液500 mL中,ivgtt(时间≥40 min),q12 h;观察组患者在对照组基础上间隔8 h给予血必净注射液(天津红日药业股份有限公司,批准文号:国药准字Z20040033,规格:10 mL/支)100 mL加入0.9%氯化钠注射液500 mL中,ivgtt,bid。两组患者均治疗5~7d。
1.4 观察指标及疗效评价标准
(1)观察两组患者治疗前后血浆内毒素水平。试剂盒购自上海榕柏生物技术有限公司,严格按试剂盒说明书操作。(2)观察两组患者治疗前后血浆炎症因子[肿瘤坏死因子α(TNF-α)、白细胞介素6(IL-6)、IL-6/IL-10]水平。试剂盒购自南京金益柏生物科技有限公司,严格按试剂盒说明书操作。(3)观察两组患者临床疗效。参考全身炎症反应综合征(SIRS)、急慢性生理评分(APACHEⅢ)制订量表对患者症状评分[5],共10个项目,总分100分。优:自拟量表评分≥90分,患者恢复情况好;良:自拟量表评分为70~89分,患者恢复情况较好;差:自拟量表评分<70分,患者恢复情况较差。优良率=(优例数+良例数)/总例数×100%。(4)记录两组患者不良反应发生情况。
1.5 统计学方法
应用SPSS 15.0软件对数据进行统计分析。计量资料以±s表示,采用t检验;计数资料和等级资料均以例数和/或率表示,前者采用χ2检验,后者采用秩和检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗前后血浆内毒素水平比较
治疗前,两组患者血浆内毒素水平比较,差异无统计学意义(P>0.05);治疗后,两组患者血浆内毒素水平均显著降低,且观察组水平显著低于对照组,差异均有统计学意义(P<0.05),详见表1。
表1 两组患者治疗前后血浆内毒素水平比较(±s,pg/mL)Tab 1 Comparison of plasma endotoxin levels between 2 groups before and after treatment(±s,pg/mL)

表1 两组患者治疗前后血浆内毒素水平比较(±s,pg/mL)Tab 1 Comparison of plasma endotoxin levels between 2 groups before and after treatment(±s,pg/mL)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.control group,#P<0.05
治疗后12.61±24.1*#16.60±24.0*组别观察组对照组n 50 50治疗前27.42±17.2 25.31±16.1
2.2 两组患者治疗前后血浆炎症因子水平比较
治疗前,两组患者TNF-α、IL-6及IL-6/IL-10水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者TNF-α、IL-6及IL-6/IL-10水平均显著降低,且观察组水平显著低于对照组,差异均有统计学意义(P<0.05),详见表2。
表2 两组患者治疗前后血浆炎症因子水平比较(±s)Tab 2 Comparison of plasma inflammatory factors levels between 2 groups before and after treatment(±s)
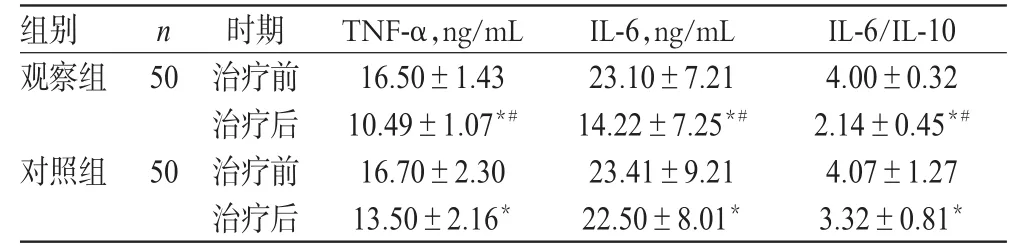
表2 两组患者治疗前后血浆炎症因子水平比较(±s)Tab 2 Comparison of plasma inflammatory factors levels between 2 groups before and after treatment(±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.control group,#P<0.05
IL-6/IL-10 4.00±0.32 2.14±0.45*#4.07±1.27 3.32±0.81*组别观察组n 50对照组50时期治疗前治疗后治疗前治疗后TNF-α,ng/mL 16.50±1.43 10.49±1.07*#16.70±2.30 13.50±2.16*IL-6,ng/mL 23.10±7.21 14.22±7.25*#23.41±9.21 22.50±8.01*
2.3 两组患者临床疗效比较
观察组患者优良率为98.00%,显著高于对照组的78.00%,差异有统计学意义(P<0.05),详见表3。

表3 两组患者临床疗效比较[例(%%)]Tab 3 Comparison of clinical efficacies between 2 groups[case(%%)]
2.4 不良反应
两组患者在治疗过程中均未见明显不良反应发生。
3 讨论
肠道是人体内最大的细菌存储区和内毒素集聚区,这些内毒素均由革兰氏阴性杆菌释放,被腹膜大量吸收后,最终进入人体的血液循环,发展为内毒素血症[6-7]。内毒素作为革兰氏阴性杆菌导致疾病的启动因子,与体内的巨噬细胞接触可以诱生释放出诸多炎症因子,例如TNF-α、IL-6和IL-10等,这些因子可以直接或间接地发挥局部效应,进而导致SIRS,严重者会发展成为脓毒性休克[8]。
本研究结果显示,观察组患者治疗后体内的血浆内毒素、TNF-α、IL-6及IL-6/IL-10水平均明显低于对照组,说明血必净注射液联合亚胺培南西司他丁对腹腔重症感染患者进行治疗,可以有效改善其内毒素及炎症因子水平。TNF-α作为整个细胞因子网络中较为关键的一员,在循环反应中诞生时间较早,并且会迅速释放达到高峰,并诱导其他相关因子的产生和分泌。TNF-α可刺激单核巨噬细胞释放出IL-10和IL-6,并呈现剂量依赖性[9-10]。IL-6能够在TNF-α的诱导下释放,成为促使炎症加重的重要因子。IL-6除了侵害血管的内皮细胞以及激活体内的炎症细胞之外,还可以诱导急性期的蛋白合成、分泌,进而在SIRS的发病过程中起到十分重要的作用,故IL-6在整个循环过程中的水平可反映SIRS的严重程度[11]。IL-10作为一种较为多见的抗炎症因子,通常是由于辅助性T细胞以及内毒素等不断刺激单核巨噬细胞所释放[12]。IL-10可以有效抑制单核的巨噬细胞以及多形核白细胞分泌TNF-α、IL-10、IL-6、IL-12和趋化因子等,进而防止组织受损,发挥抗炎功能。SIRS是体内促炎-抗炎平衡紊乱的结果,促炎因子以及抗炎因子的比例和SIRS的预后有着相关性[13]。
本研究结果还显示,观察组患者的临床疗效优良率显著高于对照组,说明血必净注射液联合亚胺培南西司他丁对腹腔重症感染患者的疗效较好。腹腔重症感染的治疗关键在于杀灭体内的病原体。临床上多种抗菌药物可以有效地清除革兰氏阴性杆菌。然而需注意,内毒素作为革兰氏阴性菌胞壁结构的重要成分之一,抗菌药物在清除细菌的同时也可能会使得内毒素从体内的细菌胞壁上释放出来,进而成为游离态内毒素[14]。中药注射剂血必净注射液由红花、赤芍、川芎、丹参和当归等成分构成,具有清热解毒、活血化瘀以及扶正祛邪之功,可以减少内毒素以及各种炎症因子的释放,有效中和内毒素,抑制革兰氏阴性菌,并抑制炎症因子的分泌[15]。
综上所述,血必净注射液联合亚胺培南西司他丁治疗腹腔重症感染疗效显著,能明显控制患者内毒素以及炎症因子的释放,且安全性较高。但本研究样本较小、观察时间较短,有待扩大样本后进一步研究。
[1] 任建安.腹腔真菌感染[J].中国感染与化疗杂志,2011,11(2):111.
[2] 吴新军,王雷,秦玉刚,等.腹腔感染与血清降钙素原水平变化的相关性分析[J].中华医院感染学杂志,2013,23(14):3418-3420.
[3] 谢剑锋,杨毅.1例重症腹腔感染的诊治[J].中华急诊医学杂志,2013,22(2):210-212.
[4] 林浩,陈杰,刘立玺,等.超早期肠内营养对重度急性胰腺炎大鼠肠黏膜屏障功能的影响[J].世界华人消化杂志,2014,25(13):1785-1792.
[5] 齐文杰,张淑文.全身炎症反应综合征评分在急性感染患者顶后中的价值[J].临床和实验医学杂志,2002,1(2):76-79.
[6] 翁明钢,梁赣锋,沈扬,等.肠道去污剂对肝硬化患者肝功能、血浆内毒素、肿瘤坏死因子α及降钙素原水平的影响[J].中国现代医生,2014,52(15):4-6.
[7]Woo SM,Choi YK,Cho SG,et al.A new herbal formula,KSG-002,suppresses breast cancer growth and metastasis by targeting NF-κB-dependent TNF-α production in macrophages[J].Evid Based Complement Alternat Med,2013,2013(1):258-259.
[8] Costa DL,Rocha RL,Carvalho RM,et al.Serum cytokines associated with severity and complications of kala-azar [J].Pathog Glob Health,2013,107(2):78-87.
[9] 叶勇,马金良,余继海,等.血必净在门静脉高压症术后的应用[J].安徽医药,2015,19(1):82-86.
[10] 沈绚丽,杨建锋,楼立兰.经皮穿刺腹腔置管引流治疗重症急性胰腺炎并发腹腔感染的效果分析[J].中华医院感染学杂志,2014,24(6):1491-1493.
[11] 丁卉,丁茂文,陈丽珠,等.耐碳青霉烯类肠杆菌科细菌的分布及耐药性分析[J].药物流行病学杂志,2014,23(10):608-611.
[12] 殷娜,邓小明.外科重症监护病房腹腔感染相关脓毒症病原菌分布及耐药性分析[J].重庆医学,2014,43(7):812-815.
[13] 王燕萍,李德榜,董春禄.国产美罗培南与进口亚胺培南/西司他丁预防重症急性胰腺炎腹腔感染的随机对照研究[J].中国药房,2012,23(18):1682-1684.
[14] 张霖,赵明敬,赵威.微生态制剂对慢性肝衰竭患者肠道菌群与血浆内毒素及细胞因子的影响[J].中华医院感染学杂志,2015,25(2):262-264.
[15] 林孝银.乌司他丁对感染性休克患者血清白介素-6、10和降钙素原水平的影响[J].药物流行病学杂志,2014,23(1):12-14.
(编辑:黄 欢)
Clinical Observation of Xuebijing Injection Combined with Imipenem and Cilastatin in the Treatment of Severe Abdominal Infection
LIU Moran1,XIAO Yin2,HUANG Jialing1,TIAN Hairong1,CAI Qibo1(1.Dept.of Clinical Laboratory,the Third Affiliated Hospital of Qiqihar Medical College,Heilongjiang Qiqihar 161000,China;2.Dept.One of Oncology,the Third Affiliated Hospital of Qiqihar Medical College,Heilongjiang Qiqihar 161000,China)
OBJECTIVE:To observe clinical efficacy and safety of Xuebijing injection combined with imipenem and cilastation in the treatment of severe abdominal infection,and its effects on plasma endotoxin and inflammatory factors.METHODS:During Apr.2013-Apr.2016,100 patients with severe abdominal infection in our hospital were divided into observation group and control group according to random number table,with 50 cases in each group.Both groups were given Imipenem and cilastation sodium for injection 0.5 g added into 0.9%Sodium chloride injection 500 mL,ivgtt(≥40 min),q12 h.Eight hours later,observation group was additionally given Xuebijing injection 100 mL added into 0.9%Sodium chloride injection 500 mL,ivgtt,bid;Both groups were treated for 5-7 d.The levels of plasma endotoxin and inflammatory factors(TNF-α,IL-6,IL-6/IL-10)were compared in 2 groups before after treatment,and clinical efficacies and the occurrence of ADR was recorded.RESULTS:Before treatment,there was no statistical significance in plasma endotoxin or inflammatory factor levels between 2 groups(P>0.05).After treatment,plasma endotoxin and inflammatory factor levels of 2 groups were decreased significantly,and the observation group was significantly lower than the control group,with statistical significance(P<0.05).The excellent and good rate of observation group was 98.00%,which was significantly higher than 78.00%,with statistical significance(P<0.05).No obvious ADR was found in 2 groups.CONCLUSIONS:Xuebijing injection combined with imipenem and cilastation show significant therapeutic efficacy for severe abdominal infection,can effectively control the release of endotoxin and inflammatory factors with good safety.
Xuebijing injection;Imipenem and cilastation;Severe abdominal infection;Endotoxin;Inflammatory factor
R512.5
A
1001-0408(2017)23-3271-03DOI10.6039/j.issn.1001-0408.2017.23.29
2017-01-23
2017-06-25)
*主管技师。研究方向:抗细菌与真菌感染。电话:0452-2697258。E-mail:13845213704@163.com
#通信作者:主治医师。研究方向:肿瘤学。电话:0452-2697354。E-mail:15946494903@163.com

