贝伐珠单抗联合FOLFIRI方案治疗晚期结肠癌的临床观察
周 芳,王建军,程传耀,卢 红(河南大学淮河医院肿瘤科,河南开封 475000)
贝伐珠单抗联合FOLFIRI方案治疗晚期结肠癌的临床观察
周 芳*,王建军,程传耀,卢 红(河南大学淮河医院肿瘤科,河南开封 475000)
目的:观察贝伐珠单抗联合伊立替康+亚叶酸钙+氟尿嘧啶(FOLFIRI)方案治疗晚期结肠癌的疗效、毒副反应及患者生存率。方法:选择我院肿瘤科2010年1月-2014年8月收治的113例晚期结肠癌患者作为研究对象,按照随机数字表法分为观察1组(40例)、观察2组(39例)和对照组(34例)。3组化疗方案均为FOLFIRI方案,观察1组、2组在此基础上分别联用贝伐珠单抗注射液5、7.5 mg/kg,14 d为1个周期,均治疗8个周期。比较3组患者的临床疗效,治疗前后血管内皮生长因子A(VEGF-A)阳性率、免疫指标(T细胞亚群中CD3+、CD3+CD4+、CD3+CD8+细胞所占比例)、毒副反应发生率及1年/2年生存率。结果:观察1组、2组患者的临床总有效率均显著高于对照组,VEGF-A阳性率均显著低于对照组,差异均有统计学意义(P<0.05)。3组患者CD3+、CD3+CD4+、CD3+CD8+所占比例均较治疗前显著降低,但观察1组、2组患者的显著高于对照组,差异均有统计学意义(P<0.05)。观察1组及对照组患者的高血压(3~4级)发生率均显著低于观察2组,观察1组和观察2组患者的白细胞减少(3~4级)发生率均显著低于对照组,差异均有统计学意义(P<0.05)。3组患者1年生存率比较,差异无统计学意义(P>0.05);观察1组、2组患者的2年生存率均显著高于对照组,差异有统计学意义(P<0.05)。结论:不同剂量贝伐珠单抗联合FOLFIRI方案治疗晚期结肠癌均有明显增效作用,可有效抑制VEGF-A,并发挥免疫保护和抗毒副作用,延长患者生存期;低剂量贝伐珠单抗的高血压发生率更低,安全性更高。
晚期结肠癌;贝伐珠单抗;化疗;毒副反应;免疫保护
结肠癌为常见消化道肿瘤,世界卫生组织(WHO)的相关调查研究显示,全球每年约100万人罹患结肠癌[1]。该病主要由基因遗传或机体肠黏膜上皮细胞病变引起,手术为其有效治疗手段。但该病发病隐匿,约25%的患者发病时已经失去手术机会,故其临床治疗以化疗为主。化疗易对机体免疫功能造成损伤,严重者会难以耐受药物毒副反应。近年的大量临床研究发现,分子靶向药物联合化疗方案可有效提高晚期结肠癌患者的临床疗效并延长生存期[2-3]。贝伐珠单抗为典型的分子靶向药物,已有研究证实其对恶性肿瘤具有增效、减毒作用。本研究观察了贝伐珠单抗联合伊立替康+亚叶酸钙+氟尿嘧啶(FOLFIRI)方案治疗晚期结肠癌的疗效、毒副反应及患者生存率,并分析其机制,现报道如下。
1 资料与方法
1.1 纳入、排除与脱落标准
纳入标准:(1)经病理组织学、影像学检查确诊为Ⅳ期结肠癌;(2)Karnofsky(KPS)评分≥70分;(3)预计生存期>5个月;(4)初次就诊。
排除标准:(1)严重心、肺、肝、肾功能异常者;(2)既往心肌梗死、高血压病史者;(3)存在化疗禁忌证者;(4)有放/化疗史者。
脱落标准:(1)因各种原因要求退出本研究者;(2)因无法耐受而导致治疗中断者。
1.2 研究对象
本研究为前瞻性研究。选择我院肿瘤科2010年1月-2014年8月收治的113例晚期结肠癌患者作为研究对象,按照随机数字表法分为观察1组(40例)、观察2组(39例)和对照组(34例)。其中,观察1组患者男性22例,女性18例;年龄36~69岁,平均年龄(56.2±8.1)岁;KPS评分73~84分,平均KPS评分(77.0±3.2)分;病理类型为腺癌33例,黏液腺癌7例。观察2组患者男性24例,女性15例;年龄38~67岁,平均年龄(55.9±7.7)岁;KPS评分72~85分,平均KPS评分(77.6±4.0)分;病理类型为腺癌28例,黏液腺癌11例。对照组患者男性22例,女性12例;年龄38~67岁,平均年龄(55.7±7.0)岁;KPS评分71~83分,平均KPS评分(77.3±3.6)分;病理类型为腺癌26例,黏液腺癌10例。3组患者的性别、年龄、KPS评分和病理类型等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。本研究方案经我院医学伦理委员会审核通过,患者均知情同意并签署知情同意书。
1.3 治疗方法
3组患者化疗方案均为FOLFIRI方案:盐酸伊立替康注射液(江苏恒瑞医药股份有限公司,批准文号:国药准字H20061276,规格:5 mL∶100 mg)180 mg/m2,加至0.9%氯化钠注射液500 mL中静脉滴注(90 min内),d1;注射用亚叶酸钙(江苏恒瑞医药股份有限公司,批准文号:国药准字H32022391,规格:100 mg)400 mg/m2,加至0.9%氯化钠注射液250 mL中静脉滴注(持续2 h),d1;氟尿嘧啶注射液(上海旭东海普药业有限公司,批准文号:国药准字H31020593,规格:10 mL∶0.25 g)400 mg/ m2,静脉推注,d1;之后给予氟尿嘧啶静脉泵入,2 400 mg/m2(持续46 h)。14 d为1个周期[4]。治疗期间均常规给予升白细胞、止吐药物。观察组患者在对照组基础上联用贝伐珠单抗注射液[Roche Pharma(Schweiz)Ltd.,注册证号:S20120069,规格:400 mg(16 mL)/瓶],观察1组的使用剂量为5 mg/kg,观察2组为7.5 mg/kg,均加至0.9%氯化钠注射液500 mL中静脉滴注,14 d为1个周期。3组患者均治疗8个周期。
1.4 观察指标
(1)观察3组患者临床疗效。参照《实体瘤治疗疗效评价标准——RECIST》[5]进行评价——完全缓解(CR):所有可见目标病灶和非目标病灶均消失,肿瘤标志物水平恢复至正常范围,且持续时间≥4周;部分缓解(PR):基线病灶的长径总和缩小30%以上,肿瘤标志物浓度有所下降,持续时间≥4周;疾病稳定(SD):目标病灶未缩小但长径总和增大不超过20%,肿瘤标志物浓度无明显变化;疾病进展(PD):基线病灶长径总和增加20%以上或有新病灶出现,肿瘤标志物浓度升高。总有效=CR+ PR。(2)观察3组患者治疗前后血管内皮生长因子A(VEGF-A)的阳性率。于治疗前后抽取3组患者外周血5 mL,以1 500 r/min(离心半径为6 cm)离心15 min,采用酶联免疫吸附试验法检测VEGF-A水平,VEGF-A质量浓度在15.625~1 000 pg/mL即判定为阳性。试剂盒由上海超研生物科技有限公司提供,严格按试剂盒说明书操作。(3)观察3组患者治疗前后免疫指标水平。于治疗前后抽取3组患者外周血5 mL,应用流式细胞术检测T细胞亚群中CD3+、CD3+CD4+和CD3+CD8+所占比例。(4)记录3组患者毒副反应发生率。参照《恶性肿瘤化疗的毒副作用及其防治》中相关标准对毒副反应进行评价,分为0~4级[6]。由于1级和2级的毒副反应较轻,予以相应措施可获得缓解,因而本研究仅比较3级和4级毒副反应发生率。其中,胃肠道反应、神经毒性通过症状观察确定,出血/血栓、血小板减少、白细胞减少通过血常规检测确定。(5)记录3组患者生存期。对3组患者进行2年随访,记录失访情况以及1年与2年生存率。
1.5 统计学方法
应用SPSS 19.0软件对数据进行统计分析。计量资料符合正态分布,用±s表示,两组间比较采用t检验,多组间比较采用F检验。计数资料和等级资料均以例数或率表示,前者两组间比较采用χ2检验、多组间比较采用H检验,后者采用Z检验。P<0.05为差异有统计学意义。
2 结果
2.1 脱落情况
观察1组患者脱落2例,其中1例因经济原因中途放弃治疗,1例为无法耐受毒副反应中断治疗;观察2组患者脱落1例,因经济原因中途放弃治疗;对照组无脱落病例。最终纳入统计的合格病例数为观察1组38例、观察2组38例、对照组34例。
2.2 3组患者临床疗效比较
观察1组患者的临床总有效率为42.1%(16/38),观察2组为39.5%(15/38),均显著高于对照组的17.6%(6/ 34),差异均有统计学意义(P<0.05),详见表1。
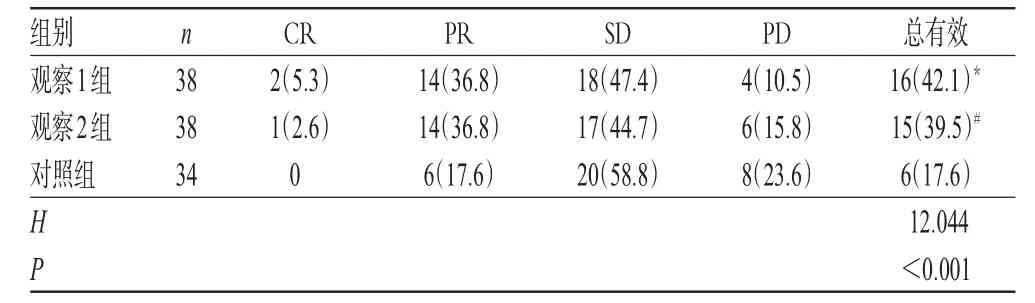
表1 3组患者临床疗效比较[例(%%)]Tab 1 Comparison of clinical efficacies among 3 groups[case(%%)]
2.3 3组患者治疗前后VEGF-A阳性率比较
治疗前,3组患者的VEGF-A阳性率比较,差异无统计学意义(P>0.05);治疗后,观察1组和观察2组患者VEGF-A阳性率分别为31.6%、28.9%,显著低于对照组的55.9%,差异均有统计学意义(P<0.05),详见表2。
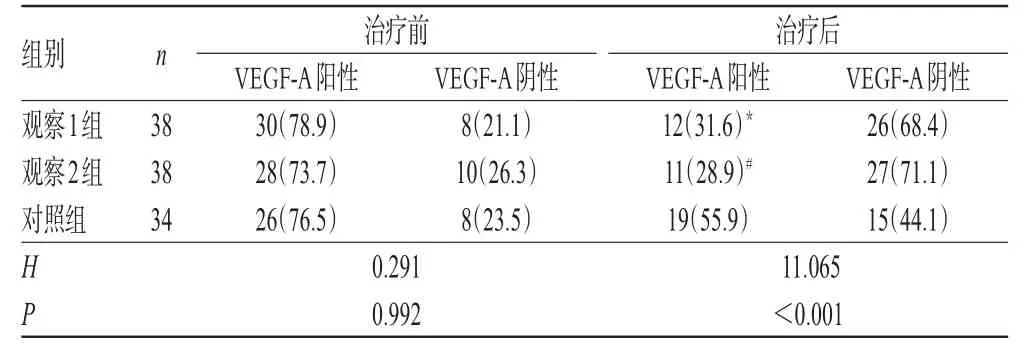
表2 3组患者治疗前后VEGF-A阳性率比较[例(%%)]Tab 2 Comparison of positive rate of VEGF-A among 3 groups before and after treatment[case(%%)]
2.4 3组患者治疗前后免疫指标比较
治疗前,3组患者CD3+、CD3+CD4+、CD3+CD8+所占比例比较,差异均无统计学意义(P>0.05);治疗后,3组患者CD3+、CD3+CD4+、CD3+CD8+所占比例均较治疗前显著降低,但观察1组和观察2组均显著高于对照组,差异均有统计学意义(P<0.05),详见表3。
2.5 3组患者毒副反应发生情况比较
3组患者的胃肠道反应、出血/血栓、血小板减少和神经毒性(3~4级)的发生率比较,差异均无统计学意义(P>0.05);观察1组和对照组的高血压(3~4级)发生率均显著低于观察2组,观察1组和观察2组的白细胞减少(3~4级)发生率均显著低于对照组,差异均有统计学意义(P<0.05),详见表4。
2.6 3组患者1年与2年生存率比较
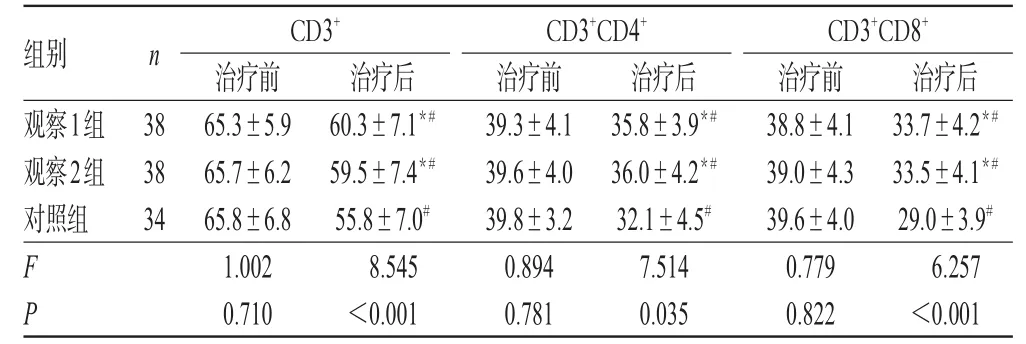
表3 3组患者治疗前后免疫指标比较(%%)Tab 3 Comparison of immune indexes among 3 groups before and after treatment(%%)

表4 3组患者毒副反应(3~4级)发生情况比较[例(%%)]Tab 4 Comparison of occurrence of ADR(grade 3~4)among 3 groups[case(%%)]
随访期间,观察1组和对照组患者各有1例失访,时间为随访开始后1年内。3组患者1年生存率比较,差异无统计学意义(P>0.05);观察1组和观察2组患者2年生存率均显著高于对照组,差异均有统计学意义(P<0.05),详见表5。
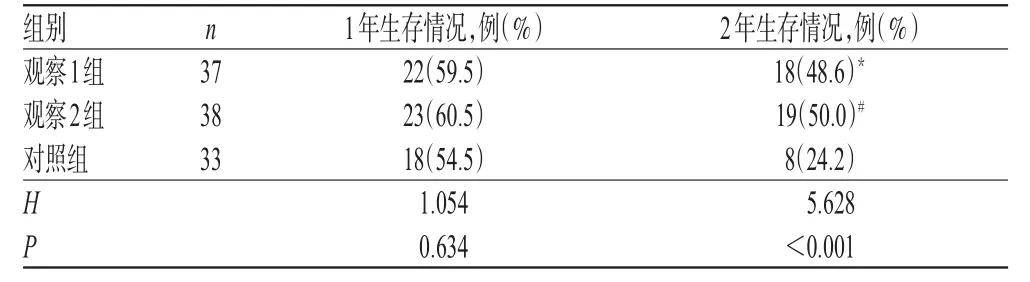
表5 3组患者1年与2年生存率比较[例(%%)]Tab 5 Comparison of 1-year and 2-year survival rates among 3 groups[case(%%)]
3 讨论
FOLFIRI方案为晚期结肠癌临床治疗的常用化疗方案,其药物的联合应用可有效阻止癌细胞的增殖、浸润,并诱使癌细胞调亡。但化疗存在选择性不强的缺陷,对机体的损伤作用难以避免,如何增强化疗疗效并减轻毒副作用已经成为临床重点研究课题[7]。
本研究为探析贝伐珠单抗在晚期结肠癌临床治疗中的应用价值,将单纯FOLFIRI化疗与FOLFIRI化疗联合不同剂量的贝伐珠单抗治疗晚期结肠癌的疗效进行对比,结果显示观察1组、观察2组患者治疗总有效率均显著高于对照组,提示不同剂量贝伐珠单抗的应用均具有明显增效作用。肿瘤组织的生长主要通过新生血管提供所需氧气和营养物质。血管生成过程复杂,首先需从预先存在的血管中出芽,并进行套叠生长、分裂与分化而形成新生血管[8]。新生血管的形成涉及多因子和多信号,其中VEGF发挥了关键作用。研究显示,一旦切断肿瘤新生血管,肿瘤将会因失去营养供给而停止生长甚至萎缩死亡[9]。针对该观点,抗血管生成的抗肿瘤药物已经成为结肠癌的临床治疗新思路。贝伐珠单抗为重组的VEGF单克隆抗体,属典型的抗血管生成药物,可特异性结合VEGF并抑制其生物活性,有效抑制血管内皮细胞增殖,从而抑制新生血管的生成,最终阻断肿瘤组织的营养供应,减缓或阻止肿瘤生长。本研究对3组患者治疗前后的VEGF-A水平进行检测,结果显示,治疗后观察1组和观察2组患者VEGF-A阳性率下降幅度均大于对照组,提示不同剂量贝伐珠单抗均可通过对新生血管的抑制实现增效作用。目前,国内外有关贝伐珠单抗在结肠癌中的应用研究已有较多报道,其中将其联合FOLFIRI化疗作为一线治疗的研究结果均显示疾病控制率与有效率高于单纯化疗组,其增效作用得以证实[10-11],与本研究结论一致。另外,肿瘤进展与患者生存期有直接关系,若肿瘤得到有效控制,则生存期可大幅延长。本研究中,观察1组和观察2组患者的2年生存率均高于对照组,表明贝伐珠单抗联合FOLFIRI方案可更有效控制肿瘤进展,使患者生存期得到延长,2年随访结束时的生存率更高。
肿瘤的发生、发展和转移均与患者免疫功能有明显相关性,因而对于恶性肿瘤患者而言,免疫功能的评估也是临床疗效的重要判定指标。晚期结肠癌患者多处于免疫抑制状态,免疫功能低下,机体抗肿瘤能力和抗毒副反应能力也因此减弱[12]。由于宿主抗肿瘤反应以T淋巴细胞介导的细胞免疫反应为主,因此本研究选取T淋巴细胞亚群指标评估患者免疫功能。结果显示,观察1组和2组患者采取贝伐珠单抗联合FOLFIRI方案治疗8个周期后CD3+、CD3+CD4+、CD3+CD8+所占比例均降低,但高于对照组,下降幅度较小,提示贝伐珠单抗的应用可起到免疫保护的作用。
大量研究表明,贝伐珠单抗除可实现化疗的增效作用外,还具有抗毒副反应的作用,有利于减轻化疗毒副反应[13-14]。笔者认为,贝伐珠单抗抗毒副作用的实现与其可增强机体免疫功能具有相关性。贝伐珠单抗的应用,减弱了机体因化疗所致的免疫抑制作用,使患者对化疗不良反应的抵抗能力增强,毒副反应减轻。本研究中,3组患者毒副反应均以胃肠道反应、出血/血栓、高血压、血小板减少、白细胞减少和神经毒性为主,其中观察1组和观察2组患者的白细胞减少(3~4级)发生率均低于对照组,表明贝伐珠单抗的应用有效降低了白细胞减少(3~4级)发生率。白细胞减少与免疫功能有关,贝伐珠单抗的应用具有增强机体免疫的作用,因而可有效避免白细胞减少。高血压为贝伐珠单抗的常见不良反应,发生率可高达40%[15]。贝伐珠单抗引起高血压的原因主要在于其可能降低外周微血管密度及内皮细胞一氧化氮含量,使平滑肌松弛、血管扩张,从而导致血压升高[16]。本研究在毒副反应的统计过程中仅记录3~4级毒副反应,因而观察1组和观察2组患者的高血压发生率均低于有关报道[17]。同时,观察1组高血压(3~4级)发生率为2.6%,观察2组为15.8%,表明低剂量贝伐珠单抗可减少高血压的发生。另外,本研究样本量较小,观察1组和观察2组患者胃肠道反应、出血/血栓、高血压和神经毒性等毒副反应发生率与对照组接近,贝伐珠单抗的抗毒副反应作用仅在白细胞减少方面得到体现,其在晚期结肠癌患者中的应用优势有待进一步探索。
综上所述,不同剂量贝伐珠单抗联合FOLFIRI方案治疗晚期结肠癌均有明显增效作用,可有效抑制VEGF-A,发挥免疫保护和抗毒副作用,延长患者生存期。低剂量贝伐珠单抗的高血压不良反应发生率较低,安全性更高。但本研究样本量较小,故该结论仍需大样本、高质量的研究加以证实。
[1] 吕畅,王红芳,阎雪莹.以血管内皮生长因子及其受体为靶点的抗肿瘤药的研究进展[J].中国药房,2016,27(13):1851-1853.
[2] 魏世东,孙劲文.贝伐单抗联合化疗治疗晚期结直肠癌疗效分析[J].临床和实验医学杂志,2014,13(4):292-294.
[3] 徐琦,刘碧霞,顾琳慧,等.不同剂量贝伐单抗在荷结肠癌细胞裸鼠中对伊立替康分布的影响[J].肿瘤防治研究,2016,43(4):263-266.
[4] 陈芬,江千秋,焦兰,等.DC-CIK联合化疗加靶向治疗对晚期结肠癌的临床疗效观察[J].现代肿瘤医学,2015,23(12):1686-1690.
[5] 杨学宁,吴一龙.实体瘤治疗疗效评价标准:RECIST[J].循证医学,2004,4(2):85-90、111.
[6] 段庚仙.恶性肿瘤化疗的毒副作用及其防治[J].肿瘤研究与临床,2004,16(5):353-354.
[7] 赛福丁·克尤木,布力布·吉力斯汉,唐勇,等.FOLFOX-6化疗方案联合贝伐单抗靶向治疗转移性结肠癌的疗效[J].实用癌症杂志,2015,30(8):1200-1202.
[8] 张满赐,赵敏.贝伐单抗在治疗结肠癌患者中的疗效观察[J].现代消化及介入诊疗,2015,20(1):55-56.
[9] Greenberger S,Boscolo E,Adinib I.Corticosteroid suppression of VEGF-A in infantile hemangioma-derived stem cells[J].New Engl J Med,2010,362(11):1005-1013.
[10] 马宁,王朝杰,周云.化疗联合贝伐珠单抗治疗结直肠癌肝转移的临床观察[J].中国药房,2015,26(35):4995-4997.
[11] 张骥杰,倪国华,吴书庆,等.贝伐单抗联合IFL方案治疗晚期结肠癌的临床研究[J].江苏医药,2014,40(19):2331-2333.
[12] 丁医峰,李华.贝伐单抗联合FOLFOX化疗在老年结直肠癌患者中的安全性和有效性[J].中国老年学杂志,2016,36(9):2175-2177.
[13] 赵静,张文,李文桦,等.贝伐单抗联合化疗治疗晚期结直肠癌的临床观察[J].中国癌症杂志,2011,21(10):799-802.
[14] Thanapprapasr D,Hu W,Sood AK,et al.Moving beyond VEGF for anti-angiogenesis strategies in gynecologic cancer[J].Curr Pharm Design,2012,18(19):2713-2719.
[15] 何干,杨强,李启刚,等.西妥昔单抗或贝伐单抗联合FOLFOX4方案治疗晚期直肠癌患者的临床观察[J].中国药房,2016,27(8):1078-1081.
[16] 武晓楠,赵赟博,伍建宇,等.贝伐单抗联合卡培他滨治疗转移性结直肠癌的临床观察[J].中国医学科学院学报,2010,32(4):417-420.
[17] 刘洋,尤振宇,苏晓辉,等.贝伐单抗结合化疗治疗晚期结肠癌的生存分析[J].现代肿瘤医学,2015,23(10):1394-1398.
(编辑:晏 妮)
Clinical Observation of Bevacizumab Combined with FOLFIRI Plan in the Treatment of Advanced Colon Cancer
ZHOU Fang,WANG Jianjun,CHENG Chuanyao,LU Hong(Dept.of Oncology,the Affiliated Huaihe Hospital of Henan University,Henan Kaifeng 475000,China)
OBJECTIVE:To observe therapentic efficacy of bevacizumab combined with irinotecan+leucovorin+fluorouracil(FOLFIRI)plan in the treatment of advanced colon cancer,toxic reaction and patients’survival rate.METHODS:A total of 113 patients with advanced colon cancer admitted to the oncology department in our hospital from Jan.2010 to Aug.2014 were randomized into observation group 1(40 cases),observation group 2(39 cases)and control group(34 cases).Three groups
FOLFIRI;observation group 1 and 2 were additionally given Bevacizumab injection 5 and 7.5 mg/kg 14 d as a treatment course,for 8 cycles.Clinical efficaices as well as the positive rate of VEGF-A,immune indexes(the proportion of CD3+,CD3+CD4+,CD3+CD8+in T cell subset)before and after treatment,the incidence of toxic reaction,1-year and 2-year survival rates were compared among 3 groups.RESULTS:The total response rate of observation group 1 and 2 were significantly higher than control group,and the positive rate of VEGF-A in observation group 1 and 2 were significantly lower than control group,with statistical significance(P<0.05).The proportion of CD3+,CD3+CD4+and CD3+CD8+in 3 groups were significantly lower than before treatment,but observation group 1 and 2 were significantly higher than control group,with statistical significance(P<0.05).The incidence of grade hypertension(grade 3-4)in observation group 1 and control group were lower than observation group 2;the incidence of leucopenia(grade 3-4)in observation group 1 and 2 were significantly lower than control group,with statistical significance(P<0.05). There was no statistical significance in 1-year survival rate among 3 groups(P>0.05).2-year survival rate of observation group 1 and 2 were significantly higher than control group,with statistical significance(P<0.05).CONCLUSIONS:For advanced colon cancer,different doses of bevacizumab combined with FOLFIRI have significant synergistic effect,can effectively inhibit VEFGA,play a role of immune protection and anti-toxic side effects,and prolong the survival time.The incidence of hypertension in patients treated with low-dose bevacizumab is relatively lower and the safety is better.
Advanced colon cancer;Bevacizumab;Chemotherapy;ADR;Immune protection
R735.3+5;R979.1
A
1001-0408(2017)23-3261-05
2016-09-07
2016-11-08)
*副主任医师,硕士。研究方向:恶性肿瘤的综合治疗。电话:0371-23906706。E-mail:zhouyuan_711@163.com
DOI10.6039/j.issn.1001-0408.2017.23.26

