改性沸石对生活饮用水中无机氟的吸附研究
王林裴 周迎春 李松亚 郑亚哲 彭新然(.漯河出入境检验检疫局,漯河 46000;.天津大学环境学院,天津 0007;.启迪桑德环境资源股份有限公司,北京 00)
改性沸石对生活饮用水中无机氟的吸附研究
王林裴1周迎春1李松亚2郑亚哲3彭新然1
(1.漯河出入境检验检疫局,漯河 462000;2.天津大学环境学院,天津 300072;3.启迪桑德环境资源股份有限公司,北京 101102)
本文对人造沸石进行改性从而得到效果比较好的吸附材料,即用0.5mol/L的硫酸钛溶液浸泡24h,并在70℃条件下烘10h后得到的负载钛沸石(Ti-Z)样品。以这种改性沸石作为实验用吸附剂,探究其对饮用水中F-的吸附性能,同时也考查了几种不同环境因素对改性沸石吸附性能的影响,通过动力学、吸附等温线等分析实验初步探究其吸附机理。
改性沸石;生活饮用水;无机氟;吸附
在我国,沸石的价格低廉、储量丰富、来源广,人造沸石作为吸附剂不仅环保且热稳定性好,经过改性后除氟性能良好,稳定可靠。我国现行饮用水含氟卫生标准参考GB5749-2006《生活饮用水卫生标准》氟化物不超过1.0mg/L[1],超过此限度易出现氟斑牙、氟骨病,甚至其他神经、心脏疾病等。为了研发高效除氟吸附剂,本论文尝试多种改性方法并从中筛选出了效果较好的用无机盐—硫酸钛制备改性沸石材料,用于去除饮用水中的F-[2-3],研究了该材料的吸附性能并初步探讨其吸附机理。该课题的研究对防止地方性氟病,改善人体健康状况有重要意义,对寻找潜在的高效除氟材料具有一定的实用价值。
1 材料与方法
1.1 材料与试剂
氟化钠、柠檬酸三钠、人造沸石、氯化钠、硫酸钛、盐酸、氢氧化钠、硝酸钠、磷酸钠、碳酸钠、冰醋酸(均购于国药集团化学试剂有限公司,分析纯)。
1.2 仪器与设备
702型复合氟离子选择电极(上海罗素科技有限公司);磁力搅拌器(85-1型),六联电动搅拌器(JJ-3型),电子天平(CP114),奥豪斯仪器(上海)有限公司;数控超声波清洗仪(KQ3200DE型),水浴恒温振荡器(KQ3200DE型),超纯水仪(UPT-11-10T)。
1.3 制备方法
(1)预处理:先用纯水清洗沸石(约2~3次),以除去沸石里面的杂质;在70℃条件下烘10h至干燥,置于瓶中密封备用。
(2)称取10g沸石,加入100mL 0.5mol/L的硫酸钛溶液中,搅拌约30mi后静置,浸泡24h;弃上清液后再用纯水洗涤3~5次,置于70℃条件下烘10h,干燥后密封保存。
2 结果与讨论
2.1 投放量的影响
(1)未改性沸石与改性沸石(Ti-Z)的吸附性能比较
沸石改性前后对F-的吸附效果比较如图1所示。

图1 人造沸石与Ti-Z的吸附效果比较
由图可知,经硫酸钛改性后的沸石吸附效率远高于未改性沸石,吸附效果较好,可用作吸附F-的吸附剂。
(2)最佳投放量
实验中选用1.0、2.0、4.0、6.0、8.0g/L作为投放量,室温条件(25℃)下,在相同的初始浓度C0=50mg/L的F-溶液中进行实验,结果如下图2所示。
由图分析,Ti-Z投放量为4g/L时,吸附容量与去除率都较高,因此,综合吸附量和去除率两方面考虑,以此作为最佳投放量。
2.2 吸附动力学
为了研究Ti-Z吸附F-的动力学行为,对图2(a) 中的吸附散点数据采用不同模型进行拟合,拟合结果如图3,拟合参数见表1。

图2(a)吸附容量与投加量关系

图2(b)去除率与投加量关系

表1 Ti-Z的吸附动力学参数
注:K1—准一级动力学吸附速率常数;K2—准二级反应速率常数;Kp—粒子内扩散常数;A—初始吸附速率;B—解吸常数。
由表1可以看到,准二级动力学模型的线性拟合度较高,线性相关系数均能在0.990以上,且由该方程计算得到的qe值与测量值相近。因此,准二级动力学模型最适合描述Ti-Z吸附F-的动力学过程。
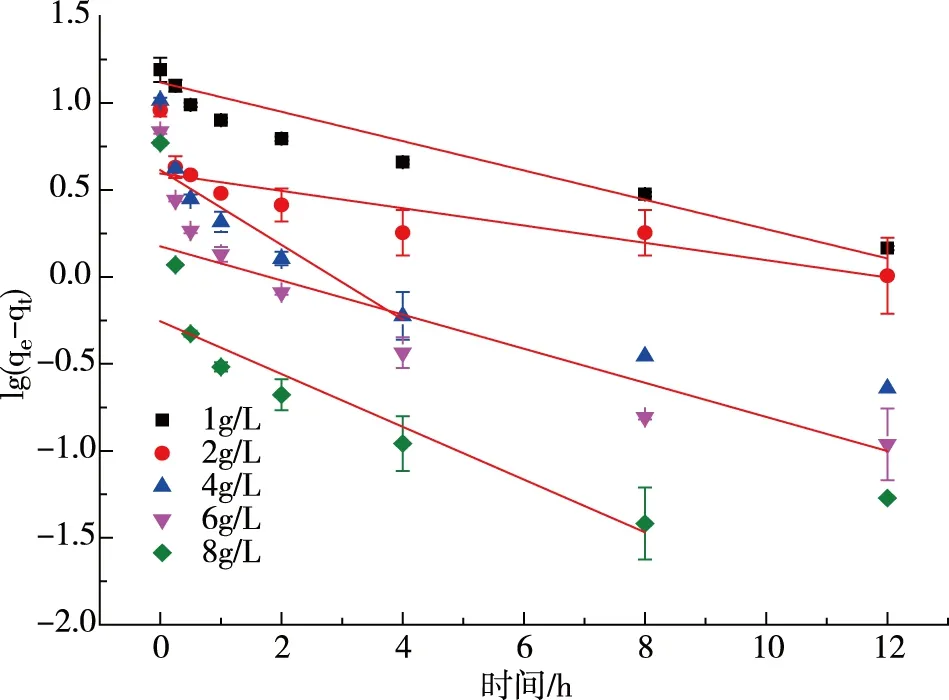
图3 (a)准一级动力学
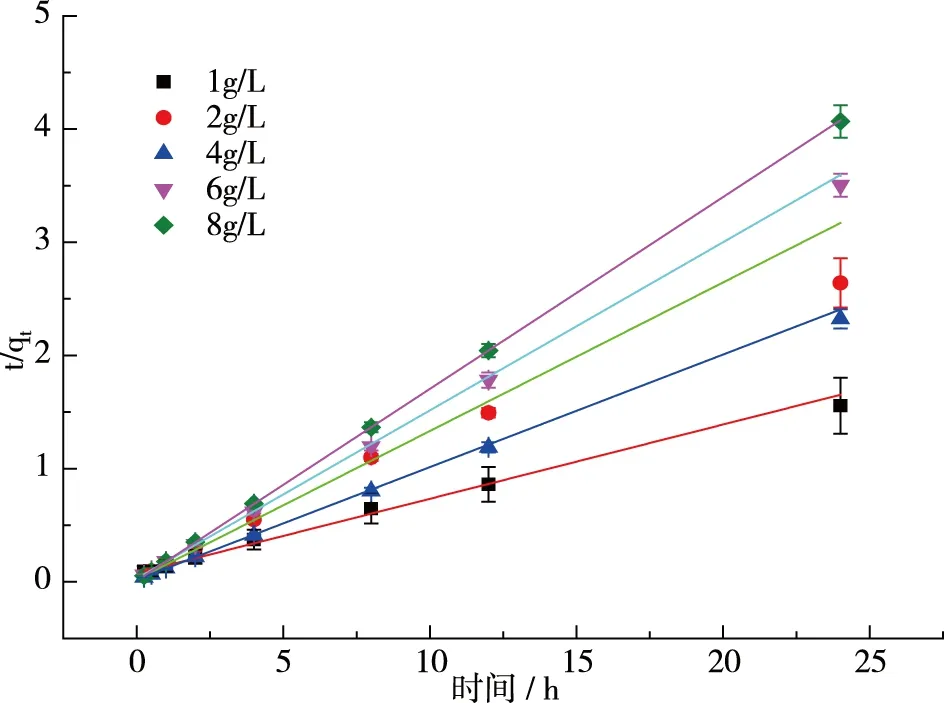
图3 (b)准二级动力学

图3 (c)Elovich模型

图3 (d)粒子内扩散模型
粒子内扩散模型拟合R2较低,说明是以化学吸附为主,仅有少量F-通过内扩散被固定吸附。
2.3 F-初始浓度的影响
分别配制初始浓度C0=4.77、8.69、24.13、52.78mg/L的四种溶液在室温下进行实验,F-去除率结果见图4。
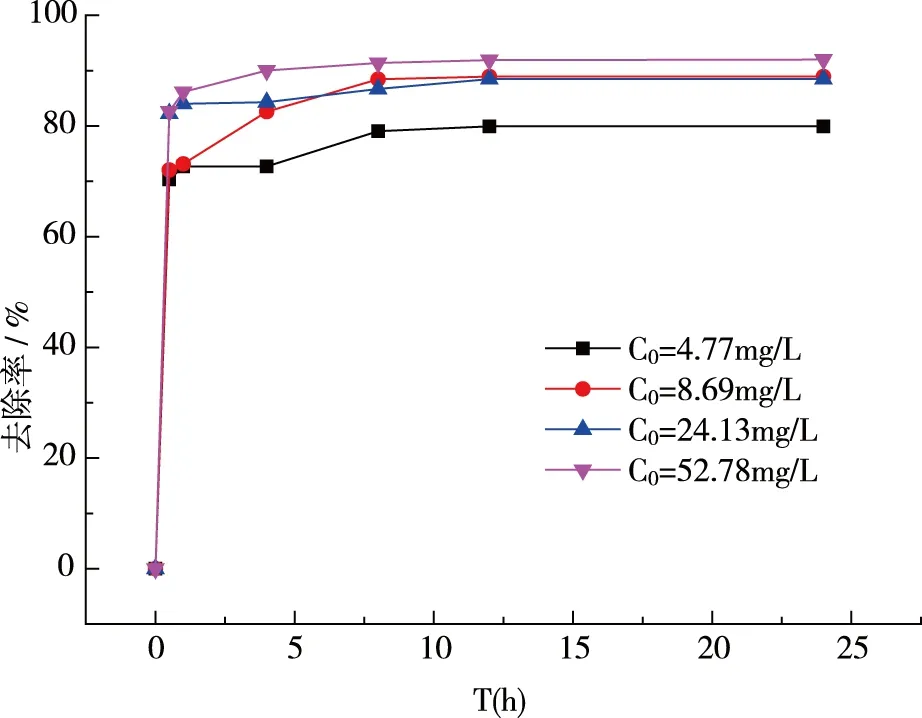
图4 初始浓度对去除率的影响
由图4,C0=4.77mg/L的溶液F-去除率可以达到79.5%左右,C0=52.78mg/L时,可以达到92%。但是当C0=52.78mg/L时吸附容量并不能随之增加。因此,随着初始浓度的增加,去除率逐渐增大,但是并不会无限增大,这是因为吸附剂的吸附位点有限,到达一定程度后会达到饱和状态,吸附效果并非越来越好。
2.4 pH的影响
配制初始浓度为4.77、24.65、53.76mg/L的F-溶液在室温下进行吸附试验。由图5可知,吸附量随着pH的增加而减小,在pH=3时最大。这是由于在溶液pH
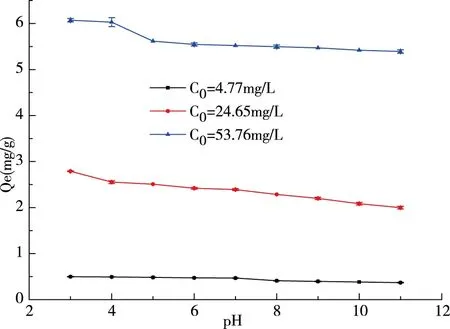
图5 (a)pH对吸附容量的影响
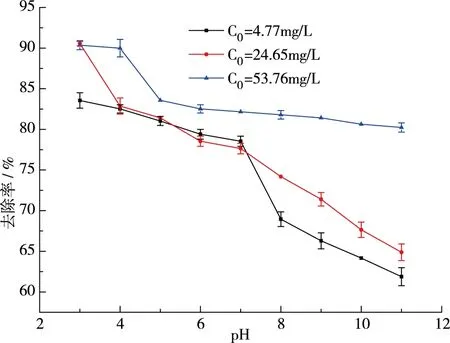
图5 (b)pH对去除率的影响
pH对吸附的影响归属于材料表面电荷情况。Ti-Z吸附F-前后电位变化如图5(c)所示。吸附F-以后,电位值随着pH增加而下降,结合图5(a)和5(b),吸附量呈减小趋势,其与Zeta电位的相关性可以解释为当表面电荷减少或变为负值时,材料对OH-的吸附使得吸附剂对F-的吸附性减弱,表明该吸附过程是以静电吸附为主导[6]。

图5 (c)Ti-Z吸附F-前后Zeta电位变化
2.5 共存离子的影响

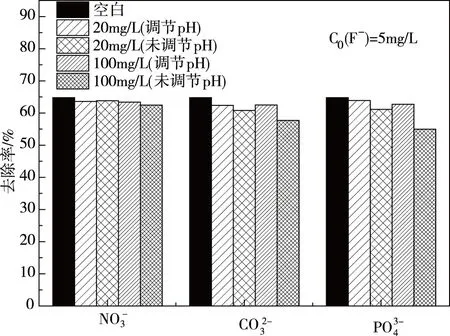
图6 共存离子对Ti-Z吸附F-的影响

2.6 温度的影响
(1)不同反应温度下的吸附性能比较
用初始浓度为5mg/L的F-溶液为模拟水样(pH相同)。控制温度分别在15℃、20℃、25℃、30℃、35℃条件下反应,直至吸附平衡,结果如图7。
由图7可知,用Ti-Z对不同浓度的F-溶液吸附时,在15~20℃范围内,随着温度的升高,吸附容量逐渐增大,在20℃时吸附容量达到最大,25~30℃范围内,又逐渐下降,由此可知,该吸附属于放热过程,高温对吸附不利。因此,为了使吸附效果好并减少能源消耗,可在室温下进行。

图7 温度对吸附容量的影响
(2)吸附等温线
将不同温度下Ti-Z对F-的吸附实验数据用Langmuir和Freundlich 吸附等温式进行非线性拟合,如图8,拟合参数见表2。

图8 15℃下用不同模型拟合
从拟合参数来看,Freundlich模型的拟合度较高,R2均能达到0.99以上,随着温度的升高,n值与Kf均是从15℃到20℃逐渐增大,后又逐渐下降,即适当温度有利于吸附进行,温度过高对吸附不利,
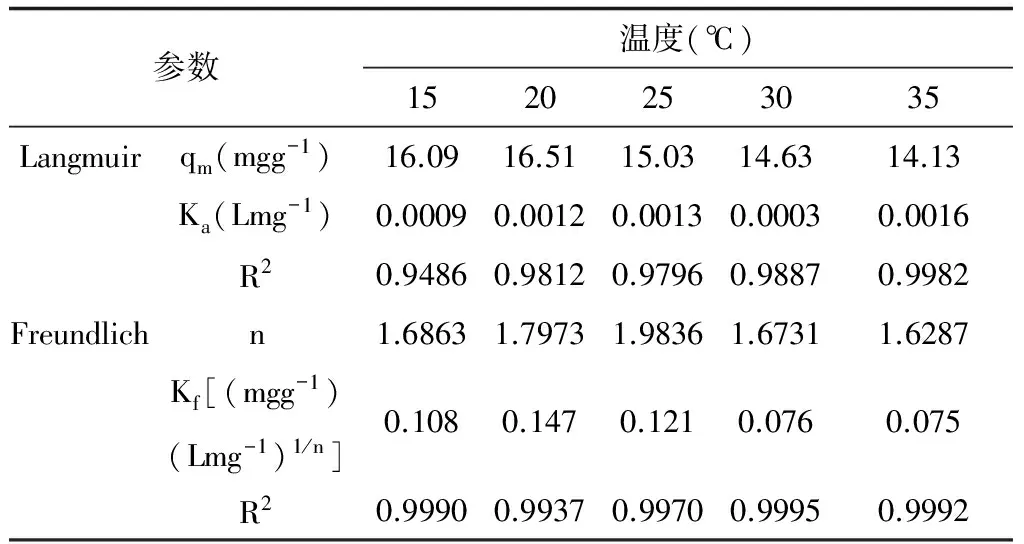
表2 两种等温吸附模型参数
说明该吸附过程放热;而n >1则说明Ti-Z对F-的吸附过程较容易进行,属于优惠吸附。
2.7 实际水样的除氟研究
在氟污染地区采集生活饮用水原水进行研究,配制合适的标准曲线,测其电位得出原水中氟离子浓度约为4.37mg/L,投入适量的改性沸石进行实验测定,结果比较如图9所示。
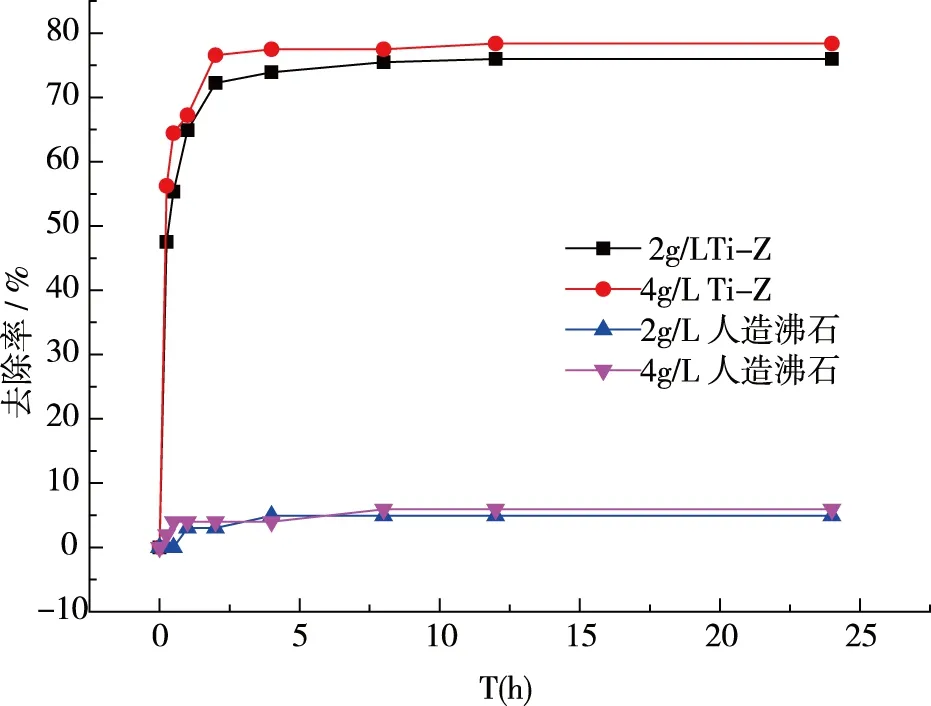
图9 沸石改性前后对实际水样F-的去除效果
由此可知,改性沸石对实际水样中F-的去除具有一定的效果,吸附后F-浓度能够达到标准。
2.8 水体富营养化程度对除氟效果影响
从附近郊区及距离工厂较近的地方分别采集水体富营养化程度不同的原水,进行测定比较,分析得出结果如表3。由于自然水体中含有杂质较多,F-在水中的扩散受阻,与其竞争吸附位点,从而影响吸附剂有效地对F-进行吸附,导致去除率下降。与2.3部分实验模拟含氟水进行对比,初始浓度约为4.73、8.59mg/L的含氟水去除率由原来的79.95%、88.92%(参考4.77、8.69mg/L这两个浓度点)降低到56.2%、69.8%,说明富营养化程度大的水体对除氟效果影响较大。
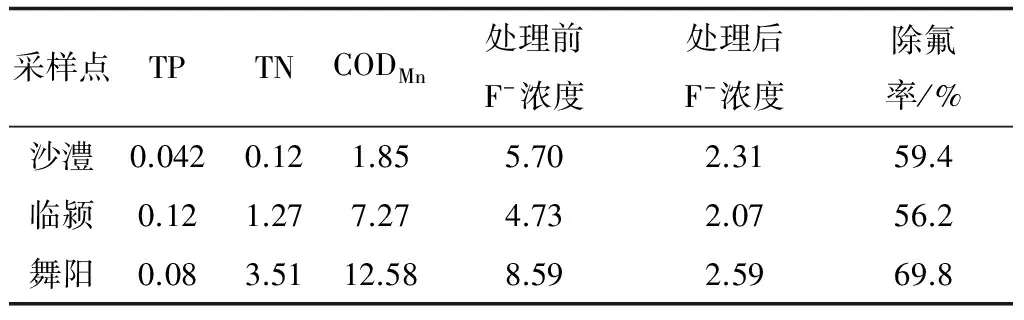
表3 实际水样除氟效果 单位:mg/L
注:表中所列数据均为平行测定的平均值。
2.9 再生沸石除氟实验
用硫酸钛对沸石再生后,其除氟率见表4。由表4可知, 随着硫酸钛溶液浓度的增加,再生后的改性沸石的除氟率先上升后下降,3.0%硫酸钛溶液再生的沸石除氟率最高为62.4%,再生条件的优化需要进一步研究。处理1m3水大概需要改性沸石4.0kg,改性沸石Ti-Z所用原料天然沸石价格低廉,且可以再生反复利用,再生后对氟离子仍有较好的吸附效果,从而大大节约成本。
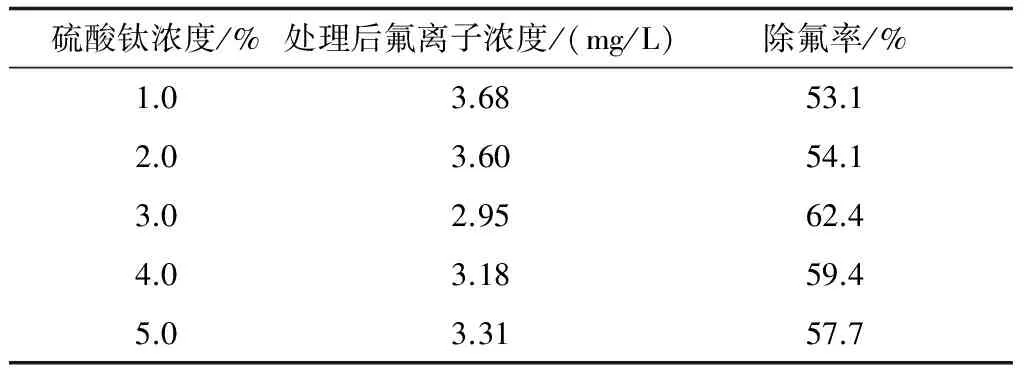
表4 不同浓度硫酸钛溶液再生沸石的除氟效果
注:处理前模拟水样含氟量为7.84 mg/L。
3 结论
(1)实际生活中,天然高氟水的F-浓度范围为7~10mg/L,投加适宜的Ti-Z吸附后能够使F-浓度降低到1.0mg/L以下,低于国内饮用水允许含量(1.0 mg/L),可以作为高氟地区的除氟剂。
(2)Ti-Z对水中F-的吸附在8h内达到平衡,投放量为4g/L时吸附效果较好,高温对吸附不利;pH=3时,吸附效果最好;CO32-、PO43-和NO3-的存在会影响氟的吸附,影响程度为PO43->CO32->NO3-。准二级动力学方程更符合Ti-Z的吸附行为。热力学吸附等温式的非线性拟合和等温式参数结果表明Freundlich模型最适合描述F-在水中和Ti-Z上的分配情况。
(3)沸石作为一种天然矿石,来源广、机械强度好,且无毒无害。文中采用的沸石改性和再生方法简单、操作方便,便于掌握和推广。
[1] 中华人民共和国卫生部,中国国家标准化管理委员会. GB5749-2006生活饮用水卫生指标[S].2006.
[2] Bhatnagar A, Kumar E, Sillanp M. Fluoride removal from water by adsorption-A review [J]. Chem Eng J, 2011, 171(3):811-840.
[3] 边艳芳,李响.饮用水除氟技术研究现状与新进展[J]. 天津建设科技, 2013, 23(05):79-80.
[4] Mourabet M, Boujaady H E, Rhilassi A E, et al. Defluoridation of water using Brushite: Equilibrium, kinetic and thermodynamic studies [J]. Desalination, 2011, 278(1-3):1-9.
[5] Liu Q S, Zheng T, Wang P, et al. Adsorption isotherm, kinetic and mechanism studies of some substituted phenols on activated carbon fibers [J]. Chemical Engineering Journal, 2010,157(2-3):348-356.
[6] Chubar N I, Kanibolotskyy V A, Strelko V V, et al. Adsorption of phosphate ions on novel inorganic ion exchangers [J]. Colloid and Surf., 2005, 255(1-3):55-63.
[7] Garg P, Chaudhari S. Adsorption of fluoride from drinking water on magnesium substituted hydroxyapatite[C]//International Conference on Future Environment and Energy,2012:180-185.
[8] Kamble S P, Deshpande G, Barve P P, et al. Adsorption of fluoride from aqueous solution by alumina of alkoxide nature: Batch and continuous operation [J].Desalination, 2010, 264(1-2):15-23.
[9] Viswanathan N, Meenakshi S. Selective fluoride adsorption by a hydrotalcite/chitosan composite[J]. Appl. Clay Sci. ,2010, 48(4):607-611.
[10] Viswanathan N, Sairam C S, Meenakshi S. Sorption behaviour of fluoride on carboxylated cross-linked chitosan beads[J]. Collid Surf.B, 2009,68(1):48-54.
Study on adsorption of inorganic fluoride in drinking water by modified zeolite
Wang Linpei1, ZhouYingchun1, Li Songya2, Zheng Yazhe3, Peng Xinran1
(1.Luohe Entry-Exit Inspection and Quarantine Bureau, Luohe 462000;2.School of Environmental Science and Engineering, Tianjin University ,Tianjin 300072; 3.Beijing Sound Environment Group Ltd, Beijing 101102)
In this paper, zeolite was soaked with 0.5mol/L titanium sulfate solution for 24 hours and baked at 70 ℃ for 10h for modification. The adsorption properties for F-in drinking water, and effects of several different environmental factors on the adsorption properties of the modified zeolite were also investigated. By kinetic and adsorption isotherm, the mechanism of adsorption was explored.
modified zeolite; domestic drinking water; fluoride; adsorption
2017-04-18; 2017-05-28修回
王林裴(1989-),女,硕士研究生,研究方向:化学分析。E-mail:15136920547@163.com
彭新然(1964-),男,工程师,研究方向:化学分析。E-mail:lhcciblab@aliyun.com
X52
A

