辽东楤木叶皂苷成分及其药学研究进展
邹淑君,许树军,李靖,吕邵娃,肖洪彬*
(1.黑龙江中医药大学药学院,黑龙江 哈尔滨 150040;2.黑龙江中医药大学实验中心, 黑龙江 哈尔滨 150040)
辽东楤木叶皂苷成分及其药学研究进展
邹淑君1,许树军2,李靖1,吕邵娃1,肖洪彬2*
(1.黑龙江中医药大学药学院,黑龙江 哈尔滨 150040;2.黑龙江中医药大学实验中心, 黑龙江 哈尔滨 150040)
围绕辽东楤木叶的主要药效物质皂苷类成分及皂苷类物质抗肿瘤活性、保肝活性、遗传毒性、毒理学等相关研究报道进行系统的综述,为其深入研究及开发利用提供参考。
辽东楤木叶;皂苷成分;抗肿瘤;保肝作用;遗传毒性;毒理
辽东楤木(AraliaelataSeem)又称刺老牙、龙芽楤木等,为五加科楤木属多年生落叶灌木植物,营养价值丰富。传统中医药认为其具有补气安神、强精滋肾、祛风活血、除湿止痛的功能[1]。自上世纪50年代起, 国内外学者通过实验证实皂苷类成分是辽东楤木中主要的药效成分[2]。主要有抗肿瘤作用、降血糖作用、改善肝功能等[3]。但叶资源在早期并未得到重视,近年逐渐证明辽东楤木叶药用价值很高。叶可以再生,如果加以充分利用,将会产生巨大的社会价值。本文对辽东楤木叶的皂苷类成分及其相关药学研究作一综述,为辽东楤木叶的进一步研究和开发利用提供指导。
1 皂苷类化学成分研究
目前,确定从辽东楤木叶中分离出的皂苷类成分有近60种。基本上是以齐墩果酸、常春藤、刺囊酸和caulophyllogenin等五环三萜类皂苷元为主[3],它们经常在3位和(或)28位与糖连接成单糖链或多糖链苷。糖基主要有D-葡萄糖、L-阿拉伯糖、L-鼠李糖、D-葡萄糖醛酸等。从辽东楤木叶中分离出的主要三萜皂苷的结构式见图1~图4。图中-H代表氢原子,-glc代表β-D-葡萄吡喃糖基,-gal代表β-D-吡喃半乳糖基,-rha代表α-L-鼠李吡喃糖基,-ara代表-α-L-阿拉伯糖基,-xyl代表β-D-吡喃木糖基,-glcA代表葡萄糖醛酸基。

图1 辽东楤木叶中分离出的齐墩果酸型三萜皂苷的结构
目前,从辽东楤木叶中分离得到的齐墩果酸型三萜皂苷23种,结构式见图1。其中皂苷1、2为本实验室从辽东楤木叶中分离,皂苷3见于文献[4-5]中,皂苷4、5见于文献[4],皂苷6见于文献[6-7]中,皂苷7、8、21见于文献[5],皂苷9见于文献[8-9],皂苷10、11、12见于文献[10],皂苷13见于文献[5],皂苷14见于文献[10],皂苷15见于文献[11-12],皂苷16、17、18、19见于文献[11],皂苷20见于文献[13-15]中,皂苷22见于文献[14,16-17],皂苷23见于文献[17]中。
从辽东楤木叶中分离得到的常春藤型三萜皂苷20种,结构见图2。其中皂苷1、2、3、4分别见于文献[4,6,12,17]中,皂苷5、12、16见于文献[11-12],皂苷6、7见于文献[4],皂苷8、9见于文献[5],皂苷10见于文献[10],皂苷11见于文献[16],皂苷13、14、15见于文献[11],皂苷17见于文献[18],皂苷18见于文献[13-14,18-19],皂苷19见于文献[14,17]中,皂苷20见于文献[13,16-17,20]中。

图2 辽东楤木叶中分离出的常春藤皂苷元型三萜皂苷的结构
从辽东楤木叶中分离得到的刺囊酸三萜皂苷13种,结构见图3。其中皂苷1见于文献[8,16],皂苷2、3、4、5见于文献[5],皂苷6见于文献[16],皂苷7为自己实验室分离,皂苷8、9见于文献[10],皂苷10见于文献[21],皂苷11见于文献[20],皂苷12见于文献[15],皂苷13见于文献[5,20]中。

图3 辽东楤木叶中分离出的刺囊酸型三萜皂苷的结构
从辽东楤木叶中分离得到的caulophyllogenin型三萜皂苷4种,结构见图4。其中皂苷1见于文献[8],皂苷2见于文献[5],皂苷3见于文献[16],皂苷4见于文献[20]。
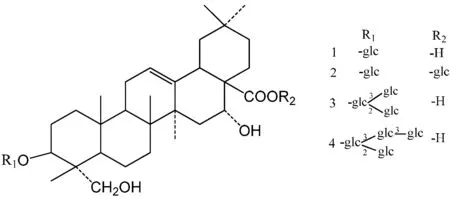
图4 辽东楤木叶中分离出的caulophyllogenin型三萜皂苷的结构
2 药学研究
目前,针对辽东楤木叶中成分的药效药理作用研究报道的有抗肿瘤作用及保肝作用。尤其是抗肿瘤作用已经取得系统性进展。也有对其遗传毒性及毒理学研究的报导。
2.1 抗肿瘤作用研究
针对辽东楤木叶总皂苷成分进行了系统性体内外抗肿瘤实验研究。体外实验多采用MTT法进行,并深入进行抗肿瘤作用机理的研究。有报道的实验研究结果证明总皂苷对人上皮性卵巢癌SKOV3细胞、胃癌BGC细胞、结肠癌HT-29 细胞、结肠癌细胞HCT-8、乳腺癌MCF-7细胞、肝癌细胞BEL-7402、肺腺癌细胞A549等均有抑制或杀伤作用,而且呈现量效关系。作用机理应与诱导细胞凋亡、抑制蛋白表达和改变细胞周期分布有关。体内实验分别采用人A549肺腺癌裸鼠模型、人乳腺癌MCF-7荷瘤小鼠模型、H22小鼠腹水瘤模型、小鼠肉瘤细胞S180为移植性肿瘤进行测试,结果显示楤木叶总皂苷具有体内抗肿瘤活性,且能够增强荷瘤小鼠的免疫细胞功能。发现楤木叶总皂苷对肿瘤抑制率随浓度增加不断增加。作用机理与其能够抑制肿瘤细胞分裂、增殖、诱导细胞凋亡或与升高机体细胞因子水平有关[22-23]。
另外,为寻找抗肿瘤作用有效成分,张艳等[16]先后对18种辽东楤木叶中不同类型皂苷成分进行体外抗血癌HL60、肺腺癌A549和前列腺癌DU145的实验研究,结果证明各种皂苷均显示出一定的毒活性。并且3-O-β-D-吡喃葡萄糖基(1→4)-β-D-吡喃葡萄糖基齐墩果酸显示出特别突出的抑制活性,其对HL60、A549和DU145的半数抑制率IC50值仅分别为15.62、11.25、7.95μmol/L。匡海学等[13]选择7种楤木叶皂苷成分进行体外抗肝癌HepG2、肺腺癌A549和卵巢癌SKOV3实验研究,结果证明不同结构的皂苷对三种肿瘤细胞显示不同的毒理活性。尤其对HepG2、A549表现较好的抑制作用,IC50值分别都在100 μmol/L以下。3-O-[β-D-葡萄吡喃糖基(1→2)][β-D-葡萄吡喃糖基(1→3)]-β-D-葡萄吡喃糖基刺囊酸及3-O-[β-D-吡喃葡萄糖基-(1→3)-β-D-吡喃葡萄糖基-(1→3)][β-D-吡喃葡萄糖基-(1→2)]-β-D-吡喃葡萄糖基刺囊酸-28-O-β-D-葡萄糖酯对三种细胞表现出突出的抑制活性。
2.2 保肝作用研究
王丽岩等[24]通过实验证明辽东楤木叶总皂苷对四氯化碳、D-半乳糖胺导致急性肝损伤引起的血清谷丙转氨酶(ALT)和谷草转氨酶(GOT)升高有明显的降低作用,而对硫代乙酰胺导致的ALT、GOT升高作用不明显。说明辽东楤木叶总皂苷对小鼠急性肝损伤有一定的保护作用,作用机理是通过肝细胞内酶系统的诱导作用而使肝细胞的核酸、蛋白质、糖原的合成及能量的合成增加, 保护肝细胞膜的正常结构。此外,Saito S.等[6]对该植物叶皂苷类成分对实验性肝损伤抑制作用进行了构效关系研究,结果证明以齐墩果酸或常春藤皂苷元为苷元的皂苷。仅在皂苷元的3位上连有糖链的单糖链皂苷对肝细胞无保护作用,而在皂苷元的3位和28位均有糖链的双糖链皂苷却对肝细胞有保护作用,且分子中具有5个单糖的双糖链皂苷的肝细胞保护作用最强。
2.3 遗传毒性研究
吴勃岩等[25]等采用小鼠骨髓嗜多染红细胞徽核试验, 小鼠骨髓细胞染色体畸变试验对辽东楤木叶总皂苷进行遗传毒性研究,按每日50 mg/kg、150 mg/kg、300 mg/kg给药7天。结果表明,楤木叶总皂苷在试验的剂量范围内,不诱发小鼠骨髓嗜多染红细胞微核的增加。对小鼠骨髓细胞染色体没有致畸变作用,提示楤木叶总皂苷对遗传物质无损伤作用。并以小鼠骨髓嗜多染红细胞(PCE)微核率为指标探讨楤木叶总皂甙对环磷酰胺(CP) 诱发的小鼠染色体突变的拮抗作用。结果显示楤木叶总皂苷对小鼠体细胞无致突变性。能明显抑制CP 诱发的小鼠体细胞的遗传损伤。说明辽东楤木叶总皂苷对化学诱变剂引起的染色体断裂有保护作用, 即具有抗突变作用[26]。
2.4 毒理学研究
本课题组李凤金等通过大鼠口服给药方式对辽东楤木叶皂苷提取物进行了急性毒性及长期毒性实验研究。急毒实验大鼠分别每天以1.00、2.15、4.64和10.00 g/kg的剂量灌胃给药1次,连续给药14天。结果表明因用药不良反应所造成的发病率及死亡率都随剂量的增加而增大。其中对雌性大鼠的半数致死量LD50值为3.16 g/kg;对雄性大鼠的LD50值为5.84 g/kg。长毒实验大鼠分别每天以60、180和540 mg/kg的剂量灌胃给药1次,连续给药12周,再恢复4周后被处死进行血液、生化和组织病理学分析。结果表明,在整个期间大鼠饮食没有明显变化,但高剂量雄性大鼠有逐渐增重现象。服药期间,大鼠血红蛋白和红细胞平均容量会明显升高,恢复期总蛋白和球蛋白又明显降低。服药期大鼠的胸腺、肾上腺及脑的重量会有变化,但各器官没有组织病理学变化。说明大鼠以540 mg/kg的剂量每天口服给药不会产生明显的毒性作用。可见辽东楤木叶总皂苷口服有一定的急性毒性,但控制一定的量不会产生明显慢性中毒现象[27]。
3 总结与展望
总之,现有的研究显示,目前从辽东楤木叶中分离得到的皂苷多为三萜皂苷,且以齐墩果酸型、常春藤皂苷元和刺囊酸型三萜皂苷居多,Caulophyllogenin型皂苷数量相对较少。提取的皂苷物质具有抗肿瘤作用,肝保护作用,无遗传毒性,并且口服时控制剂量慢性毒性较小,有很高的药用价值[28-29]。随着研究的不断进行,将会有更多成分从辽东楤木叶中分离出来。总皂苷的药理活性可能是某些成分起了主要作用,也可能是综合作用的结果。因此各种药理活性作用的构效关系如何还有待进一步实验研究确认。
辽东楤木叶生长快速、再生能力强、总量多,应该成为医药开发的重要原料。以前对辽东楤木叶的研究集中在成分分离及总皂苷抗肿瘤活性及机理方面,其他方面的活性研究还很少,为能更广泛的利用辽东楤木叶资源,开发其新的药用价值,应对其进行拓展研究。同时应促进人工培育,增加该药用植物资源的产量和应用。
[1] 赵淑玲,王瀚,王让军,等.野生植物辽东楤木的研究进展[J].绵阳师范学院学报,2014,33(8):83-88.
[2] 张桂娟. 辽东楤木化学成分及其生物活性研究进展[J]. 黑龙江医药,2014,27(4):798-801.
[3] 李凤金,肖洪彬.辽东楤木化学成分和药理作用研究进展[J]. 中国中医药科技,2015,22(3): 353-355.
[4] 杨国红,周建,宋长春. 龙牙楤木叶中苷类成分的化学研究[J].中草药,1995,26(10): 513-517.
[5] Yan Zhang,Ying Peng,Lingzhi Li, et al.Studies on cytotoxic triterpene saponins from the leaves of Aralia elata[J]. Food Chemistry, 2013, 138(1): 208-213.
[6] Saito S,Ebashi D,Sumita S,et al.Comparision of cytoprotective effect of saponins isolated from leaves of A elata. SEEM with synthesized bisdesmosides of oleanolic acid and hederagenin on carbontetrachloride-induced heptic injury[J]. Chem Pharm Bull,1993,41(8):1395-1401.
[7] 马志强.刺龙芽化学成分和生物活性的研究[D]. 沈阳:沈阳药科大学,2004.
[8] 张艳, 胡燕, 赵雷. 龙牙楤木叶化学成分的分离与鉴定[J]. 沈阳药科大学学报, 2012, 29(1): 5-8.
[9] MS Kamel,K Ohtani,HA Hassanean,et al.Triterpenoidal saponins from Cornulaca monacantha[J]. Die Pharmazie, 2000, 55(6):460-462.
[10] M Zhi-Qiang,Z Yan,C Cheng-Ke,et al. Two new triterpenoid saponins from the leaves of Aralia elata [J]. Journal of Asian Natural Products Research, 2013,15(8):849-854.
[11] Saito S, Sumita S, Tamura N, et al. Saponins from the leaves of Aralia elata Seem. (Aralia ceae) [J]. Chem Pharm Bull,1990,38(2): 411-414.
[12] Kim J S, Shim S H, Chae S, et al. Saponins and other constituents from the leaves of Aralia elata [J]. Chem Pharm Bull,2005,53(6): 696-700.
[13] 张雷,王志财,郭明全, 等.辽东楤木叶中3个皂苷的鉴定[J].中草药, 2004,35(9):969-971.
[14] Mingquan Guo,Lei Zhang,Zhiqiang Liu.Analysis of Saponins from Leaves of Aralia elata by Liquid Chromatography and Multi-stage Tandem Mass Spectrometry[J]. Analytical Sciences the International Journal, 2009, 25(6):753-758.
[15] 王秋红,王琦,王知斌,等. 辽东楤木叶有效部位中楤木皂苷Ⅴ、Ⅵ及总皂苷质量控制[J].中成药,2013,35(9):1950-1953.
[16] Yan Zhang, Zhiqiang Ma, Chong Hu, et al. Cytotoxic triterpene saponins from the leaves of Aralia elata [J]. Fitoterapia, 2012, 83(4):806-811.
[17] 宋丽丽. 辽东楤木叶中化学成分的研究[D].长春:吉林大学,2006.
[18] Kuang H X, Sun H, Zhang N, et al. Two new spaonin, congmuyenoside A and B from the levaes of Aralia elate collectd in Heilongjiang, China[J]. Chem Pharm Bull,1996,44(11): 2183-2185.
[19] 张雷,陈燕萍,王志才,等. 辽东楤木叶中皂苷Congmuyenoside B(2)的分离与鉴定[J]. 分析化学,2007,35(8): 1221-1224.
[20] HX Kuang,ZB Wang,QH Wang,et al. Triterpene Glucosides from the Leaves of Aralia elata and Their Cytotoxic Activities[J]. Chemistry & Biodiversity, 2013,10(4):703-710.
[21] Wang Q H, Zhang J, Ma X, et al. A new triterpenoid saponin from the leaves of Aralia elata [J]. Chin J Nat Med, 2011, 9(1): 17-21.
[22] 张秀萍,孙达辰,肖洪彬. 辽东楤木叶总皂苷抗肿瘤作用研究进展[J].中国实验方剂学杂志,2015,21(11):232-234.
[23] 王春梅,薛晓鸥,张广美.辽东楤木协同顺铂抑制SKOV3-DDP生长的作用及机理[J].中医药信息,2013,30(3):24-28.
[24] 王丽岩,肖洪彬,王鸣慧.辽东楤木叶总皂苷抗急性肝损伤的实验研究[J].中医药信息,2009,26(2):29-30.
[25] 吴勃岩,张韵娴,齐彦,等.龙牙楤木叶总皂试的遗传毒性研究[J].中医药学报,1999,27(6):47.
[26] 吴勃岩,闻杰,张韵娴,等.龙牙楤木叶总皂苷抗诱变性研究[J].中医药信息,2000,17(4):74.
[27] Fengjin Li, Xiaoli He, Wenying Niu , et al. Sub-chronic safety evaluation of the ethanol extract of Aralia elata leaves in Beagle dogs[J].Regulatory Toxicology and Pharmacology,2016(79):1-11.
[28] 尹丽颖,仲丽丽,边晓燕,等.辽东楤木叶总皂苷对人胃癌BGC细胞凋亡的影响[J].中医药学报,2012,40(3):12-14.
[29] 王春梅,张广美.辽东楤木叶总皂苷对卵巢癌细胞的抑制作用及其对线粒体凋亡途径的影响[J].中医药学报,2011,39(1):17-19.
Pharmaceutical Research Progress of Saponins from Leaves ofAraliaElata
ZOU Shu-jun1, XV Shu-jun2, LI Jing1, LV Shao-wa1, XIAO Hong-bin2
(1.CollegeofPharmacy,HeilongjiangUniversityofChineseMedicine,Harbin150040,China;2.ExperimentCenter,HeilongjiangUniversityofChineseMedicine,Harbin150040,China)
This research reviewed the researches about saponins fromAraliaelata, in terms of its anti-tumor activity, liver protective activity, genetic toxicity and toxicology, to provide references for deep study and its utilization.
Leaves ofAraliaeleta; Saponins; Anti-tumor; Liver protective effect; Genetic toxicity; Toxicology
2016-09-12
2016-11-21
中国博士后科学基金面上项目(2014M551289);国家“十二五”重大新药创制科技重大专项(2011ZX11102)
邹淑君(1974-),女,博士,副教授,黑龙江中医药大学在站博士后工作人员,主要从事药物分析研究工作。
*通讯作者:肖洪彬(1957-),男,教授,博士生导师,主要从事中药药理学研究工作。
R284;R285
A
1002-2392(2017)04-0111-04

