乌鲁木齐市妊娠早中晚期甲状腺激素水平的参考范围
宋晓平,隋 霜,迪丽胡马·吐尔逊
(新疆维吾尔自治区人民医院产科,新疆 乌鲁木齐 830001)
乌鲁木齐市妊娠早中晚期甲状腺激素水平的参考范围
宋晓平,隋 霜,迪丽胡马·吐尔逊
(新疆维吾尔自治区人民医院产科,新疆 乌鲁木齐 830001)
目的 评估乌鲁木齐市妊娠期妇女各期特异性血清游离三碘甲状腺原氨酸(FT3)、游离甲状腺素(FT4),血清促甲状腺激素(TSH)的正常参考范围。方法 选取新疆维吾尔自治区人民医院妇产科门诊进行常规孕期检查的正常妊娠妇女663例作为研究组,非妊娠期妇女185例作为对照组,根据美国国家临床生化研究院(NACB)指南的推荐,采用电化学发光法测定FT3、FT4、血清TSH、抗甲状腺球蛋白抗体(TgAb)、抗甲状腺过氧化物酶抗体(TPOAb)。结果 妊娠早、中、晚期血清FT3三组比较差异有统计学意义,F=155.20,P<0.05;随着孕期增加,FT3水平呈下降趋势,妊娠早、中、晚期两两比较差异均有统计学意义(t值分别为0.18、0.19、0.76,均P<0.05);血清FT3在妊娠早期、妊娠中期、妊娠晚期的参考值范围分别为:3.43~9.94pmol/L、3.53~5.74pmol/L、3.56~5.19pmol/L。妊娠早、中、晚期血清FT4三组比较差异有统计学意义,F=100.78,P<0.05;随着孕期增加,FT4水平呈下降趋势,妊娠早、中、晚期两两比较差异均有统计学意义(t值分别为0.71、0.74、0.94,均P<0.05);血清FT4在妊娠早期、妊娠中期、妊娠晩期的参考值范围分别为:9.94~20.21pmol/L、9.69~17.77pmol/L、7.28~15.99pmol/L。妊娠早、中、晚期血清TSH三组比较差异有统计学意义,H=59.88,P<0.05;随着孕期增加,TSH水平呈上升趋势,妊娠早、中、晚期两两比较差异均有统计学意义(t值分别为0.34、0.23、-1.15,均P<0.05);血清TSH在妊娠早期、妊娠中期、妊娠晚期的参考值范围分别为:0.06~4.80mIU/L、0.29~5.84mIU/L、0.65~7.64mIU/L。结论 乌鲁木齐市妊娠期妇女的血清甲状腺激素水平具备地域上的特异性,与非妊娠期差异较大,与美国甲状腺学会(ATA)建议的妊娠期甲状腺功能指标参考范围结果差别较大。
妊娠;参考范围;促甲状腺激素;甲状腺素
妊娠期是女性一生中的特殊生理时期,受妊娠期胎盘分泌大量激素及母体免疫状态的影响,妊娠不同时期甲状腺激素水平变化呈现不同特点。近年来研究发现妊娠期甲状腺功能异常可能导致流产、早产、新生儿神经系统发育异常等不良妊娠结局[1],故越来越受到各界相关学科的重视。目前还没有公认的妊娠各期甲状腺激素参考范围用于临床诊断和治疗[2],中华医学会内分泌学分会和中华医学会围产医学分会在我国《妊娠和产后甲状腺疾病诊治指南》中建议需要建立妊娠期各阶段本单位或者本地区特异的血清甲状腺功能指标参考值[3]。目前新疆乌鲁木齐市妊娠女性整个孕期甲状腺功能检测方面尚属空白。故本研究采用横断面观察,试图建立该地区妊娠早、中、晚不同阶段孕妇血清甲状腺相关激素水平的正常参考值范围。
1对象与方法
1.1研究对象
选取2014年1月至2014年12月在新疆维吾尔自治区人民医院妇产科门诊进行常规孕期检查的正常妊娠妇女663例作为研究组,根据孕周将研究组分为妊娠早期组、妊娠中期组、妊娠晚期组。孕1~12周末为妊娠早期,孕13~27周末为妊娠中期,孕28~40周为妊娠晚期。同时选取2014年1月至2014年12月在本院体检中心查体正常的健康非妊娠育龄女性185例作为对照姐。所有研究对象均知情同意。
1.2入选标准
研究对象的入选标准根据美国临床生化研究院(NACB)建议标准进行筛选,硏究组的筛选条件:①查体未触及甲状腺肿大;②妊娠前及妊娠期间未服用影响甲状腺功能的药物(不包括雌激素类);③无甲状腺相关疾病的既往史;④甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPOAb)阴性;⑤无自身免疫性疾病;⑥妊娠期间无妊娠剧吐症状;⑦无甲状腺疾病的家族史;⑧经超声检查确定为单胎妊娠;⑨无滋养层细胞疾病;⑩无先兆子痫;促甲状腺激素受体抗体(thyrotrophin receptor antibody,TRAb)阴性者;抗甲状腺球蛋白抗体(thyroglobulin antibody,TGAb)阴性者;饮食常规服用加碘盐。
入选对照组的标准如下:①不孕病史;②平素月经周期正常;③无甲状腺相关疾病的既往史;④未服用影响甲状腺功能的药物;⑤查体未触及甲状腺肿大;⑥TPOAb阴性;⑦TGAb阴性;⑧无自身免疫性疾病;⑨TRAb阴性者;⑩无甲状腺疾病的家族史。
1.3检测指标
入选对象于清晨采集空腹静脉血5mL,静置离心,分离血清。采用罗氏Cobas e601电化学发光全自动免疫分析仪使用电化学免疫分析法测定游离三碘甲状腺原氨酸(free triiodothyronine,FT3)、游离甲状腺素(free triiodothyronine,FT4)、促甲状腺激素(thyroid stimulating hormone,TSH)、TPOAb、TGAb水平,其检测试剂盒均由罗氏(瑞士)提供。TPOAb的正常范围为0~34IU/mL,TPOAb>34IU/mL为阳性,总变异系数≤15%;血清TGAb的正常范围为0~115IU/mL,TGAb>115IU/mL为阳性,总变异系数≤15%。血清TSH的正常范围为0.27~4.20mIU/L,总变异系数≤10%;FT3的正常范围3.10~6.80pmol/L,总变异系数≤10%;FT4的正常范围为12.0~22.0pmol/L,总变异系数≤10%。
1.4统计学方法

2结果
2.1一般资料分析
研究组及对照组一般情况见表1。各组年龄具有均衡性,比较差异无统计学意义(P>0.05)。


组别例数(n)年龄(岁)孕周(周)妊娠早期组17828.37±0.269.23±1.78妊娠中期组22228.78±0.2322.34±3.25妊娠晚期组26328.50±0.2336.72±3.62对照组(非妊娠组)18528.33±0.27-
2.2妊娠各期甲状腺激素水平变化
2.2.1各组血清FT3变化和比较
妊娠早、中、晚期血清FT3三组比较差异有统计学意义,F=155.20,P<0.05。随着孕期增加,FT3水平呈下降趋势,妊娠早、中、晚期两两比较差异均有统计学意义(t值分别为0.18、0.19、0.76,均P<0.05)。与对照组比较,妊娠早期FT3略高于对照组,较对照组升高4.5%,差异有统计学意义(t=-0.18,P<0.05);妊娠中期逐渐下降,略低于对照组,差异无统计学意义(t=0.006,P=0.89);妊娠晚期下降明显,明显低于对照组,差异有统计学意义(t=0.59,P<0.05),见表2。

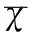
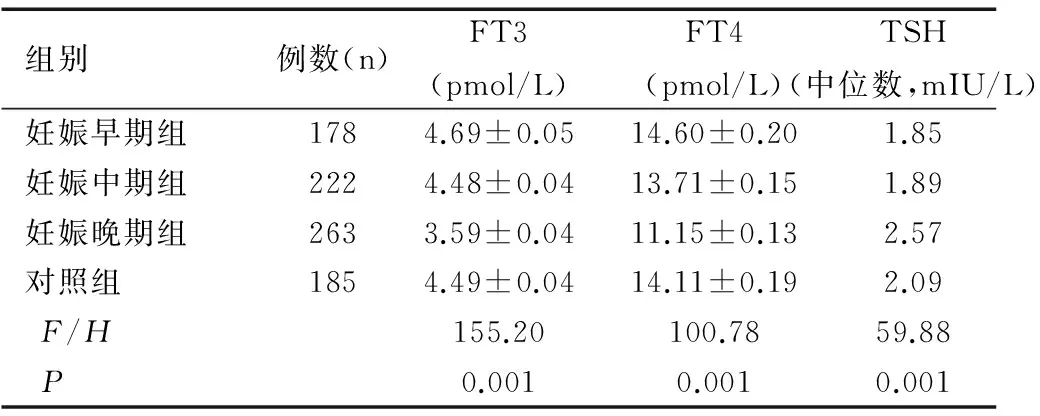
组别例数(n)FT3(pmol/L)FT4(pmol/L)TSH(中位数,mIU/L)妊娠早期组1784.69±0.0514.60±0.201.85妊娠中期组2224.48±0.0413.71±0.151.89妊娠晚期组2633.59±0.0411.15±0.132.57对照组1854.49±0.0414.11±0.192.09F/H155.20100.7859.88P0.0010.0010.001
2.2.2各组血清FT4变化和比较
妊娠早、中、晚期血清FT4三组比较差异有统计学意义,F=100.78,P<0.05。随着孕期增加,FT4水平呈下降趋势,妊娠早、中、晚期两两比较差异均有统计学意义(t值分别为0.71、0.74、0.94,均P<0.05)。与对照组比较,妊娠早期血清FT4较对照组升高3.5%,至中期下降不明显,差异无统计学意义(t=0.03,P=0.82);至妊娠晚期下降明显,明显低于正常对照组,差异有统计学意义(t=0.23,P<0.05),见表2。
2.2.3各组血清TSH变化和比较
妊娠早、中、晚期血清TSH三组比较差异有统计学意义,H=59.88,P<0.05。随着孕期增加,TSH水平呈上升趋势,妊娠早、中、晚期两两比较差异均有统计学意义(t值分别为0.34、0.23、-1.15,均P<0.05)。与对照组比较,妊娠早期TSH水平明显低于对照组,差异有统计学意义(t=-0.34,P<0.05);妊娠中期逐渐上升,略低于对照组,差异无统计学意义;妊娠晚期上升明显,明显高于对照组(t=-0.81,P<0.05),见表2。
2.3妊娠各期血清FT3、FT4、TSH指标的参考范围
血清FT3在妊娠早期、妊娠中期、妊娠晚期的参考值范围分别为:3.43~9.94pmol/L、3.53~5.74pmol/L、2.39~5.19pmol/L;血清FT4在妊娠早期、妊娠中期、妊娠晩期的参考值范围分别为:9.94~20.21pmol/L、9.69~17.77pmol/L、7.28~15.99pmol/L;血清TSH在妊娠早期、妊娠中期、妊娠晚期的参考值范围分别为:0.06~4.80mIU/L、0.29~5.84mIU/L、0.65~7.64mIU/L,见表3。
表3 妊娠各期血清 FT3、FT4、TSH指标的参考范围
Table 3 Reference ranges of serum FT3, FT4 and TSH in each period of pregnancy

组别例数(n) 百分比(%) P2.5thP50.0thP97.5thFT3(pmol/L) 对照组1853.434.475.75 妊娠早期组1783.434.639.94 妊娠中期组2223.534.455.74 妊娠晚期组2632.393.565.19FT4(pmol/L) 对照组18510.0913.9119.72 妊娠早期组1789.9414.3020.21 妊娠中期组2229.6913.5217.77 妊娠晚期组2637.2810.9215.99TSH(mIU/L) 对照组1850.482.094.56 妊娠早期组1780.061.854.80 妊娠中期组2220.291.895.84 妊娠晚期组2630.652.577.64
3讨论
甲状腺激素对胎儿神经发育有重要的作用,而胎儿在20周后甲状腺功能才逐渐发育成熟,因此,胎儿在早孕期的甲状腺激素主要来源于母体,如果母亲出现甲状腺功能减退,包括亚临床甲状腺功能减退,将对子代的脑神经发育造成不可逆的影响[2]。根据国内外研究发现[3-4],只筛查高危妊娠人群有30%~80%的甲状腺疾病漏诊,因此对于整个妊娠人群进行普遍筛查优于只筛查高危妊娠人群。因此及时发现和治疗甲状腺功能减退对对预防和减少产科并发症,保证胎儿正常发育有着重要意义[5]。
3.1妊娠各期血清TSH变化
TSH是垂体前叶TSH细胞分泌的促进甲状腺生长和机能的激素。由于绒毛膜促性腺激素(hCG)和TSH有相同的α亚单位、相似的β亚单位和受体亚单位,因此,在早孕期hCG的上升反馈性抑制TSH,使TSH在早孕期下降,并且对甲状腺细胞TSH受体有轻度刺激作用,血清hCG水平和TSH水平呈现明显负相关,呈镜像关系,在孕10~12周hCG达高峰时,此时TSH降至最低。随着hCG水平在中晚孕期逐渐下降,TSH水平在中孕期和晚孕期逐渐升高[6]。由于近年来研究发现亚临床甲状腺功能减退可以导致流产和早产的发病率增加2~3倍,可以降低出生后代的智商8~10分[7]。因此,妊娠各期TSH的特异性参考值显得越来越重要。本研究结果显示期TSH妊娠早期的中位数为1.85mIU/L,参考范围为0.06~4.80mIU/L,TSH在妊娠早期孕期最低,中晚孕期逐渐升高,妊娠中期的中位数为1.89mIU/L,参考范围为0.29~5.84mIU/L,妊娠晚期中位数为2.57mIU/L,参考范围为0.65~7.64mIU/L,明显超出了美国甲状腺学会(ATA)指南推荐的2.5mIU/L,与2008年阎玉琴等报告的碘适量地区早孕期TSH参考值0.03~4.51mIU/L相近,还有张春艳[8]报道的成都地区的早孕期TSH参考值0.01~4.94mIU/L相似。腾卫平[9]在其研究中发现妊娠妇女平均孕周为7.4周(n=3 741),T1期(孕周1~12周末)血清TSH参考范围0.69~5.64mIU/L(中位数是1.66mIU/L),上限值也明显高于2.5mIU/L;采用这一特异性参考范围T1期的亚临床甲状腺功能减退的患病率是4.0%;如果采纳以ATA提出的TSH>2.5mIU/L为标准,该研究T1期的亚临床甲状腺功能减退的患病率高达27.8%,患病率差异近7倍,这一差异使大家不得不思考ATA提出的TSH>2.5mIU/L标准在我国妊娠妇女中应用的合理性。复习相关文献,发现各地区报道的TSH在早孕期的参考范围均高于ATA指南推荐的2.5mIU/L,波动在3.58~4.94mIU/L[10-11],仅吴坚敏等[12]报道的浙江余姚地区的孕早期TSH值为0.06~2.59mIU/L,接近2.5mIU/L。造成妊娠期血清TSH这种差异的原因可能主要是我国人群血清TSH水平的普遍升高,仍然需要大规模的调查。
3.2妊娠各期血清FT3和FT4变化
血浆中三碘甲腺原氨酸(triiodothyronine,T3)和四碘甲腺原氨酸(tetraiodothyronine,T4)是与甲状腺结合球蛋白(thyroxine binding globulin,TBG)结合的甲状腺激素,没有生物学活性,其高低不能反映甲状腺的功能状态。FT3和FT4不与TBG结合,是游离状态的、具有生物学活性的甲状腺激素,由于其含量不受TBG影响,可以特异性地反映甲状腺的功能状态,因此在甲状腺功能亢进和甲状腺功能减退的诊断、病情严重程度评估、疗效监测等方面有重要的应用价值。本研究结果发现,孕早FT3水平高于对照组,较对照组升高4.5%(P<0.05),孕早FT4水平略高于对照组(P>0.05),较对照组升高3.5%,早孕期FT3和FT4水平最高,随着孕期增加,两者水平均逐渐下降,低于对照组水平(P<0.05)。这与我国《妊娠和产后甲状腺疾病诊治指南》中指出的妊娠早期血清FT4水平较非妊娠时升高的趋势一致,升高的幅度略小于指南中的10%~15%;与2014年申妍在济南地区的研究结果孕早期FT4升高5%的结果相似。但本研究印证了妊娠早期血清值FT4较非妊娠时期部分升高这一事实。孕早期升高的FT3和FT4对于胎儿早期发育非常重要:因此时胎儿尚不能合成甲状腺激素,孕妇甲状腺激素需满足其自身和胎儿发育的双重需要。至中晚孕期,随着hCG水平逐渐下降和TSH水平逐渐升高,FT3和FT4水平下降趋势也逐渐稳定。因此,对不同方法和不同孕周应建立方法特异性和孕周特异性参考值范围。
3.3妊娠各期血清FT3、FT4、TSH指标的参考范围
本研究调查的地区是新疆乌鲁木齐,新疆地处亚欧大陆腹地,环境中碘资源缺乏,食盐加碘作为行之有效的防治碘缺乏病策略自1995年实施以来,取得了很大的成效,碘缺乏病得到了明显的控制。我国原卫生部2010年食品安全国家标准《食用盐碘含量(征求意见稿)》在征求意见稿的编制说明中提到,尿碘含量新疆为适宜水平(100~200g/L)。本调查结果血清FT3在妊娠早期、妊娠中期、妊娠晚期的参考值范围分别为:3.43~9.94pmol/L、3.53~5.74pmol/L、2.39~5.19pmol/L;血清FT4在妊娠早期、妊娠中期、妊娠晩期的参考值范围分别为:9.94~20.21pmol/L、9.69~17.77pmol/L、7.28~15.99pmol/L;血清TSH在妊娠早期、妊娠中期、妊娠晚期的参考值范围分别为:0.06~4.80mIU/L、0.29~5.84mIU/L,0.65~7.64mIU/L。与文献报道的参考范围,有一定差异。这种差异可能与地区、生活习惯、碘元素充裕程度、所用实验仪器及试剂等的不同有关。这提示对妊娠期甲状腺功能评价的重要性,不能单一用孕前激素水平参考范围进行判断,而延误妊娠期甲状腺疾病的治疗和胎儿发育的检测。
[1]李桂娟,林彩莲.妊娠母体甲状腺功能减退与母婴妊娠结局的相关性分析[J].中国妇幼健康研究,2016,27(5):643-646.
[2]Maraka S,Mwangi R,McCoy R G,etal.Thyroid hormone treatment among pregnant women with subclinical hypothyroidism: US national assessment[J].BMJ,2017,356:i6865.
[3]De Groot L,Abalovich M,Alexander E K,etal.Management of thyroid dysfunction during pregnancy and postpartum:an Endocrine Society clinical practice guideline[J].J Clin Endocrinol Metab,2012,97(8):2543-2565.
[4]Springer D,Jiskra J,Limanova Z,etal.Thyroid in pregnancy: from physiology to screening[J].Crit Rev Clin Lab Sci,2017,54(2):102-116.
[5]Alexander E K,Pearce E N,Brent G A,etal.2017 guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and the postpartum[J].Thyroid,2017,27(3):315-389.
[6]Khan I,Okosieme O E,Lazarus J H.Current challenges in the pharmacological management of thyroid dysfunction in pregnancy[J].Expert Rev Clin Pharmacol,2017,10(1):97-109.
[7]Yim C H.Update on the management of thyroid disease during pregnancy[J].Endocrinol Metab(Seoul),2016,31(3):386-391.
[8]张春艳.成都地区妊娠妇女甲状腺激素正常参考值范围的建立及甲状腺疾病的筛查[D].南充:川北医学院,2014.
[9]滕卫平.对妊娠早期TSH参考范围上限值的新认识[J].中华内分泌代谢杂志,2014,30(12):1039-1040.
[10]杨小猛,赵丹,陈书恩,等.正常孕妇妊娠各期甲状腺激素参考范围的建立及其临床意义[J].分子诊断与治疗杂志,2014,6(1):33-36.
[11]胡璐璐.郑州地区妊娠期妇女血清甲状腺激素水平参考值的相关研究[D].郑州:郑州大学,2014.
[12]吴坚敏,叶淼,俞如葵.余姚地区妊娠妇女甲状腺激素参考范围调查[J].中国卫生检验杂志,2015,25(18):3166-3168.
[专业责任编辑:李春芳]
Reference range for thyroid hormone level in early, middle and late stage of pregnancy in Urumqi City
SONG Xiao-ping, SUI Shuang, Dilihumaer TUMAXUN
(Department of Obstetrics, Xinjiang Uygur Autonomous Region People’s Hospital, Xinjiang Urumqi 830001, China)
Objective To establish normal reference ranges for specific serum FT3, FT4 and TSH in different pregnancy stages of pregnant women in Urumqi City. Methods A total of 663 normal pregnant women receiving routine prenatal examination in department of obstetrics and gynecology of Xinjiang Uygur Autonomous Region People’s Hospital were chosen as study group, and 185 non-pregnant women were chosen as control group. According to the guidelines of United States National Institute of Clinical Biochemical (NACB), FT3, FT4, serum TSH, thyroglobulin antibody (TGAb) and thyroid peroxidase antibody (TPOAb) were detected by electrochemiluminescence method. Results Difference in serum FT3 in early, middle and late stage of pregnancy was statistically significant among three groups (F=155.20,P<0.05). FT3 level declined with increase of pregnancy and difference in pairwise comparison among early, middle and late pregnancy stage had statistical significance (tvalue was 0.18, 0.19 and 0.76, respectively, allP<0.05). Reference range of serum FT3 in early, middle and late stage was 3.43-9.94pmol/L, 3.53-5.74pmol/L and 3.56-5.19pmol/L, respectively. Difference in serum FT4 in early, middle and late pregnancy stage had statistical significance (F=100.78,P<0.05). FT4 level decreased with pregnancy time increase and difference in pairwise comparison among early, middle and late pregnancy stage had statistical significance (tvalue was 0.71, 0.74 and 0.94, respectively, allP<0.05). Reference range of serum FT4 in early, middle and late pregnancy stage was 9.94-20.21pmol/L, 9.69-17.77pmol/L and 7.28-15.99pmol/L, respectively. Difference in serum TSH in early, middle and late pregnancy stage showed statistical significance (H=59.88,P<0.05). TSH level increased with advancing of pregnancy stage and difference in pairwise comparison among early, middle and late pregnancy stage was statistically significant (tvalue was 0.34, 0.23 and -1.15, respectively, allP<0.05). Reference range of serum TSH in early, middle, and late stage was 0.06-4.80mIU/L, 0.29-5.84mIU/L and 0.65-7.64mIU/L, respectively.Conclusion Thyroid hormone level of pregnant women in Urumqi has region specificity and it is very different from that of non-pregnant women and from thyroid function index reference range suggested by American Thyroid Association (ATA).
pregnancy; reference range; thyroid stimulating hormone; thyroxine
2016-12-18
新疆维吾尔自治区人民医院院内项目:妊娠期妇女甲状腺疾病的筛查的前瞻性研究(编号:20130228)
宋晓平(1977-),女,副主任医师,硕士研究生,主要从事围产医学的研究。
迪丽胡马·吐尔逊,主任医师。
10.3969/j.issn.1673-5293.2017.07.026
R714.2
A
1673-5293(2017)07-0832-04

